慢性心力衰竭時運動鍛煉改善血管內皮功能的臨床觀察
高艷玲 林宏揚 葛志明(煙臺毓璜頂醫院ICU,山東 煙臺 264000)
以往研究多認為,慢性心力衰竭時患者感到乏力是由于心臟泵功能障礙,不能向骨骼肌輸送足夠的氧,呼吸困難是由于肺淤血。運動可使心功能惡化而要求病人限制體力活動。近年來越來越多的研究對此提出質疑,因為研究發現患者的運動能力不僅與心臟功能有關,而且與外周血管內皮功能的改變有非常密切的關系,心臟功能改善的時程小于運動耐力改善的時程,即運動耐力的改善滯后于心臟功能的改善。但是,目前系統的有關運動鍛煉對血管內皮功能影響的臨床研究較少。
1 對象與方法
1.1 研究對象 心力衰竭組入選病例均為穩定型冠心病合并心衰患者,急性冠狀動脈綜合征、伴有活動性心肌炎、未矯正的瓣膜病、合并腎功能不全者不在研究之列。按照紐約心臟協會心功能分級標準將慢性心衰患者分成NYHAⅡ、Ⅲ、Ⅳ級共3組,每組依據是否進行運動鍛煉又分為兩個亞組。其中,對照組18例,男10例,女8例,年齡 (64±11)歲,HYHAⅡ級組24例,男14例,女10例,年齡 (63±11)歲,包括運動鍛煉 (組)患者12例,男7例,女5例;Ⅲ級組29例,男17例,女12例,年齡 (64±13)歲,包括運動鍛煉 (組)患者17例,男9例,女8例;Ⅳ級組23例,男14例,女9例,年齡 (65±12)歲,包括運動鍛煉 (組)患者12例,男7例,女5例。每一組的兩亞組之間性別比例、年齡相近,具有可比性 (均P>0.05);心衰各組、對照組患者之間的性別比例、年齡相近,具有可比性 (均P>0.05)。
1.2 研究方法
1.2.1 治療方案 所有慢性心力衰竭患者入院后均給予常規藥物治療如血管緊張素轉換酶抑制劑、地高辛,無禁忌證者應用β-受體阻滯劑,并根據病情適當選擇應用利尿劑和硝酸酯類藥物,病情嚴重者給予低流量吸氧。運動訓練組則在上述治療的基礎上按照指定的方法〔1〕進行運動訓練。
1.2.2 標本的采集與保存 入院后24 h內進行外周血的抽取,常規分離血清及血漿標本放入-70℃冰箱保存;8 w后返回再次進行外周血的抽取和保存,集中檢測血清NOS、MDA和血漿vWF因子、ET、AngⅡ水平。
1.2.3 試劑 NOS、MDA試劑盒由南京建成生物工程研究所提供;vWF因子試劑盒由上海太陽生物技術公司提供;ET、AngⅡ試劑盒由北京北方生物技術研究所提供。
1.3 統計學處理 應用SPSS10.0統計軟件進行統計學分析,數據以±s表示,計量資料比較用單因素方差分析;各組治療前后的比較及各亞組之間參數的比較用非配對t檢驗。
2 結果
2.1 治療前不同心功能分級的心衰患者各組之間比較 各組心衰患者的血漿ET、AngⅡ、vWF因子和血清MDA、tNOS、iNOS濃度隨心衰程度加重而上升,且各組之間的差別均有統計學意義(P<0.05);血清 cNOS隨心衰程度加重而降低,cNOS在NYHAⅢ級與NYHAⅣ級組之間差別無統計學意義(P>0.05),其余各組之間比較差別有統計學意義(P<0.05)。見表1。
2.2 常規治療組與常規治療+運動鍛煉組間的比較 兩種治療方案均可使血漿 ET、AngⅡ、vWF因子和血清 MDA、tNOS、iNOS濃度下降,而血清cNOS濃度上升,但常規治療+運動鍛煉組這種改變更明顯(P<0.05)。見表2~表4。
表1 治療前不同心功能心衰患者ET、AngⅡ、vWF因子、NOS亞型濃度的改變(±s)

表1 治療前不同心功能心衰患者ET、AngⅡ、vWF因子、NOS亞型濃度的改變(±s)
與對照組比較:1)P<0.05;與NYHAⅡ級比較:2)P<0.05;與NYHAⅢ級比較:3)P<0.05
?
表2 心衰患者不同療法ET,AngⅡ濃度比較(±s)

表2 心衰患者不同療法ET,AngⅡ濃度比較(±s)
與相同心功能級別常規組比較:1)P<0.05,下表同
?
表3 心衰患者不同療法vWF因子、tNOS濃度比較(±s)
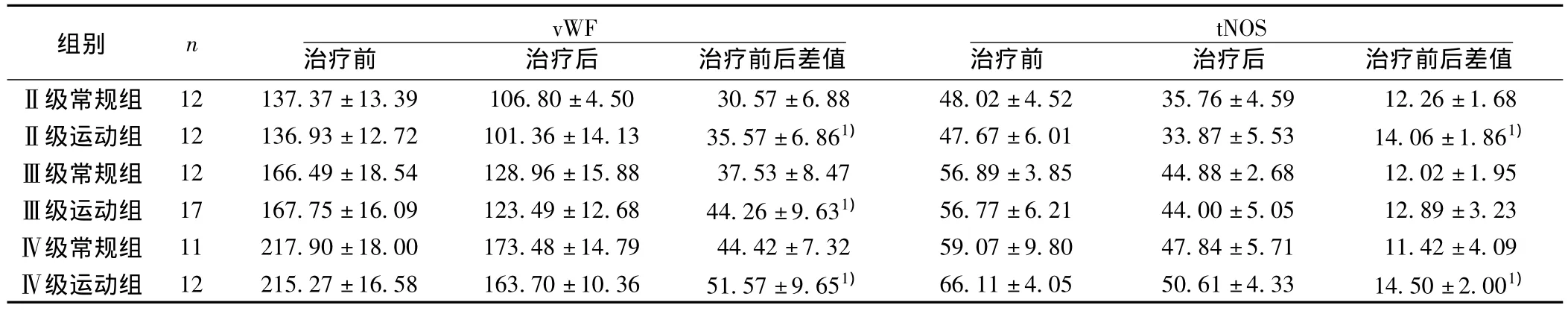
表3 心衰患者不同療法vWF因子、tNOS濃度比較(±s)
?
表4 心衰患者不同療法iNOS、cNOS濃度比較(±s)
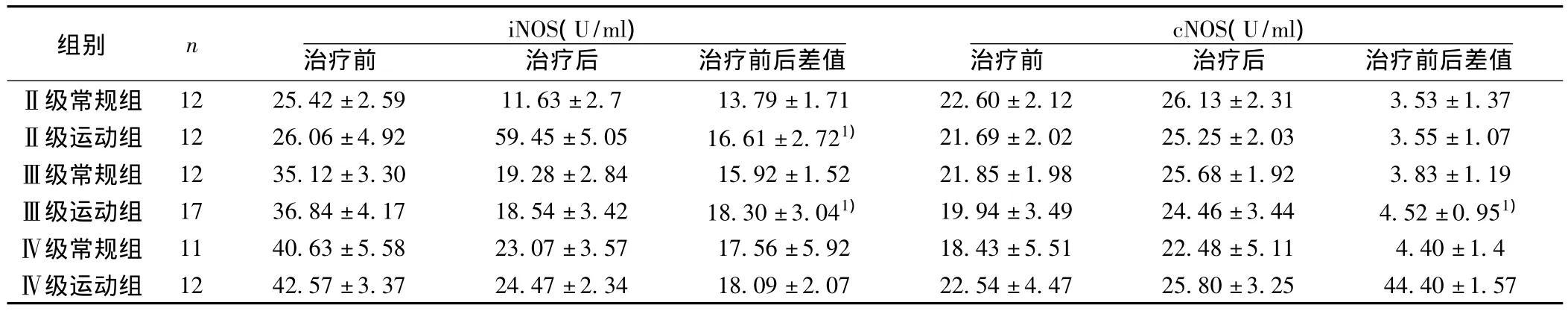
表4 心衰患者不同療法iNOS、cNOS濃度比較(±s)
?
3 討論
既往研究認為心衰患者進行運動可增加心肌的耗氧量,使血流動力學狀態惡化,故特別強調休息對心衰患者的必要性〔2〕。
近年來研究發現CHF患者的運動耐受能力不僅與心臟功能有關,而且與外周血管內皮功能的改變有非常密切的關系〔3〕:慢性心衰患者應用血管緊張素轉換酶抑制劑后,患者的心臟功能可明顯改善,但運動能力的改善要明顯滯后〔4〕;嚴重慢性心力衰竭患者進行心臟移植術后,即使心臟功能已基本恢復,運動能力仍需一段時間的訓練才能逐漸恢復〔4〕,這都提示慢性心力衰竭患者的運動能力不僅僅與心臟功能有關,外周內皮功能改變可能參與運動能力的改變〔5,6〕,因此提出心衰患者應該在藥物治療的基礎上盡可能地進行適量的運動,以改善患者的生存質量。
心力衰竭時,組織器官缺血缺氧、細胞內酸中毒、兒茶酚胺分泌增加等可損傷血管內皮細胞的結構、功能,造成血管舒張/收縮異常,動脈阻力增加,加重心臟功能受損,兩者互為因果,在心衰的發展過程中發揮重要作用〔7,8〕。
ET、AngⅡ是內皮細胞合成、分泌的血管收縮因子,心衰時水平增加;NOS有三種亞型:iNOS、eNOS、nNOS。生理情況下機體只持續、小量表達eNOS、nNOS,對維持心血管系統正常的生理功能起著重要作用,iNOS主要在病理條件下表達,有細胞毒性,與含鐵酶結合導致線粒體呼吸作用和細胞功能的損害,對心臟起著負性作用〔8〕。vWF因子是由內皮細胞合成的,介導血小板與內皮下膠原的黏附反應以及高切應力下的血小板之間的聚集反應,促進血小板的黏附與聚集。而且只有當內皮細胞受到損傷后才釋放到血液中,是目前研究內皮功能中最有價值的指標〔9,10〕。
在防治血管內皮功能不全的措施中,運動療法由于方法簡單、安全而在慢性心衰患者的康復治療中受到重視。運動鍛煉本身對心臟收縮力無影響,但可逆轉異常的骨骼肌結構與生化改變、改善血管內皮功能,從而適應機體對血流量和氧需求的增加〔11,12〕。
Yi等應用快速起搏制作犬心衰模型并分為:單純起搏組、起搏加每日運動(起搏器關閉)組和起搏加每日運動(起搏器打開)組,觀察冠狀動脈對花生四烯酸的擴張反應。結果表明,每日運動組僅有輕度心衰,無論起搏器是否關閉,冠狀動脈對花生四烯酸的擴張反應起搏前后無明顯改變;與此相反,單純起搏組心衰程度較重,冠狀動脈對花生四烯酸的擴張反應遲鈍〔13〕,產生這種結果的機制尚不十分明了。因為花生四烯酸是由內皮細胞的環氧化酶轉化成具有血管擴張作用的前列腺素類物質而發揮血管擴張作用,因此有人推斷,運動訓練使血管擴張能力改善主要是由于內皮功能的改善。
本文研究結果顯示,慢性心衰時ET、AngⅡ、vWF因子、tNOS、iNOS、MDA水平上升,而cNOS水平下降,并且這種改變的程度與心功能下降的程度有關,心功能越差,改變越明顯;其中ET、AngⅡ、vWF因子、tNOS、iNOS水平在不同心功能患者間的差別非常顯著,而cNOS雖然在心衰各組與對照組之間的差別顯著,但在NYHAⅢ級與NYHAⅣ級患者之間差異無顯著性,提示心衰時NOS的改變主要在iNOS,iNOS的增加在心衰的發展變化中發揮重要作用;治療后這種改變減輕,且運動鍛煉組這種改變更明顯,提示運動鍛煉對心衰時內皮功能改變的有益影響。
從慢性心力衰竭患者的病理生理學改變可以推斷,循環衰竭越嚴重,越能從運動訓練中獲益。截至目前,大多數研究均在病情穩定的心衰患者中進行,不包括NYHAⅣ級的心力衰竭患者。在本文進行的研究中,我們讓NYHAⅣ級心衰患者進行被動性肢體及呼吸肌的運動訓練,結果發現他們也能從這種治療中獲益。
1 Sharma R,Davidoff MN.Oxidative stress and endothelial dysfunction in heart failure〔J〕.Congest Heart Fail,2002;8(3):165-72.
2 Drexler H,Coats AJ.Explaining fatigue in congestive heart failure〔J〕.Annu Rev Med,1996;47(2):241-56.
3 Stamatis Adamopoulos,Parissis JT,Kremastinos DT.Endothelial dysfunction in chronic heart failure:clinical and therapeutic implications〔J〕.Eur J Intern Med,2002;13(4):233-9.
4 Alain Cohen-Solal,Chabnam Guiti,Christophe Geyer,et al.Exercise training in chronic heart failure:why〔J〕?Heart Fail Rev,1999;3(4):287-97.
5 Linke A,Schoene N,Gielen S,et al.Endothelial dysfunction in patients with chronic heart failure:systemic effects of lower-limb exercise training〔J〕.J Am Coll Cardiol,2001;37(2):392-7.
6 Hambrecht R,Fiehn E,Weigl C,et al.Regular physical exercise corrects endothelial dysfunction and improves exercise capacity in patients with chronic heart failure〔J〕.Circulation,1998;98(24):2709-15.
7 Bank AJ,Lee PC,Kubo SH.Endothelial dysfunction in patients with heart failure:relationship to disease severity〔J〕.J Card Fail,2000;6(1):29-36.
8 Linke A,Recchia F,Zhang X,et al.Acute and chronic endothelial dysfunction:implications for the development of heart failure〔J〕.Heart Fail Rev,2003;8(1):87-97.
9 Sabelis LW,Senden PJ,Fijnheer R,et al.Endothelial markers in chronic heart failure:training normalizes exercise-induced vWF release〔J〕.Eur J Clin Invest,2004;34(9):583-9.
10 Lip GYH,Blann A.Willebrand factor:a marker of endothelial dysfunction in vascular disorders〔J〕?Cardiovasc Res,1997;34(2):225.
11 Gielen S,Erbs S,Schuler G,et al.Exercise training and endothelial dysfunction in coronary artery disease and chronic heart failure.From molecular biology to clinical benefits〔J〕.Minerva Cardioangiol,2002;50(2):95-106.
12 Wisl?ff U,St?ylen A,Loennechen JP,et al.Superior cardiovascular effect of aerobic interval training versus moderate continuous training in heart failure patients:a randomized study〔J〕.Circulation,2007;115(6):3086-94.
13 Yi GH,Zwas D,Wang J.Chronic exercise training preserves prostaglandin-induced dilation of epicardial coronary artery during development of heart failure in awake dogs〔J〕.Prostaglandins Other Lipid Mediat,2000;60(1):137-51.

