轉爐釩渣氧壓酸浸過程V-Fe-H2O系的電位—pH圖
張廷安, 牟望重, 豆志河, 呂國志, 劉 燕
(東北大學 材料與冶金學院 多金屬共生礦生態化利用教育部重點實驗室,沈陽 110819)
釩是一種具有戰略價值的金屬元素,因具有較高的強度、硬度、較優的耐腐蝕性能而被廣泛地應用于各類合金中。世界上已經探明的釩資源儲量中有98%共生于釩鈦磁鐵礦中。我國是釩資源大國,儲量居世界第4位,僅次于南非、俄羅斯、美國。其中,四川攀枝花地區的釩鈦磁鐵礦儲量近100億t,占世界儲量的11%。釩鈦磁鐵礦在冶煉過程中含釩鐵水吹煉產生的轉爐渣中釩含量為3%~15%,是目前世界上提釩的主要原料[1?2]。
目前,從含釩原料中提釩的方法主要有鈉鹽焙燒?酸 浸[3]/水浸[4]法、空白焙燒?堿浸[5]/酸浸[6]法、鈣鹽焙燒?酸浸[7]/堿浸[8]法及氧化焙燒?酸浸法[9]等。其中,鈉鹽焙燒效果較好,對原料的適應性較強,近年來得到了廣泛的應用。該工藝的主要問題在于焙燒煙氣中含有Cl2及HCl等有害氣體,嚴重污染大氣環境;同時,釩的回收率有待進一步提高[10]。與傳統工藝相比,氧壓酸浸技術取消了焙燒工藝段,縮短了工藝流程,減少了物料用量,避免了焙燒過程中有害氣體的排放,提高了釩的綜合利用率,是一種低碳環保型綠色冶金新工藝。
電位—pH圖是研究濕法冶金過程重要的熱力學依據。目前,對于 V?H2O體系的研究僅限于常溫、常壓條件(25 ℃、0.1 MPa)[11];雖有學者在150 ℃下對Fe?H2O體系進行了研究,但其研究對象為硫化礦的FeS?H2O體系[12?14];而目前對于轉爐釩渣氧壓酸浸過程V-Fe-H2O系電位—pH圖的研究未見報道。為此,本文作者繪制了氧分壓為 0.5 MPa及不同溫度(60、100、150、200℃)下V-H2O 系、Fe-H2O 系、V-Fe-H2O系的電位—pH圖,為轉爐釩渣的氧壓酸浸過程提供了熱力學依據,并以此為基礎進行了氧壓酸浸實驗,對理論計算結果進行了驗證。
1 熱力學計算
1.1 高溫電位—pH圖的計算方法
濕法冶金過程中物質在水溶液中發生的基本反應可用式(1)表示。

式中:Ab和 Ba分別為氧壓酸浸過程中特定種類的釩和鐵化合物。
根據反應有無電子參加,高溫條件下氧化還原反應體系的φT及溶解?沉淀反應體系(無電子參加,z=0)的pHT的計算公式如式(2)和(3)所示[15]。
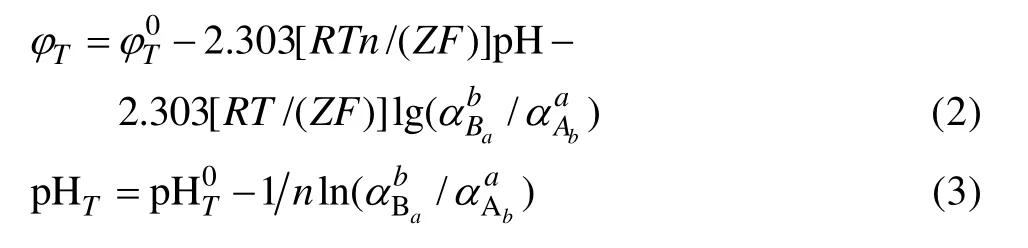


式中:αT和βT為給定溫度下的常數,只與選擇的標準態、溶劑、溫度以及離子類型有關,而與個別離子性質無關。表1所列為60~200 ℃下4種離子類型的αT和 βT[16]。
電解質的平均活度因子隨溫度而變,根據文獻[17]報道,采用Debye–Hückel方程式計算溫度高于25 ℃水溶液中各離子的平均活度因子。
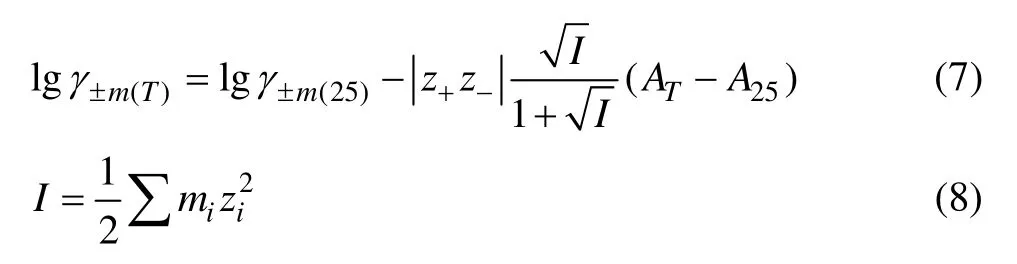
式中:γ±為溶液中電解質的平均活度因子(以摩爾濃度計算);I為水溶液的離子強度;z+為正離子的電荷數;z-為負離子的電荷數;AT為常數,其值隨溫度的變化而變化,如表2所列。
本文作者采用戴維斯公式計算 25 ℃水溶液中電解質的活度因子:
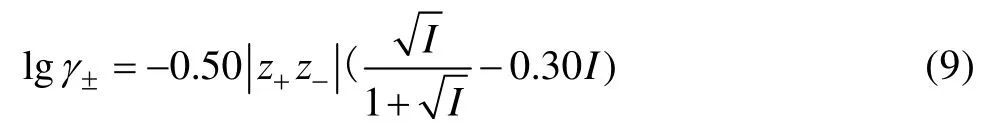
據文獻[10]報道,式(9)的平均誤差約為1.6%,是目前較為精確的計算方法。
1.2 高溫下V-H2O系的電位—pH圖
根據文獻[11?12,18?19]中的熱力學數據,采用式(4)和(5)的計算方法,分別得到了溫度為 25、60、100、150和200 ℃,氧分壓為0.5 MPa,V-H2O系中各反應的φ0值及pH0值,結果如表3和4所列。根據式(7)和(9)的活度因子計算方法,代入表2中的AT值,得到不同溫度下V-H2O系各物質的活度因子,如表5所列。 取V-H2O系中各離子的質量濃度為0.1 mol/kg,得到各物質在不同溫度下的活度。

表1 60~200 ℃時4種離子類型的αT和βT值[16]Table 1 Values of αT and βT for calculating four kinds of ions at 60~200 ℃[16]

表2 不同溫度下的AT值Table 2 AT values at different temperatures from 25 ℃ to 300 ℃
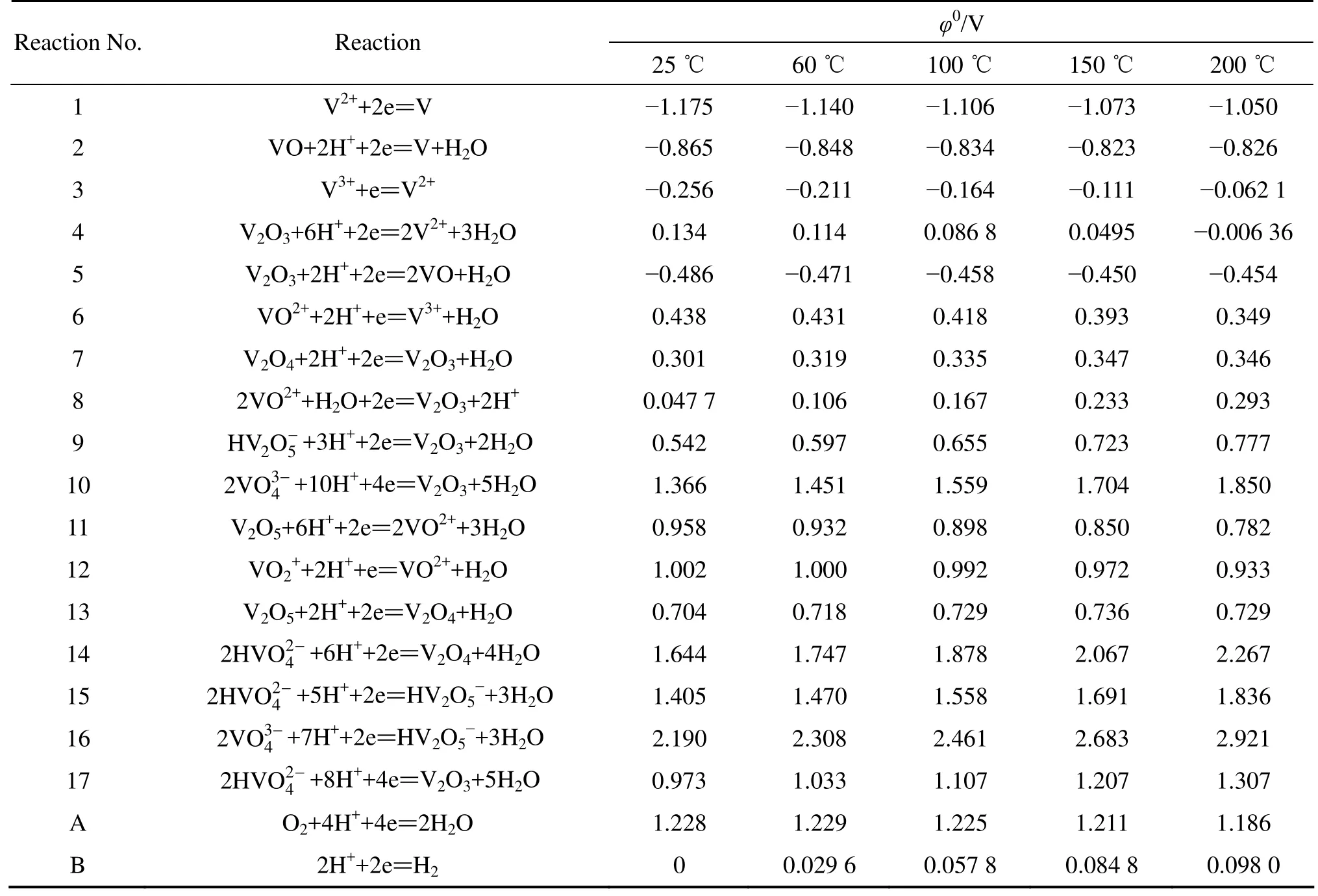
表3 V-H2O系各反應在不同溫度下的φ0值Table 3 φ0 values of various reactions in V-H2O system at different temperatures
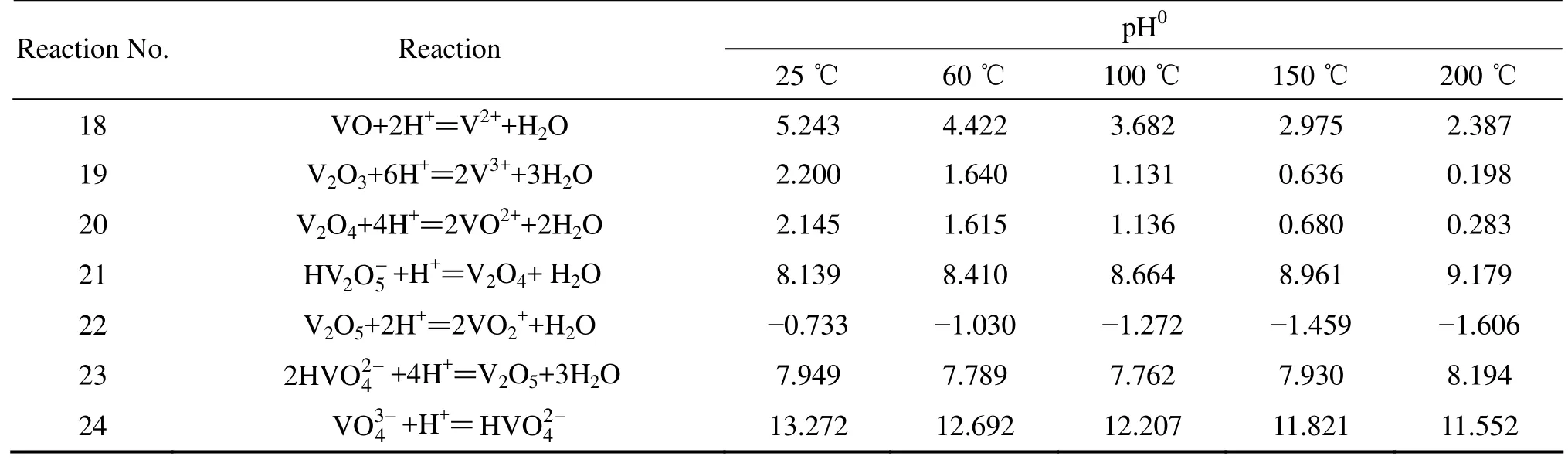
表4 V-H2O系各反應在不同溫度下的pH0值Table 4 pH0 values of various reactions in V-H2O system at different temperatures
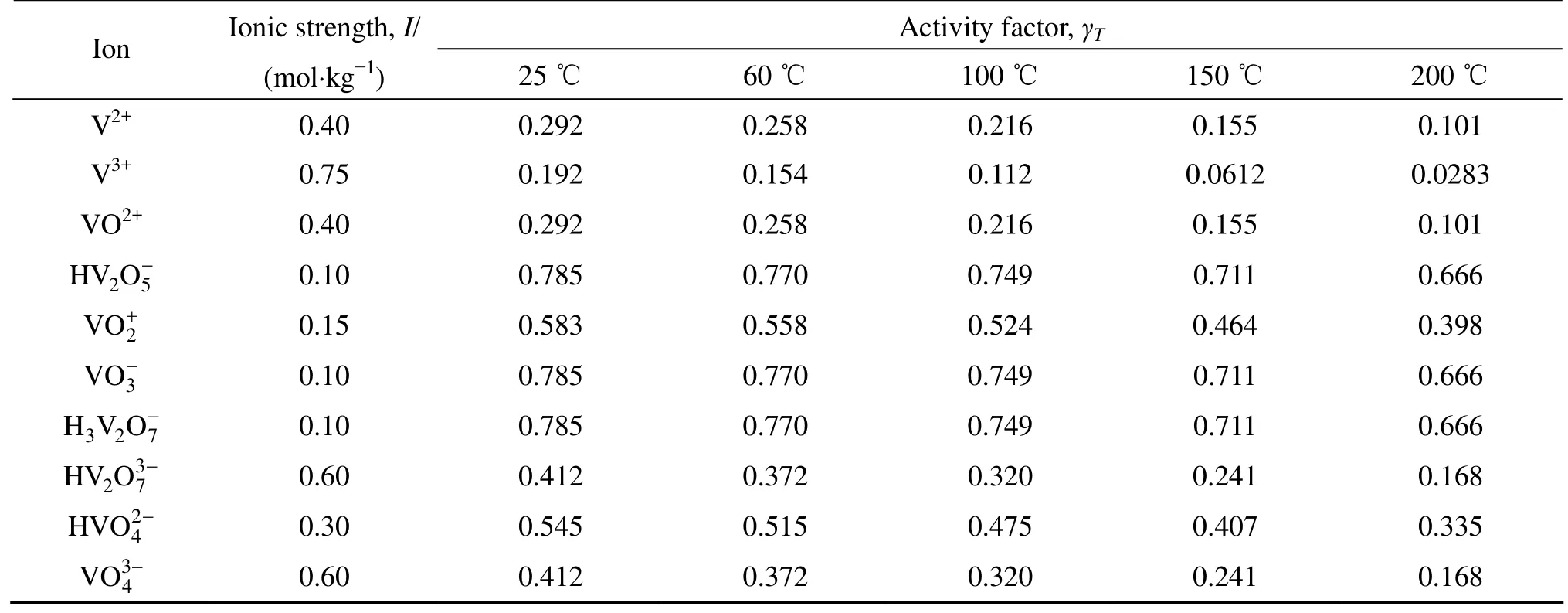
表5 V-H2O系各物質在不同溫度下的活度因子Table 5 Activity factors for substances in V?H2O system at different temperatures
根據V-H2O系中各反應的不同類型,分別采用式(2)和(3)計算各反應的φ或pH表達式并繪圖,即可得到氧分壓為0.5 MPa、溫度分別為60、100、150和200℃ V-H2O系的φ—pH圖(見圖1)。
由圖1可知,在水的穩定區范圍內,釩主要以固體氧化物的形式存在,但在pH<2的酸性條件下,有V3+、VO2+和VO2+3種水溶性離子存在;在pH>8的堿性條件下,有 H VO、H V2O和VO等離子存在,這些穩定區的存在從熱力學角度驗證了采用酸浸或堿浸工藝從轉爐釩渣中提釩的可行性。
針對轉爐釩渣的氧壓酸浸工藝進行熱力學研究,主要考察在pH<2的酸性條件下可溶性釩離子穩定區的變化情況。由表3可知,隨著溫度由60 ℃升高到200 ℃, 構成 V3+穩定區的反應(3)對應的 φ0值由?0.211 V提高到?0.062 1 V;構成V3+、VO2+和VO2+穩定區的反應(19)、(20)和(22)對應的 pH0值分別由1.640、1.615和?1.030降低至0.198、0.283和 ?1.606。由此可知,隨著反應溫度的升高,釩的浸出反應在酸性條件下所需要達到的標準氧化還原電位逐漸升高,所需酸濃度逐漸增大,從熱力學角度對釩的浸出是不利的。但由于φ0及pH0值變化不大,并不影響渣中釩在酸性條件下能夠被充分浸出的熱力學結果;同時,對于在密閉體系下進行的氧壓浸出反應,為了強化浸出過程,必須提高浸出溫度來加快反應速度并活化反應的動力學因素。因此,實際浸出過程選擇的溫度不宜過低[20]。
1.3 高溫下Fe-H2O系的電位—pH圖
不同溫度下 Fe-H2O系 φ—pH圖的繪制方法與V-H2O 的一致,根據文獻[11?12,18?19]中的熱力學數據,得到Fe-H2O系各反應在不同溫度條件下的φ0及pH0,結果分別如表6和7所列,各物質的活度因子如表8所列。取Fe-H2O水溶液中各離子濃度為0.1 mol/kg,經過計算得到氧分壓為0.5 MPa,溫度分別為60、100、150和200 ℃時Fe-H2O系的φ—pH圖(見圖2)。
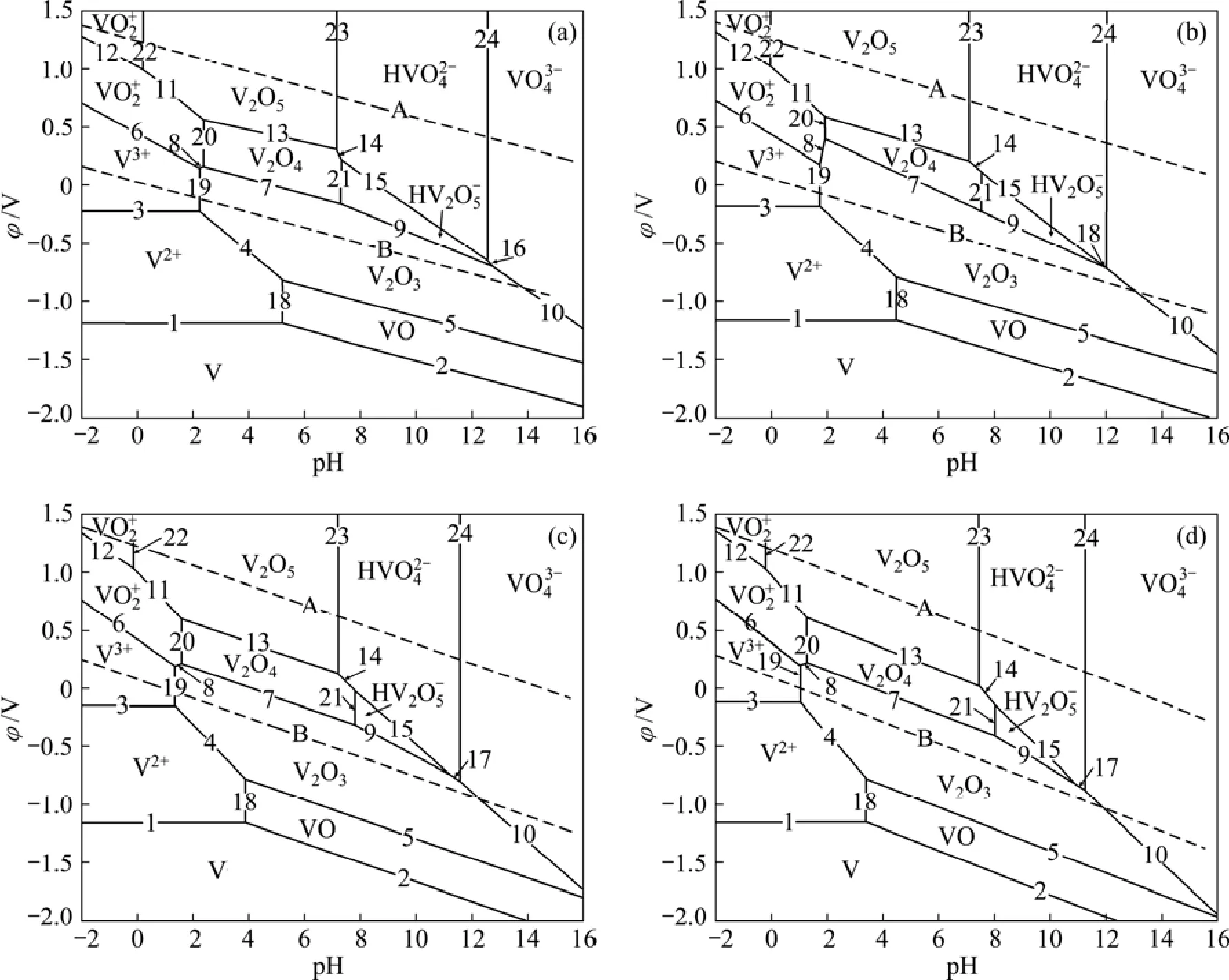
圖1 不同溫度下氧分壓為0.5 MPa時V-H2O系的φ—pH圖Fig.1 φ—pH diagrams of V-H2O system at oxygen partial pressure of 0.5 MPa and different temperatures: (a)60 ℃; (b)100 ℃;(c)150 ℃; (d)200 ℃
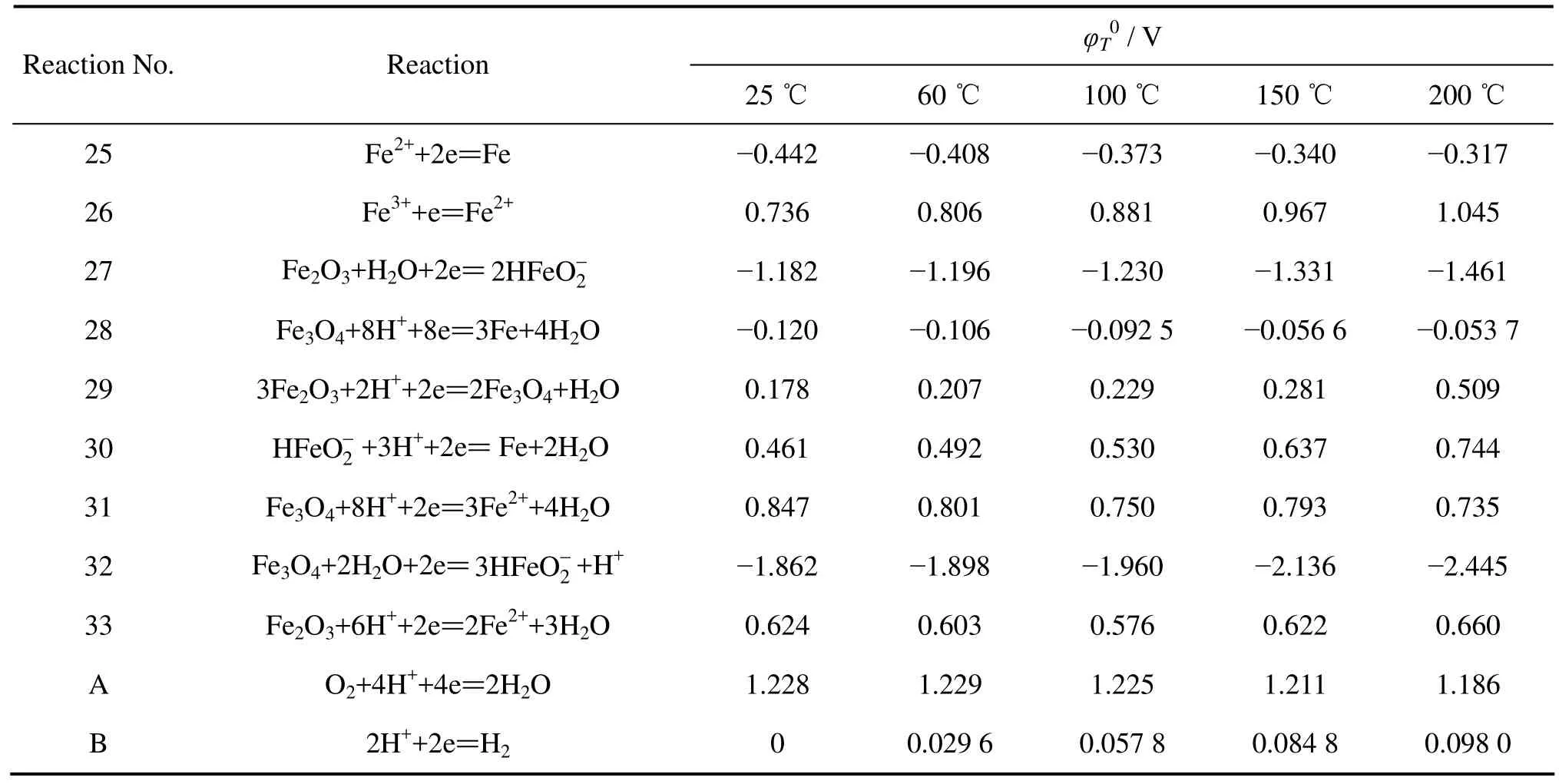
表6 Fe-H2O系各反應在不同溫度下的φ0值Table 6 φ0 values of various reactions in Fe-H2O system at different temperatures
由圖2可知,在水的穩定區范圍內,鐵除一部分以 Fe2O3及 Fe3O4等固體氧化物的形式存在外,其余均呈可溶性離子狀態。在pH<2的酸性條件下,以Fe2+和 Fe3+的形態存在;在 pH>14的堿性條件下,以HFeO2?的形式存在。當氧化還原電位較低時,出現鐵的鈍化區。由此可知,在氧壓酸浸條件下,釩渣中的鐵以Fe2+及Fe3+的形態存在于浸出液中。由于釩渣是由含釩鐵水在轉爐中通過氧氣吹煉而形成,氧化條件充分,因此,渣中主要以鐵的氧化物形式存在,而浸出液中一部分Fe3+的存在提高了浸出體系的氧化還原電位。
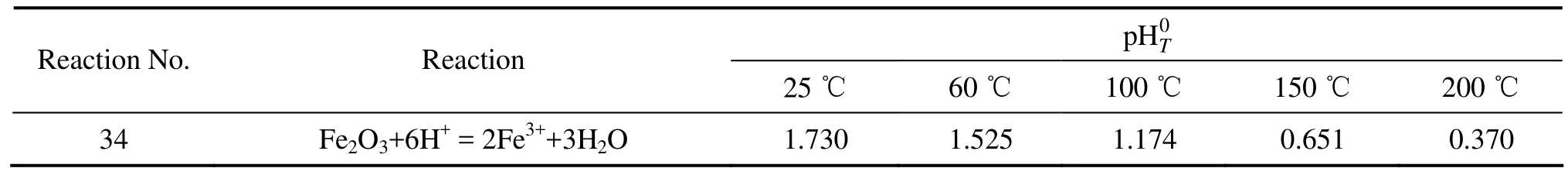
表7 Fe-H2O系各反應在不同溫度下的pH0值Table 7 pH0 values of various reactions in Fe-H2O system at different temperatures
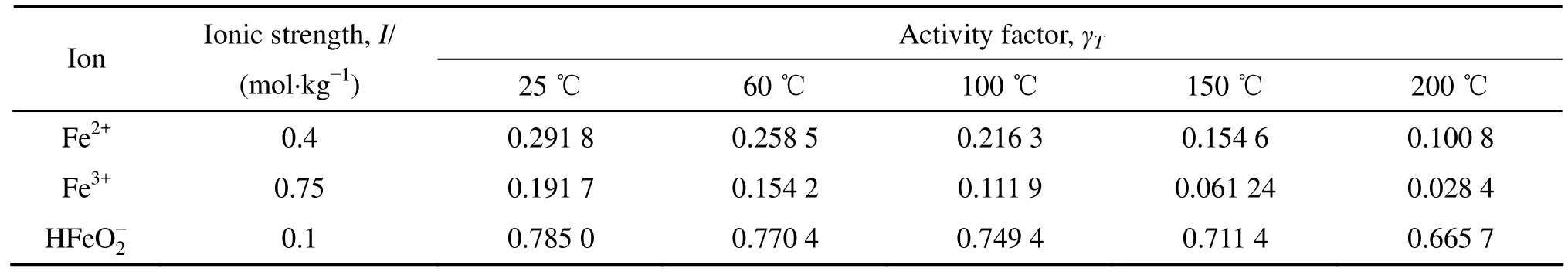
表8 Fe-H2O系各物質在不同溫度下的活度因子Table 8 Activity factors for substances of Fe-H2O system at different temperatures
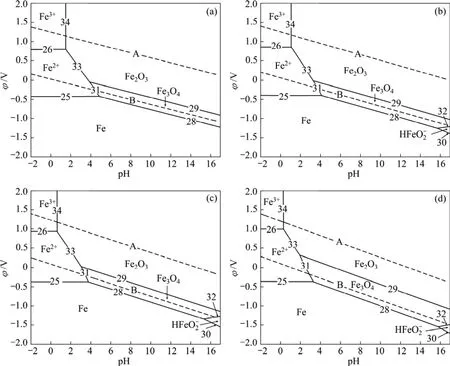
圖2 高溫下氧分壓為0.5 MPa時Fe-H2O系的φ—pH圖Fig.2 φ—pH diagrams of Fe-H2O system at high temperatures and oxygen partial pressure of 0.5 MPa: (a)60; (b)100 ℃; (c)150℃; (d)200 ℃
由表6和7可知,隨著溫度由60 ℃提高到200 ℃,構成Fe3+穩定區的φ0值由0.806 V提高到1.045 V,pH0值由1.525降低到0.370;Fe2+的φ0值由?0.408 V提高到?0.317 V。可見,隨著溫度的提高,Fe2+和Fe3+的浸出需要浸出體系具有更高的氧化還原電位以及更高的酸濃度。從熱力學角度考慮,溫度的提高抑制了低溫、低酸條件下鐵的浸出,根據從轉爐渣中提釩時應盡可能減少進入浸出液雜質的原則,提高溫度是有利的;但從動力學角度考慮,提高溫度將加快反應的浸出速率,促進鐵氧化物的溶解,反而不利于除雜過程。因此,需要進行轉爐渣的氧壓酸浸實驗,以確定合適的浸出溫度。
1.4 高溫下V-Fe-H2O系的φ—pH圖
轉爐釩渣通過鐵水吹煉產生,釩和鐵主要以尖晶石的形式共存于渣中。根據圖1和2及文獻[11?12,18?19]中的熱力學數據,得到V-Fe-H2O系各反應在不同溫度下的φ0及pH0值,結果分別如表9和10所列。根據表5和8中各物質的活度因子,取V-Fe-H2O系水溶液中各離子濃度為 0.1 mol/kg,經過計算得到氧分壓為0.5 MPa,溫度分別為 60、100、150和200 ℃時V-Fe-H2O系的φ—pH圖(見圖3)。
由圖3可知,釩鐵尖晶石(FeO·V2O3)的穩定區幾乎全部包含在水的穩定區范圍內,且不隨溫度變化而改變。在氧壓酸浸工藝的酸性條件下,可溶性 V3+、VO2+和VO2+的穩定區全部包含在Fe3+和Fe2+的穩定區范圍內,表明轉爐釩渣的氧壓酸浸工藝在浸出可溶性釩離子的同時,伴隨著Fe3+和Fe2+的浸出。從熱力學的分析可知,試圖通過改變溫度及酸濃度等因素控制氧化還原電位,在保證釩充分浸出的同時鐵不浸出而使鐵與釩分離是不可行的,浸出液還需要進行凈化除雜以生產高純度的釩制品。
由圖1~3可知,隨著溫度的提高,可溶性釩、鐵離子的穩定區對應的氧化還原電位逐漸增大,pH值逐漸降低。熱力學分析表明,提高溫度對于有價元素釩以及雜質鐵的浸出都是不利的;同時綜合考慮溫度對反應速率等動力學因素的影響,還需要進行氧壓酸浸實驗來驗證熱力學計算結果的準確性。
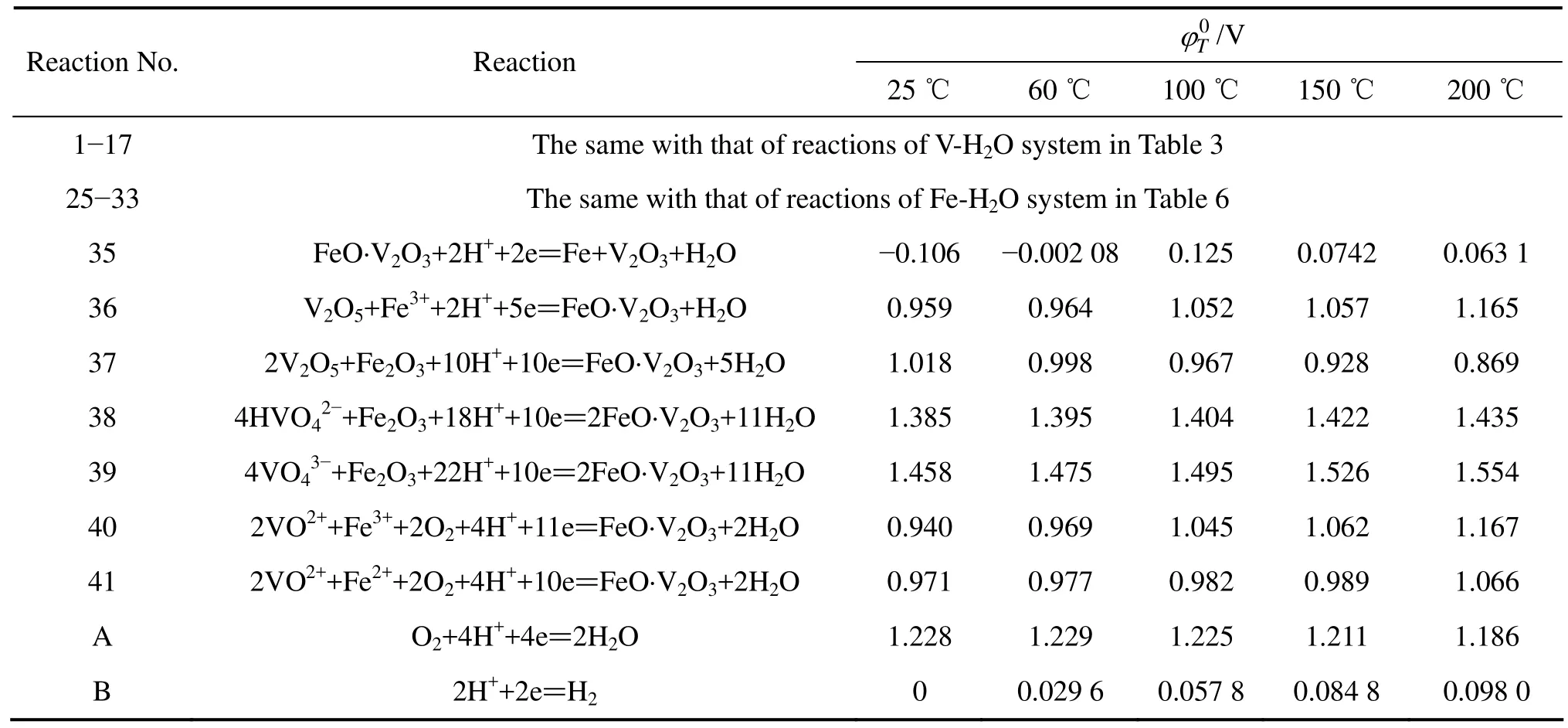
表9 V-Fe-H2O系各反應在不同溫度下的φ0值Table 9 φ0 values of various reactions in V-Fe-H2O system at different temperatures

表10 V-Fe-H2O系各反應在不同溫度下的pH0值Table 10 pH0 values of various reactions in V-Fe-H2O system at different temperatures

圖3 不同溫度下氧分壓為0.5 MPa時V-Fe-H2O系的φ—pH圖Fig.3 φ—pH diagrams of V-Fe-H2O system at oxygen partial pressure of 0.5 MPa and different temperatures: (a)60 ℃; (b)100 ℃;(c)150 ℃; (d)200 ℃
2 實驗
2.1 原料
實驗用轉爐釩渣取自四川攀枝花地區,其主要化學成分見表11。釩渣的XRD譜如圖4所示。實驗用浸出劑由98%的化學純濃硫酸稀釋至一定濃度范圍,氣體為工業瓶裝純氧。

表11 轉爐渣的化學成分Table 11 Chemical composition of converter slags (mass fraction, %)
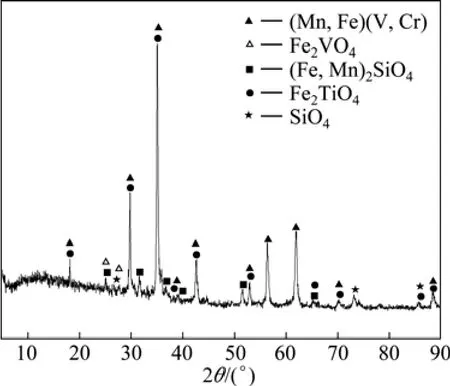
圖4 轉爐渣的XRD譜Fig.4 XRD pattern of converter slags
由圖4及表11可知,轉爐釩渣中主要成分為含鉻、錳的釩鐵尖晶石相,還包括鐵橄欖石相、鈦鐵尖晶石相和石英相等,成分復雜。
2.2 實驗儀器及方法
實驗裝置主要包括KCFD2?10型永磁旋轉攪拌加壓反應釜、Pulverisette5行星式高能球磨機、2XZ?1型旋片式真空泵及ZK?82B型真空干燥箱。
將轉爐渣與一定濃度的硫酸溶液按所設定的液固比調漿后置入加壓反應釜內,檢查氣密性后開始通氧、攪拌、加熱。浸出結束后,采用真空抽濾泵對浸出礦漿進行液固分離,量取濾液體積并稱取濾渣質量。取樣分析,釩、鐵浸出率通過浸出液及浸出渣的計算方法如下:

式中:ηi為釩、鐵的浸出率(i=V, Fe),%;m0為原礦加入質量,g;wi為原礦中釩、鐵的質量分數,%;ci為浸出液中釩、鐵離子的濃度,g/L;V為浸出液體積,L;w′i為浸出渣中釩、鐵的質量分數,%;m為浸出渣質量,g。
2.3 檢測方法
使用美國Leeman公司制造的Prodigy XP型全譜直讀等離子光譜儀(ICP)對浸出液中的釩、鐵離子濃度進行檢測;使用日本理學3070e型X熒光光譜儀對浸出渣中釩、鐵元素含量進行表征。
3 結果與討論
在氧分壓0.5 MPa、粒度范圍0.055~0.075 mm、液固比15:1、浸出時間120 min、攪拌速度500 r/min、初酸濃度200 g/L的條件下,溫度對轉爐釩渣浸出率的影響如圖5所示。由圖5可知,隨著溫度由60 ℃升高到140 ℃,釩的浸出率由65.48%提高到96.87%;當溫度繼續升高到180 ℃時,釩的浸出率為97.07%,趨于穩定。鐵的浸出率在60 ℃為77.32%,在120 ℃增加到88.33%;隨著溫度繼續提高到180 ℃,鐵的浸出率略有提高,增加到91.56%。
由不同溫度下釩、鐵浸出率的變化趨勢可知,轉爐釩渣的氧壓酸浸過程主要由反應動力學因素控制,提高溫度能強化反應動力學過程,提高反應速率,縮短固液反應時間[20],進而增大釩、鐵的浸出率。由圖4可知,轉爐渣中存在著鐵橄欖石等難溶相,是造成鐵浸出率略低于釩浸出率的主要原因。氧壓酸浸的目的在于提釩的同時,使其他元素盡可能少的進入浸出液。實驗結果表明,在釩充分浸出的同時,鐵的浸出率也在90%左右。溫度繼續升高至140 ℃以上,釩的浸出率趨于穩定而鐵的浸出率略有提高。因此,浸出溫度不宜超過140 ℃,實驗結果與φ—pH圖計算結果相符合。
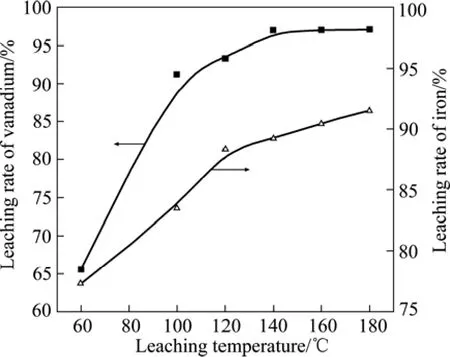
圖5 浸出溫度對釩、鐵浸出率的影響Fig.5 Effect of leaching temperature on leaching rate of vanadium and iron
4 結論
1) 由不同溫度下V-H2O系的φ—pH圖可知,在水的穩定區范圍內,在pH<2的酸性條件下,釩主要以V3+、VO2+和 V O3種水溶性離子形態存在,為轉爐渣采用氧壓酸浸工藝提取釩提供了熱力學條件。
2) 由不同溫度下Fe?H2O系的φ—pH圖可知,在水的穩定區范圍內,在pH<2的酸性條件下,鐵主要以Fe2+和Fe3+形態存在。熱力學分析表明,隨著氧壓酸浸工藝的進行,轉爐渣中的鐵氧化物將以可溶性鐵離子形式進入浸出液。
3) 由不同溫度下V-Fe-H2O系的φ—pH圖可知,在pH<2的酸性條件下,V3+、VO2+和 V O的穩定區一直位于Fe3+和Fe2+的穩定區范圍內。隨著溫度由60℃提高到200 ℃,可溶性釩、鐵離子穩定共存區的pH值逐漸降低,氧化還原電位逐漸提高。熱力學分析表明,采用氧壓酸浸工藝能將轉爐渣中的釩充分浸出,但不能通過一步浸出在提釩的同時將釩、鐵分離,生產釩制品時浸出液需要進行進一步凈化。
4) 由不同溫度下轉爐釩渣的氧壓酸浸實驗結果可知,在溫度 140 ℃、氧分壓 0.5 MPa、粒度0.055~0.075 mm、液固比15:1、浸出時間120 min、攪拌速度500 r/min、初酸濃度200 g/L的條件下,釩的浸出率為 96.87%,鐵的浸出率為 89.25%,實驗結果與熱力學計算結果相符合。
[1]MOSKALYK R R, ALFANTAZI A M. Processing of vanadium:A review[J]. Minerals Engineering, 2003, 16: 793?805.
[2]NAVARRO R, GUZMAN J, SAUCEDO I, REVILLA J,GUIBAL E. Vanadium recovery from oil fly ash by leaching precipitation and solvent extraction processes[J]. Waste Management, 2006, 27: 425?438.
[3]SHELWIT H, ALIBRAHIM M. Extraction of sulfur and vanadium from petroleum coke by means of salt-roasting treatment[J]. Fuel, 2006, 85(6): 878?880.
[4]范必威, 林海玲. 方山口石煤提釩焙燒工藝研究[J]. 濕法冶金, 2001, 20(2): 79?83.FAN Bi-wei, LIN Hai-ling. Effects of roasting process on extraction of vanadium from stone coal at Fangshankou[J].Hydrometallurgy of China, 2001, 20(2): 79?83.
[5]譚愛華. 某石煤釩礦空白焙燒?堿浸提釩工藝研究[J]. 湖南有色金屬, 2008, 24(1): 24?27.TAN Ai-hua. Study on extracting V2O5by the roasting-alkaline leaching from vanadium-containing stone coal[J]. Hunan Nonferrous Metals, 2008, 24(1): 24?27.
[6]賓智勇. 釩礦石無鹽焙燒提取五氧化二釩試驗[J]. 鋼鐵釩鈦,2006, 27(1): 21?26.BIN Zhi-yong. Study on extraction of V2O5from vanadium ore by roasting and acid leaching process[J]. Iron Steel Vanadium Titanium, 2006, 27(1): 21?26.
[7]鄒曉勇, 彭清靜, 歐陽玉祝, 田仁國. 高硅低鈣釩礦的鈣化焙燒過程[J]. 過程工程學報, 2001, 1(2): 189?192.ZOU Xiao-yong, PENG Qing-jing, OUYANG Yu-zhu, TIAN Ren-guo. Research on the roasting process with calcium compounds for silica based vanadium ore [J]. The Chinese Journal of Process Engineering, 2001, 1(2): 189?192.
[8]王金超. 鈣對釩渣提釩的影響[J]. 四川有色金屬, 2004(4):27?29.WANG Jin-chao. Effect of calcium on leaching of vanadium from vanadium slag[J]. Sichuan Nonferrous Metals, 2004(4):27?29.
[9]馮其明, 何東升, 張國范, 歐樂明, 盧毅屏. 石煤提釩過程中釩氧化和轉化對釩浸出的影響[J]. 中國有色金屬學報, 2007,17(8): 1348?1352.FENG Qi-ming, HE Dong-sheng, ZHANG Guo-fan, OU Le-ming, LU Yi-ping. Effect of vanadium oxidation and conversion on vanadium leaching in extraction of vanadium from stone coal[J]. The Chinese Journal of Nonferrous Metals,2007, 17(8): 1348?1352.
[10]LI Min-ting, WEI Chang, FAN Gang, LI Cun-xiong, DENG Zhi-gan, LI Xing-bin. Pressure acid leaching of black shale for extraction of vanadium[J]. Transactions of Nonferrous Metals Society of China, 2010, 20(S1): 112?117.
[11]POST K, ROBINS R G. Thermodynamic diagrams for the vanadium-water system at 298.15 K[J]. Electrochimica Acta,1976, 21(6): 401?405.
[12]BRUCE G P, GRAHAM A W, ROY M S. Electrochemical phase diagrams for the Fe/S/H2O system under geothermal conditions[J]. Journal of Chemistry, 1985, 38(8): 643?657.
[13]王吉坤, 李存兄, 李 勇, 張紅耀, 黃 卉, 閻江峰, 劉 露, 魏昶. 高鐵閃鋅礦高壓酸浸過程中ZnS-FeS-H2O系的電位—pH圖[J]. 有色金屬: 冶煉部分, 2006(2): 2?5.WANG Ji-kun, LI Cun-xiong, LI Yong, ZHANG Hong-yao,HUANG Hui, YAN Jiang-feng, LIU Lu, WEI Chang. The E—pH diagram of ZnS-FeS-H2O system during acid leaching under high pressure of iron sphalerite[J]. Nonferrous Metals: Extractive Metallurgy, 2006(2): 2?5.
[14]牟望重, 張廷安, 呂國志, 古 巖, 豆志河. 硫化鋅加壓浸出過程的電位—pH圖[J]. 中國有色金屬學報, 2010, 20(8):1636?1644.MU Wang-zhong, ZHANG Ting-an, Lü Guo-zhi, GU Yan,DOU Zhi-he. φ—pH figure during oxidative pressure leaching of zinc sulfide[J]. The Chinese Journal of Nonferrous Metals, 2010,20(8): 1636?1644.
[15]鐘竹前, 梅光貴. 濕法冶金過程[M]. 長沙: 中南工業大學出版社, 1988: 1?10.ZHONG Zhu-qian, MEI Guang-gui. Hydrometallurgy process[M]. Changsha: Central South University of Technology Press, 1988: 1?10.
[16]田彥文, 翟秀靜, 劉奎仁. 冶金物理化學簡明教程[M]. 北京:化學工業出版社, 2007: 225?227.TIAN Yan-wen, ZHAI Xiu-jing, LIU Kui-ren. Short course of metallurgical physical chemistry[M]. Beijing: Chemical Industry Press, 2007: 225?227.
[17]黃子卿. 電解質溶液理論導論[M]. 北京: 科學出版社, 1983:83?87.HUANG Zi-qing. Introduction of electrolyte solutions theory[M].Beijing: Science Press, 1983: 83?87.
[18]楊顯萬. 高溫水溶液熱力學數據計算手冊[M]. 北京: 冶金工業出版社, 1983: 523?674.YANG Xian-wan. Handbook of thermodynamic data in aqueous solutions at high temperature[M]. Beijing: Metallurgical Industry Press, 1983: 523?674.
[19]伊赫桑·巴倫. 純物質熱化學數據手冊[M]. 程乃良, 牛四通,徐桂英, 譯. 北京: 科學出版社, 2003: 716?726.BARIN I. Thermochemical data of pure substances[M]. CHENG Nai-liang, NIU Si-tong, XU Gui-ying, transl. Beijing: Science Press, 2003: 716?726.
[20]馬榮駿. 濕法冶金原理[M]. 北京: 冶金工業出版社, 2007:324.MA Rong-jun. Principle on hydrometallurgy[M]. Beijing:Metallurgical Industry Press, 2007: 324.

