Fenton氧化強(qiáng)化處理經(jīng)內(nèi)電解預(yù)處理的絡(luò)合銅廢水的研究
劉娉婷 蘭善紅 溫南興
(東莞理工學(xué)院 化學(xué)與環(huán)境工程學(xué)院,廣東東莞 523808)
隨著印制電路板行業(yè)的迅速發(fā)展,其生產(chǎn)廢水的處理也成為亟待解決的難題。其中以絡(luò)合銅廢水處理難度最大,無法直接采用傳統(tǒng)的生物和物化工藝對其進(jìn)行處理。內(nèi)電解是一種對印制電路板行業(yè)廢水有較好處理效果的方法,對絡(luò)合銅有較高的去除效率,然而內(nèi)電解出水COD仍較高,達(dá)不到排放要求[1-4]。有文獻(xiàn)[5]指出,采用Fenton高級氧化法直接處理絡(luò)合銅廢水,可以同時達(dá)到較好地破絡(luò)和顯著降COD的效果。但直接采用Fenton試劑進(jìn)行處理,雙氧水和亞鐵離子的消耗量大,處理成本高。
本研究采用Fenton氧化法處理內(nèi)電解法預(yù)處理絡(luò)合銅廢水的出水。內(nèi)電解可為Fenton氧化反應(yīng)提供亞鐵離子,減少Fenton反應(yīng)的投藥量;Fenton氧化法又可彌補(bǔ)內(nèi)電解的不足,較大程度降低COD,既經(jīng)濟(jì)又高效。
1 材料和方法
1.1 主要實(shí)驗(yàn)儀器和材料
試驗(yàn)用試劑:硫酸,鹽酸,硫酸汞,硫酸銀,重鉻酸鉀,鄰菲羅琳,硫酸亞鐵銨,鹽酸羥銨,乙酸,氫氧化鈉,乙酸鈉,乙醇,硫酸鋁鉀,鉬酸銨,以上試劑均為分析純;雙氧水 (50%),工業(yè)用鹽酸 (30%),鐵碳燒鑄填料 (鐵碳比3∶1),鐵粉,硝酸 (優(yōu)級純)。
儀器及設(shè)備:AA6000型原子吸收分光光度計,721/722可見分光光度計,雷磁精密型pH計,CH-02型臺式加熱器,壓差式BOD測定儀,WT603-K1/1000電子天平,內(nèi)電解+Fenton處理中試裝置。
1.2 實(shí)驗(yàn)方法
1.2.1 單因素實(shí)驗(yàn)方法
影響Fenton氧化反應(yīng)的因素有雙氧水投加量、亞鐵投加量、初始pH值、反應(yīng)時間和溫度等。Fenton氧化工藝在工業(yè)應(yīng)用中一般在常溫條件下運(yùn)行,因此本次單因素實(shí)驗(yàn)選取雙氧水投加量、亞鐵投加量、初始pH值和反應(yīng)時間四個因素進(jìn)行考察。
1)內(nèi)電解出水
將絡(luò)合銅廢水調(diào)節(jié)pH值后充滿中試裝置中內(nèi)電解流化床床體,投加適量的鐵炭復(fù)合填料 (約反應(yīng)器1/4高度,使用前用廢水浸泡24 h,確保活性炭吸附飽和)投加到內(nèi)電解流化床反應(yīng)器內(nèi),以間歇進(jìn)水的方式運(yùn)行反應(yīng)器獲得其30 min出水,測定其COD值以及Fe2+濃度。
2)H2O2/COD質(zhì)量比
分別取200 mL 1)中的水樣置于6個250 mL的錐形瓶中,保持反應(yīng)條件為:pH=3.0,F(xiàn)e2+/H2O2質(zhì)量比為0.2~0.3,H2O2/COD質(zhì)量比分別設(shè)為0.5、1.0、2.0、3.0、4.0、6.0時,攪拌條件下反應(yīng)90 min,取出反應(yīng)后水樣調(diào)節(jié)pH至9.0,靜置30 min,確保雙氧水分解完全,取其上清液測定COD。
3)Fe2+/H2O2質(zhì)量比
分別取200 mL 1)中水樣置于6個250 mL的錐形瓶中,保持雙氧水投加量為2)中確定的最佳投加量,初始pH=3.0,保持溶液中Fe2+/H2O2質(zhì)量比分別為0.2、0.3、0.4、0.5、0.8、1.0,攪拌條件下反應(yīng)90 min,取出反應(yīng)后水樣調(diào)節(jié)pH至9.0,靜置30 min,取其上清液測定COD。
4)初始pH值
分別取200 mL 1)中水樣置于6個250 mL的錐形瓶中,保持雙氧水投加量為2)中確定的最佳投加量,亞鐵為3)中確定的最佳投加量,攪拌條件下反應(yīng)90 min,考察反應(yīng)初始pH分別為2.0~10.0時COD的去除效果。
5)反應(yīng)時間
取500 mL 1)中水樣置于1個500 mL的細(xì)口瓶中,保持雙氧水投加量為2)中確定的最佳投加量,亞鐵為3)中確定的最佳投加量,反應(yīng)初始pH為4)中確定的最佳值,攪拌條件下反應(yīng),分別取反應(yīng)不同反應(yīng)時間的樣品,調(diào)節(jié)pH至9.0,靜置30 min,確保雙氧水分解完全,取其上清液測定COD和銅的濃度。
1.2.2 中試實(shí)驗(yàn)方法
采用中試裝置對絡(luò)合銅廢水進(jìn)行處理,中試裝置所用材料為透明PVC,具體尺寸如下圖所示。
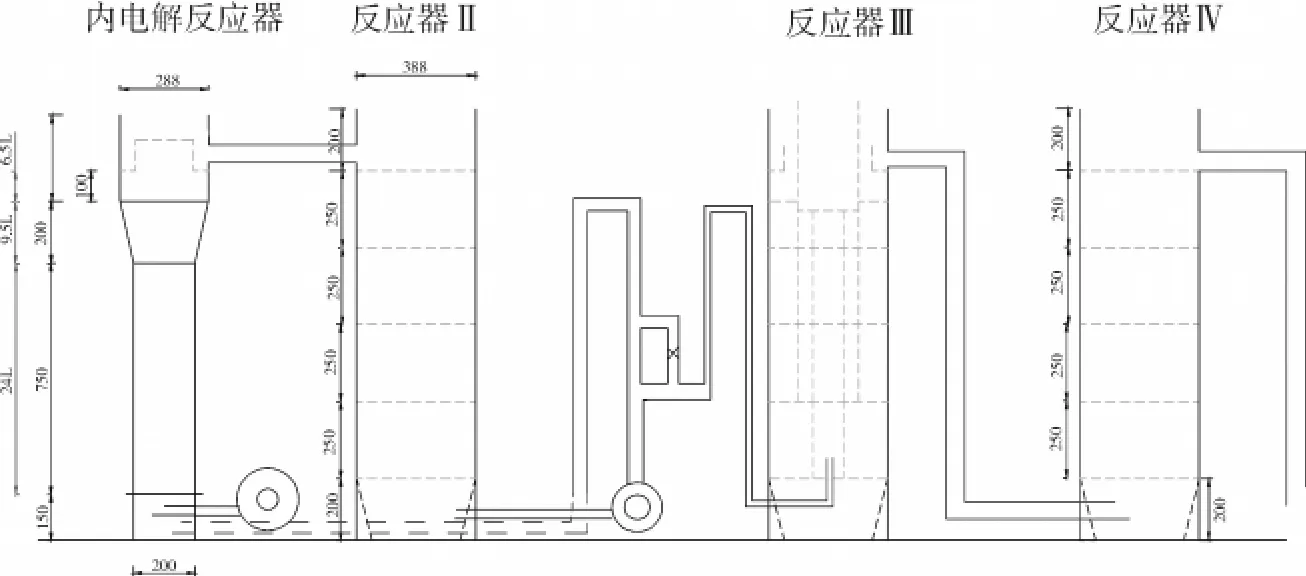
圖1 中試裝置示意圖
中試實(shí)驗(yàn)采用兩種不同的運(yùn)行方式,分別為混合運(yùn)行和串聯(lián)運(yùn)行。混合運(yùn)行是將雙氧水投加在反應(yīng)器Ⅱ里,使得在大流量回流時內(nèi)電解反應(yīng)器中也進(jìn)行Fenton反應(yīng);串聯(lián)運(yùn)行是將雙氧水投加到反應(yīng)器Ⅲ中,內(nèi)電解與Fenton氧化先后進(jìn)行。
2 結(jié)果與討論
2.1 單因素試驗(yàn)結(jié)果與討論
2.1.1 雙氧水投加量影響
保持初始pH=3.0,亞鐵濃度295.19 mg/L,反應(yīng)時間90 min,研究H2O2/COD質(zhì)量比分別為0.5、1.0、2.0、3.0、4.0、6.0時,F(xiàn)enton氧化法對COD的去除率,以及整個工藝COD總?cè)コ剩浣Y(jié)果如圖2所示。從圖中可以看出COD的去除率隨雙氧水投加量的增加而逐漸增大,當(dāng)[H2O2]/[COD]=0.5時,F(xiàn)enton氧化對COD的去除率為73.59%,[H2O2]/[COD]=6.0時去除率達(dá)到94.87%。

圖2 雙氧水投加量對Fenton氧化的影響
在Fenton反應(yīng)中雙氧水作為底物,是產(chǎn)生OH·的最直接物質(zhì),而OH·又是Fenton反應(yīng)中直接氧化有機(jī)物的氧化劑,因此增加雙氧水的投加量會促進(jìn)OH·的產(chǎn)生,從而促進(jìn)Fenton氧化的進(jìn)行。由圖2可知,[H2O2]/[COD]≤2.0時,COD 隨 H2O2量的增加而顯著下降,當(dāng)[H2O2]/[COD]≥3.0時,COD隨H2O2的量的增加下降幅度變小。Dutta等[6]的研究表明,H2O2是HO·的捕捉劑,隨著H2O2濃度的增加,對羥基自由基的捕捉作用也隨之增加,從而消耗一部分羥基自由基,降低雙氧水的有效利用。其從反應(yīng)機(jī)理中可知其反應(yīng)為:HO·+H2O2→HO2·+H2O2,HO·+HO-2→HO2·+OH-,生成的HO2·的氧化能力不如HO·[7],而且投加大量的雙氧水會將大量亞鐵氧化為Fe3+,從而消耗了部分雙氧水。由于內(nèi)電解已經(jīng)將銅去除到較低的水平,F(xiàn)enton進(jìn)水銅的濃度只有21.4 mg/L,且主要為游離態(tài)銅離子,在加堿后基本可以完全去除,當(dāng)[H2O2]/[COD]≧1.0時,銅的去除率可達(dá)到100%。
對于雙氧水投加量的確定除了考察處理效果外還要考慮經(jīng)濟(jì)性,這就涉及雙氧水的效能Q,即單位雙氧水投入的有效利用情況,如圖3所示,降解單位COD所需的雙氧水量Q隨[H2O2]/[COD]增加呈線性上升,其關(guān)系為 Q=1.0234R+0.2249,其中 Q=[H2O2]/[ΔCOD,R=[H2O2]/[COD]。

圖3 雙氧水效能(Q=[H2 O2]/[ΔCOD],R=[H2 O2]/[COD],r2=0.9996)
由關(guān)系式可以看出,[H2O2]/[COD]每增加1.0,降解單位COD所需的雙氧水就會增加1.0234。當(dāng)雙氧水投加量為0時,要降解一個單位的COD就需要0.2249個單位的雙氧水,這也是雙氧水利用率最高的時候,但顯然不可能達(dá)到最高的利用率,只可以無限接近。因此在投加一定量雙氧水時可以分多次投加,在保證投加量一定的前提下降低廢水中雙氧水濃度,從而提高雙氧水的利用率。根據(jù)圖2所示,[H2O2]/[COD]=2.0時如果再添加雙氧水,COD 的去除率沒有明顯的增加,[H2O2]/[COD]從1.0升到2.0時COD的去除率增加了7.95%,而從2.0到6.0時,[H2O2]/[COD]每增加1.0時,COD去除率平均增幅才達(dá)到2.48%。因此將H2O2的投加量確定為[H2O2]/[COD]=2.0,此時COD的最終去除率達(dá)到91.69%。
2.1.2 亞鐵量的影響
保持初始pH=3.0,反應(yīng)時間為90 min,[H2O2]/[COD]=2.0,反應(yīng)后調(diào)節(jié)pH=9,絮凝沉淀后取上清液測定COD,其隨Fe2+/H2O2的變化情況如圖4所示。其中Fe2+/H2O2=0.20是屬于不外加亞鐵的情況,因?yàn)閮?nèi)電解出水中本身就含有110.0 mg/L的亞鐵量。

圖4 亞鐵量對COD的影響
從圖中可以看出當(dāng)Fe2+/H2O2為0.20和0.30時Fenton氧化對COD的去除率為86.23%,之后繼續(xù)投加亞鐵,COD的去除率開始下降,當(dāng)Fe2+/H2O2>0.50時,COD的去除率又開始上升,這是因?yàn)槿芤褐蠪e2+和Fe3+總量的增加,導(dǎo)致混凝沉淀時鐵的氫氧化物對有機(jī)物的吸附量增加,從而抵消Fenton反應(yīng)去除率的下降。
為此,測定了Fenton氧化出水加堿絮凝前Fe2+/H2O2為0.30和1.0的COD,結(jié)果如表1所示。從表1的數(shù)據(jù)中可以看出,F(xiàn)e2+/H2O2=0.3時,F(xiàn)enton反應(yīng)所直接引起的COD去除率遠(yuǎn)大于Fe2+/H2O2=1.0時的COD的去除率,因此可以確定Fe2+/H2O2=0.50之后COD去除率上升的原因是氫氧化鐵和氫氧化亞鐵絮凝沉淀的吸附作用抵消Fenton氧化效果降低的結(jié)果。因此Fe2+/H2O2=0.20是最佳亞鐵量。

表1 Fenton反應(yīng)后絮凝沉淀前COD去除率
2.1.3 初始pH值影響
保持H2O2/COD=2.0,F(xiàn)e2+/H2O2=0.20~0.30,反應(yīng)時間90 min,pH值對COD去除率的影響如圖5所示。

圖5 不同pH值條件下Fenton氧化的處理效果
從圖5可知,當(dāng)pH在2.0~4.0的范圍內(nèi)COD的去除效果較好,當(dāng)4.0≦pH≦7.0時COD的去除率略有下降,pH>7.0后COD的去除率下降顯著,說明在堿性條件下Fenton氧化的效果不佳。這是因?yàn)樵趬A性條件下雙氧水的穩(wěn)定性降低,很容易分解成水和氧氣,降低了雙氧水的利用率,而且堿性條件下亞鐵都生成氫氧化物沉淀,進(jìn)而被氧化成氫氧化鐵,大大降低HO·的生成量,甚至不生成,使氧化過程靠新生成的氧氣和雙氧水自身的氧化性進(jìn)行。因此Fenton氧化不應(yīng)在堿性條件下進(jìn)行,最好初始pH為3.0。
2.1.4 反應(yīng)時間的確定
保持[H2O2]/[COD]=2.0,F(xiàn)e2+/H2O2=0.20~0.30,初始pH=3.0,處理時間與COD和銅的去除率關(guān)系如圖6所示。
從圖6中可以看出,隨著Fenton反應(yīng)的進(jìn)行,COD和總銅的去除率在不斷上升,說明在反應(yīng)剛開始時,F(xiàn)enton氧化具有較高的反應(yīng)速率,當(dāng)反應(yīng)進(jìn)行到60 min后,COD的去除率曲線趨于平緩,此時COD的去除率基本達(dá)到最大值。而對于銅的去除率則在30 min就達(dá)到了最大值,此時的銅離子濃度為0.5 mg/L。由于,F(xiàn)enton氧化工藝主要用于去除COD,因此選擇60 min為Fenton氧化的最佳反應(yīng)時間。
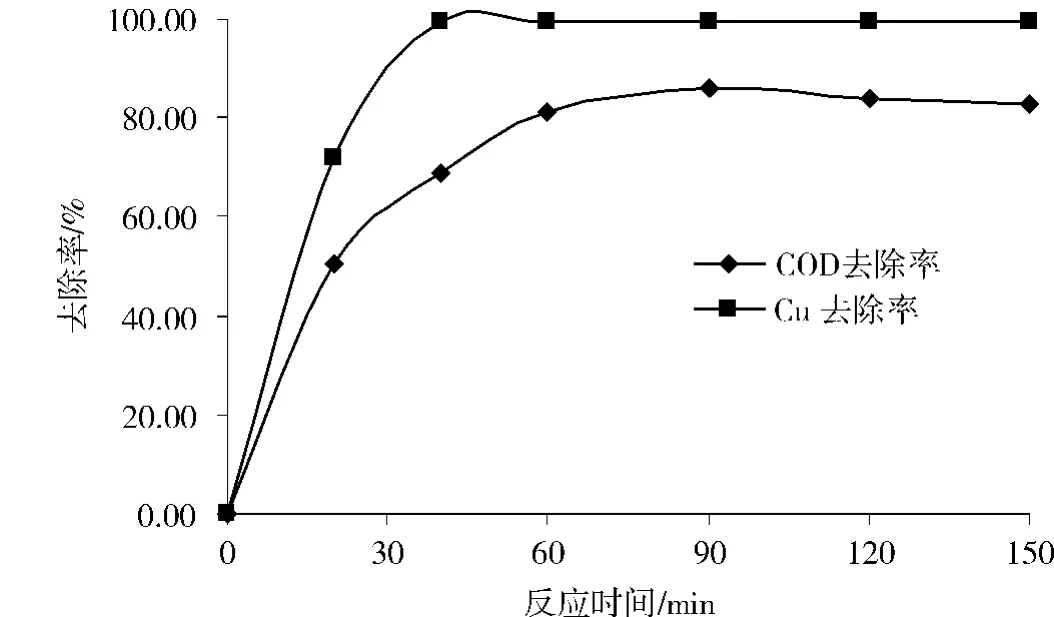
圖6 Fenton氧化時間對處理效果影響
2.2 中試實(shí)驗(yàn)
通過單因素實(shí)驗(yàn),確定了Fenton氧化強(qiáng)化處理經(jīng)內(nèi)電解處理的絡(luò)合銅廢水出水的最佳反應(yīng)條件,中試試驗(yàn)在此條件下進(jìn)行,通過考察內(nèi)電解與Fenton氧化混合運(yùn)行和串聯(lián)運(yùn)行時的處理效果,結(jié)果如表2所示。

表2 不同運(yùn)行方式時COD去除率%
從表2中可以看出,混合運(yùn)行時的COD去除率為80.56%,串聯(lián)運(yùn)行時內(nèi)電解出水的COD去除率為27.12%,F(xiàn)enton氧化絮凝出水的COD去除率為87.04%,在內(nèi)電解出水的基礎(chǔ)上Fenton氧化將COD的去除率提升了近60%。將兩種處理工藝對COD的去除效果做對比,可以看出串聯(lián)運(yùn)行時的處理效果明顯比混合運(yùn)行時的處理效果好,這是因?yàn)閮?nèi)電解和Fenton氧化都對大分子有機(jī)物有較強(qiáng)的去除能力,但Fenton氧化的氧化能力比內(nèi)電解強(qiáng),將內(nèi)電解和Fenton反應(yīng)放在同一個反應(yīng)器中會導(dǎo)致Fenton試劑在開始時就氧化初始的進(jìn)水,而內(nèi)電解又無法降解Fenton氧化后剩下的COD,同時在反應(yīng)器中有鐵碳填料,會影響到Fenton氧化中Fe2+和Fe3+的平衡,最終導(dǎo)致雙氧水的利用率不高,而且Fenton反應(yīng)所形成的大量沉淀物會留在內(nèi)電解填料中,阻礙鐵碳微電池形成,進(jìn)一步降低處理效果,同時增加填料結(jié)塊的可能。當(dāng)將這兩個反應(yīng)工序分開時內(nèi)電解先將大分子的有機(jī)物分解成較小的分子,并且打開了一些難斷裂的化學(xué)鍵,當(dāng)內(nèi)電解反應(yīng)出水進(jìn)入Fenton反應(yīng)器后,F(xiàn)enton試劑又可以進(jìn)一步降解內(nèi)電解反應(yīng)后形成的小分子物質(zhì)和一些內(nèi)電解無法降解的有機(jī)物,從而最大限度地利用了雙氧水。而且分開運(yùn)行又解決了Fenton反應(yīng)形成的沉淀物堆積在鐵碳填料中的問題。同時還可以看出Fenton強(qiáng)化氧化后,COD的去除率顯著上升,這也說明Fenton反應(yīng)對內(nèi)電解出水具有較好的強(qiáng)化效果。
3 結(jié)論
1)單因素實(shí)驗(yàn)確定Fenton氧化的雙氧水投加量為[H2O2]/[COD]=2.0,最佳亞鐵投加量為Fe2+/H2O2=0.20~0.30,初始pH為3.0,反應(yīng)時間為60 min。在此最佳條件下Fenton氧化對COD的去除率可以達(dá)到81.35%。
2)通過中試實(shí)驗(yàn)確定串聯(lián)運(yùn)行時的處理效果比混合運(yùn)行時的效果好,混合運(yùn)行時COD去除率為80.56%,串聯(lián)運(yùn)行時COD的去處率在內(nèi)電解的基礎(chǔ)上提升近60%,最終去除率為87.04%,銅的總?cè)コ蔬_(dá)到99.86%。
[1]何明,梁振駒,李紅進(jìn).鐵屑內(nèi)電解法處理PCB絡(luò)合廢水[J].水處理技術(shù),2008,34(6):84-86.
[2]李輝.鐵碳微電解-Fenton氧化聯(lián)合處理染料廢水研究[D].哈爾濱:哈爾濱工業(yè)大學(xué),2006.
[3]孫旭輝,賈宇宇,馬軍,等.微電解-Fenton聯(lián)合工藝處理硝基苯廢水效能研究[J].水處理技術(shù),200935(1):74-78.
[4]張琦.酸化-Fenton氧化-混凝法處理印制電路板有機(jī)廢水研究[D].哈爾濱:東北農(nóng)業(yè)大學(xué)資源與環(huán)境學(xué)院,2009.
[5]彭軍,胡勇為.Fenton試劑在印制電路板工業(yè)廢水處理中的應(yīng)用[J].工業(yè)用水與廢水,2006,37(3):31-34.
[6]Duttu K,Mukhopadhyay S,Bhattacharjee S,et al.Chemical oxidation of methylene blue using a Fenton -like reaction[J].Journal of Hazardous Material,2001,84(1):57 -71.
[7]祁佩時,趙俊杰,劉云芝,等.Fenton試劑深度處理稠油石化廢水的反應(yīng)動力學(xué)[J].化工學(xué)報,2011,62(2):491-494.

