水楊醛縮對氯苯胺Co(Ⅱ)配合物的合成、表征及其熒光性質研究
霍涌前
(延安大學化學與化工學院,陜西 延安 716000)
席夫堿是指含有亞氨基C=N的一類化合物,該類化合物通常是通過含活潑羰基的化合物與胺及其氨基衍生物等作用形成,由于含有N、O原子,有多個配位點,能與多種過渡金屬進行配位[1~4],可作為螯合劑、生物活性劑、分析試劑和催化劑,廣泛應用于化工生產和科學研究。水楊醛類席夫堿配合物具有一定的發光性能,部分席夫堿有光致變色性能,在當前的有機化合物光致發光研究中有著重要的意義[5,6]。水楊醛縮苯胺類化合物具有良好的光致變色性能[7]。目前,國內關于一維鏈狀鈷的席夫堿配合物的發光性能研究較少。
作者在此以水楊醛和對氯苯胺為原料合成了水楊醛縮對氯苯胺(HL),將其作為主要配體與1,4-對苯二酚以及氯化鈷(CoCl2·6H2O)反應生成了Co(Ⅱ)的配合物[Co(C6H4O2)(L)2]n,用元素分析、紅外吸收光譜、紫外可見吸收光譜對其結構進行了表征,并研究了配體水楊醛縮對氯苯胺、配合物[Co(C6H4O2)(L)2]n的發光性能。
1 實驗
1.1 試劑與儀器
CoCl2·6H2O、水楊醛、對氯苯胺、1,4-對苯二酚、氫氧化鈉、甲醇、無水乙醇,均為分析純。
UV-2550型紫外可見分光光度計、IR Prestige-21型傅立葉紅外吸收光譜儀(KBr壓片),日本島津公司;PE2400型元素分析儀,美國珀金埃爾默公司;F-4500型熒光光度計,日本日立公司。
1.2 水楊醛縮對氯苯胺(HL)的合成
將7.3272 g水楊醛溶于120 mL無水乙醇中,邊攪拌邊向其中滴加7.6542 g對氯苯胺的60 mL無水乙醇溶液,溶液立刻呈黃色。滴加完畢,在70 ℃水浴條件下,攪拌80 min,冷卻至室溫,抽濾,用無水乙醇洗滌3次,在無水乙醇中重結晶2次,得桔黃色針狀固體HL,收率40%。合成路線如圖1所示。
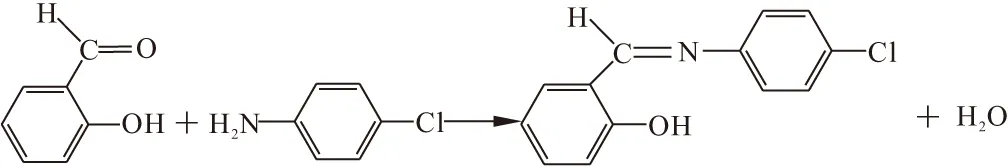
圖1 水楊醛縮對氯苯胺的合成路線
1.3 配合物[Co(C6H4O2)(L)2]n的合成
將0.4634 g(2 mmol)配體HL和0.1178 g (1 mmol) 1,4-對苯二酚置于燒杯中,用70 mL甲醇溶解,滴加0.4632 g(2 mmol)CoCl2·6H2O的30 mL甲醇溶液,磁力攪拌,溶液呈桔紅色,繼續加入0.040 g(1 mmol)NaOH的10 mL無水乙醇溶液,反應6 h后過濾,用無水乙醇洗滌1次,再用甲醇洗滌3次,自然風干,得紅色粉末狀化合物[Co(C6H4O2)(L)2]n。收率30%。
2 結果與討論
2.1 元素分析(表1)
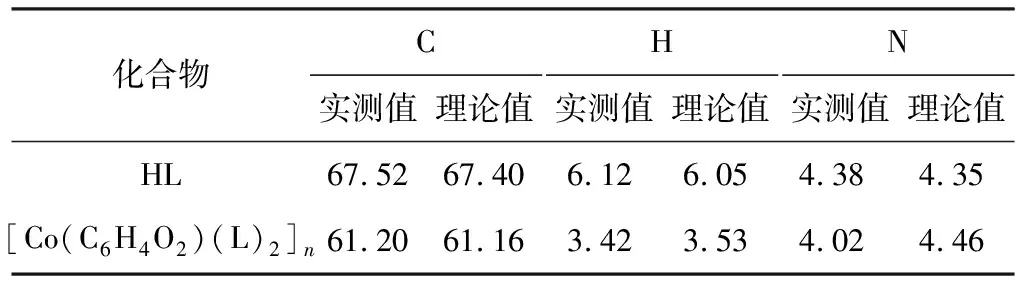
表1 配體及配合物的元素分析數據/%
由表1可見,配體和配合物的元素分析實測值和理論值基本相符,說明合成了目標化合物。
根據元素分析,推測配合物的可能結構見圖2。
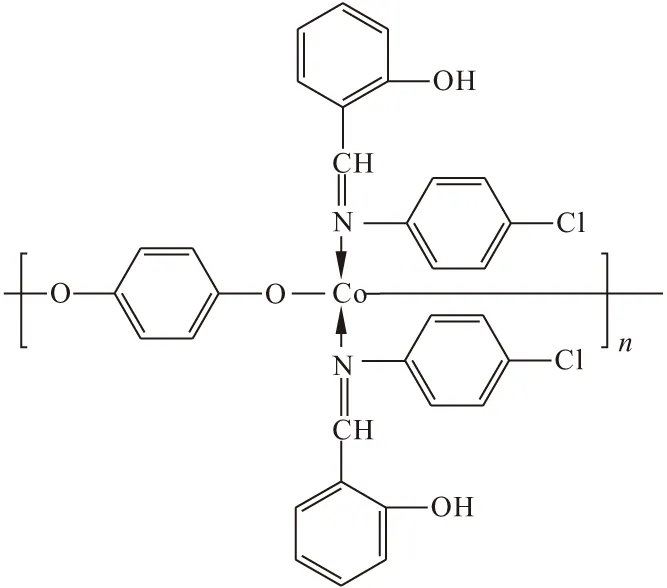
圖2 Co(Ⅱ)配合物的分子結構式
2.2 紅外光譜分析
用KBr壓片,在4500~400 cm-1的中紅外區對配體及配合物的紅外吸收光譜進行測定,結果見圖3。配體及配合物的主要IR吸收數據見表2。

圖3 配體及配合物的紅外吸收光譜

表2 配體及配合物的主要IR吸收數據/cm-1
由表2可知,配體中,大于3000 cm-1處的寬峰對應酚羥基的伸縮振動ν(O-H),在配合物3476 cm-1處該峰仍然存在,說明配體的酚羥基沒有去質子化與金屬成鍵[8],進一步證明了配合物的結構;配合物和配體均有C=N雙鍵吸收峰,配體的C=N雙鍵吸收峰波數為1635 cm-1,配合物的C=N雙鍵吸收峰波數為1602 cm-1;配體的C-O吸收峰波數為1179 cm-1,配合物的C-O吸收峰波數為1150 cm-1,吸收峰值明顯藍移,表明氧原子發生了配位;在配合物中還出現了433 cm-1處的Co-N吸收峰和418 cm-1處的Co-O吸收峰。
2.3 紫外可見吸收光譜分析
以甲醇作溶劑,在200~800 nm波長范圍內對配體及配合物的紫外可見吸收光譜進行測定。
結果發現,配體的吸收峰值為236 nm、275 nm和362 nm,其中236 nm、275 nm為苯環的特征吸收帶,362 nm為亞氨基C=N的π-π*躍遷;配合物的吸收峰值分別為276 nm和366 nm,其中276 nm為苯環的特征吸收帶,366 nm為亞氨基C=N的π-π*躍遷,與配體相比,該峰值發生紅移,說明亞氨基上的N原子與鈷(Ⅱ)配位[8]。
2.4 熒光發射光譜分析
有機熒光分子除了有生色團外,還常含有一些使熒光紅移或增大發光效率的基團,稱為助色團。助色團一般為電子給體,含有n孤對電子,且n電子云幾乎可與芳環上的π軌道平行,擴大了共軛π體系。實驗發現,配體、配合物在甲醇溶液中均發綠光。對配體、配合物的甲醇溶液的熒光發射圖譜進行測定(配體和配合物的激發波長分別為416 nm和400 nm),結果見圖4。
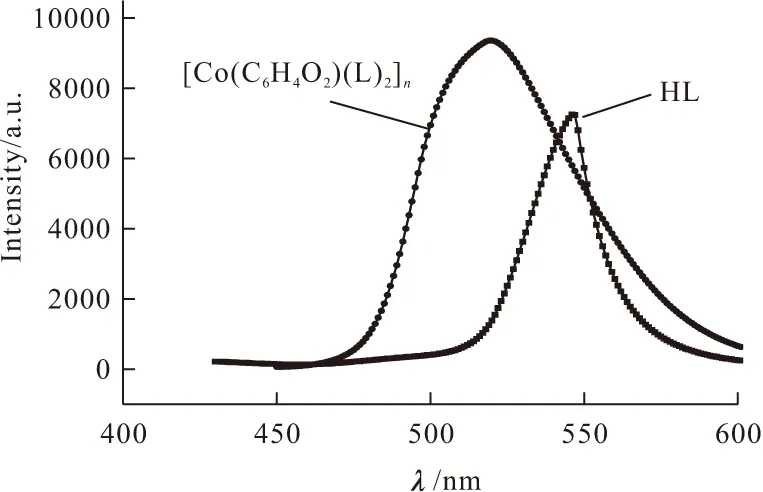
圖4 配體及配合物的熒光發射光譜
由圖4可以看出,配體水楊醛縮對氯苯胺在波長為416 nm的光激發下,在546 nm處產生了一個熒光發光峰;氯原子有孤對電子,為助色基團,配體的發光機理為L*→L發光。配合物[Co(C6H4O2)(L)2]n在波長為400 nm的光激發下,在520 nm處產生了一個較寬的熒光發光峰,相對于配體的最大發光峰值發生了藍移。這說明配位原子的孤對電子參與大共軛π鍵,與Co配位后使得熒光發射峰藍移[9]。
鈷配合物發光機理共有兩類:金屬離子微擾的配體發光[10]、配體向金屬中心鈷的電荷遷移發光[11]。配合物[Co(C6H4O2)(L)2]n與配體的發光峰形、峰值均不同,因此Co(Ⅱ)配合物的發光機理可能為配體向金屬中心鈷的電荷遷移發光。
3 結論
以1,4-對苯二酚、水楊醛縮對氯苯胺為配體,合成了Co(Ⅱ)金屬配合物[Co(C6H4O2)(L)2]n,通過元素分析、紅外吸收光譜、紫外可見吸收光譜,推測該配合物為一個鏈狀的席夫堿配合物;對配體、配合物的熒光光譜測試表明,配體、配合物在甲醇溶液中均發綠光,配體的發光機理為L*→L發光,配合物的發光機理可能為配體向金屬中心鈷的電荷轉移發光。
[1] 陳小華,吳瓊潔,梁志瑜,等.一個雙核鋅(Ⅱ)配合物[Zn2(L)2(Mf)2]的合成、結構、熱穩定性及熒光性質[J].無機化學學報,2009,25(5):910-914.
[2] 常嶺,李豪,張武.水楊醛縮鄰硝基苯胺合銅的合成與晶體結構[J].化學研究,2009,20(4):56-58.
[3] 游偉,姚成,黃偉.一個Salen型配體及其鋅(Ⅱ)和鎳(Ⅱ)配合物配位前后晶體結構及波譜的比較[J].無機化學學報,2010,26(5):867-874.
[4] 丁玉潔,劉榮梅,高建綱.新型Schiff堿及其鈰(Ⅲ)配合物的合成與表征[J].光譜實驗室,2010,27(2):541-544.
[5] 霍涌前,王升文,崔華莉,等.Schiff堿類鋅(Ⅱ)配合物的合成、晶體結構及發光性能[J].無機化學學報,2010,26(7):1274-1278.
[6] 霍涌前,任宜霞,陳小利,等.水楊醛縮對甲苯胺鈷(Ⅲ)配合物的合成、晶體結構和熒光性質[J].化學試劑,2010,32(10):877-880,902.
[7] 李銀玲,王鳳奇,甄珍,等.水楊叉縮苯胺及其衍生物的變色機理[J].物理化學學報,1998,14(11):981-987.
[8] 郝玉英,高志翔,王華,等.水楊醛縮苯胺鋅及其薄膜的譜學性能[J].光譜學與光譜分析,2006,26(3):491-495.
[9] 鄭玉嬰,吳文士.水楊醛縮氨基硫脲合鈷(Ⅱ)的晶體結構及其熒光性質[J].分子科學學報,2006,22(1):41-46.
[10] 劉停,李旭.配位聚合物[Co2(C13H10NO2)4(4,4′-bipy)2]n的合成、晶體結構、熱穩定性及熒光性質[J].無機化學學報,2010,26(4):677-681.
[11] 陳建新,劉世雄.配位聚合物{[Co2(HBTC)2(H2O)6]·C4H10N2·2H2O}n的水熱合成、結構表征及熒光性質[J].高等學校化學學報,2004,25(7):1189-1193.

