六種離子液體的合成研究
胡小梅
(1.東北農業大學生命科學學院,哈爾濱 150030;2.阿斯頓大學生命健康學院,伯明翰 B4 72ET)
保護環境,減少污染已成為現代社會面臨的巨大挑戰。有機溶劑的大量使用嚴重污染了環境,處理及回收使用過的溶劑已成為難題。近年來,環保離子液體引起了研究者極大的興趣[1]。離子液體具有熱穩定性、低揮發性、無可燃性、毒性小以及可回收利用等,因此,離子液體被認為是環境友好的反應溶劑,引起了研究者將離子液體應用于食品工業如制備食品添加劑[2-4],餐飲廢油轉化為生物柴油[5-6],以及應用于農業如農藥合成,纖維素提取等領域的濃厚興趣[7-8]。
離子液體一般由有機陽離子和無機陰離子組成。陽離子主要有四類,咪唑類、吡啶類、季銨和季磷類,以咪唑類離子液體為主要類型。廣泛采用的陰離子主要有[BF4]ˉ、[PF6]ˉ、[CH3CO2]ˉ、[CF3COO]ˉ等。本文將合成一系列離子液體并且對離子液體的合成方法進行研究和比較。以滿足離子液體大規模生產和應用的需要。
1 材料與方法
1.1 主要試劑和儀器
化學藥品采購于Fisher Scientific公司,均為分析純。1HNMR核磁氫譜用德國Bruker公司Bruker AC-250 NMR核磁共振儀測定(DMSO-d6作溶劑)。
1.2 方法
氯化1-甲氧基乙基-3-甲基咪唑{[MeOEtMIM]+Clˉ}的合成:
8 mL(0.1 mol)1-甲基咪唑與 9.3 mL(0.1 mol)2-氯乙基甲基醚加入到50 mL三口燒瓶,在80℃下磁力攪拌24 h,薄層色譜監控反應進程。產品用2-氯乙基甲基醚洗2次,每次5 mL,然后在60℃條件下減壓蒸餾30 min,重結晶方法純化產品,產品收率達 16 g(90%)。
氯化1-乙氧基乙基-3-丁基咪唑{[EtOEtBuIM]+Clˉ}的合成:
7 mL(0.05 mol)1-丁基咪唑滴加到 11 mL(0.1 mol)2-氯乙基乙基醚中,反應混合物在80°C條件下攪拌48 h。產品用乙酸乙酯洗(2×7 mL),然后在60℃條件下減壓蒸餾4 h后,得到淺黃色粘稠液體,產量為11.52 g(95%)。
1-甲氧基-3-甲基咪唑雙三氟甲烷磺酰亞胺鹽{[MeOEtMIM]+[(CF3SO2)2N]ˉ}的合成:
6.15 g(0.04 mol)[MeOEtMIM]+Clˉ溶解于 10 mL丙酮中,10 g(0.04 mol)雙三氟甲烷磺酰亞胺鋰溶解于20 mL水中。雙三氟甲烷磺酰亞胺的水溶液滴加到[MeOEtMIM]+Clˉ中,反應混合物在室溫下攪拌2 h,所得產品與水溶液分層。產品直接被分離后,用水洗(2×10 mL),再減壓蒸餾1 h,產品收率為11.5 g(79%)。
1-甲氧基-3-甲基咪唑三氟甲基磺酸鹽{[MeOEtMIM]+[CF3SO3]ˉ}的合成:
6.93 g(0.04mol)[MeOEtMIM]+Clˉ的丙酮溶液滴加到6.75 g(0.04 mol)三氟甲基磺酸鈉的丙酮溶液中,在室溫下攪拌2 h,產生的氯化鈉可直接過濾,經減壓蒸餾所得產品為8.92 g(79%)。
1-乙氧基乙基-3-丁基咪唑三氟乙酸鹽{[EtOEtBuIM]+[CF3COO]ˉ}的合成:
4.46 g(0.02 mol)[EtOEtBuIM]+Clˉ的乙腈溶液滴加到2.61 g(0.02 mol)三氟乙酸鈉的丙酮溶液中,在室溫下攪拌2 h,產生的氯化鈉可直接過濾,經減壓蒸餾所得產品為3.86 g(65%)。
1-甲氧基-3-甲基咪唑甲磺酸鹽 {[MeOEtMIM]+[CH3SO3]ˉ}的合成:
32 mL(0.41 mol)甲磺酰氯緩慢滴加到32 mL(0.41 moL)1-甲氧基乙醇和 57 mL(0.41 moL)三乙胺的100 mL二氯甲烷溶液中,混合物在冰浴中攪拌4 h,產生的沉淀三乙基氯化銨直接被過濾。濾液經水洗后用無水硫酸鎂干燥,減壓蒸餾所得產品為2-甲氧基乙基甲磺酸鹽49.95 g(80%),產品經蒸餾純化。然后取2-甲氧基乙基甲磺酸鹽12.73 g(0.08 mol)與 1-甲基咪唑 57 mL(0.08 mol)混合后,在 60 °C條件下反應2 d,所得粗產品用少量乙酸乙酯洗2次,經減壓蒸餾得離子液體17.72 g(91%)。
2 結果與分析
2.1 1HNMR分析
[MeOEtMIM]+Clˉ:1HNMR(DMSO-d6)δ=9.57(s,1H,N-CH=N),7.91(t,J=1.90Hz,1H,N-CH=C),7.85(t,J=1.90Hz,1H,C=CH-N),4.42(t,J=5.05Hz,2H,N-CH2-),3.90(s,3H,N-CH3),3.71(t,J=5.05Hz,2H,-CH2-O),3.24(s,3H,O-CH3).
[EtOEtBuIM]+Clˉ:1HNMR(DMSO-d6)δ=9.55(s,1H,N-CH=N),7.92(m,1H,N-CH=C),7.88(m,1H,C=CH-N),4.39(t,J=5.05Hz,2H,N-CH2-CH2O),4.24(t,J=6.95Hz,2H N-CH2-CH2CH2),3.72 (t,J=5.05Hz,2H,-CH2O),3.43(q,J=6.95Hz,3H,O-CH2),1.77(quint,J=7.58Hz,2H,N-CH2-CH2-CH2),1.22(sext,J=7.58Hz,2H,NCH2CH2-CH2-),1.04(t,J=6.95Hz,3H,OCH2-CH3),0.88(t,J=7.58Hz,3H,N-CH2CH2CH2-CH3).
[MeOEtMIM]+[(CF3SO2)2N]ˉ:1HNMR(DMSO-d6)δ=9.09(s,1H,N-CH=N),7.72(t,J=1.90Hz,1H,N-CH=C),7.69(t,J=1.90Hz,1H,C=CH-N),4.35(t,J=5.05Hz,2H,N-CH2-),3.86(s,3H,NCH3),3.68(t,J=5.05Hz,2H,-CH2-O),3.27(s,3H,O-CH3).
[MeOEtMIM]+[CF3SO3]ˉ:1HNMR (DMSO-d6)δ=9.10(s,1H,N-CH=N),7.75(t,J=1.90Hz,1H,N-CH=C),7.70(t,J=1.90Hz,1H,C=CH-N),4.35(t,J=5.21Hz,2H,N-CH2-),3.86(s,3H,N-CH3),3.67(t,J=5.05Hz,2H,-CH2-O),3.26(s,3H,O-CH3).
[EtOEtBuIM]+[CF3COO]ˉ:1HNMR (DMSO-d6)δ=9.55(s,1H,N-CH=N),7.96(m,1H,N-CH=C),7.89(m,1H,C=CH-N),4.42(t,J=4.90Hz,2H,N-CH2-CH2O),4.26(t,J=7.11Hz,2H,N-CH2-CH2CH2),3.72(t,J=4.90Hz,2H,-CH2O),3.41(q,J=6.95Hz,3H,O-CH2),1.76(quint,J=7.11Hz,2H,CH2-CH2-CH2),1.21(sext,J=7.27Hz,2H,CH2-CH2-CH3),1.01(t,J=7.11Hz,3H,OCH2-CH3),0.84(t,J=7.27Hz,3H,CH2CH2-CH3).
[MeOEtMIM]+[CH3SO3]ˉ:1HNMR(DMSO-d6)δ=9.21(s,1H,N-CH=N),7.79(t,J=1.90Hz,1H,N-CH=C),7.57 (t,J=1.90Hz,1H,C=CH-N),4.37(t,J=5.05Hz,2H,N-CH2-),3.88(s,3H,N-CH3),3.68(t,J=5.05Hz,2H,-CH2-O),3.25(s,3H,O-CH3),2.36(s,3H,CH3SO3).
2.2 離子液體的溶解性
本文中合成的離子液體室溫下只有[MeOEtMIM]+Clˉ呈固態,其余5種離子液體室溫下均為液態。[MeOEtMIM]+Clˉ, [EtOEtBuIM]+Clˉ, [MeOEtMIM]+[CF3SO3]ˉ,[MeOEtMIM]+[CH3SO3]ˉ,[EtOEtBuIM]+[CF3COO]ˉ為易溶于水的離子液體,[MeOEtMIM]+[(CF3SO2)2N]ˉ為不易溶于水的離子液體。六種離子液體均與甲醇、丙酮、乙腈等有機溶劑混溶,與乙醚、石油醚不溶。僅[MeOEtMIM]+[(CF3SO2)2N]ˉ與乙酸乙酯相溶,其余離子液體與乙酸乙酯不溶。結果見表1。
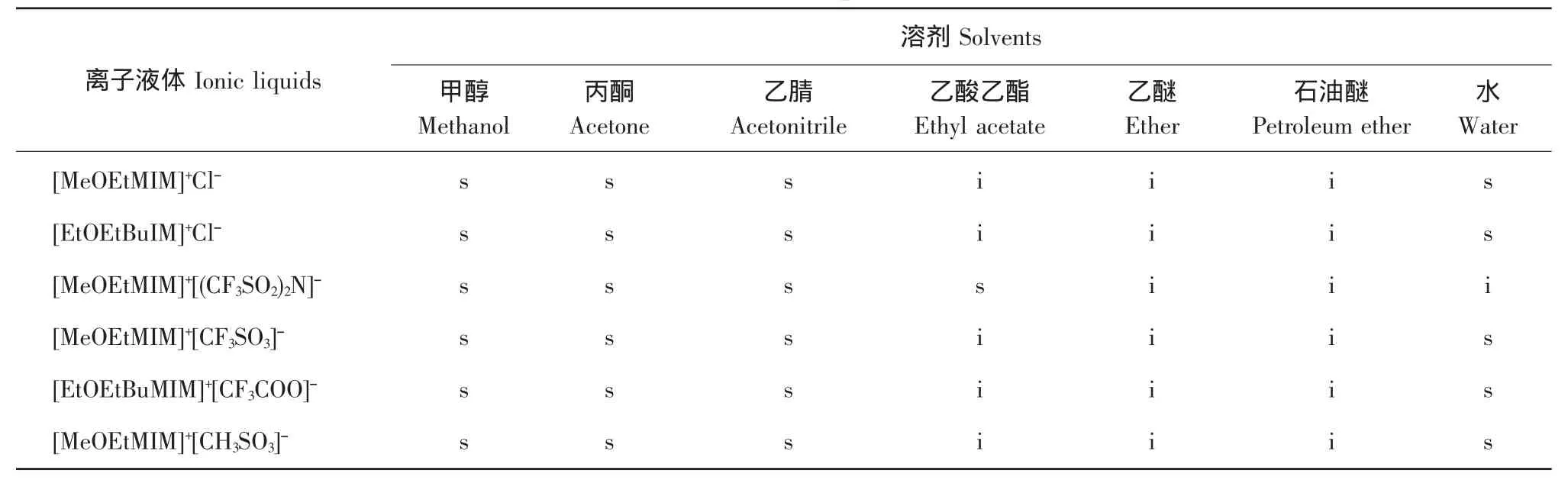
表1 離子液體與其他溶劑的溶解性Table 1 Solubility of the ionic liquids with other solvents
2.3 離子液體的合成
離子液體通常用兩步法合成,首先合成鹵鹽,然后鹵離子進一步與其它離子交換形成目標離子液體[9]。目前,鹵鹽類離子液體制備過程中采用的反應溶劑種類較多如甲苯、乙酸乙酯等。本文以氯化1-甲氧基-3-甲基咪唑的合成為例來研究在不同溶劑中的反應效率(見表2),對于幾種常用的溶劑進行研究和比較。

表2 在不同反應溶劑的中,氯化1-甲氧基乙基-3-甲基咪唑的合成Table 2 Preparation of 1-methoxyehtyl-3-methylimidazolium chloride using various solvents
3 討論
3.1 離子液體的1HNMR
[MeOEtMIM]+Clˉ、[MeOEtMIM]+[(CF3SO2)2N]ˉ、[MeOEtMIM]+[CF3SO3]ˉ具有相同的陽離子,該系列離子液體的核磁共振氫譜的峰形相同,同樣,[EtOEtBuIM]+Clˉ與 [EtOEtBuIM]+[CF3COO]ˉ核磁共振氫譜的峰型相同。其中鹵鹽離子液體[MeOEtMIM]+Clˉ和 [EtOEtBuIM]+Clˉ咪唑環上2位碳上氫的化學位移較大,分別為9.57和9.55,可能與其氫鍵較強相關。
3.2 離子液體的溶解性
陰離子為[PF6]ˉ、[(CF3SO2)2N]ˉ的離子液體多不溶于水,以 Clˉ、[CF3SO3]ˉ、[CF3COO]ˉ為陰離子的離子液體多溶于水,本研究中合成的離子液體符合一般規律。[MeOEtMIM]+[(CF3SO2)2N]ˉ為不易溶于水的離子液體,其余5種離子液體均溶于水。六種離子液體均與甲醇、丙酮、乙腈等有機溶劑混溶,與乙醚、石油醚不溶。多數已報道的離子液體與乙酸乙酯不溶,但該研究中合成的離子液體 [MeOEtMIM]+[(CF33SO2)2N]ˉ與乙酸乙酯相溶。可根據離子液體與水和丙酮、乙酸乙酯、乙醚等常用有機溶劑的溶解性,建立均相或雙相體系應用于各類化學反應。
3.3 離子液體的合成方法
鹵鹽類離子液體制備過程中采用的反應溶劑種類較多,因此將不同溶劑做以比較。由表1可知,當反應底物2-氯乙基甲基醚用作反應溶劑,反應時間較短,產品收率較高,1,1,1-三氯乙烷比乙酸乙酯和甲苯效率較高,但是毒性較大,對環境污染較大。相比較而言,2-氯乙基甲基醚作為反應底物之一促進反應正向進行,且與產品分層,因此是較好的反應溶劑。在無反應溶劑的條件下,反應效率較高,這可能由于無溶劑的加入,維持體系內的反應熱,提高反應物在單位時間內的碰撞機會。
[MeOEtMIM]+[(CF3SO2)2N]ˉ是一種不溶于水的離子液體,因此在水溶液中制備,反應可進行完全,產品易與水溶液分層,易于分離,無鹵離子干擾。以[PF6]ˉ、[(CF3SO2)2N]ˉ為陰離子的離子液體多為不易溶于水的離子液體,均可用此類方法。鈉鹽和鉀鹽比銀鹽價格低,比酸易于操作,因此是較為理想的方法。丙酮是較好的一種溶劑,既可溶解反應底物如CF3COONa或CF3SO3Na,又可使產生的NaCl析出,促進反應正向進行。對于以[CF3COO]ˉ、[CF3SO3]ˉ為陰離子的離子液體均可采用該方法。以[CH3SO3]ˉ為陰離子的離子液體,如果用CH3SO3H來制備,離子交換反應會出現反應不完全的問題,而且由于產品易與水混溶,多次水洗導致產品流失。因為CH3SO3Na難溶于丙酮,不能用上述鈉鹽方法,CH3SO3Ag難溶于水,也無法用銀鹽溶解于水來制備。因此采用磺酸鹽法制備 [MeOEtMIM]+[CH3SO3]ˉ[10]。首先1-甲氧基乙醇與甲磺酰氯反應合成2-甲氧基乙基甲磺酸鹽,然后1-甲基咪唑與2-甲氧基乙基甲磺酸鹽反應合成離子液體[MeOEtMIM]+[CH3SO3]ˉ。
4 結論
綜上所述,對于易溶于水的離子液體,如果需要高純度的離子液體,適合銀鹽的方法。考慮工業化生產成本等問題,而且其陰離子的鈉鹽和鉀鹽可以溶于丙酮,可采用鈉鹽和鉀鹽方法,操作簡單,反應完全,是較理想的制備方法。本文合成的離子液體[MeOEtMIM]+Clˉ,[EtOEtBuIM]+Clˉ,[MeOEtMIM]+[CF3SO3]ˉ,[MeOEtMIM]+[CH3SO3]ˉ和 [EtOEtBuIM]+[CF3COO]ˉ為易溶于水的離子液體,[MeOEtMIM]+[(CF3SO2)2N]ˉ為不易溶于水的離子液體,且均與甲醇、丙酮、乙腈等有機溶劑混溶,與乙醚、石油醚不溶。以上室溫離子液體均可作為反應溶劑或者萃取劑等。本文合成的一系列離子液體是具有潛力的新型溶劑。
[1]Welton T.Ionic liquids in catalysis[J].Coordination Chemistry Review,2004,248:2459-2477.
[2]Valizadeh H,Gholipour H.Imidazolium-based phosphinite ionic liquid(IL-OPPh2)asreusablecatalystandsolventfortheknoevenagel condensation reaction[J].Synthetic Communications,2010,40(10):1477-1485.
[3]胡小梅,張必弦,堿性功能化離子液體在Knoevenagel縮合反應中的應用進展[J].東北農業大學學報,2011,42(6):141-144.
[4]許丹倩,羅書平,劉寶友,等.室溫離子液體中催化合成肉桂酸芐酯[J].有機化學,2004,24(1):99-102.
[5]Ha S H,Lan M N,Lee S H,et al.Lipase-catalyzed biodiesel production from soybean oil in ionic liquids[J].Enzyme and Microbial Technology,2007,41:480-483.
[6]王文魁,包宗宏,氯鋁酸離子液體催化大豆油制備生物柴油[J].中國油脂,2007,32(9):51-53.
[7]Kilpelainen I,Xie H B,King A,et al.Dissolution of wood in ionic liquids[J].J Agric Food Chem,2007,55(22):9142-9148.
[8]Fort D A,Remsing R C,Swatloski R P,et al.Can ionic liquids dissolve wood processing and analysis of lignocellulosic materials with 1-n-butyl-3-methylimidazolium chloride[J].Green Chem,2007,9(1):63-69.
[9]Bonhote P,Dias A P,Papageorgiou N,et al,Highly conductive ambient-temperature molten salts[J].Inorg Chem,1996,35:1168-1178.
[10]Cassol C C,Ebeling G,Ferrera B,et al.A simple and practical method for the preparation and purity determination of halide-free imidazoliumionicliquids[J].AdvSynthCatal,2006,348:243-248.

