CD36基因多態性對 2型糖尿病患者血脂和 CRP的影響
鄭壽煥,李金姬,張春子,楊秀麗,李美子
(延邊大學附屬醫院,吉林延吉 133000)
CD36是一種多功能的清道夫受體,可激活細胞釋放前炎癥反應性細胞因子、白介素等[1],并參與脂質代謝及動脈粥樣硬化的發生。人 CD36基因定位于 7號染色體的 q11.2帶,該區域存在 2型糖尿病(T2DM)的易感位點。為探討 CD36內含子 3[TG]多態性對 T2DM患者血脂、C反應蛋白(CRP)的影響,我們進行了相關研究。現報告如下。
1 資料與方法
1.1 臨床資料 選擇 2004年 12月 ~2009年 12月在我院住院的 T2DM患者(T2DM組)193例,男 106例、女 87例,年齡(54.0±12.1)歲。根據血脂水平分組,即總膽固醇(TC)>6.45 mmol/L為 TC異常組,≤6.45 mmol/L為 TC正常組;TG>1.88 mmol/L為 TG異常組,≤1.88 mmol/L為 TG正常組;HDL-C<0.9 mmol/L為 HDL-C異常組,≥0.9 mmol/L為HDL-C正常組;LDL-C>3.12 mmol/L為 LDL-C異常組,≤3.12 mmol/L為 LDL-C正常組。根據 CRP分組,≤5.0 mg/L為 CRP正常組,>5.0 mg/L為CRP異常組。同期隨機選擇在我院健康體檢者 80例作為對照組,臨床和實驗室檢查均正常,排除肝、腎、內分泌和心腦血管疾病。男 38例、女 42例,年齡(45.7±17.9)歲。兩組性別、年齡具有可比性。
1.2 方法
1.2.1 CD36基因多態性檢測 ①基因組 DNA提取:抽取受檢者肘靜脈血 3 ml,用 Promega公司產Wizard 基因組 DNA純化試劑盒提取 DNA。所得DNA經紫外分光光度計定量,并置于 -70℃保存備用。②PCR擴增目的基因片段:根據美國國立衛生研究院維護的基因序列數據庫中所報告的序列設計、北京華美公司合成的 CD36內含子 3基因引物:上游引物:5′-ATTTATAAAAGAAGTTGCAC-3′,下游引物:5′-GTTTACCTACAATTTAATAA-3′;PCR循環參數:94℃預變性 3 min,94℃變性 1 min,49℃退火 1 min,72℃延伸 1 min,循環 35次,最后 72℃延伸 5 min。用 5%瓊脂糖凝膠電泳分析 PCR擴增產物。③PCR擴增產物直接測序:PCR產物用凝膠電泳 DNA回收試劑盒純化回收 DNA片段后,送北京奧萊博生物技術有限責任公司,完成 PCR擴增產物測序。
1.2.2 血脂、CRP檢測 抽取受檢者肘靜脈血 3 ml,采用日立 7600-101全自動生化分析儀檢測 TC、TG、HDL、LDL、CRP水平 。
1.3 統計學方法 采用 SPSS13.0軟件進行統計分析,CD36內含子 3[TG]重復序列多態性各組間分布情況比較采用 χ2檢驗。P≤0.05為差異有統計學意義。
2 結果
2.1 兩組 CD36內含子 3[TG]重復序列基因多態性分布比較 PCR反應擴增產物測序結果顯示,兩組CD36內含子 3全部為雜合子且存在[TG]重復序列,[TG]重復次數為 11~16次,如圖 1所示。據[TG]重復序列出現的頻數分為 11/>11、12/>12、>12/>12,各頻數在對照組中分別為 37.5%(30/80)、45.0%(36/80)、17.5%(14/80),在 T2DM組中分別為 28.5%(55/193)、50.3%(97/193)、21.2%(41/193),同頻數比較差異均無統計學意義。
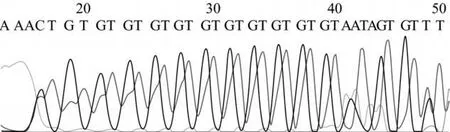
圖1 PCR擴增產物直接測序結果
2.2 CD36內含子 3[TG]重復序列基因多態性對T2DM患者血脂、CRP的影響 見表1。
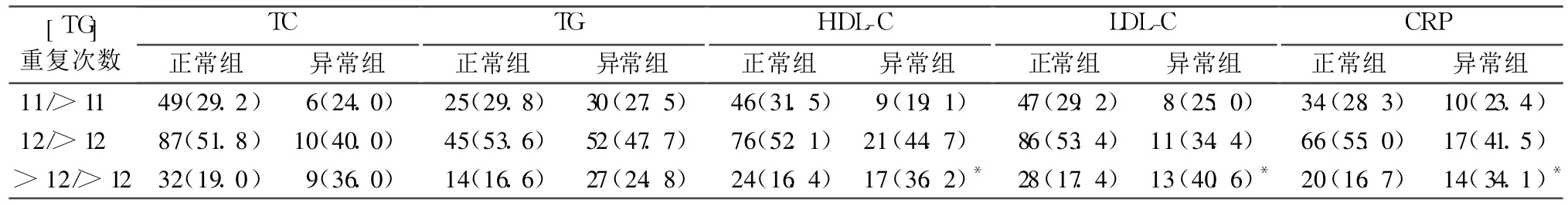
表1 CD 36內含子 3[TG]重復序列基因多態性分布時 T2DM患者血脂、CRP的影響[例(%)]
3 討論
CD36是巨噬細胞表面的一種 B類清道夫受體,廣泛存在于單核細胞、血小板、內皮細胞、視網膜色素上皮細胞、脂肪細胞等,參與炎癥、止血、免疫清除、脂質代謝和動脈粥樣硬化等病理生理過程[2]。Zhang等[3]研究指出,CD36表達增加可能是導致糖尿病患者動脈粥樣硬化的機制之一,高糖介導 CD36mRNA翻譯增加使巨噬細胞表面 CD36表達增高,為糖尿病時動脈粥樣硬化加劇提供了基礎。
目前已明確,高 LDL-C和低 HDL-C對動脈粥樣硬化的形成具有重要作用。T2DM患者脂質代謝紊亂的三聯癥(即 TG升高、LDL升高、HDL降低)是心血管疾病的危險因素[4]。高脂血癥可導致腎小球高濾過,加重糖尿病患者的腎臟損害[5]。LDL-C升高,可促進動脈中層平滑肌細胞過度增生,加速動脈粥樣硬化,增加腎小球毛細血管內壓,導致腎小球高濾過。過高的 LDL-C滯留于內皮下,經細胞氧化修飾形成氧化型低密度脂蛋白(ox-LDL)。ox-LDL能增加氧自由基的產生,從而促進腎小球內過氧化物陰離子生成,加快糖尿病腎病進展。另外,LDL-C尤其 ox-LDL具有化學趨化作用,被巨噬細胞攝取后刺激其產生生產因子和細胞因子,促進腎間質纖維化[6]。LDL-C水平增高,還可導致免疫復合物堆積,并黏附大量的巨噬細胞,兩者的復合物可釋放炎性介質[7]。對糖尿病腎病患者而言,炎性狀態使 LDL易氧化為 ox-LDL,高水平的 ox-LDL具有細胞毒作用,可損害腎小球小動脈血管內皮細胞和平滑肌細胞,造成白蛋白尿的進一步增加[8]。Sampson等[9]證實,ox-LDL與 CD36表達存在相關性,體外培養的巨噬細胞在高糖環境下細胞表面 CD36表達增高,同時伴有巨噬細胞攝取 ox-LDL增加。
CRP是機體受到損傷或發生各種急慢性炎癥后產生的一種敏感反應蛋白,是臨床上最有效的炎癥標志物之一。榮嶸等[10]研究表明,T2DM患者血清 CRP與糖尿病并發癥密切相關。CRP能直接作用于血管內皮,并促進早期動脈粥樣硬化的發生;CRP還參與血栓形成、白細胞黏附,促進單核細胞的活化及轉化,影響血管內皮細胞功能,從而加速和(或)加重 T2DM患者血管并發癥。Abrahamian等[11]研究顯示,糖尿病腎病患者增高的 CRP與增加的尿蛋白排泄有關,提示 CRP參與糖尿病腎病的發生、發展。國外研究表明[12],CD36在前炎癥因子和氧化應激介導的腎損傷中起關鍵性作用。ox-LDL通過 CD36和 PKC依賴途徑激活巨噬細胞中的轉錄因子 NF-κB。實際上 ox-LDL能觸發炎癥因子如TNF-α/β、IL-1β、IL-2、IL-6及 IFN-β/γ的分泌,而且有 ox-LDL誘導的巨噬細胞或泡沫細胞凋亡的發生機制依賴于 CD36和半胱天冬氨酸酶-3的激活。在動脈粥樣硬化斑塊中,許多前炎癥因子及抗炎癥因子被表達,這些炎癥因子可調節 CD36的表達。
本研究結果顯示,對照組與 T2DM組 CD36內含子 3[TG]重復序列基因多態性分布比較差異無統計學意義;而 T2DM各組間 HDL-C組、LDL-C組及CRP組比較差異均有統計學意義。CD36內含子 3[TG]>12/>12重復序列在 HDL-C異常組占36.2%,在 HDL-C正常組占 16.4%(P<0.05);LDL-C異常組占 40.6%,在 LDL-C正常組占 17.4%(P<0.05);在 CRP異常組占 34.1%,在 CRP正常組占16.7%(P<0.05)。說明 CD36內含子 3[TG]重復序列基因多態性與 T2DM患者的 HDL-C、LDL-C、CRP水平有關。CD36內含子 3[TG]>12/>12重復序列可能是 T2DM患者的 HDL-C水平降低、LDL-C和 CRP水平升高的遺傳因素。
綜上所述,我們認為 CD36內含子 3[TG]重復序列基因多態性與 T2DM患者 HDL-C、LDL-C、CRP水平有關。但 CD36內含子 3[TG]重復次數對 CD36的表達、血脂及 CRP的影響途徑和機制尚不明確,需進一步研究。
[1]Okamura DM,Pennathur S,Pasichnyk K,et al.CD36regulates oxidative stress and inflammation in hypercholesterolemic CKD[J].J Am Soc Nephrol,2009,20(3):495-505.
[2]高磊,鮑羿,洪斌,等.B類清道夫受體 CD36的研究進展[J].醫學分子生物學雜志,2006,3(1):61-64.
[3]Zhang HM,Zhang XL,Zhou X,et al.Mechanism linking atherosclerosis and type 2 diabetes:increased expression of scavenger receptor CD36in monocytes[J].Chin Med J(Engl),2005,118(20):1717-1722.
[4]Susztak K,Ciccone E,Mc Cue P,et al.Multiple metabolic hits converge on CD36as novel mediator of tubular epithelial apoptosis in diabetic nephropathy[J].PLoSMed,2005,2(2):e45.
[5]Athyros VG,Papageorgiou AA,Elisaf M,et al.Statins and renal function in patients with diabetes mellitus[J].Curr Med Res Opin,2003,19(7):615-617.
[6]Chen HC,Guh JY,Shin SJ,et al.Insulin and heparin suppress superoxide production in diabetic rat glomeruli stimulated with lowdensity lipoprotein[J].Kidney Int Suppl,2001,78:s124-s127.
[7]陳家堅,葉余輝,梁亮.高脂血癥患者超敏 C反應蛋白與心血管病危險因素的相關研究[J].華北國防醫藥,2009,2(1):22-23.
[8]Mojiminiyi OA,Abdella N,Moussa MA,et al.Association of C-reactive protein with coronary heart disease risk factorsin patientswith type 2 diabetes mellitus[J].Diabetes Res Clin Pract,2002,58(1):37-44.
[9]Sampson MJ,Davies IR,Braschi S,et al.Increased expression of a scavenger receptor(CD36)in monocytes from subjects with type 2 diabetes[J].Atherosclerosis,2003,167(1):129-134.
[10]榮嶸,楊敏,賈政,等.2型糖尿病患者血清超敏 C反應蛋白與多項血脂關系的研究[J].北京醫學,2008,30(5):296-298.
[11]Abrahamian H,Endler G,Exner M,et al.Association of lowgradeinflammation with nephropathy in type 2 diabetic patients:role of elevated CRP-levels and 2 different gene-polymorphisms of proinflammatory cytokines[J].Exp Clin Endocrinol Diabetes,2007,115(1):38-41.
[12]Iwao Y,Nakajou K,Nagai R,et al.CD36isone of important receptors promoting renal tubular injury by advanced oxidation protein products[J].Am J Physiol Renal Physiol,2008,295(6):F1871-F1880.

