放射外科手術系統的工作原理及臨床應用
許 鳴 華長江 趙 銳
術中放療技術(Introperative Radiation Therapy,IORT)是一種在手術中直接對腫瘤組織和腫瘤切除后的可疑腫瘤區域組織進行放射線單次大劑量照射,以最大限度的殺滅殘存腫瘤細胞,保護正常組織的放射治療方法。1964年由日本學者首先提出并應用于臨床,我國于1972年開展此項技術,我院于1986年首次開展胃癌的術中放療。由于傳統的術中放療需要在大型固定直線加速器機房內進行,病人在手術和放療過程中由于轉運帶來的感染、麻醉意外以及病人和操作人員的輻射防護等因素,制約了該項技術的發展。近年來,德國、美國等公司先后研制生產了放射外科手術系統,較好地解決了上述難題。本文以德國公司生產的“Intrabeam”為例予以介紹。該系統實質上是一臺具有自我防護、檢查功能、可移動的微型電子加速器,可直接在常規手術室內為手術病人提供放療,輻射防護要求低,移動靈活,操作簡便,可用于全身多處腫瘤的治療。
1 放射外科手術系統的構成
圖1為放射外科手術系統(Intrabeam)外觀圖。系統由XRS放射源(X-Ray Source)、控制平臺(Control cnsole)、支持承載系統(support system)、質量保證系統(quality instruments)、各種適配器(applicators)和其他附件組成。
XRS放射源(X-Ray Source):產生≤50 kV低能X射線,重1.5 kg。
控制平臺(Control cnsole):指導用戶安全快捷地執行治療方案,監控和保證治療劑量和過程的準確無誤。
支持承載系統(support system):通過電磁耦合機械臂將放射源精準地鎖定在治療位置,并可方便移動。
質量保證系統(quality instruments):包括高精度水假體和電離室,用于調試能量和計量率分布獨立驗證。
適配器(applicators):包括球型適配器(spherical applicator)、氣球適配器(balloon applicators)、針型適配器(needle applicators)等多種適配器,可用于不同部位腫瘤的放療。
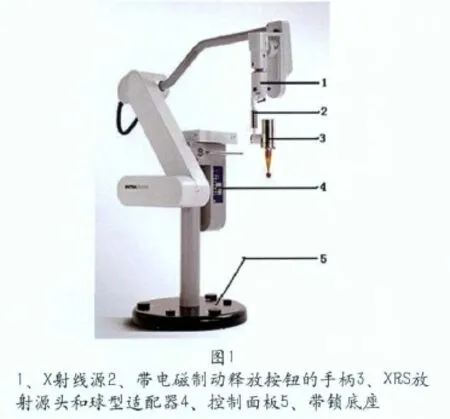
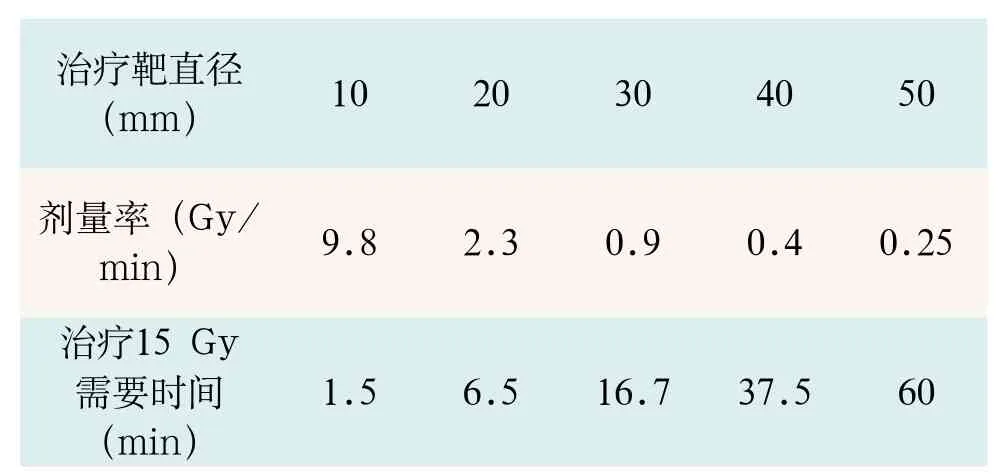
表1 典型的輻射輸出特性
2 主要技術參數及功能
2.1 主要技術參數:
管電流范圍:5 μA、10 μA、20 μA、40 μA四檔可選,誤差≤10%;
管電壓范圍:40 kV、50 kV兩檔可選,誤差≤10%;
X射線輸出穩定性:±5%(前5 min),±2%(5 min后);
輻射分布:在軟組織或水中立方反比衰減;輻射輸出特性(50 kV,40 μA),見表1;劑量輸出準確性:預置值與實測值之間的誤差不超過±5%;
輸入劑量的位置準確性:在放療直徑40 mm處誤差不超過±1 mm;
落地機架:外形尺寸1500 mm×80 mm×1940 mm,重279 kg;
2.2 主要功能
自檢功能,發現故障時,顯示錯誤信息;
內部和外部輻射監測校正功能;
輻射源均勻性自動校正功能;
XRS探頭射束偏差校準功能;
輸入環境溫度、氣壓校準輸出劑量功能;
照射時間保護功能,最長照射時間≤60 min;
治療參數選擇和設置功能;
輻射輸出安全自鎖功能,當輸出輻射源發生移動故障時,停止照射。
3 工作原理
放射外科手術系統的工作原理并不復雜,XRS放射源由其陰極發射的電子經30 kV、40 kV、50 kV三檔能量選擇的電壓加速,通過束流偏轉系統的控制形成高速電子流打在金靶上,產生最高能量50 kV的X射線,這個過程由內部監控系統進行反饋并可調。產生X線的靶端根據治 療需要可連接各種規格的適配器。常用為球形適配器,其上半圓部分為金屬鎢,可將X射線方向遮擋以保護操作人員,并形成低能、高劑量、各向同性的X線均勻地作用于治療區。各種適配器均有連接軸與XRS放射源直接相連,并使產生X線的金靶端置于適配器的圓心。支持承載系統利用電磁耦合技術確保連接放射源的適配器精準可靠地定位于治療區。整個治療方案的設定、操作均通過控制平臺實現。標準的工作流程是:外科醫生切除腫瘤后,根據腫瘤區域可疑殘余腫瘤組織情況,選擇相應的適配器和治療劑量,由控制系統確定照射時間,經物理師確認后,將適配器接上放射源,支架裝上消毒罩,適配器經過承載系統鎖定在治療位置,照射部位以輕鉛板屏蔽覆蓋以保護操作人員,全部準備工作完成后即可實施照射治療。
4 臨床應用
放射外科手術系統的獨特性在于其使用靈活、精確、安全、無需對手術室進行特殊輻射防護改造。其產生的低能X射線通過適配器各向同性發射,直接對準腫瘤組織及腫瘤切除后的殘余組織,進行單次大劑量照射,照射深度為1~2 cm,最大限度地殺死腫瘤細胞,照射范圍以外輻射能量急速下降,使周圍健康組織得到保護,因而在臨床上得到廣泛的應用。據國外文獻報道,目前該系統已成功應用于頭頸部腫瘤、顱內腫瘤、乳腺癌、膀胱癌、子宮癌等腫瘤及殘存腫瘤組織的術中放療。倫敦大學醫院的Tobias JS報告了185例直徑為0.4~4 cm的乳腺癌患者的治療結果,22例僅用術中放療,163例采用術中放療后加外放療,隨訪5 a,結果無論腫瘤控制還是乳房外形均令人滿意,僅有1例局部復發,且治療并發癥較低,僅1例出現局部皮膚放射性壞死。作者認為,術中放療的應用,使大量早期乳腺癌患者保留乳房成為可能,而療效與切除乳房根治術無差異。美國學者Algur E,Mahadevan A,Delbel C等用術中放療系統治療了24例復發和進展期直腸癌患者,其回顧分析顯示,在這組難治性病例中,患者進行術中放射治療耐受性較好,隨訪15個月,21例病例均獲得腫瘤局部控制,局部復發患者1 a生存率為92%,進展期腫瘤患者1 a生存率為100%。瑞典學者Curry WT,CosgroveGR,Hochberg FH等用術中放療系統治療腦部轉移腫瘤患者,60例患者均在接受組織活檢后,直接進行術中放射治療,結果與腫瘤切除后結合體外立體定向放射治療效果相當,81%的病例獲得腫瘤局部控制,96.6%的病例無明顯副反應發生。應用術中放療技術,日本學者已將Ⅱ期、Ⅲ期胃癌的五年生存率提高到84%和64%。
5 結語
腫瘤是嚴重危害人民健康的重大疾病,據統計,我國每年約有200~220萬新生腫瘤患者,總計有600余萬腫瘤患者,其中有60%~70%的腫瘤病人需要接受放射治療以爭取根治或姑息治療,以改善生活質量。放射外科手術系統的應用,在日益強調腫瘤患者綜合性和個體化治療的今天,無疑具有重要的意義。截止2010年5月,全球共有83臺放射外科手術系統投入使用,其中,歐洲59臺,美國17臺,亞太地區7臺。近兩年來,我國也有數家醫院引進了該設備,并投入使用。隨著時間的推移,其明顯的技術優勢必將在腫瘤的治療中得到充分的應用和發揮。
[1]Vaidya JS, Baum M, Tobias JS, et al.Targeted intra-operative radiotherapy(Targit): An innovative method of treatment for early breast cancer.Ann Oncol, 2006,12(8):1075-1080.
[2]Vaidya JS, Baum M, Tobias JS, et al.The novel technique of delivering targeted intraoperative radiotherapy(Targit)for early breast cancer.Ann Oncol,2004,28(4):447-54.
[3]Curry WT, CosgroveGR,Hochberg FH等.腦部轉移立體定向介入放射外科[J].J Neurosurg 2005,103:630-635.
[4]Algur E,Mahadevan A,Delbel C,等.術中光子放射外科系統治療復發和進展期直腸癌:24例患者回顧分析[J].SACO胃腸癌研討會,2005年1月27-29日,Hollywood,Florida,USA
[5]Takakura K,Kubo O.惡性腫瘤治療.Gan To Kagaku Ryoho.2006,27 Suppl 2:449-453.

