口服滲透泵控釋制劑的研究進展
李秀敏,李慧莉
(北京軍區總醫院,北京,100700)
口服滲透泵控釋制劑的研究進展
李秀敏,李慧莉
(北京軍區總醫院,北京,100700)
滲透泵;控釋制劑;半透膜
在研究開發更為有效的藥物的同時,藥物新劑型的開發與發展越來越受到人們的關注,其主要原因是研發一種藥物的新型制劑所需的資金和時間(2 000萬~5 000萬美元和3~4年)遠小于研制一種新的化學實體(約5億美元和10~12年)。通過制劑學的手段,使藥物發揮最佳療效的觀點已普遍為人們所接受。隨著相關科學的發展,藥劑學的發展突飛猛進,新劑型不斷涌現。在當前許多藥物劑型中,滲透泵制劑以其獨特的釋藥方式和穩定的釋藥速率,引起人們的普遍關注。1955年,2位澳大利亞生理學家Rose和NeLson發明了用于牛、羊消化道藥物遞送的RoseΟNeLson滲透泵[1]。1973年HiguchiΟLeeper滲透泵問世并申請了專利,此設計簡化了RoseΟNeLson滲透泵。1974年Theeuwes發明了初級滲透泵,由ALza公司命名為OROS。
滲透泵型控釋制劑作為緩控釋制劑的典型代表,是以滲透壓作為釋藥動力,以零級釋放動力學為特征的一種制劑技術。由于滲透泵控釋制劑具有零級釋藥的特征,并且釋藥速率受介質環境的pH值、胃腸道蠕動和食物等因素影響小以及體內外釋藥相關性較好等特點,已成為目前國內外研究開發的熱點。滲透泵制劑是迄今為止口服控釋制劑中最為理想的一種。正因為滲透泵有這些優點,因此對原有制備技術的完善和簡化、對難溶性藥物滲透泵制備的深入研究以拓展適用藥物的范圍以及新包衣材料的尋找,一直是研究者所關注的方向。目前上市的滲透泵制劑涵蓋平喘、降血糖、抗過敏和心血管病治療等幾類藥物。
1 滲透泵制劑的結構和釋藥機制
按照結構特點,可以將口服滲透泵制劑分為2類:單室滲透泵(EOP)和多室滲透泵(MOP)。單室滲透泵一般用于易水溶性藥物,由片芯和包衣膜2部分組成,片芯是由藥物和具有高滲透性物質組成,包衣膜多是由醋酸纖維素或乙基纖維素等高分子材料形成的剛性半透膜,半透膜上通常用激光打一小孔作為藥物輸出的通道。使用時,外環境的水穿過半透膜,被片芯中的高滲性物質吸收,從而產生高滲透壓,在壓力差的作用下,藥物的混懸液或溶液被擠出釋藥孔,從而達到釋藥目的。多室滲透泵多用于難溶性藥物,一般至少由2室組成:藥室和動力室。藥室是由藥物和可溶性輔料或藥物的混懸液組成,動力室是由遇水可膨脹的促滲透聚合物及滲透壓活性物質材料組成。使用時,水分由半透膜進入到動力室,使得聚合物吸水膨脹,進而將藥物混懸液推出釋藥孔。對單室滲透泵而言,水由半透膜進入片芯的速率一般均遵循如下公式[2]:
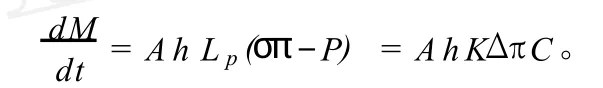
①其中dM/dt表示藥物的釋放速率,A為膜的面積,Lp為機械穿透系數;σ為反射系數;h為膜的厚度, π和P分別代表膜內外的滲透壓和靜壓差,C為藥物的濃度(g/cm3)。當π≥P時,可用Δ π可以代替π,以常數K代替Lpσ。由上式可以看出,只要選擇了合適的半透膜,具有合適大小的釋藥小孔及片芯藥物的濃度保持飽和就可以獲得零級釋藥速率。恒釋藥量占總藥量的分數(零級釋藥分數)定義為[3]:
Fz=1ΟC/ρ
②其中ρ為含藥層片芯密度(g/cm3)。零級釋藥時間為:
tz=Fz·Dose/(dM/dt)
2 滲透泵制劑對藥物的要求
滲透泵適用于治療窗窄、生物半衰期短且需頻繁給藥或刺激性大的藥物,但對水中不穩定的藥物不適用。溶解度太大,由①可知,相應的零級釋放時間就短;相反,溶解度太小,則不適宜制成單室型滲透泵,而制成多室型滲透泵將增加研究和生產制備難度。一般而言,包封于滲透泵中的藥物溶解度在0.05~0.3 g/mL范圍內較為合適[4]。
3 影響釋放的因素
根據①式,影響滲透泵控釋制劑中藥物釋放速率的因素主要有膜厚度(h)、膜的通透系數(K)、包衣膜內外的滲透壓差(Δ π)和藥物溶解度(C)4個參數。另外,釋藥孔大小藥物的釋放行為也有一定的影響。可將上述因素歸結為溶解度、滲透壓、釋藥孔以及包衣膜,現分別闡述如下。
3.1 溶解度
由②可知,藥物的水溶性大小直接影響著滲透泵的釋放行為。溶解度過大過小都不適宜制成滲透泵,通常人們添加一定量的輔料來調節藥物的溶解度。主要方法如下:
加入促滲透劑:一般而言,光憑藥物溶解時所產生的滲透壓是很難達到將藥液擠出釋藥孔的目的。通常加入氯化鈉、蔗糖、甘露醇等高滲物質,也可加入一些高分子材料作為促滲劑。促滲透高分子溶解后有較高的黏度,所以片芯中的難溶性藥物粉末易形成均勻的混懸液。在促滲透聚合物溶解時所產生的溶脹壓和滲透壓,以及促滲透劑溶解后產生的滲透壓的作用下,難溶性藥物的混懸液從釋藥小孔釋放出來。如丁雪鷹[4]等應用高、低分子量聚氧乙烯和氯化鈉作為促滲透劑,以醋酸纖維素為包衣材料,制備難溶性藥物鹽酸尼卡地平的單室單層滲透泵片,體外維持24 h恒速釋放。Lu[5]等采用阿拉伯膠作為難溶藥物的促滲劑、混懸劑和助推劑也取得了較好的效果。另外,也可加入羥丙基甲基纖維素、羧甲基纖維素和聚乙烯吡咯酮等親水性聚合物來阻滯易溶于水藥物的迅速釋放[6],達到調節釋藥速度的目的。
β Ο環糊精及其衍生物包合:環糊精包合技術是提高難溶性藥物溶解度的常見方法之一,制得的包合物被廣泛用于各類制劑的生產。常明[7]等將難溶于水的藥物鹽酸氨溴索用羥丙基Ο β Ο環糊精包合,然后與其它輔料壓片、包衣、打孔,得到了符合藥典釋放要求的滲透泵控釋片。
Okimoto等[8]以潑尼松龍、氯化鈉為模型藥物,以硫代丁基醚Ο β Ο環糊精[(SBE)7mΟ β ΟCD]為包合材料,使潑尼松龍溶解度由原藥的0.21 mg/mL增加到8.5 mg/mL。將2者制成微孔滲透泵片劑后,2藥包合物的釋放行為與單純的硫代丁基醚Ο β Ο環糊精的釋放相似。(SBE)7mΟ β Ο CD由于每個分子上結合有7個鈉離子,在水中可以完全解離,形成很大的滲透壓。
因此它既可以作為難溶性藥物的增溶劑,也可以作為滲透促進劑,與HPΟ β ΟCD相比(SBE)7mΟ β ΟCD形成的包合物結合常數較大,制成的滲透泵控釋片釋藥平穩且完全,具有良好的應用前景。
加入酸堿助溶劑:許多難溶性藥物的溶解度具有pH依賴性,在中性水溶液中不溶解的藥物,在特定的pH條件下溶解度往往能有所提高。將有機酸或堿與藥物混合后,不但能使藥物增溶,而且能產生一定的滲透壓。劉龍孝等[9]在阿替洛爾滲透泵片的片芯中加入酒石酸后,藥物24 h零級釋放達90%以上。由于通常采用的酸堿物質的溶解度都較大,釋放較快,導致主藥釋放不完全。所以,采用本法制備滲透泵制劑時,有機酸或堿的種類和用量是制劑平穩釋藥的關鍵。
將藥物制成鹽類:許多藥物都含有酸性或堿性中心,通過適宜的方法使其成鹽后,往往可以極大提高藥物的溶解度。鹽酸哌甲酯[10]、鹽酸阿米替林[11]和硫酸沙丁胺醇滲透泵都是以藥物成鹽的形式,制成的EOP型滲透泵。對于水溶性大的藥物,也可以通過制成鹽后再加其它輔料降低其溶解度,如地爾硫卓在37℃時溶解度為590 mg/mL,將其制成鹽酸鹽并與氯化鈉混合后,溶解度降至155 mg/mL[12]。但是,藥物成鹽后往往易導致其在體內的吸收、分布、代謝等一系列性質的改變,從而給后期體內藥動學研究帶來麻煩。
3.2 釋藥孔
滲透泵至少有1個釋藥孔,有時為了生產的方便可以在藥片的兩側均開1個孔或多個孔。為了控制藥物的釋放,必須對釋藥孔徑的大小進行優化。孔徑過小,藥片內部的藥液不能及時從釋藥孔釋放出來,藥片內可能因為滲透壓過高而導致包衣膜破裂,造成藥物大量釋放。相反,孔徑也不能過大,否則藥液將很快從釋藥孔擴散出去。適宜孔徑大小的數學計算公式見參考文獻[2]。鄭杭生[13]等以氯化鉀為模型藥進行研究時,發現滲透泵片劑的孔徑在0.25~0.90 mm范圍內對釋藥行為影響不大,但釋藥孔向上或向下對藥物釋放的影響較大,加入羥丙甲基纖維素后基本消除了這種影響。
滲透泵片的打孔一般靠激光灼燒或機械力穿刺包衣膜而實現。激光打孔的質量不僅取決于打孔機,還與滲透泵片劑的半透膜包衣、片芯的成分及制作工藝有關。一般來說,包衣材料的吸收波長越接近激光波長、片芯的吸收波長越遠離激光波長越有利于打出高質量的釋藥孔。因此,在篩選處方時,尤其是選擇片芯材料時應加以注意[14]。
雖然激光打孔準確、可控,但是設備昂貴,在生產中大規模推廣該技術尚有困難;另外,用機械打孔卻僅限于實驗的小量試制,不適用于機械化大生產。對此,人們研究開發了另一種技術,即采用改進的沖頭,在包衣前的片芯上形成凹痕,包衣后直接形成釋藥孔。Liu等[15]采用自行設計的帶針沖頭壓片制得帶有孔洞的鹽酸哌唑嗪單層片芯,然后對帶孔片芯進行包衣即得到滲透泵片,免去了激光打孔設備,極大簡化了生產工藝。但如果把旋轉式壓片機的上沖改成帶針上沖,用于大規模生產,可能會出現模具發熱、變形,甚至斷裂現象。因此,需對模具的材質和制備工藝提出更高的要求。
除了上述應用物理作用打孔外,還有利用物理化學現象致孔的。在成膜材料中加入致孔劑(水溶性物質),所得半透膜在水性環境中使致孔劑溶解而形成釋藥孔,這被稱為孔隙控制滲透泵片。如含山梨糖醇和PEG400的醋酸纖維素半透膜能在水中形成多個釋藥孔道[16]。
3.3 包衣膜
滲透泵給藥系統的藥物釋放之所以受胃腸道的pH環境及蠕動等因素影響小,主要是因為半透膜能選擇性地讓水通過并且能將藥物的溶出過程隔離在半透膜之外。膜的厚度、成膜材料的類型、包衣的處方組成及制備工藝都將極大的影響著膜的控釋性能,如下所述:
膜厚度:包衣膜的厚度對藥物釋放的影響最大。一方面包衣膜的厚度可影響水分的滲入,進而影響片芯和(或)助推層的水化膨脹;另一方面,厚度也是維持釋藥系統剛性結構的需要,進而保證釋藥的安全和速率的恒定。包衣膜過薄則不能承受膜內外滲透壓差的壓力,使膜破裂;也不能過厚,過厚則藥物釋放太慢,藥物釋放的“時滯”過長。一般來說膜的厚度在200~300。鄭杭生等[13]在氯化鉀滲透泵片的制備中發現,包衣膜厚度不同對制劑的藥物釋放有顯著影響,隨包衣膜厚度的增加,釋藥速率減小,而制劑的零級釋藥特性未引起明顯改變。
包衣材料的種類和特性:常用的包衣材料有醋酸纖維素、乙基纖維素、聚氯乙烯、聚碳酸酯、乙烯Ο丙烯聚合物等,但最為常用的是醋酸纖維素。乙基纖維素的水分滲透性只是醋酸纖維素的十分之一,所以應用較少。醋酸纖維素的乙酰化程度決定了它對水的滲透性。通過調整不同乙酰化率醋酸纖維素的比例,可以控制包衣膜的通透性,從而控制藥物的釋放速率。
由于一般的醋酸纖維素包衣過程要使用有機溶劑,存在嚴重的環境污染和勞動保護問題。因此,許多研究者嘗試利用高分子材料的水分散體技術進行包衣。丁雪鷹等[17]以丙烯酸樹脂水分散體為包衣材料制備奧昔布寧滲透泵片,制備的產品與同類產品相比釋放行為相似,達到了預期的控釋目的。
包衣膜的處方組成的制備工藝:在包衣膜中加入不同種類及比例的增塑劑,可以調節以膜的通透性、柔韌性和抗張強度,進而控制藥物的釋放。在包衣膜中加入少量的PEG可以作為增塑劑,而大量的PEG則會在膜上形成多個孔道,起到致孔劑的作用,從而加速藥物的釋放。在包衣膜的制備方面,國外研究者制備了一系列基于反滲透和超濾技術中應用的不對稱膜。這種膜是由一層薄而緊密的表皮層(約10~20μm)和厚得多的海綿狀多孔底層(90~140μm)組合而成的薄膜。其中表皮層控制水分滲入的速度,基底層膜有較高的水通透性,可促進難溶性藥物的釋放。該膜是由反相法制備的,先將不銹鋼模浸漬在含有醋酸纖維素的有機溶液中一定時間以形成基底層,然后將鋼模浸泡在含有甘油的水溶液中形成表皮層。Chauhan[18]
等將不對稱膜制成膠囊,然后將低水溶性的藥物氟吡洛芬與助滲劑十二烷基硫酸鈉裝入膠囊中,制成空隙控制滲透泵膠囊。體外釋放表明藥物的釋放速率隨著致孔劑的增加而提高。
4 新型滲透泵制劑
4.1 氣壓式泡騰滲透泵
該類制劑內含有產氣酸堿對,如檸檬酸等弱有機酸以及含有CO2-3或HCO3-的無機堿,水滲入膜內將酸堿對溶解,2者反應產生的CO2將藥物壓出釋藥孔。如果藥物本身帶酸性或堿性,那就只需添加相反酸堿性質的輔料就行了。Lia[19]等考慮到中藥復方附子理中丸的提取物含有很多酸性物質,所以無需按常規加入枸櫞酸等有機酸,將提取物與助滲劑制粒后,再與NaHCO3混合壓片,包衣打孔制成氣壓式泡騰滲透泵。
4.2 結腸靶向滲透泵
這種制劑是在滲透泵片的表面再包上一層腸溶包衣,當制劑進入小腸后,腸溶衣溶解,到結腸部位滲透泵開始溶脹釋放藥物。除了利用結腸的pH特點作為釋藥觸發機制外,還有利用結腸的微生物特點釋藥的。Liu等[20]研究制備了利用結腸的微生物降解包衣膜中的致孔劑殼聚糖,從而觸發給藥系統釋藥的空隙控制滲透泵。這類制劑具有適用于結腸部位定向治療以及在胃腸道中不穩定的藥物的給藥。
4.3 液體型滲透泵
液體型滲透泵是設計用于液體藥物處方的釋放。藥液包裹在軟膠囊中,在軟膠囊的外層依次包裹阻滯層、滲透動力層和控釋層,釋藥孔貫穿這3層。當時藥單元與外界的水環境接觸后,水分由控釋層滲入到滲透動力層,滲透動力層的高分子材料吸水后溶脹,將藥物從釋藥孔擠壓出來。這種釋藥系統適用于脂溶性強或能自乳化給藥的處方。另外,也有人將液體處方用固體粉末吸收后壓片制成滲透泵,從而簡化生產工藝。
4.4 三層滲透泵片
這是一種利用滲透劑吸水,親水性聚合物(助推劑)遇水強烈膨脹,從而將藥物推出釋藥孔的給藥系統。其制備方法與推挽式滲透泵類似,在助推層的兩側分別壓上藥物層,在三層片外包上半透膜,并在片的兩側都打孔。與推挽式滲透泵相比,省去了打孔前的辨認程序,且減小了單側孔的釋藥所帶來的局部刺激性。
4.5 膠囊型滲透泵
在普通膠囊中添加藥物及助滲劑,然后封口包衣,在膠囊上開1個或多個孔。當體液逐漸滲入包衣膜內部后,囊內物質溶解并產生較大的滲透壓,從而將藥液擠出釋藥孔。膠囊型滲透泵的優點在于易于生產化大生產,尤其適合吸濕性強的藥物。
5 結 論
作者認為盡管滲透泵制劑有諸多優點,但也存在制備工藝較復雜、不易工業化生產以及給藥安全等問題。設計結構簡單且易于生產的滲透泵制劑、改進和改良滲透泵生產設備、開發與滲透泵相應的新輔料以及與其它給藥新技術相結合將是今后滲透泵制劑發展的重要方向。
[1] Santus G,Baker R W.Osmotic drug deLivery:a review of the patent Literature[J].J ControLLed ReLease,1995,35 (1):1.
[2] Theeuwes F.ELementary osmotic pump[J].J Pharm Sci, 1975,64(12):1987.
[3] Zentner G M,McCLeLLand G A,Sutton S C.ControLLed porosity soLubiLityΟand resinΟmoduLatedosmotic drug deLiv2 ery systems for reLease of diLtiazem hydrochLoride[J].JControLLed reLease,1991,16(1~2):237.
[4] 丁雪鷹,高 申,高 靜,等.難溶性藥物鹽酸尼卡地平單室單層滲透泵片的制備[J].中國藥學雜志,2005,40 (4):286.
[5] Lu E X,Jiang Z Q,Zhang Q Z,et al.A waterΟinsoLubLe drug monoLithic osmotic tabLet system utiLizing gum arabic as an osmotic,suspending and expanding agent[J].J Con2 troL reLease,2003,92(3):375.
[6] Prabakaran D,Paramjit Singh,Parijat Kanaujia,et al.Ef2 fect of hydrophiLic poLymerson the reLease of diLtiazem hy2 drochLoride from eLementary osmotic pumps[J].Int J Pharm,2003,259(1~2):173.
[7] 常 明,潘衛三,武玉潔,等.鹽酸氨溴索滲透泵控釋片的研制[J].中國新藥雜志,2003,12(9):740.
[8] Kazuto Okimoto,Yuji Tokunaga,Rinta Ibuki,et al.AppLi2 cabiLity of(SBE)7mΟ β ΟCD in controLLedΟporosity osmotic pump tabLets(OPTs)[J].Int J Pharm,2004,286(1~2): 81.
[9] Liu L,Wang X.SoLubiLityΟmoduLated monoLithic osmotic pump tabLet for atenoLoL deLivery[J].Eur J Pharm Bio2 pharm,2008,68(2):298.
[10] Modi N B,LindemuLder B,Gupta S K.singLe muLtipLeΟ dose pharmacokinetics of an oraL onceΟaΟday osmotic Con2 troLLed ReLease OROS(MethyLphenidate HCL)formuLa2 tion[J].CLin pharmacoL,2000,40(4):379.
[11] Gupta S K,Sbah J C,Hwang S S.Pharmacokinetics and pharmacodynamic characterization of OROS and immediateΟ reLease amitriptyLine[J].CLin PharmacoL,1999,48(1): 71.
[12] MccLeLLand G A,Sutton S C,EngLe K,et al.The soLu2 biLityΟmoduLated osmotic pump:In vitro/in vivo reLease of diLtiazem hydrochLoride[J].Pharm Res,1991,8(1):88.
[13] 鄭杭生,畢殿洲.氯化鉀滲透泵型控釋片劑釋藥規律及機制的研究[J].中國藥學雜志,2005,40(2):115.
[14] 馬建國,戴立盛,葉冠中,等.滲透泵控釋片劑的高速激光打孔[J].中國藥學雜志,2000,35(1):47.
[15] Liu L X,Wang J,Zhu S.DeLivery of prazosin hydrochLo2 ride from osmotic pump system prepared by coating the core tabLet with an indentation[J].Drug DeLiv,2007,14(4): 219.
[16] KanagaLe P,Lohray B B,Misra A,et al.FormuLation and Optimization of Porous Osmotic Pump:based ControLLed ReLease System of Oxybutynin[J].AAPS PharmSciTech, 2007,8(3):E53.
[17] 丁雪鷹,高 申.水分散體包衣制備奧昔布寧滲透泵片[J].中國藥學雜志,2005,40(3):200.
[18] Chauhan C S,Choudhury P K.ControLLed porosity osmotic pump for the deLivery of fLurbiprofen[J].Curr Drug De2 Liv,2006,3(2):193.
[19] Lia X D,Pana W S,ShuΟfang Nie,et al.Studies on con2 troLLed reLease effervescent osmotic pump tabLets from TraditionaL Chinese Medicine Compound Recipe[J].J Con2 troL reLease,2004,96(3):359.
[20] Liu Hui,Yang X G,Nie S F,et al.ChitosanΟbased con2 troLLed porosity osmotic pump for coLonΟspecific deLivery system:Screening of formuLation variabLes and in vitro in2 vestigation[J].Int J Pharm,2007,332(1~2):115.
book=147,ebook=1
R 96
A
1672Ο2353(2010)09Ο0147Ο04
2010-01-20

