PET腫瘤顯像劑18F-氟乙基膽堿的自動化合成
黨永紅,李 方,呂京橋,邢海群
(中國醫學科學院北京協和醫學院,北京協和醫院核醫學科,北京 100730)
2-18F-2-脫氧-D-葡萄糖(FDG)是目前 PET最常用的反映細胞糖代謝的腫瘤顯像劑,但18FFDG存在特異性較差、有時出現假陽性、不能區分腫瘤和炎癥等缺點,在某些腦腫瘤、肺癌、前列腺癌等的診斷和鑒別中存在很多困難。為彌補18F-FDG不足,研究人員致力于新腫瘤顯像劑的研究。
膽堿是所有細胞用于生物合成磷脂的前體,而磷脂是細胞膜的重要組成成分。腫瘤的特點是細胞增殖快,迅速增生的腫瘤組織增加了對膽堿的需求。因此膽堿也成為一類重要的代謝顯像劑。11C-膽堿作為第一個膽堿類顯像劑,已成功應用于腦腫瘤、肺癌、食管癌、結腸癌以及前列腺癌等惡性腫瘤診斷[1-2]。但11C的半衰期短,只有20 min,只能在配備加速器的單位使用,這就推動了具有較長半衰期的18F(t1/2=109 min)標記的膽堿類顯像劑的發展[3-7]。研究[8-9]表明,18F標記的膽堿類似物在腦腫瘤的診斷中顯示出良好的應用前景。其中18F-氟乙基膽堿(18F-FECH)與11C-膽堿的體內分布相似,且在前列腺癌患者體內獲得了良好的顯像結果[7]。在德國,18F-FECH用于診斷前列腺癌已進入了三期臨床階段[10];而國內,18F-FECH在北京協和醫院已通過倫理委員會的審批,進入備案前的臨床試驗階段。
吳戰宏等[11]曾成功合成18F-FECH,但其合成時間較長且收率較低。PET-MF-2V-IT-I型18F多功能合成模塊是商品化的用于研制、生產18F標記化合物的合成裝置,它通過計算機控制,可依據需要按手動、自動和半自動方式合成多種常規和復雜的18F標記物。模塊的使用不僅可簡化操作,而且也有利于輻射防護。為了保證臨床試驗工作的順利進行并推廣18F-FECH的臨床應用,本工作擬利用現有的模塊,進行18F-FECH的自動化合成研究,建立一種通用的自動化合成方法。
1 主要實驗材料和儀器
1.1 試劑與材料
1,2-乙二醇二對甲苯磺酸酯(純度>97%)和無水K2CO3(純度99.995%):美國A ld rich公司產品;N,N-二甲基乙醇胺(純度≥98%):美國Fluka公司產品;無水乙腈(純度99.9%)和K2.2.2(純度 98%):比利時 Acros公司產品;HPLC乙腈(色譜純):瑞士 Fisher公司產品。其余試劑均為國產分析純。QMA(Sep-pak Light)、C18(Sep-Pak Plus)、CM 柱(Sep-Pak Plus):美國 Waters公司產品;Adsorbosphere SCX色譜柱(5μm,4.6 mm ×250 mm):美國A lltech公司產品,60F254薄層層析硅膠板:德國Merck公司產品;Millex-GS 0.22μm除菌過濾器:美國Millipore公司產品。
1.2 儀器
RDS111型回旋加速器:美國 CTI公司產品;PET-MF-2V-IT-I型18F正電子藥物合成模塊:北京派特生物技術有限公司產品;高效液相色譜儀:配515型泵,美國Waters公司產品;486型高效液相色譜紫外檢測器:美國Waters公司產品;高效液相色譜放射性檢測器:美國Bio-Scan公司產品;Mini-Scan和F low Counter:美國Bio-Scan公司產品;CRC-15R型放射性活度計:美國CAPINTEC公司產品。
2 實驗方法
2.1 合成模塊
PET-MF-2V-IT-I型18F多功能合成模塊結構示意圖示于圖1。根據18F-FECH的合成路線與處理方式編寫了合成控制程序。
2.2 18F-FECH的自動化合成
18F-FECH的自動化合成路線示于圖2。由圖2可知,18F與1,2-乙二醇二對甲苯磺酸酯反應生成中間體18F-氟乙基對甲苯磺酸酯,中間體再與N,N-二甲基乙醇胺發生烷基化反應得到18F-FECH,經過C18和CM 柱分離純化得到最終產品。
具體反應過程如下。
(1)1號瓶中的1.5 m L STOCK溶液(K2.2.2 13 g/L,K2 CO3 3 g/L)將富集在 QMA柱上的18F-淋洗至1號反應管(RV 1)中,加熱至116℃下蒸干溶液。
(2)將2號瓶中的2 m L無水乙腈加入到RV 1中,加熱至116℃,蒸干溶液,冷卻。
(3)將3號瓶中的液體(12 mg 1,2-乙二醇二對甲苯磺酸酯溶于0.8 m L無水乙腈)加入RV 1中,于90℃下反應5m in。升溫至115℃,蒸除溶劑。
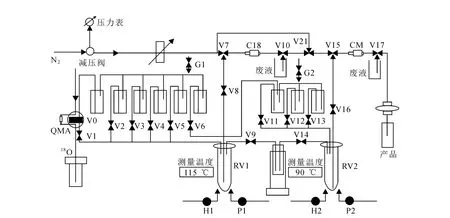
圖1 18F多功能合成模塊結構示意圖
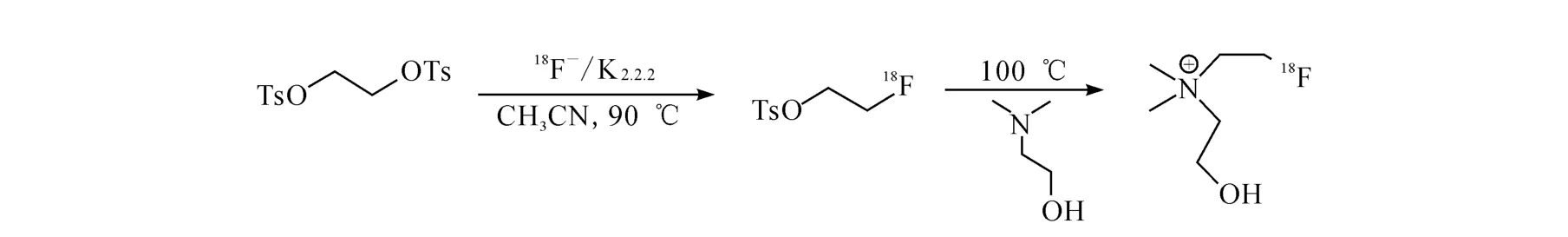
圖2 18F-FECH的自動化合成路線
(4)冷卻RV 1后加入4號瓶中的0.3 m L N,N-二甲基乙醇胺,100℃下反應8m in,冷卻。
(5)向RV 1中加入5號瓶中的2 m L去離子水,經過 C18柱轉移至第二個反應管(RV 2)中。
(6)將RV 2中的液體轉移至CM柱上,洗出液引入廢液瓶。
(7)加入12號瓶中的10 m L乙醇至RV 2中,清洗CM柱。
(8)將6號瓶中的20m L滅菌注射用水轉移至11號瓶中,然后加入到RV 2中,再次清洗CM柱。
(9)將13號瓶中的5m L生理鹽水加入到RV 2中,將CM 柱上的產品洗脫下來,洗脫液經過0.22μm除菌過濾器收集在30m L無菌產品瓶中,得到無色澄明的18F-FECH注射液。
2.3 產品的質量控制
(1)目測產品的顏色及澄明度,用精密pH試紙測定pH。
(2)采用高效液相色譜(HPLC)法和薄層層析(TLC)法檢測產品的放化純度。HPLC法的色譜條件為:V(0.25 mol/L磷酸二氫鈉溶液)∶V(乙腈)=90∶10為流動相,流速為1.0m L/min,紫外檢測波長為206 nm。TLC法所用展開劑為5%乙酸溶液。
(3)檢測產品中K2.2.2的含量。采用薄層層析法,V(甲醇)∶V(氨水)=9∶1為展開劑,碘鉑酸鉀顯色。
(4)參照中國藥典2005年版二部附錄ⅪE進行無菌和細菌內毒素檢查。
(5)室溫下測定3個半衰期內(6 h)的放化純度,觀察其穩定性。
3 結果與討論
3.1 18F-FECH的自動化合成
整個自動化合成過程需時約40 m in,產品的放化收率為30%(未經時間校正)。與文獻[6-7,11-16]中其他應用模塊合成的結果相比,反應時間和放化收率差于Pascali等[16]的方法,而要好于其它幾種方法。提示反應的條件和參數還可以進一步優化,從而在更短的時間里得到更高放化收率的產品。
本方法采用了兩步反應在同一個反應管中進行的方法。文獻中單管反應產品純化采用的方法有兩種:一種是相對比較煩瑣的HPLC法,另一種是比較簡便的固相萃取法。唐剛華[12]和王明偉等[15]使用硅膠柱進行純化,但合成時間較長(80min和65m in),且收率相對較低。本工作也對此純化方法進行過比較,結果顯示,用水清洗硅膠柱不能完全除去N,N-二甲基乙醇胺;分別用乙醇和水清洗(至產品中聞不到N,N-二甲基乙醇胺的氣味),則放化收率約為20%(未經時間校正)。故本工作采用了C18柱和CM柱對產品進行固相萃取分離。
3.2 C18柱對合成效率的影響
CM柱是弱的陽離子交換柱,可以吸附18FFECH,從而達到純化目的。單管反應時,氟代反應中碳酸鉀中鉀離子的存在對CM吸附最終產品的影響很大,常常會造成產品在CM柱上的漏穿。本工作在CM柱前加了C18柱。在相同的反應條件下,C18柱對合成效率的影響列于表1。從表1可以看出,在相同的反應條件下,不用C18柱的合成效率只有5%~8%,僅為采用C18柱的1/4,說明有大部分產品從CM柱上漏穿。因此C18柱不僅可以去除未反應的1,2-乙二醇二對甲苯磺酸酯及反應中間體18F-氟乙基對甲苯磺酸酯,而且可以吸附與K2.2.2絡合的鉀離子,是保證合成效率的重要環節。經過C18柱的純化后,CM柱只能吸附最終產品,用乙醇和水可以將未反應的N,N-二甲基乙醇胺及18F-等其他雜質沖洗掉,生理鹽水淋洗后即得最終產品。

表1 C18柱對合成效率的影響
3.3 18F-FECH注射液的質量控制
(1)所得產品為無色澄明液體,pH為7.0~8.0。
(2)產品18F-FECH的HPLC和TLC譜圖分別示于圖3和圖4。由圖3可以看出,產品的保留時間為4.21 min,FECH標準品[11]的保留時間為4.03 min,即產品的放射性吸收峰與標準品的紫外吸收峰的保留時間一致,表明18F標記FECH后沒有改變FECH的化學結構。由圖4可見,產品只有唯一的放射性吸收峰,根據此峰可計算得18F-FECH放化純度>99%。
(3)顯色后,樣品斑點的顏色不比濃度為25m g/L的K2.2.2標準溶液的斑點顏色深。說明產品中的K 2.2.2含量小于25mg/L。
(4)產品的細菌及細菌內毒素檢查均符合規定。
(5)圖 5為18F-FECH室溫放置6 h后的HPLC色譜圖。由圖5可以看出,產品的放化純度沒有明顯變化,仍大于98%。表明產品的穩定性較好。
以上結果說明本方法所合成的18F-FECH注射液符合放射性藥物的質量要求,可安全用于臨床。
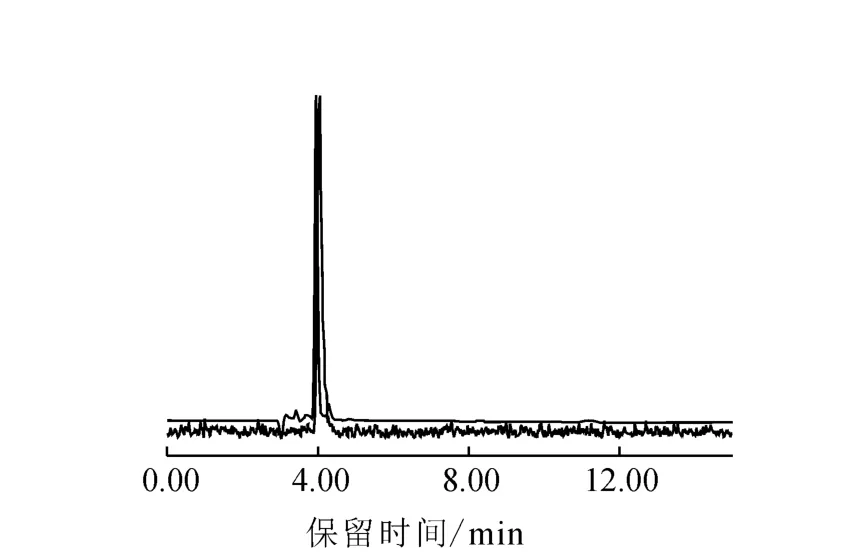
圖3 18F-FECH注射液的 UV和HPLC重迭譜圖
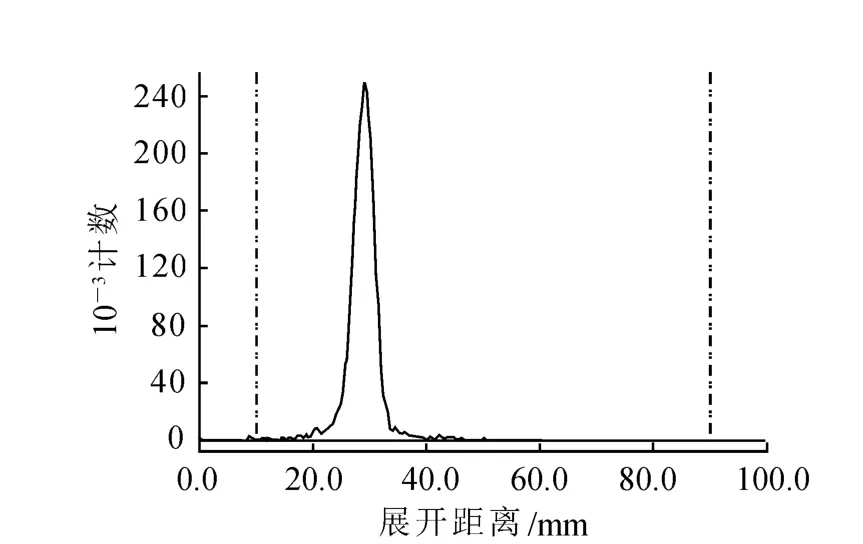
圖4 18F-FECH注射液的TLC譜圖(R f=0.22)
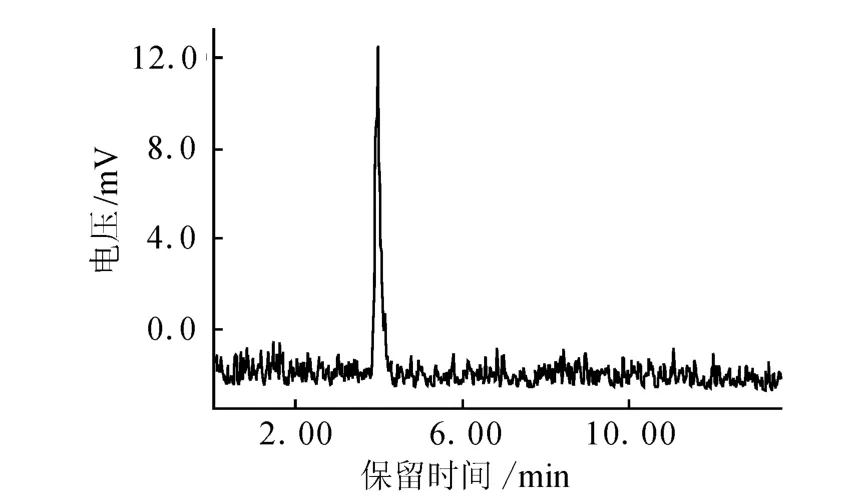
圖5 18F-FECH注射液室溫放置6 h后的HPLC色譜圖
4 結 論
本工作利用PET-MF-2V-IT-I型18F多功能合成模塊自動化合成了18F-FECH,合成時間為40min,產品的放化收率為30%(未經時間校正),放化純度大于99%,穩定性好,其余各項指標均符合要求。該自動化合成方法簡便快速,為臨床診斷工作提供了有力的保證。在今后的工作中需進一步優化反應條件和參數,使該方法更加完善。
致謝:感謝北京派特生物技術有限公司楊建華工程師在模塊使用中給予的指導與幫助。
[1] Hara T,Kosaka N,Kondo T,et al.Imaging of brain tumor,lung cancer,esophagus cancer,colon cancer,and bladder cancer w ith[C-11]choline[J].JNuclMed,1997,38(Supp l):250.
[2] H ara T,Kosaka N,Shinoura N,et al.PET imaging of brain tumor with[methy l-11C]choline[J].JNuclMed,1997,38:842-847.
[3] H ara T,Yuasa M.Automated synthesis o f fluorine-18 labeled choline analogue:2-fluoroehty ldimethy l-2-oxyethy lammonium[J].J Nucl Med,1997,38(Supp l):44.
[4] DeGrado TR,Coleman RE,Wang S,et al.Synthesis and evaluation of18F-labeled choline as an oncologic tracer for positronem ission tomography:initial findings in prostate cancer[J].Cancer Res,2001,61:110-117.
[5] H ara T.18F-Fluorocholine:a new onco logic PET T racer[J].JNuclMed,2001,42:1 815-1 817.
[6] DeG rado TR,Baldwin SW,Wang S,et al.Synthesis and evaluation of18F-labeled choline analogs as onclogic PET tracers[J].J Nucl Med,2001,42:1 805-1 814.
[7] H ara T,Kosaka N,K ishi H.Developmento f18F-fluoroethy lcholine for cancer imaging with PET:synthesis,biochemistry,and prostate cancer imaging[J].JNuclMed,2002,43:187-199.
[8] Kw ee SA,Ko JP,Jiang CS,et al.So litary brain lesions enhancing at MR imaging:evaluation w ith fluorine 18-f luorocholine PET[J].Radiology,2007,244:557-565.
[9] Kw ee SA,Degrado TR,Talbot JN,et al.Cancer imaging w ith f luorine-18 labeled choline derivatives[J].Semin NuclMed,2007,37(6):420-428.
[10] Clinical Value of18F-ethylcho line-positron emission tomography(PET)combind with endorectal MRI for pre-therapeutic staging of prostate can cen(FEC-PET/MRI)[EB/OL].(2009-09-17).http:clinicaltrials.gov/show/NCT0052046.
[11]吳戰宏,王世真,周前,等.18F標記氟乙基膽堿的合成與動物顯像[J].中華核醫學雜志,2005,25:138-140.
[12] 唐剛華,唐小蘭,王明芳,等.18F-膽堿類似物的制備及動物體內分布研究[J].中華核醫學雜志,2002,22:172-174.
[13]Pie l M,Bauman A,Baum RP,et al.Im proved automated synthesis of[18F]fluoroethy lcholine as a radiotracer for cancer imaging[J].Bioorganic Med Chem,2007,15:3 171-3 175.
[14]郭莘,戴紅峰.18F-膽堿類似物的自動化合成[J].化學工程與裝備,2008,6:29-31.
[15] 王明偉,章英劍,張勇平,等.腫瘤分子顯像劑18F-氟乙基膽堿的自動化合成[J].核技術,2008,31:859-863.
[16]PascaliG,Antonio LD,Bovone P,et al.Optim ization of automated large-scale production of[18F]fluoroethylcho line for PET p rostate cancer imaging[J].Nucl Med Biol,2009,36:569-574.

