鹽酸洛美沙星注射液與利巴韋林注射液配伍穩定性考察
李紅月,羅朝利,宋 暢
(中國人民解放軍北京軍區北戴河療養院,河北 秦皇島 066001)
鹽酸洛美沙星(lomefloxacin hydrochloride,LFLX)系第3代喹諾酮類廣譜抗菌藥物,目前廣泛應用于治療敏感細菌引起的呼吸道、泌尿生殖道、膽道、腸道、皮膚軟組織感染以及中耳炎、鼻竇炎等。利巴韋林(rihbavirin,RIB)為具有抑制病毒活性的合成核苷酸類衍生物。筆者對上述2種藥物的配伍穩定性進行了研究,現報道如下。
1 儀器與試藥
7550型紫外-可見分光光度計(上海分析儀器廠);PC數據處理裝置;PHS-3C型酸度計(上海虹益儀器儀表有限公司);HH-400型電熱恒溫培養箱(北京市朝陽區廣營醫療器械廠)。洛美沙星對照品(中國藥品生物制品檢定所,批號為0452-200001);鹽酸洛美沙星注射液(吉林康乃爾藥業有限公司,批號為200209120);利巴韋林原料(藥用規格);鹽酸洛美沙星原料(藥用規格);利巴韋林注射液(上海通用藥業股份有限公司第三公司,批號為0212771)。
2 方法與結果
2.1 測定波長選擇
配制鹽酸洛美沙星對照品溶液(質量濃度為8 μg/mL)及利巴韋林溶液(質量濃度為10 μg/mL),分別在200~400 nm波長范圍內掃描。結果鹽酸洛美沙星在282.0 nm波長處有最大吸收,利巴韋林在206.0 nm波長處有最大吸收,這與文獻[1-2]報道基本相符。鹽酸洛美沙星與利巴韋林配伍時紫外吸收光譜顯示,鹽酸洛美沙星在282.0 nm波長處,利巴韋林、葡萄糖無干擾,故采用282.0 nm作為吸收波長測定鹽酸洛美沙星含量;利巴韋林在206.0 nm波長處,鹽酸洛美沙星有干擾,葡萄糖無干擾,故采用雙波長-等吸收點法[3],以 206.0 nm為測定波長,以267.0 nm為參比波長,測定利巴韋林含量。紫外吸收光譜見圖1。
2.2 方法學考察
標準曲線繪制:精密量取鹽酸洛美沙星注射液與利巴韋林注射液的混合液(每mL含鹽酸洛美沙星0.4 mg,利巴韋林0.5 mg)2.0,3.0,4.0,5.0,6.0,7.0 mL,置 100 mL 量瓶中,加蒸餾水稀釋至刻度。以水為空白,分別在 282.0,206.0,267.0 nm 波長處測定各自的吸光度(A,ΔA),并將各自的 A值對質量濃度(C)作線性回歸,回歸方程見表1。
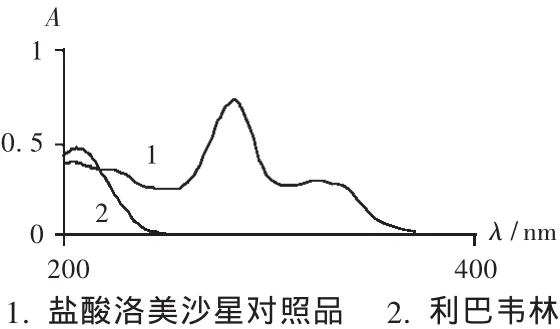
圖1 紫外吸收光譜圖
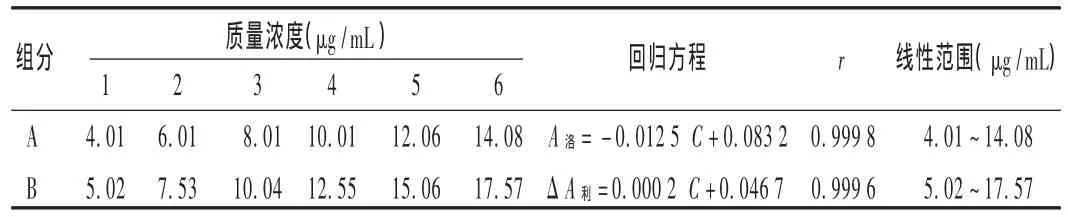
表1 鹽酸洛美沙星和利巴韋林的標準曲線
精密度試驗:選擇標準曲線繪制項下第3種溶液,依法測定5次。結果的 RSD都小于1.06%,表明儀器精密度良好。
重現性試驗:取同批樣品5份,依法測定。結果的 RSD=1.89%(n=5),表明方法重現性良好。
加樣回收試驗:取已知含量、不同質量濃度的配伍液,分別定量加入鹽酸洛美沙星及利巴韋林原料,依法測定。結果見表2。
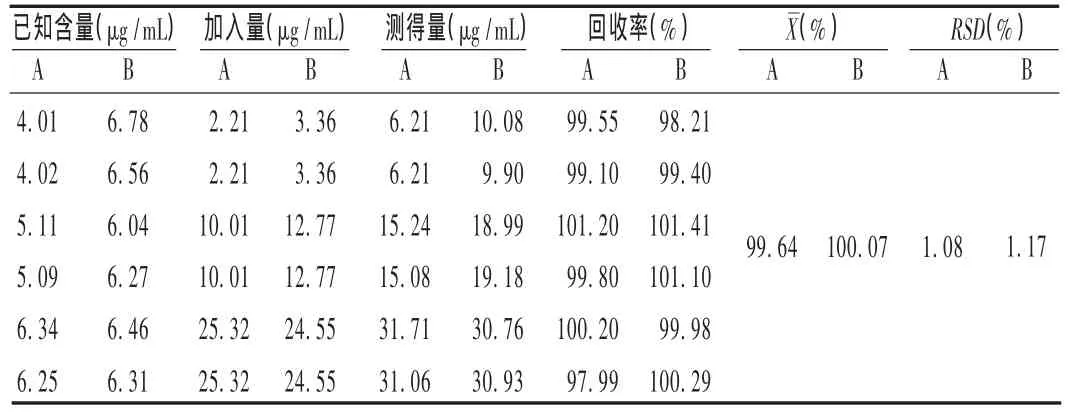
表2 加樣回收試驗結果(n=6)
2.3 樣品穩定性測定
精密量取利巴韋林注射液2.5 mL(模擬臨床用藥量),置250 mL量瓶中,用鹽酸洛美沙星注射液稀釋至刻度,混勻,分別在25℃和37 ℃下放置 0,1,2,4,6 h,觀察外觀、顏色及測定 pH,結果無沉淀產生。同樣時間間隔,精密取樣,稀釋后在200~400 nm波長范圍內掃描,觀察吸收峰峰位及峰形,結果在25℃下6 h內吸收峰峰位及峰形無變化,在37℃下6 h內吸收峰峰位及峰形有變化。在282.0,206.0,267.0 nm 波長處測定各自的吸光度(A,ΔA),代入各自的回歸方程,以0 h的含量為100%,計算相對百分含量(標示量)。配伍液的pH及含量變化見表3。
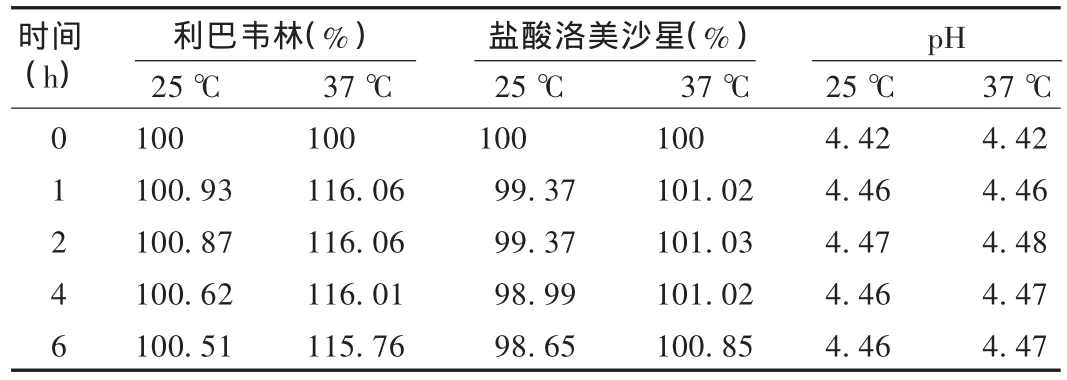
表3 配伍液pH及含量變化
3 討論
鹽酸洛美沙星注射液與利巴韋林注射液配伍,在25℃溫度下6 h內配伍液外觀、pH、含量無明顯變化,兩藥可配伍使用;在37℃條件下,利巴韋林含量明顯升高,具體原因有待進一步研究。建議臨床兩藥配伍使用時,應在25℃ 下6 h內輸完。
[1]陳 漪.天門冬氨酸洛美沙星與利巴韋林注射液配伍穩定性[J].臨床藥學,2002,14(3):152.
[2]劉亞軍,謝燕萍.紫外分光光度法測定利巴韋林葡萄糖注射液中利巴韋林的含量[J].海峽藥學,2000,12(2):30.
[3]安登魁.藥物分析[M].第2版.北京:人民衛生出版社,1986:317.