基于納米氧化鋅-還原氧化石墨烯的分子印跡基于納米氧化鋅-還原氧化石墨烯的分子印跡

摘要利用水熱法合成了納米氧化鋅-還原氧化石墨烯(rGO)復合材料,采用傅里葉變換紅外光譜、X 射線衍射和X 射線光電子能譜確定此復合材料的價態結構。以ZnO-rGO 作為光電化學傳感器的光電轉換材料,以土霉素(OTC)為模板分子,通過電聚合OTC 和吡咯(Py)的方法構建分子印跡光電化學傳感器。將聚吡咯(PPy)膜中的OTC 洗脫后,在PPy 膜中留下OTC 的特異性“印跡孔穴”,從而可對OTC 選擇性識別。在優化的條件下,此傳感器的光電流變化值與OTC 濃度(0.1~200 nmol/L)的對數值具有良好的線性關系,檢出限為0.05 nmol/L(S/N=3)。采用此傳感器對市售牛奶和蜂蜜中的OTC 進行測定,回收率為95%~107%。
關鍵詞光電化學傳感器;氧化鋅-還原氧化石墨烯;聚吡咯;分子印跡;土霉素
土霉素(OTC)是一種廣譜抗菌藥物,具有抗菌性能好、成本低和副作用少等特點[1],被廣泛用于畜牧業和魚類養殖[2]。殘留在環境中的OTC 會導致細菌產生抗藥性,人類食用含有OTC 殘留的食品會導致OTC 在體內積聚并對人體造成損害[3]。2019 年,我國發布的食品安全國家標準(GB 31650—2019)[4]規定牛奶中的OTC 殘留量不得超過100 μg/kg。因此,開發簡單、快速和靈敏檢測食品中OTC 的方法具有重要的應用價值。
目前,常用OTC 檢測方法主要有高效液相色譜法(HPLC)[5]、液相色譜-質譜聯用法[6]、熒光法[7]和電化學法[8-9]等。色譜法的準確度高,但是樣品前處理方法復雜,并且需要昂貴的儀器和專業的操作人員,難以普遍應用,因此需要研究一種簡便、高效的食品中痕量OTC 的檢測方法,以更好地保障食品安全和消費者健康。光電化學傳感器(Photoelectrochemical sensor, PEC sensor)結合了傳統光化學和電化學技術的優點,實現了檢測信號和激發信號完全分離,可以降低背景噪音的干擾,因此具有更高的靈敏度,受到了研究者的廣泛關注[10]。半導體光活性材料在PEC 傳感器中起著極其重要的作用,近年來,研究者已經開發了多種可有效地將紫外光或可見光轉化為光電流的光活性半導體材料,如TiO2[11]、ZnO[12]和Co3O4[13]等。
ZnO 是一種n 型半導體,具有性能穩定、無毒和價廉等優點,在制備ZnO 時可以通過調控合成條件得到不同形貌和光催化性能的ZnO;但是, ZnO 的寬帶隙能(3.20~3.37 eV)限制了其對可見光的吸收,并且ZnO 受到光激發時,其價帶上的電子躍遷到導帶,從而產生電子-空穴對,但導帶上的電子不穩定,容易回到價帶,導致光生電子-空穴對復合率較高[14-15]。研究者采用在ZnO 中摻雜金屬離子[16]或貴金屬[17]、將ZnO 和其它光催化劑進行復合[18]以及通過添加石墨烯及其氧化物[19-21]等方法,改善了ZnO 對可見光的吸收能力,降低了光生電子-空穴對的復合率。還原氧化石墨烯(rGO)是一種比表面積大且化學性質穩定的二維納米材料,廣泛應用于電化學傳感器[22-23]和光電催化[24-27]等領域。Hwa 等[23]采用水熱法合成了摻雜錫(Sn)的氧化鋅(Sn-ZnO),并與rGO 反應,通過超聲分散的方法得到Sn-ZnO/rGO 復合納米材料,將其用于電化學檢測藥物氟他胺,檢出限(LOD)低至7.3 nmol/L。Fadillah 等[26]以醋酸鋅和氧化石墨烯(GO)為前驅體,通過水熱法合成了ZnO-rGO 納米花狀材料。添加GO 不僅可調控納米ZnO 的形貌,而且在誘導形成ZnO 固有缺陷方面具有重要作用,所得ZnO-rGO 納米花用于催化降解土壤中的腐殖酸,降解率可達98.5%。
PEC 傳感器的檢測靈敏度高,但是不具有選擇性;此外,由于食品基質成分復雜,因此需要設計一種選擇性高的PEC 方法檢測食品中的抗生素殘留。分子印跡技術(MIT)可獲得特異性識別目標分子的分子印跡聚合物(MIP)[28-29],將MIP 用作識別元件,結合電化學[30]、熒光[31-33]和光電檢測[34-35]等方法可測定OTC。Zhang 等[34]采用高溫煅燒葡萄糖酸鋅的方法制備了ZnO/C 復合納米材料,將ZnO/C 作為光電敏感材料修飾摻雜氟的SnO2 透明導電玻璃(FTO),并通過電聚合的方法制備光電傳感器,對OTC 的LOD低至8.75 pmol/L。Bai 等[35]通過水熱法合成了中空的ZnS-CdS 納米籠狀材料,在ZnS-CdS-FTO 上通過電聚合鄰苯二胺和OTC 的方法制備MIP,將OTC 洗脫后得到的PEC 傳感器能對目標分子OTC 進行特異性識別,檢測范圍為1 nmol/L~3 μmol/L。目前,將ZnO-rGO 作為光電敏感材料的分子印跡傳感器測定OTC的研究尚未見報道。
本研究采用水熱法合成了ZnO-rGO 復合納米材料,采用離心法將ZnO-rGO 修飾到FTO 電極上,然后在ZnO-rGO-FTO 表面通過電聚合吡咯(Py)和OTC 的方法制備分子印跡PEC 傳感器(MIP-ZnO-rGOFTO)。此傳感器靈具有靈敏度高、穩定性和抗干擾性能好等優點,被成功用于市售牛奶和蜂蜜樣品中OTC 的測定。
1 實驗部分
1.1 儀器與試劑
CHI620E 電化學工作站(上海辰華儀器公司);Crossbeam340/550 掃描電子顯微鏡(德國Zeiss 公司);JEM-1200 EX 透射電子顯微鏡(日本電子);Bruker D8 ADVANCE X 射線衍射儀(德國Bruker 公司);Kratos Axis Ultra DLD X 射線光電子能譜儀(日本島津公司);氘鹵鎢燈光源裝置(北京紐比特公司);Zetasizer Nano ZS 納米粒度分析儀(英國馬爾文公司);Nicolet iS 50 傅里葉紅外光譜儀(美國Thermo Scientific 公司);Lambda 950 紫外可見分光光度儀(美國PerkinElmer 公司)。電化學測試均采用三電極體系:工作電極為FTO 或修飾FTO(深圳市力科光電玻璃公司),鉑絲和Ag/AgCl 電極分別作為對電極和參比電極。
六水合硝酸鋅、二水合檸檬酸鈉、OTC、氯霉素(Chloramphenicol, CAP)、四環素(Tetracycline,TC)和金霉素(Chlortetracycline, CTC)購自阿拉丁試劑有限公司。所用試劑均為分析純;實驗用水均為二次蒸餾水。
1.2 實驗方法
1.2.1 ZnO-rGO的合成
采用水熱法[36]制備ZnO-rGO。稱取0.08 g GO 加入到燒杯中,加入25 mL 蒸餾水,超聲1 h 制得分散液;稱取2.97 g 六水合硝酸鋅和0.94 g 二水合檸檬酸鈉置于燒杯中,加入25 mL 蒸餾水溶解;將超聲后得到的GO 分散液緩慢加入到上述含有硝酸鋅和檸檬酸鈉的溶液中,滴加2 mol/L NaOH 調節pH=9.0,再繼續攪拌30 min;將混合液倒入100 mL 反應釜中,在180 ℃下反應12 h。反應結束后,采用乙醇和蒸餾水對所得材料進行洗滌,然后置于真空干燥箱內,于60 ℃干燥9~10 h,研磨至粉末狀,即得到ZnO-rGO復合納米材料。ZnO 的制備過程除未加GO 外,其它過程與ZnO-rGO 的制備過程一致。
1.2.2 ZnO-rGO修飾FTO(ZnO-rGO-FTO)的制備
稱取40 mg ZnO-rGO,加入到2 mL異丙醇中,再加入40 μL Nafion,超聲30 min得到ZnO-rGO分散液。將FTO 依次用乙醇和蒸餾水超聲清洗并烘干,將其導電面留出0.5 cm × 0.5 cm 的面積,剩余部分貼上透明膠帶。將FTO 放入到裝有ZnO-rGO 分散液的離心管中離心5 次(離心轉速由慢到快,共離心10 min)后晾干,即得到ZnO-rGO-FTO。采用同樣的方法制備ZnO 修飾的FTO(ZnO-FTO)。
1.2.3 分子印跡電極(MIP-ZnO-rGO-FTO)和非印跡電極(NIP-ZnO-rGO-FTO)的制備
以ZnO-rGO-FTO 為工作電極,鉑絲電極為對電極, Ag/AgCl 電極(3 mol/L KCl 溶液)為參比電極,在含2 mmol/L Py 和1 mmol/L OTC 的50 mmol/L 磷酸鹽緩沖溶液(PBS, pH=7.0)中進行電化學聚合,聚合條件為:掃描速率50 mV/s,電位范圍0~0.9 V,掃描15 圈。聚合完成后,用蒸餾水潤洗電極,隨后置于乙第2 期彭友元等:基于納米氧化鋅-還原氧化石墨烯的分子印跡光電化學傳感器測定土霉素257醇-水(1∶1, V/V)混合溶液中浸泡15 min,對OTC 進行洗脫,得到的電極即為MIP-ZnO-rGO-FT。制備NIP-ZnO-rGO-FTO 時,除聚合過程中不加OTC 外,其余制作步驟與MIP-ZnO-rGO-FTO 的制備方法相同。
1.2.4 PEC測試
在三面遮光的石英比色皿中進行PEC 測試,工作電極為FTO 電極或修飾FTO 電極,采用可見光作為激發光。以0.2 mol/L Na2SO4 溶液(50 mmol/L PBS, pH=7.0)作為電解液,電位恒定為0 V, 采用電流-時間曲線法(i-t)進行PEC 測試,以40 s 為1 個循環,設定光電流測定時間,其中20 s 遮光, 20 s 不遮光。在優化的實驗條件下,將MIP-ZnO-rGO-FTO 分別在不同濃度的OTC 標準溶液中孵育12 min 后,在0.2 mol/L Na2SO4 溶液(50 mmol/L PBS, pH=7.0)中測定電極的光電流。
1.2.5 實際樣品分析
牛奶和蜂蜜購自當地超市,按照文獻[33]的方法進行處理。首先,在10 mL 離心管中依次加入2.0 mL牛奶、2.0 mL 蒸餾水和1.0 mL 三氯乙酸,或2.0 mL 蜂蜜和3.0 mL PBS(50 mmol/L, pH=7.0),超聲30 min后,將混合物以10000 r/min 離心15 min,上層清液用0.22 μm 濾膜過濾,測定前,采用PBS 進行適當稀釋。將MIP-ZnO-rGO-FTO在樣品溶液中孵育12 min 后,按照1.2.4 節方法測定光電流。
2 結果與討論
2.1 ZnO-rGO的結構和形貌表征
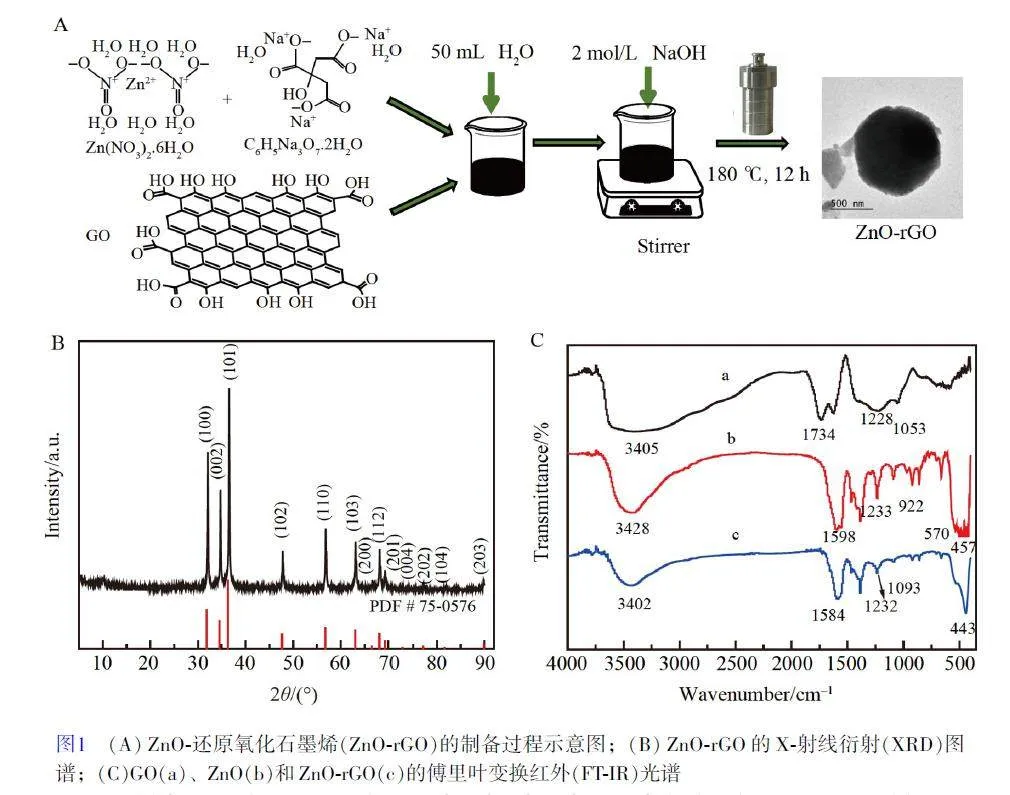
ZnO-rGO 的制備過程如圖1A 所示, ZnO-rGO 的X-射線衍射(XRD)圖見圖1B,其XRD 圖譜與ZnO的特征衍射峰一致(標準卡號:75-0576)。在2θ為31.84°、34.50°、36.34°、47.65°、56.73°、63.01°、66.54°、68.12°、69.26°、72.76°、77.16°、81.61°和89.87°處共觀察到13 個衍射峰,分別對應ZnO 的(100)、(002)、(101)、(102)、(110)、(103)、(200)、(112)、(201)、(004)、(202)、(104)和(203)平面。圖1C 為GO、ZnO 和ZnO-rGO 的傅里葉變換紅外(FT-IR)光譜圖, GO 的FT-IR 光譜(曲線a)在3405 cm?1 處的寬峰對應于O—H 基團[37], 1734 cm?1 處的峰對應于C=O 的伸縮振動[38];曲線b 中457 cm?1 處的峰為ZnO 的特征峰,對應于Zn—O 鍵[39],在920 cm?1 處的小峰對應于Zn 的拉伸振動[40];ZnO-rGO 的FT-IR 光譜(曲線c)在3440 cm?1 處有O—H 基團的寬吸收帶,此吸收峰強度弱于GO 中對應的吸收峰,在曲線c 中未觀察到C=O 伸縮振動峰(1734 cm?1 左右);1100 cm?1 附近的弱峰歸屬于rGO的C—O 拉伸振動[21]。與GO 的紅外光譜相比, ZnO-rGO 紅外譜圖中的含氧基團(O—H 基團和C=O 官能團)的吸收峰強度顯著降低,證明了GO 被有效還原。
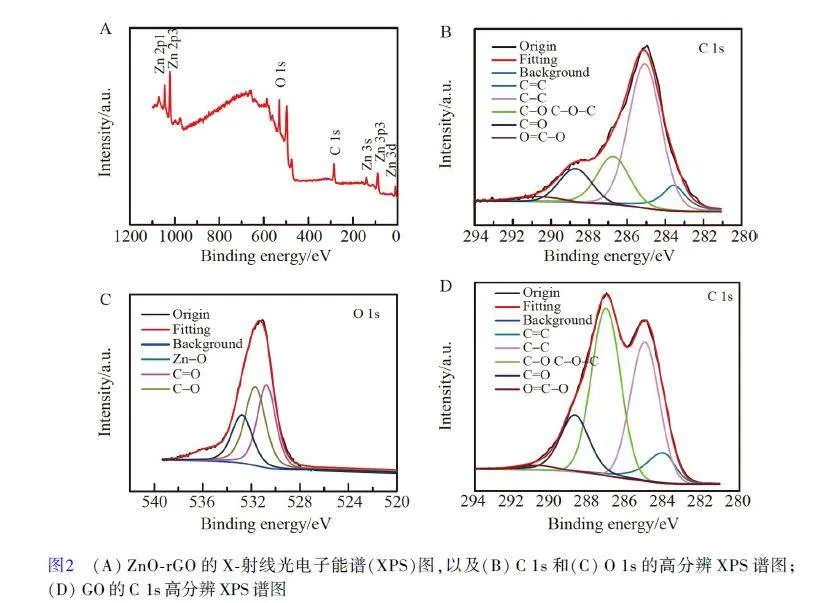
通過X-射線光電子能譜(XPS)進一步確認材料中所含元素以及元素的價態。圖2A 為ZnO-rGO 的XPS 全譜圖,出現的Zn 2p1、Zn 2p3 和O 1s 譜峰證明存在ZnO。圖2B 為ZnO-rGO 中C 1s 的精細譜圖,在283.6、285.1、286.7、288.7 和290.6 eV 處的峰分別對應C=C、C—C、C—O、C=O 和O—C=O官能團;圖2C 為O 1s 的精細譜圖,在530.7 eV 處的峰對應ZnO 中的Zn—O 鍵, 531.7 eV 處的峰對應rGO 表面的C—OH 或C—O—C 官能團[ 41]。圖2D 為GO 中C 1s 的XPS 譜圖,在GO 的C1s 譜中,287.1 eV 處的峰對應C—O 官能團;而在ZnO-rGO 的C 1s 譜中(圖2B),主峰為C—C 官能團。在由GO制備ZnO-rGO 的過程中,材料中的含氧官能團含量降低, GO 被還原,此結果與圖1C 的FT-IR 結果一致。
通過掃描電子顯微鏡(SEM)對ZnO 和ZnO-rGO 的形貌進行分析。如圖3A 和圖3B 所示, ZnO 為圓盤狀且大小均勻;由ZnO-rGO 的SEM 圖(圖3C 和圖3D)可見, ZnO 均勻地分散在片狀的rGO 上。通過納米粒度分析儀測得ZnO-rGO 中的ZnO 粒徑在340~620 nm 之間,平均粒徑約為451 nm。
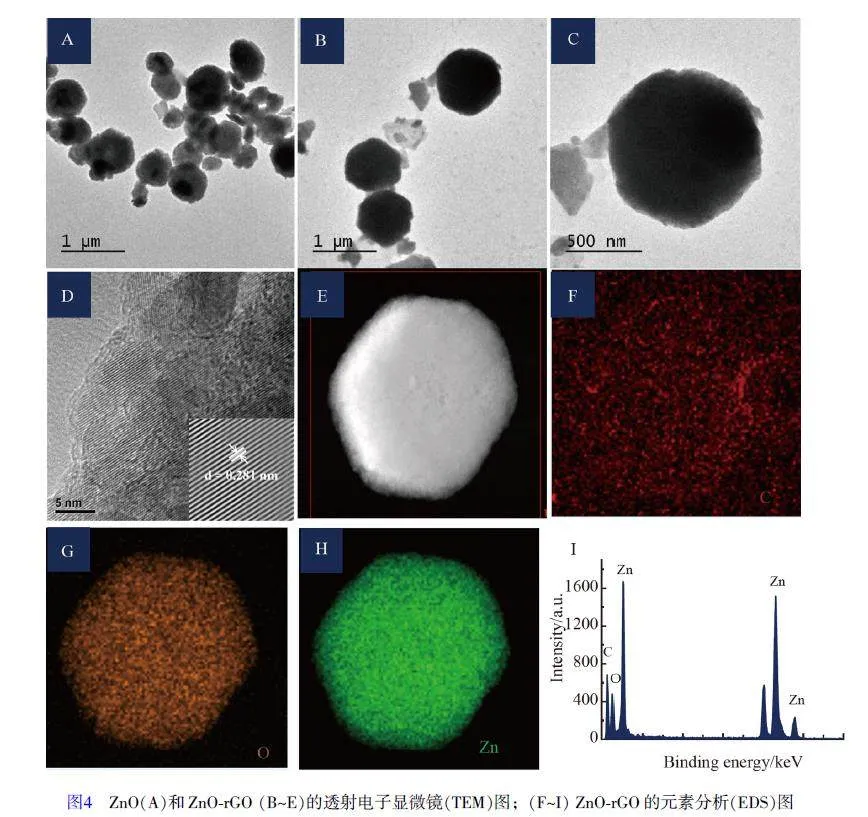
采用透射電子顯微鏡(TEM)進一步分析了ZnO 和ZnO-rGO 的形態特性(圖4)。與ZnO相比(圖4A),在Zn-rGO 的TEM 圖(圖4B 和4C)中可見六邊形的ZnO 沉積在片狀rGO 上;在圖4D 和4E 中可觀察到ZnO 清晰的晶格平面,證實了ZnO 的高度結晶性質, ZnO 晶格間距為0.281 nm,對應于ZnO 晶體的(100)晶面。rGO 和ZnO 晶體之間的緊密界面接觸可使光激發過程中產生的電子快速轉移,從而改善材料的光催化性能[25]。Zn-rGO 的元素映射圖(EDS,圖4F~4I)展示了C、O 和Zn 元素的分布情況, EDS 圖譜表明存在Cu,這是由于分析時采用銅網襯底所致;EDS 中不存在其它元素,證明Zn-rGO具有較高的純度。
2.2 ZnO-rGO的紫外-可見吸收光譜分析
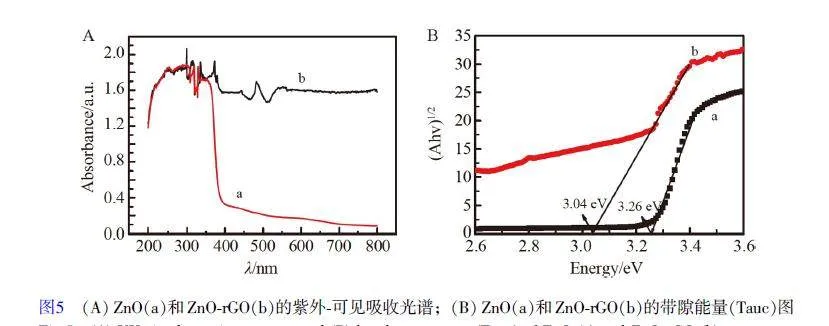
ZnO 和ZnO-rGO 的紫外-可見吸收光譜如圖5A 所示,在200~400 nm 波長范圍內, ZnO(曲線a)和ZnO-rGO(曲線b)均有較強的吸收,但是在400 nm 以上ZnO 的吸收大幅下降。與ZnO 相比, ZnO-rGO 對可見光區域的光吸收能力顯著增強,說明ZnO-rGO 可增強對可見光的利用效率,提高光催化性能。在Tauc 圖[42]中通過外推曲線中的線性區域分析制備的材料的帶隙能量。ZnO 和ZnO-rGO 的Tauc 曲線如圖5B 所示,可見ZnO 的禁帶寬度為3.26 eV, ZnO-rGO 的禁帶寬度為3.04 eV。以上結果表明,通過引入rGO 層, ZnO-rGO 的能帶間隙縮小,從而擴大了ZnO 的光吸收范圍。
2.3 Py和OTC在ZnO-rGO-FTO上的電聚合
以ZnO-rGO-FTO 為工作電極,在含有Py 和OTC 的溶液中進行電化學聚合(Py 濃度為2 mmol/L,OTC 濃度為1 mmol/L)。在聚合過程中, OTC 通過氫鍵和靜電作用進入到聚吡咯(PPy)膜中。采用乙醇-水(1∶1, V/V)混合溶液洗脫OTC 后,得到的電極即為MIP-ZnO-rGO-FTO。NIP-ZnO-rGO-FTO 的制備過程與MIP-ZnO-rGO-FTO 相同,只是在聚合過程中不加OTC。
2.4 分子印跡傳感器的的電化學阻抗譜(EIS)表征及光電流響應
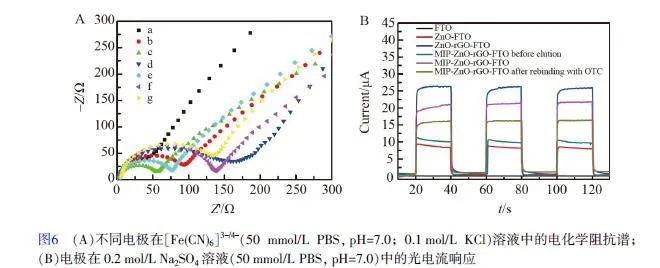
圖6A 為不同電極在[Fe(CN)6]3–/4–溶液中的EIS 譜圖,其中,高頻部分的半圓直徑大小對應電極的電子傳遞阻抗,直線部分對應擴散過程。FTO 的阻抗譜基本為一條直線(曲線a),說明在FTO 上的電化學過程主要受擴散控制,電阻較小;將ZnO 修飾到FTO 上時,由于ZnO 是半導體,因此ZnO-FTO 電阻增大(曲線b);與ZnO-FTO 相比, ZnO-rGO-FTO 的電阻(曲線c)降低,說明rGO 具有良好的導電性。當形成PPy 聚合物膜后,電極的電阻增大(曲線d);將模板分子OTC 洗脫后, MIP-ZnO-rGO-FTO 電極的電阻再次降低(曲線e),而NIP-ZnO-rGO-FTO 在洗脫前后的電阻變化很小(曲線f 和g)。
圖6B 為不同電極的光電流響應。FTO 電極的光電流基本為零。當采用ZnO 和ZnO-rGO 修飾FTO后,光電流增大,并且ZnO-rGO-FTO 的光電流顯著高于ZnO-FTO。聚合完成后,電極的光電流顯著降低,這是由于形成了PPy 聚合物膜。將OTC 洗脫后, MIP-ZnO-rGO-FTO 的峰電流顯著升高,這是由于分子印跡電極上存在著與OTC 空間結構和結合位點相匹配的“印跡孔穴”。將MIP-ZnO-rGO-FTO 置于OTC 溶液中孵育12 min 后,電極上的光電流再次降低,這是由于OTC 占據了聚合膜中的“印跡孔穴”,阻礙了電子的傳遞,從而使得光電流減弱,這也說明了所制備的MIP-ZnO-rGO-FTO可對OTC 進行定量測定。
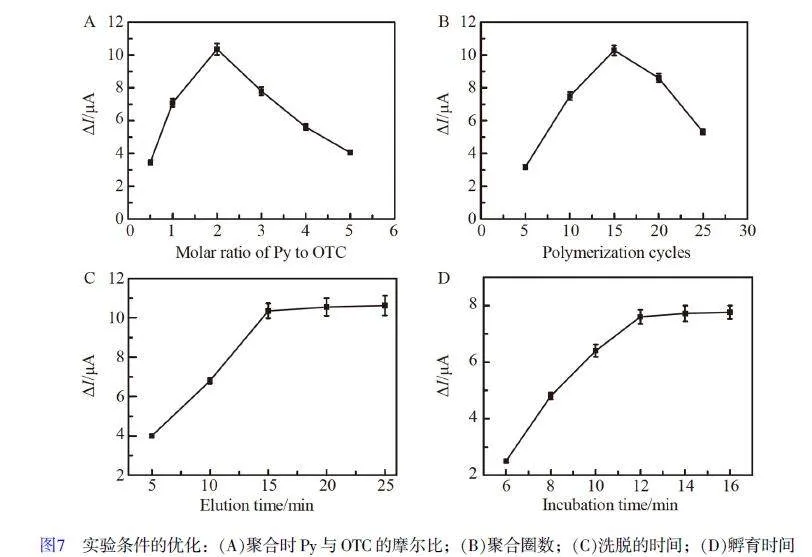
2.5 實驗條件的優化
2.5.1 Py與OTC的比例以及聚合圈數的選擇
電聚合時功能單體與模板分子的比例會影響MIP 中印跡位點的數量,從而影響傳感器對模板分子的識別能力。固定OTC 的濃度為1 mmol/L, Py 的濃度分別選擇0.5、1、2、3、4 和5 mmol/L,得到Py與OTC 的摩爾比分別為0.5、1、2、3、4 和5 時制備的MIP-ZnO-rGO-FTO。如圖7A 所示, Py 與OTC的摩爾比為2 時,制備的傳感器在洗脫前后的光電流變化值最大。在電聚合過程中,當Py 濃度較低時,形成的聚合物膜不穩定;當Py 濃度較大時,會使得OTC 在PPy 中嵌入較深,從而不易被洗脫。因此,后續實驗選擇電聚合時Py 與OTC 的摩爾比為2∶1(OTC 的濃度為1 mmol/L)。
隨著電聚合圈數增多,形成的PPy厚度增加,穩定性提高,并且PPy中嵌入的OTC越多。然而,當電聚合圈數超過15圈時,所制備的MIP-ZnO-rGO-FTO在洗脫前后的光電流變化值反而降低(圖7B),其原因是聚合圈數過多時, PPy的厚度增加,使得OTC洗脫難度增大。因此,在后續實驗中電聚合圈數選擇15圈。
2.5.2 洗脫劑和洗脫時間的選擇
分別選擇蒸餾水、乙醇、乙醇和水的混合溶液、乙腈、乙腈和水的混合溶液進行洗脫,結果表明,乙醇-水(1∶1, V/V)混合溶液可以對PPy 中的OTC 進行有效洗脫,并且不會破壞PPy 的穩定性。將聚合后的電極浸泡在乙醇-水(1∶1, V/V)中,每隔5 min 將電極取出測定光電流。結果表明,浸泡15 min 后,光電流的變化值達到最大(圖7C),因此,選擇在乙醇-水(1∶1, V/V)中浸泡15 min 進行OTC 的洗脫。
2.5.3 孵育時間的選擇
將MIP-ZnO-rGO-FTO 在50 nmol/L OTC 溶液中孵育,隨著孵育時間延長,電極的光電流逐漸降低,光電流變化值(ΔI)不斷增大;當孵育超過12 min 后,ΔI 基本保持不變(圖7D),說明印跡位點對于OTC 的吸附基本達到飽和。因此,孵育時間選擇12 min。
2.6 MIP-ZnO-rGO-FTO對OTC的響應
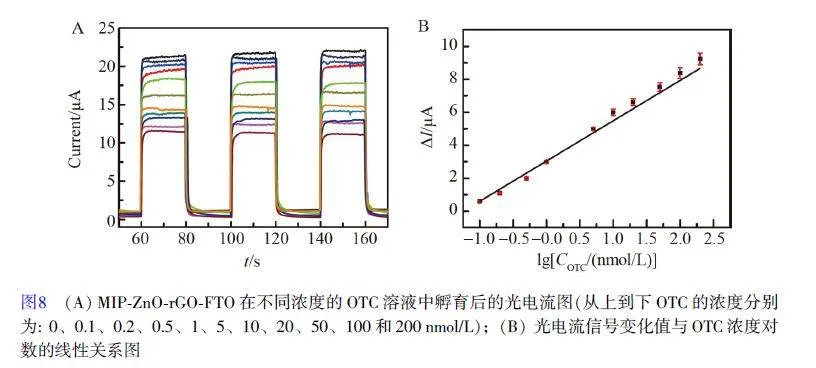
在優化的實驗條件下,將MIP-ZnO-rGO-FTO 分別在不同濃度的OTC 標準溶液中孵育12 min 后,在0.2 mol/L Na2SO4 溶液(50 mmol/L PBS, pH=7.0)中測定電極的光電流。隨著OTC 濃度增大, MIP-ZnOrGO-FTO 光電流逐漸減小(圖8A)。在0.1~200 nmoL/L 濃度范圍內, MIP-ZnO-rGO-FTO 孵育前后光電流的變化值(ΔI)與OTC 濃度的對數呈線性關系(圖8B),線性方程為ΔI(μA)=2.444×lg[COTC/(nmol/L)+3.043(R2=0.9809),檢出限(S/N=3)為0.05 nmol/L。rGO 作為電子接受體,可快速地轉移光催化過程中ZnO 表面產生的光生電子,有利于光生電子與空穴分離,從而提高ZnO-rGO 的光催化性能;MIP-ZnO-rGO-FTO 中的“印跡孔穴”是電子傳輸的重要通道,當溶液中存在OTC 時, OTC 可進入“印跡孔穴”中,阻礙光生電子的傳輸,從而使光電流降低。本方法與文獻報道的OTC 分子印跡傳感器性能的比較見表1,可見制備的傳感器具有較低的檢出限。
2.7 MIP-ZnO-rGO-FTO的穩定性、重現性和選擇性
測試了MIP-ZnO-rGO-FTO 的穩定性、重現性和選擇性。連續光照25 次, MIP-ZnO-rGO-FTO 的光電流響應的相對標準偏差(RSD)為2.8%;將MIP-ZnO-rGO-FTO 于4 ℃避光保存10 d 后,光電流值僅降低3.0%,說明MIP-ZnO-rGO-FTO 具有較好的穩定性。在相同的條件下制備7 根MIP-ZnO-rGO-FTO 電極,其光電流響應的RSD 為3.6%,說明此傳感器的制備重現性較好。
選取CAP、TC 和CTC 作為結構類似物以考察MIP-ZnO-rGO-FTO 的選擇性,將結構類似物和OTC的濃度比設為5∶1(OTC 的濃度為50 nmol/L)。當MIP-ZnO-rGO-FTO 在OTC 溶液中孵育后,光電流降低值約為7.69 μA,而對其它3 種結構類似物的響應僅約為0.60 μA;NIP-ZnO-rGO-FTO 對OTC 和CAP、TC 和CTC 的光電化學響應無明顯差別,均約為0.50 μA。CAP、TC 和CTC 對OTC 的檢測基本沒有影響,原因是在MIP-ZnO-rGO-FTO 上存在可對OTC 進行特異性識別的“印跡孔穴”,而NIP-ZnO-rGO-FTO不存在印跡位點,僅依靠非特異性吸附結合,因此對OTC 及其結構類似物響應較低且基本接近。
2.8 實際樣品分析
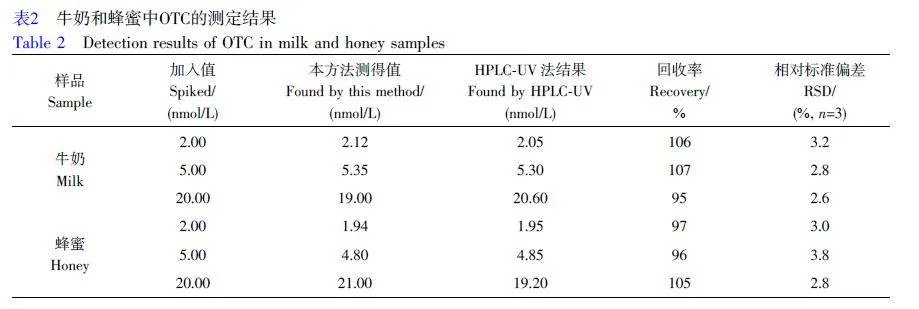
采用本方法測定了市售牛奶和蜂蜜中的OTC,結果如表2 所示,樣品中均未檢出OTC。樣品的加標回收率在95%~107%之間;采用HPLC-紫外檢測(HPLC-UV)法[33]測定了樣品加標后的OTC 含量,所得結果與MIP-ZnO-rGO-FTO 測定結果一致,說明本研究制備的傳感器用于測定OTC 具有較高的準確度。
3 結論
采用水熱法一步合成了ZnO-rGO,通過引入rGO,縮小了ZnO 的能帶間隙,促進了ZnO-rGO 對可見光的吸收;同時, rGO 作為電子接受體,可以快速轉移光催化過程中ZnO 表面產生的光生電子,從而提高ZnO-rGO 的光催化性能。在ZnO-rGO-FTO 表面通過電聚合方法制備了MIP 膜,得到MIP-ZnO-rGOFTO,當溶液中的OTC 占據MIP-ZnO-rGO-FTO 上的印跡孔穴時,傳感器的光電流降低,從而可以利用印跡電極上的光電流降低值對OTC 進行定量測定。此傳感器制備過程簡單,結合分子印跡技術可實現OTC 的高靈敏和特異性檢測,檢出限(S/N=3)為0.05 nmol/L。將此傳感器用于市售牛奶和蜂蜜中OTC 的測定,結果令人滿意。本研究制備的的分子印跡PEC 傳感器在食品中抗生素含量監測方面具有良好的應用前景。
References
[1] NAIK L, SHARMA R, MANN B, LATA K, RAJPUT Y S, SURENDRA NATH B. Food Chem. , 2017, 219: 85-92.
[2] OSIKOYA A Q, GOVENDER P P. Electroanalysis, 2021, 33(2): 412-420.
[3] HUANG H C, HUANG S Y, LIN C I, LEE Y D. Anal. Chim. Acta, 2007, 582(1): 137-146.
[4] GB 31650—2019. National Food Safety Standard-Maximum Residue Limits for Veterinary Drugs in Foods. National Standards of the People′s Republic of China.
食品安全國家標準-食品中獸藥最大殘留限量. 中華人民共和國國家標準. GB 31650—2019.
[5] SALEH H, ELHENAWEE M, HUSSIEN E M, AHMED N, IBRAHIM A E. Food Anal. Methods, 2021, 14(1): 36-43.
[6] GAJDA A, JABLONSKI A, BLADEK T, POSYNIAK A. J. Agric. Food Chem. , 2017, 65(2): 494-500.
[7] WU H, CHEN Y, XU M, LING Y, JU S, TANG Y, TONG C. Sci. Total Environ. , 2023, 860: 160533.
[8] WANNASRI N, UPPACHAI P, SEEHAMART K, JANTRASEE S, BUTWONG N, MUKDASAI K, ISA I M, MUKDASAI S.ACS Omega, 2022, 7(49): 45654-45664.
[9] GASHU M, ARAGAW B A, TEFERA M. J. Food Compos. Anal. , 2023, 117: 105128.
[10] MAHALA C, SHARMA M D, BASU M. ACS Appl. Nano Mater. , 2020, 3(2): 1999-2007.
[11] BAI X, GAO W, ZHOU C, ZHAO D, ZHANG Y, JIA N. Microchim. Acta, 2022, 189(3): 90-98.
[12] DAS A, DEKA T, KUMAR P M, BHAGAVATHIACHARI M, NAIR R G. Adv. Powder Technol. , 2022, 33(2): 103434.
[13] HUANG X, SHEN Q, LIU J, YANG N, ZHAO G. Energy Environ. Sci. , 2016, 9(10): 3161-3171.
[14] YAN Y, LI Q, WANG Q, MAO H. RSC Adv. , 2021, 11(56): 35644-35652.
[15] KANG Z, GU Y, YAN X, BAI Z, LIU Y, LIU S, ZHANG X, ZHANG Z, ZHANG X, ZHANG Y. Biosens. Bioelectron. ,2015, 64: 499-504.
[16] ZIA T H, SHAH A H A. Colloids Surf. , A, 2021, 630: 127586.
[17] GEA S, SITUMORANG S A, PASARIBU N, PILIANG A F R, ATTAURRAZAQ B, SARI R M, PASARIBU K M,GOUTIANOS S. J. Mater. Res. Technol. , 2022, 19: 2730-2741.
[18] BAGAL I V, JUN S, CHOI M, ABDULLAH A, WASEEM A, AHN S, KULKARNI M A, CHO Y H, RYU S W. Appl. Surf.Sci. , 2023, 613: 156091.
[19] LI Y, WANG W, GONG H, XU J, YU Z, WEI Q, TANG D. J. Mater. Chem. B, 2021, 9(34): 6818-6824.
[20] MIRIKARAM N, PEREZ-MOLINA A, MORALES-TORRES S, SALEMI A, MALDONADO-HóDAR F J, PASTRANAMARTINEZ L M. Nanomaterials, 2021, 11(6): 1576-1593.
[21] LI F, NI B, ZHENG Y, HUANG Y, LI G. Surf. Interfaces, 2021, 26: 101375.
[22] YANG S L, LI G, FENG J, WANG P Y, QU L B. Electrochim. Acta, 2022, 412: 140157.
[23] HWA K Y, SANTHAN A, TATA S K S. Microchem. J. , 2021, 160: 105689.
[24] LEE J H, VELMURUGAN P, RAVI A V, OH B T. Environ. Chem. Ecotoxicol. , 2020, 2: 141-149.
[25] JAIN N, SHARMA S, PURI N K. J. Mater. Sci.: Mater. Electron. , 2022, 33(3): 1307-1323.
[26] FADILLAH G, SALEH T A, MUNAWAROH H, WAHYUNINGSIH S, RAMELAN A H. Environ. Sci. Pollut. Res. ,2022, 29(7): 9883-9891.
[27] HUANG M, LIN J, LI R, SU Y, ZHAO X, LIU Y, CHEN W J, LIAN X, CHEN X, PAN X. ACS Appl. Nano Mater. , 2022,5(2): 1828-1835.
[28] CHEN L, WANG X, LU W, WU X, LI J. Chem. Soc. Rev. , 2016, 45(8): 2137-2211.
[29] AHMAD R, GRIFFETE N, LAMOURI A, FELIDJ N, CHEHIMI M M, MANGENEY C. Chem. Mater. , 2015, 27(16): 5464-5478.
[30] YANG Y, SHI Z, CHANG Y, WANG X, YU L, GUO C, ZHANG J, BAI B, SUN D, FAN S. Food Chem. , 2021, 363:130337.
[31] WANG J, ZOU L, XU J, ZHANG R, ZHANG H. Anal. Chim. Acta, 2021, 1161: 338326.
[32] WANG J, LI X, ZHANG R, FU B, CHEN M, YE M, LIU W, XU J, PAN G, ZHANG H. J. Mater. Chem. B, 2022, 10(35):6777-6783.
[33] XU Y, HUANG T, WANG S, YAN Y. J. Food Compos. Anal. , 2022, 108: 104427.
[34] ZHANG H, PAN Q, CAI W, SHI X, YANG D P, LIN H, QIU E. Food Chem. , 2023, 426: 136535.
[35] BAI X, ZHANG Y, GAO W, ZHAO D, YANG D, JIA N. Biosens. Bioelectron. , 2020, 168: 112522.
[36] ZHU Q, ZHANG K, HUANG Y, LIU R, PAN Y, ZHANG H, WANG P, ZHANG S, PAN D, GUO Z. J. Nanostruct. Chem. ,2022, 12(2): 277-289.
[37] LIU X, PAN L, ZHAO Q, LV T, ZHU G, CHEN T, LU T, SUN Z, SUN C. Chem. Eng. J. , 2012, 183: 238-243.
[38] RAVICHANDRAN P K, MUNUSAMY C. Environ. Sci. Pollut. Res. , 2023, 30(10): 28259-28273.
[39] BANO N, HUSSAIN I, EL-NAGGAR A M, ALBASSAM A A. Appl. Phys. A: Mater. Sci. Process. , 2019, 125(3): 215.
[40] SHI L, GUNASEKARAN S. Nanoscale Res. Lett. , 2008, 3(12): 491-495.
[41] HU Shi-Ying, SHEN Jia-Yan, HAN Jun-Shan, HAO Ting-Ting, LI Xing. Chem. J. Chin. Univ. , 2023, 44(2): 20220462.
胡詩穎, 沈佳艷, 韓峻山, 郝婷婷, 李星. 高等學校化學學報, 2023, 44(2): 20220462.
[42] YANG N Q, LI J. Eur. Phys. J. Plus, 2021, 136(9): 965-975.
[43] CHEN Y, TANG Y, LIU Y, ZHAO F, ZENG B. J. Hazard. Mater. , 2022, 434: 128907.
[44] WANG X, CAO Y, HU X, CAI L, WANG H, FANG G, WANG S. Microchem. J. , 2023, 190: 108606.
福建省自然科學基金項目(No. 2020J01771)資助。

