帕金森病腦深部電刺激術后電極錯位修正2例報道及文獻回顧
楊森 麥榮康 鄭勇

【摘要】 目的 探討帕金森病(PD)腦深部電刺激(DBS)術后療效不佳與電極錯位的關系,以及靶點調整時機和方法、術后療效改善分析。方法 回顧性分析深圳大學第二附屬醫院2020年9月—2021年4月收治的2例因植入電極錯位導致療效不佳的DBS術后患者,分別行更換靶點和原靶點重新植入的修正手術,觀察結果,結合文獻加以總結。結果 患者1的刺激靶點由雙側丘腦底核(STN)更換為雙側內側蒼白球(GPi),術前、術后藥物關期刺激下UPDRS運動評分改善率32.1%,藥物開期可改善46.4%;患者2行原左側STN靶點電極取出并重新植入,術前、術后藥物關期刺激下UPDRS運動評分改善率21.4%,藥物開期可改善35.7%。結論 腦深部電刺激術后,在明確診斷為與電極位置錯位相關的療效不佳時,有必要進行個體化的修正手術。
【關鍵詞】 帕金森病;腦深部電刺激;電極錯位;修正手術
【中圖分類號】 R651? 【文獻標志碼】 B? 【文章編號】 1672-7770(2024)03-0357-04
腦深部電刺激術(deep brain stimulation,DBS)是目前臨床上治療帕金森病(Parkinsons disease,PD)、特發性震顫(essential tremor,ET)及肌張力障礙的主要手術方式[1]。DBS術中電極植入靶點的準確性是影響術后療效的最關鍵因素,通過嚴格的患者選擇、影像學規劃及精細的手術操作,配合術中電生理、術中影像輔助及副反應測試,一般可獲得良好的癥狀控制[1]。電極錯位會給術后程控帶來困難,極易引發刺激周圍神經結構所引起的副反應,當術后程控及藥物治療均無法進一步得到滿意的癥狀控制時,可考慮采用修正手術調整電極位置[2]。隨著DBS的廣泛臨床應用,術后程控患者逐漸增多,使得修正手術的需求也逐漸增長,相關的研究正引起醫務工作者的重視。本研究回顧性分析深圳大學第二附屬醫院2020年9月—2021年4月收治的2例PD患者,因DBS術后療效欠佳,分別行更換靶點及原靶點重新植入修正手術治療,結合文獻復習探討PD患者DBS術后療效欠佳時修正手術的診治思路。現報告如下。
1 資料與方法
1.1 患者1
1.1.1 一般資料 患者女,57歲,因外院DBS術后3年療效不佳于2020年9月入院。患者首次手術在PD發病14年時,主要表現為四肢肌張力增高、行走困難,藥物難以改善。首次手術靶點為雙側丘腦底核(subthalamic nucleus,STN),術后1個月(植入設備為美敦力Activa RC)程控時行走困難、肢體僵硬緩解低于預期,在外院多次程控,效果不滿意。患者為進一步診治于深圳大學第二附屬醫院神經內科門診咨詢、程控,主要通過逐步增加刺激電壓、調整藥物組合及劑量來維持適度的肌張力緩解程度。當左側STN電極電壓達到3.5 V時即出現右側肢體麻木,右側STN電極電壓上升至3.0 V以上即出現左側肢體異動,過低的電壓則肌張力難以緩解。反復調校后將左側STN刺激參數調整為單極模式C+8-,2.7 V、60 μs、130 Hz,右側STN刺激參數調整為單極模式C+4-,3.0 V、60 μs、130 Hz予維持。服藥美多巴等效劑量(modopar equivalent dose,MED)為475 mg,藥物關期刺激下Hoehn yahr分期為Ⅳ期,UPDRS Ⅲ評分56。經與神經內科醫師溝通,結合患者溝通后意愿,決定行電極修正手術。入院后在為期12 h的洗脫期后,進行1.5倍左旋多巴等效劑量沖擊試驗,改善率為44.6%,出現肢體異動。
1.1.2 影像學檢查 修正手術前行1.5 T核磁共振成像(magnetic resonance imaging,MRI)掃描(T1軸冠矢位、T2軸冠位),手術當天在局麻下安裝立體定向頭架行1 mm薄層計算機斷層掃描(computer tomography,CT)掃描,導入Surgiplan手術計劃系統,結合參考值、可視化定位雙側STN,重新定位雙側STN理想靶點,可知雙側實際植入電極位置與理想靶點比較均稍深、偏內、偏后(圖1),證實患者病情控制不良、程控困難原因為與電極相關的位置不良。
1.1.3 方法及預后 因患者癥狀主要以肌張力異常增高伴異動為主,故修正手術方案為更換刺激靶點由雙側STN至雙側蒼白球內側核(Globu Pallidus interna,GPi)。手術過程中,首先拔除雙側STN刺激電極,后在電生理、宏刺激及副反應測試下,植入雙側GPi電極,改全麻將雙側刺激電極與原有延伸導線連接、固定,測試通暢。術后復查頭部CT導入計劃系統,融合見電極位置滿意(圖1B)。圍手術期未出現與電極相關并發癥,術后20 d開機程控,刺激參數為左側Gpi C+6-,2.3 V、90 μs、150 Hz,右側Gpi C+3-,2.5 V、90 μs、150 Hz。術前、術后1個月藥物關期刺激下UPDRS運動評分較術前改善32.1%。術后藥物等效劑量不變,開期延長,關期縮短,開期運動評分較術前同期最好情況下可改善46.4%,程控過程中未再出現右側肢體麻木及左側肢體異動等反應。
1.2 患者2
1.2.1 一般資料 患者女,68歲,因PD患者DBS術后4年右側下肢震顫加重1年于2021年4月入院。患者首次DBS手術在PD發病5年時,主要表現為四肢不自主震顫,藥物難以改善。手術靶點為雙側STN。術后1個月(植入設備為美敦力Activa RC)藥物關期改善率最高可達約48%,開期改善率最高可達約56%;近1年效果下降,表現為右側下肢震顫明顯加重,藥物治療無效。修正手術前的最佳刺激參數為左側STN C+2-,2.2 V、90 μs、120 Hz(更高的電壓導致眼球活動異常),右側STN C+7-,3.0 V、90 μs、120 Hz。服藥MED為375 mg,患者藥物關期刺激下Hoehn yahr分期Ⅲ期,UPDRS Ⅲ評分42。入院后在12 h洗脫期后進行1.5倍左旋多巴等效劑量沖擊試驗,改善率為33.3%。
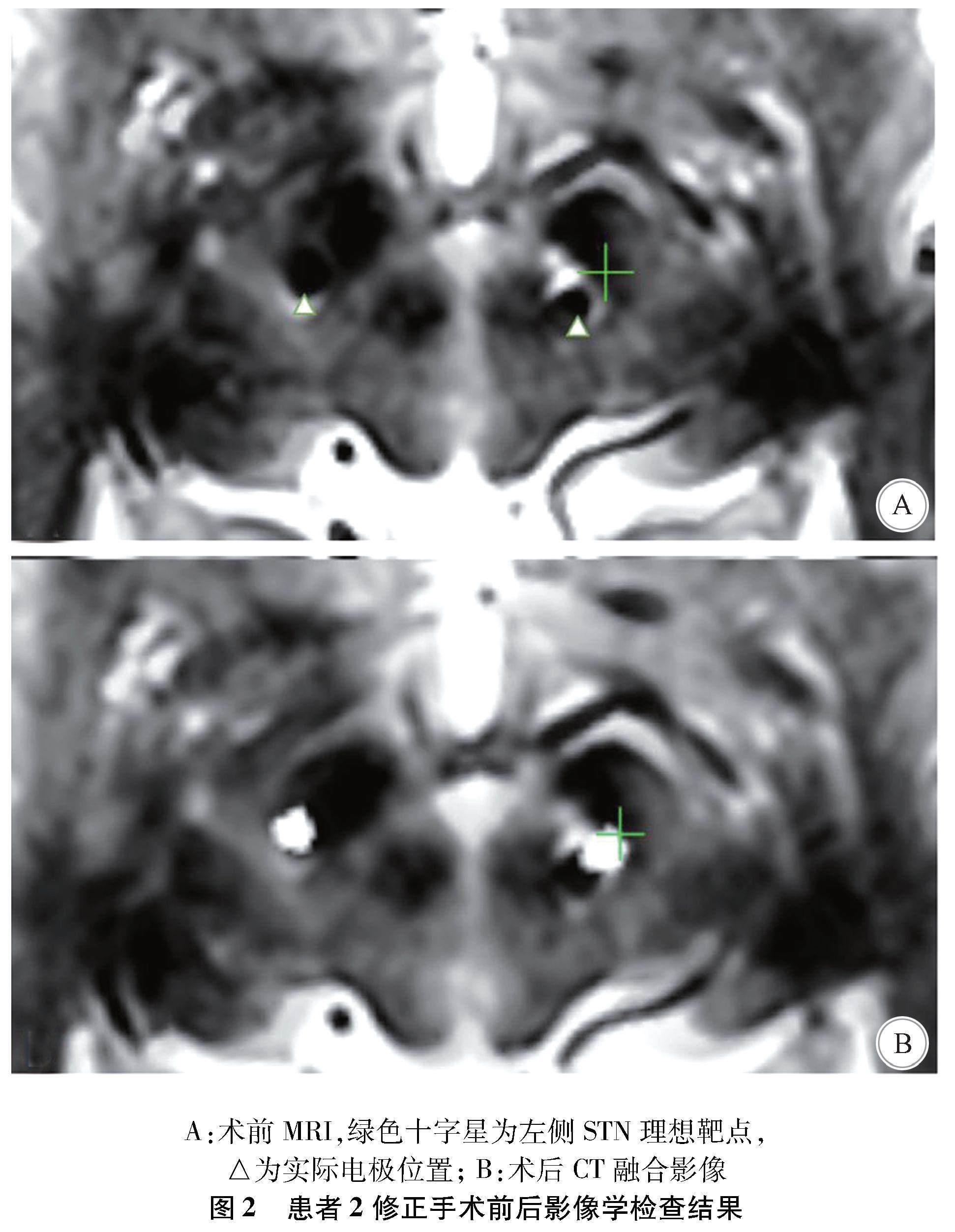
1.2.2 影像學檢查 修正手術前行1.5 T MRI掃描(T1軸冠矢位、T2軸冠位),手術當天在局麻下安裝立體定向框架,行1 mm薄層CT掃描,導入Surgiplan手術計劃系統,重新定位左側STN理想靶點,可見實際電極位置偏內、偏后(圖2),右側STN電極位置滿意。
1.2.3 方法及預后 再次手術僅考慮修正左側STN電極,以原顱骨骨孔規劃新穿刺道,注意避開原有電極通道。術中先緩慢拔除原左側STN電極,然后在電生理、宏刺激和副反應測試下重新植入靶點,后改全麻將左側電極與原有延伸導線連接并固定,測試通暢。術后復查頭部CT導入計劃系統,融合見電極位于理想靶點與原電極位置中間(圖2B)。術后20 d開機,刺激參數為左側STN C+6-,2.9 V、90 μs、120 Hz,右側同前。術前、術后1個月對比藥物關期刺激下UPDRS運動評分改善21.4%。術后藥物等效劑量不變,開期延長,關期縮短,開期運動評分較術前同期最好情況下可改善35.7%,右側下肢震顫明顯改善,肌張力降低,刺激電壓上升到3.5 V未見出現異動。
2 討 論
DBS逐漸成為PD及運動障礙疾病的主要外科治療手段,術后效果直接取決于DBS電極位置的準確性[2]。電極錯位將對術后程控造成很大困難,直接影響癥狀的改善率。Rolston等[3]認為因電極錯位導致的療效欠佳是導致DBS術后再次手術的最主要原因,而目前關于電極錯位修正手術的報道卻很少,這一問題在臨床中可能廣泛存在,但尚缺乏專門研究。
DBS術后短期的治療重點在于預防與手術相關的顱內出血,此時如再次手術的目的是處理與手術操作相關的并發癥;隨著術后時間的延長,再次手術的目的主要是處理與電極硬件相關的各種問題,如電極感染/皮膚感染、線路斷路及電極錯位導致的療效下降[4]。
由于DBS的手術技術進展迅速,過早的報道已無參考價值。Cabral等[5]完成的一項META分析納入了2017年—2021年針對不同靶點的共一萬余側DBS術后患者的研究,將硬件相關的負性事件分為高電阻、電極/導線折斷、感染、電極錯位、脈沖發生器故障等分別進行分析,這可能反映出目前DBS術后遠期再次手術的主要原因。
異常的電阻改變反映出電路某部分的損壞,可能是局部腦組織變性,也可能是電極-腦組織界面的理化性質改變(如產生了微小的局部氣栓等),電阻的改變導致刺激電流的變化,增加程控困難[6]。電極/導線的折斷一般是由于身體異常的姿勢,導致了局部明顯異常的壓力所致。感染可能是局部的皮膚感染,也可能是顱內的電極感染,多發生于電極在顱骨鎖的卡槽處、耳后切口及胸前的脈沖刺激器埋置處,常見于葡萄球菌或金黃色葡萄球菌在微小的皮膚破潰處出現繁殖,并未得到及時處理[7];當電極感染嚴重而抗生素治療無效,需要拔除刺激電極[4,78],治愈后重新植入電極者不可歸入修正手術的范疇內。
本研究中的修正手術是為了改善PD患者在DBS術后與電極錯位相關的療效不佳。雖然目前已有多種技術確保電極植入的準確性,但總體來看,電極錯位在DBS中的發生率仍在2.47%左右[9]。造成電極位置不理想或療效下降的因素有很多,術中腦脊液丟失、氣顱、腦室容積、手術時間等因素對首次手術的電極位置影響較大[10]。王滔等[11]的研究認為,DBS術后電極有發生向靶點內側、后側及深部偏移的傾向;本研究的2例患者首次DBS術后均可見不同程度地向內、后側偏移(圖1、圖2)證實了這種觀點。
即使首次準確植入,隨著術后時間延長,電極電阻的變化、導線在顱骨鎖上的松動或局部外力等多種情況,均可導致觸點的移位,造成療效波動[2]。當發現患者存在電極錯位情況,程控或藥物治療無法進一步提高療效時,修正手術的目的在于調整刺激電極位置或更換靶點以達到更好的臨床療效,當考慮更換靶點時尤其需要結合患者臨床特點進行個體化考量。有研究[1213]指出,STN-DBS主要通過減藥和調整刺激位點控制異動癥,而GPi-DBS具有直接抑制異動癥的作用。國外學者如Frizon等[14]報道的電極錯位病例,大多數是予STN原位修正,僅在少數伴有明顯異動的患者中將靶點改至GPi取得滿意的改善。本研究中患者1的表現符合僵直型PD的典型表現,療效不理想主要表現在四肢肌張力增高伴左側上肢難以解決的異動癥狀,故將靶點由雙側STN修正為雙側GPi,取得了良好的效果。
不同的刺激電極有不同的觸點間距,本研究中所植入的刺激電極包含了4個觸點,每個觸點1.5 mm,間距0.5 mm,共跨越7.5 mm的范圍,在大多數情況下,沿電極觸點跨越范圍內的縱向偏差可通過調節電極觸點來解決,故針對原靶點的修正手術,重點在于糾正與電極垂直方向的偏差。杜婷婷等[15]研究認為,與電極垂直方向修正的平均距離為2.8 mm(測量平面為AC-PC平面下3.5 mm),術后取得了滿意的效果。
具體的手術方法不一而足,部分學者在植入電極時將原有電極作為參考(結合術中影像如X線透視),避免植入電極滑入原有隧道,可在新電極植入完成后拔除;為防止拔除過程出血,可對舊電極做保留處理;也可將手術分為2期進行,先1期拔除原有電極,2期再行植入,這樣既可以避免滑入原有腦內隧道,又可以保證再次植入時電生理監測結果的準確性[14]。本研究采用首先拔除原電極,同時重新置入新電極的方法。患者2的療效減弱主要表現為DBS術后右側下肢震顫加重,反復程控效果差,增加藥物劑量又誘發肢體異動等不良反應,修正手術的目的是將左側STN電極向前、外側進行適度移動。雖然在規劃該例患者的穿刺入路時特別注意了規避原電極隧道,但是術后融合影像仍可見電極偏離預定靶點,實際落于理想靶點與原靶點之間,修正距離為1.8 mm(測量平面為AC-PC平面下3.5 mm)。Falowski等[16]認為新路徑應與原電極隧道保留至少2 mm的距離,否則電極極易滑入原有隧道,影響修正手術效果;該研究術后藥物關期下最好的改善率僅為21.4%,與已有的文獻報道結果相比較(改善率多為24%~44.6%)偏低[16],不能排除原穿刺道影響了電極尖端位置的可能,因此更理想的電極穿刺通道規劃方式或許可以帶來更好的結果。術中保留原電極進行電生理監測,通過對比兩電極的電生理結果,復核植入的靶點準確性,或許是一種值得積極嘗試的方法,但采用此種方式時可能需要更加巧妙地設計植入通道。