15 種醫院口腔抑菌制劑微生物限度檢查方法的建立*
趙慧雯,馮 斌
(軍事口腔醫學國家重點實驗室·國家口腔疾病臨床醫學研究中心·陜西省口腔生物工程技術研究中心·中國人民解放軍空軍軍醫大學第三附屬醫院藥劑科,陜西 西安 710032)
醫院制劑是指醫院制劑室按藥品標準或協定處方制成的一類適應本院臨床需要而市場未能供應的制劑,具有制備數量少、周期短、品種多、供應及時等優點[1]。醫院制劑應保證質量穩定,微生物是衡量制劑安全性的重要指標,故需建立科學可靠的微生物限度檢查方法[2]。口腔類制劑因臨床主要用于抑菌消炎、控制感染、促進修復等,多含有抑菌成分,因此對該類制劑進行微生物限度檢查時,應先消除自身的抑菌活性,以保證方法的適用性,從而真實準確地反映制劑被微生物污染的情況[3]。本研究中基于2020年版《中國藥典(四部)》通則1105,1106,1107 項下要求,擬采用平皿法、薄膜過濾法和培養基稀釋法對15 種口腔抑菌制劑進行微生物限度適用性檢查[4],從而保障臨床用藥的質量可控和安全有效。現報道如下。
1 儀器、試藥與菌株
1.1 儀器
LDZX - 30KBS 型壓力蒸汽滅菌器(上海申安醫療器械廠);XY500JC 型電子天平(常州市幸運電子設備有限公司,精度為0.01 g);HFsafe-1800TE型生物安全柜(上海力申科學儀器有限公司);BSD-TX345型臺式恒溫振蕩器(上海博訊實業有限公司);HH 系列電熱恒溫水浴鍋(北京科偉永興儀器有限公司);LRH - 250F 型生化培養箱,M250FI型霉菌培養箱(上海一恒科學儀器有限公司);VORTEX-5 型渦旋混合器(海門市其林貝爾儀器制造有限公司);EX30 系列生物顯微鏡(寧波舜宇儀器有限公司);PHS - 4C + 型酸度計(成都世紀方舟科技有限公司);API 型微生物鑒定系統(法國Bio-Mérieux 公司);HTY - 602 型集菌儀(杭州泰林生物技術設備有限公司)。
1.2 試藥
醋酸氯己定口崩片(成分為醋酸氯己定等,批號為220908),醋酸氯己定洗劑(成分為醋酸氯己定等,批號為211008),復方替硝唑溶液(成分為替硝唑、醋酸氯己定等,批號為211014),碘甘油(成分為碘等,批號為210927),甲醛甲酚涂劑(成分為甲醛、甲酚等,批號為211013),硼酸甘油涂劑(成分為硼酸等,批號為220629),人工唾液(成分為氯化鈉、羥苯乙酯等,批號為211021),脫敏糊劑(成分為多聚甲醛、乙醇等,批號為210919),干髓糊劑(成分為多聚甲醛等,批號為211010),鋅麝酚醛糊劑(成分為氧化鋅、麝香草酚等,批號為211006),牙周塞糊劑(成分為氧化鋅、鞣酸等,批號為211007),甲硝唑膜(成分為甲硝唑等,批號為210922),復方克林霉素膜(成分為克林霉素磷酸酯等,批號為211010),多聚甲醛新失活劑(成分為多聚甲醛、鹽酸可卡因等,批號為211020),多聚甲醛牙髓失活劑(成分為多聚甲醛、鹽酸可卡因等,批號為211005),分別為制劑1-15,均為空軍軍醫大學第三附屬醫院的醫院制劑;胰酪大豆胨瓊脂及液體培養基(TSA,TSB,批號分別為2009032,2103015),沙氏葡萄糖瓊脂及液體培養基(SDA,SDB,批號分別為2010302,2009202),麥康凱瓊脂及液體培養基(批號分別為2008272,2008202),溴化十六烷基三甲銨瓊脂培養基(USP,批號為2009212),甘露醇氯化鈉瓊脂培養基(MSA,批號為2003262),pH 7.0 無菌氯化鈉-蛋白胨緩沖液(批號為2108202),均購自北京三藥科技有限公司;0.9%無菌氯化鈉溶液(四川科倫藥業股份有限公司,批號為M21030902C)。
1.3 菌株
金黃色葡萄球菌Staphylococcus aureus[CMCC(B)26003],銅綠假單胞菌Pseudomonas aeruginosa[CMCC(B)10104],枯草芽孢桿菌Bacillus subtilis[CMCC(B)63501],白色念珠菌Candida albicans[CMCC(F)98001],黑曲霉Aspergillus niger[CMCC(F)98003],大腸埃希菌Escherichia coli[CMCC(F)44102],均購自中國醫學細菌保藏管理中心,試驗菌株均為第2代。
2 方法與結果
2.1 溶液制備
菌液:將金黃色葡萄球菌、銅綠假單胞菌、枯草芽孢桿菌分別接種于TSB 中,35 ℃培養24 h;將白色念珠菌接種于SDB 中,25 ℃條件下培養3 d。均用0.9%無菌氯化鈉溶液(稀釋液1)制成適宜濃度的菌懸液。將黑曲霉接種于SDA 中,25 ℃條件下培養7 d,加入5 mL 含0.05%聚山梨酯80 的0.9%無菌氯化鈉溶液,洗脫孢子,收集孢子懸液,并制成適宜濃度的孢子懸液。
供試品溶液:取樣品10 g/10 mL/100 cm2,各2份,置250 mL 玻璃瓶中,加入pH 7.0 無菌氯化鈉-蛋白胨緩沖液(稀釋液2)稀釋至100 mL,45 ℃條件下恒溫振蕩15 min,制成1∶10(m/V)的供試品溶液Ⅰ。取10 mL,加稀釋液2適量,混勻,分別制成1∶20(m/V)、1∶50(m/V)的供試品溶液Ⅱ、Ⅲ。
2.2 需氧菌總數、霉菌和酵母菌總數計數方法適用性試驗
2.2.1 平皿法
試驗組:取2.1 項下供試品溶液9.9 mL,置無菌試管中,加入含菌量不大于10 000 cfu / mL 的試驗菌液0.1 mL,混勻。分別取適量,注入2 個平皿,各1 mL。分別注TSA(需氧菌計數)、SDA(霉菌和酵母菌計數)各20 mL,溫度均不超過45 ℃。前者35 ℃條件下倒置培養2~3 d,后者25 ℃條件下倒置培養2~5 d。
供試品對照組:取2.1 項下供試品溶液適量,以稀釋液2替代菌液,同試驗組方法操作。
菌液對照組:取稀釋液2 適量替代供試品溶液,加入試驗菌,同試驗組方法操作。
2.2.2 薄膜過濾法
試驗組:取2.1 項下供試品溶液Ⅰ1 mL,加入含100 mL 稀釋液2 的濾器中,濾過,用稀釋液2 沖洗濾膜3~8 次,每次100 mL,最后1 次沖洗液中加入含菌量不大于100 cfu的試驗菌液1 mL,取出濾膜,貼于相應平板培養基,按規定條件倒置培養、計數。
供試品對照組:取2.1 項下供試品溶液Ⅰ適量,以稀釋液2替代菌液,同試驗組方法操作。
菌液對照組:取稀釋液2 適量替代供試品溶液,加入試驗菌,同試驗組方法操作。
2.2.3 回收比計算
菌株回收比(%)=(試驗組菌落數-供試品對照組菌落數)/菌液對照組菌落數×100%。
2.2.4 驗證試驗
制劑1-5、9-11、14-15 需氧菌總數檢查均采用薄膜過濾法,其余制劑均采用平皿法;制劑1-3、6-8、12 - 13 霉菌和酵母菌檢查均采用平皿法,其余制劑均采用薄膜過濾法,試驗菌回收比均在0.5~2.0 范圍內。詳見表1和表2(僅列出了最優檢查方法)。
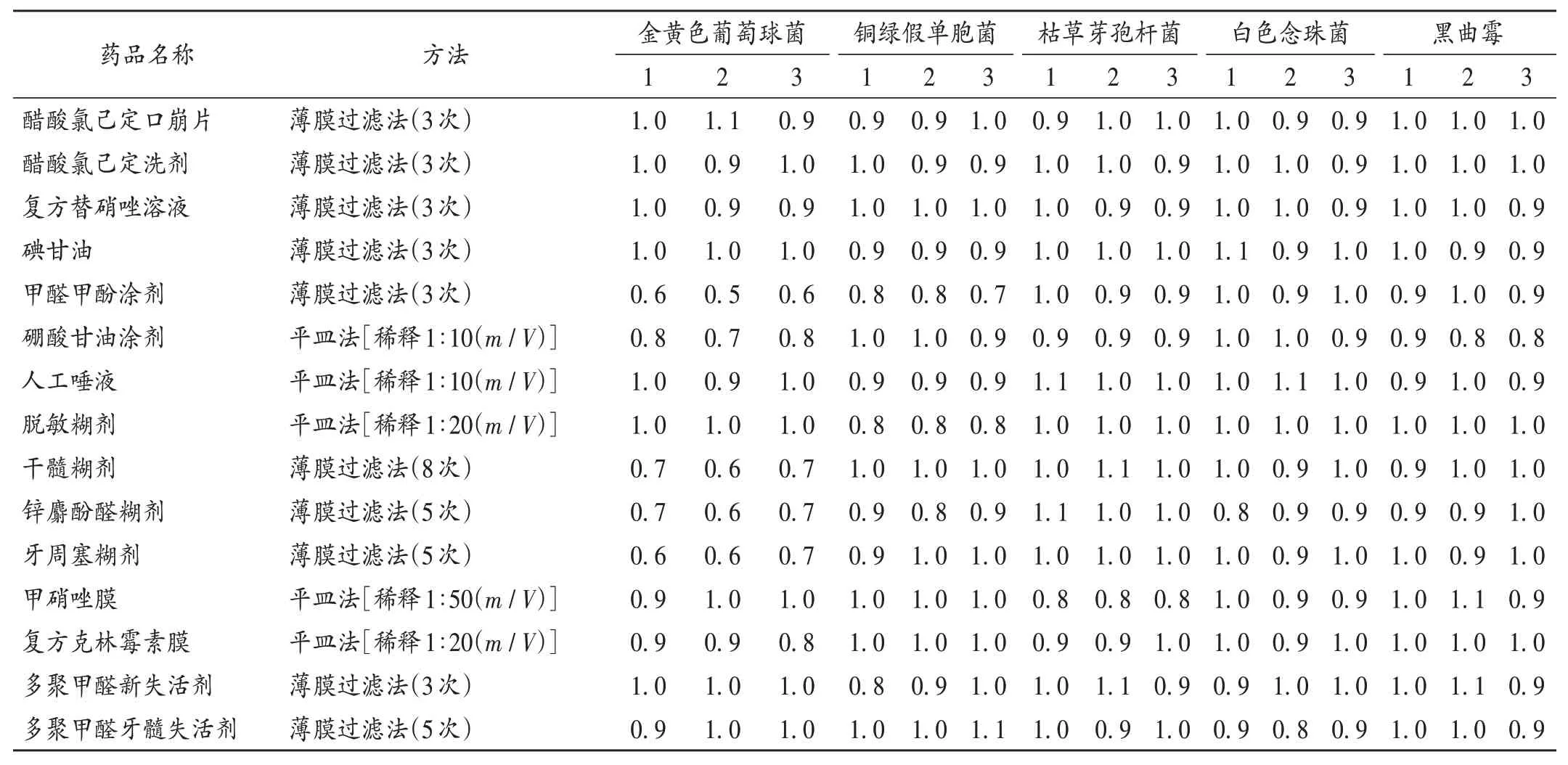
表1 需氧菌回收試驗結果(n=3)Tab.1 Results of the recovery test of aerobic bacteria(n = 3)
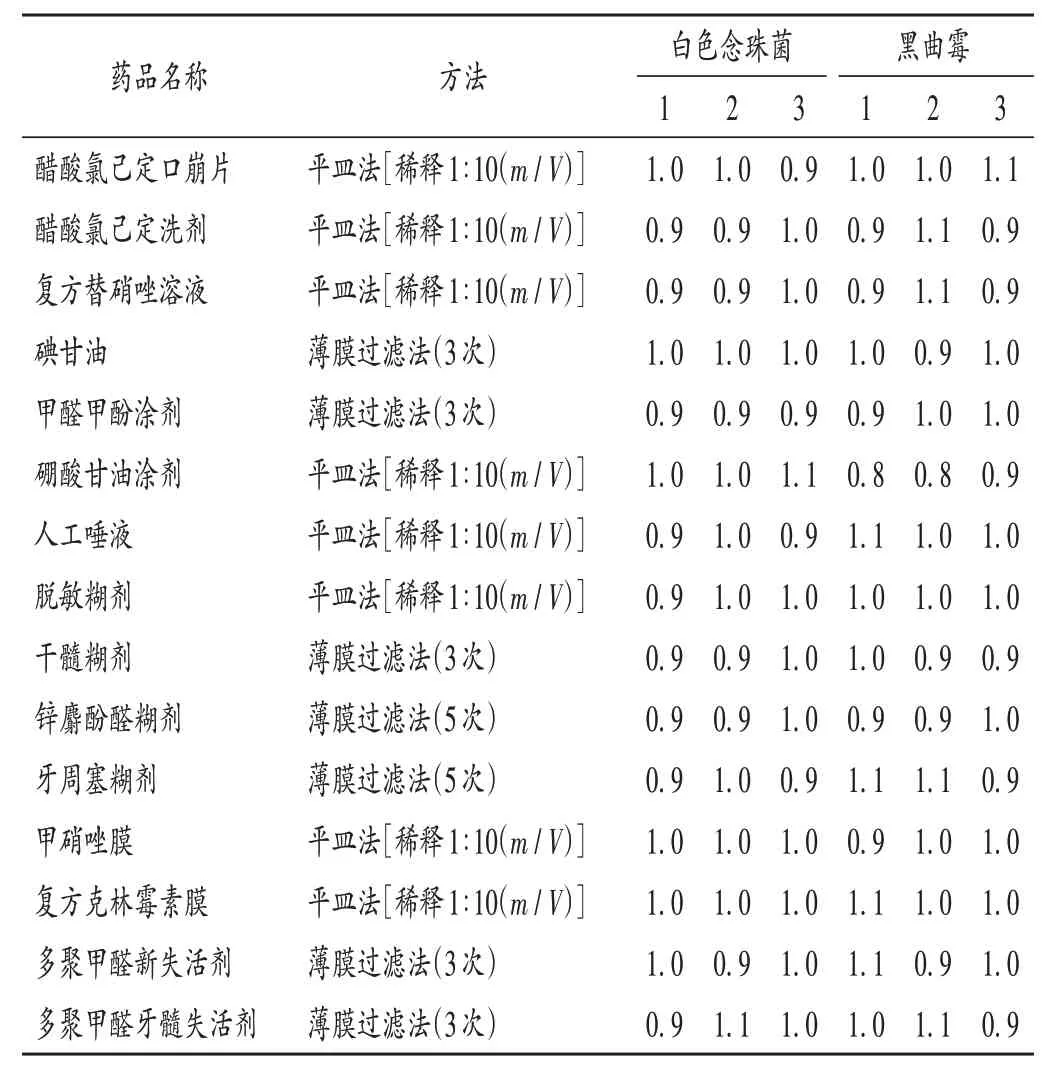
表2 霉菌及酵母菌回收試驗結果(n=3)Tab.2 Results of the recovery test of molds and yeasts(n = 3)
2.3 控制菌檢查法適用性試驗
2.3.1 金黃色葡萄球菌
培養基稀釋法:取2.1 項下供試品溶液Ⅰ10 mL,加入不少于100 mL的TSB中,加入不大于100 cfu 的相應試驗菌液1 mL,混勻,35 ℃條件下培養18 h;取TSB 劃線接種于MSA,35 ℃條件下培養18 h,觀察結果。以此作為試驗組。
薄膜過濾法:取2.1項下供試品溶液Ⅰ10 mL,加入含100 mL 稀釋液2 的濾器中,濾過,用稀釋液2 沖洗濾膜3~8 次,每次100 mL,取出濾膜,接種至100 mL TSB中,同時加入不大于100 cfu 的試驗菌液1 mL,35 ℃條件下培養18 h。將上述培養物接種于MSA,35 ℃條件下培養18 h,觀察結果。以此作為試驗組。
2.3.2 銅綠假單孢菌
采用培養基稀釋法和薄膜過濾法,按2.3.1項下方法操作,以TSB 35 ℃條件下培養18 h后,將其劃線接種于USP,35 ℃條件下培養18 h,觀察結果。以此作為試驗組。
2.3.3 大腸埃希菌
采用培養基稀釋法和薄膜過濾法,按2.3.1項下方法操作,以TSB 35 ℃條件下培養18 h 后,取1 mL 接種至100 mL麥康凱液體培養基中,42 ℃條件下培養24 h,取培養物劃線接種于麥康凱瓊脂培養基上,35 ℃條件下培養18 h,觀察結果。以此作為試驗組。
以上3種控制菌檢查均另設陽性對照組(以稀釋液2替代供試品溶液,加入試驗菌,同試驗組方法操作)、陰性對照組(以稀釋液2替代供試品溶液,不加試驗菌,同試驗組方法操作)。
2.3.4 驗證試驗
控制菌檢查,制劑1-3、5、9-11、14-15采用薄膜過濾法,其余采用培養基稀釋法,試驗組相應陽性菌均能正常檢出。詳見表3(僅列出最優檢查方法)。
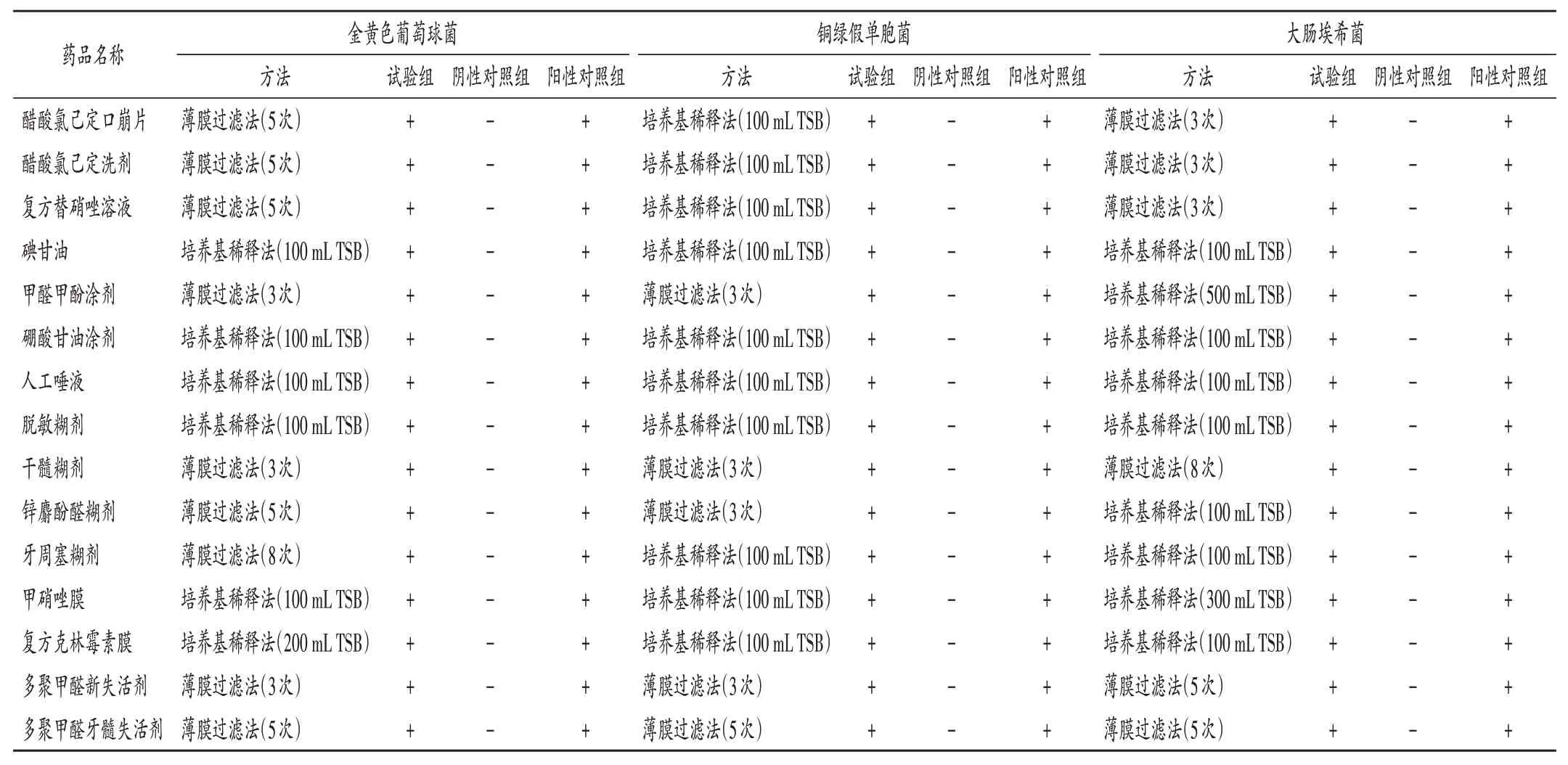
表3 控制菌檢查法適用性試驗結果Tab.3 Results of applicability test of control bacteria detection
3 討論
常見的口腔疾病包括牙齦炎、牙周炎、牙髓炎、復發性口腔潰瘍等,臨床用藥多采用局部治療方式以消除口腔炎癥,控制術后感染,故醫院口腔制劑多含有抑菌成分。不同單位生產的制劑,即使所含主要成分相同,由于采用的制備工藝和輔料不同,制劑仍可能表現出不同的抑菌特性,故微生物限度檢查方法應具有針對性和適用性[1]。
本研究中建立了15種含抗菌藥物及消毒防腐劑的醫院口腔制劑的微生物限度檢查方法。抗菌藥物中替硝唑和甲硝唑均屬硝咪唑類,能抑制細菌DNA 的合成,從而干擾其生長、繁殖,對厭氧菌的活性較高[5-6];克林霉素磷酸酯為克林霉素衍生物,主要通過作用于細菌核糖體的50 S 亞基,從而抑制細菌合成蛋白質,對革蘭陽性菌的抑制作用較強[7],對于含上述成分的制劑可采用平皿法和培養基稀釋法進行檢查。消毒防腐劑中醋酸氯己定為季銨鹽類陽離子表面活性劑,通過破壞細胞膜而產生抑制活性[8];碘、氧化鋅具有化學活性,可與細菌內的多種有機物發生氧化反應,從而把大部分細菌殺滅[9-10];甲醛、甲酚、羥苯乙酯可使菌體蛋白變性從而發揮殺菌作用[11-13];硼酸通過與氨基結合,鞣酸和麝香草酚通過與氫鍵或疏水鍵結合,從而使菌體蛋白變性,還可通過抑制細菌代謝所需酶的活性發揮抑菌作用[14-16],上述成分組成復方制劑后抑菌作用更強,故需聯合采用培養基稀釋法、薄膜過濾法等方法進行檢查。
本研究針對制劑劑型和所含抑菌成分采用了不同的試驗方法,對于抑菌活性較強的制劑,采用平皿法若在最低稀釋級無法進行方法適用性試驗時,可增加稀釋液或培養基體積或采用薄膜過濾法進行檢查,以消除抑菌活性。
綜上所述,本研究中建立的方法操作便捷,結果準確,為醫院制劑微生物限度質量控制提供了可靠的檢測手段,對于保障制劑質量具有重要意義,同時也為類似抑菌制劑的檢查提供了研究思路。

