脾竇岸細胞血管瘤伴地中海貧血一例
楊丹萍,王盛錦,田大廣
昆明醫科大學第二附屬醫院,云南 昆明 650101,1.肝膽外科,2.胃腸外科
脾竇岸細胞血管瘤(littoral cell angioma,LCA)是由Falk等最早于1991年報道并命名,是一種臨床上罕見的脾臟良性腫瘤[1]。文獻報道其起源于脾血竇特殊的竇岸細胞,具有內皮細胞和組織細胞雙重分化特征[2]。臨床上大多數患者無明顯癥狀,在體檢時發現異常,少數可出現左上腹痛、脾功能亢進等表現。本例患者出現肝臟腫大、脾臟腫大、貧血、出血、感染等脾功能亢進的表現。LCA診斷主要依靠組織病理學檢查,僅依靠臨床表現和影像學表現,很難將其與其他脾臟良性或惡性腫瘤鑒別開來。本例患者LCA伴地中海貧血,尚不清楚二者之間是否有關聯,現報道如下。
病例
患者男性,32歲,因“乏力1個月、腹瀉7 d”于2021年3月9日入院,5年前體檢時發現脾腫大,偶有牙齦出血、鼻出血,無腹痛、腹脹、嘔血、便血。查體:腹部平坦,腹部無壓痛、反跳痛,脾臟中度腫大。實驗室檢查:血小板73×109/L,紅細胞2.90×1012/L,血紅蛋白48 g/L,總蛋白51.0 g/L,白蛋白33.6 g/L。地中海貧血基因檢測示CD17和βE突變。影像學檢查可見肝臟、脾臟明顯腫大,多個臟器受壓變形,脾臟血管增粗,見圖1。患者入院后紅細胞、血小板進一步降低,白細胞升高,肝功能、凝血功能異常,請血液科會診,行相關檢查后診斷為脾腫大、肝腫大、地中海貧血,給予輸血、輸液等對癥支持治療。但因腫大的脾臟壓迫胰腺和腎臟以及脾臟占位性質未明,于2021年3月10日行開腹全脾切除術。術后病理:腫瘤由大小不一,互相吻合或網的血管腔組成,表面覆有單層內皮細胞,見圖2。免疫組化:CD21(+),CD8(+),SMA(+),CD31(血管+),CD3(+),CD20(+),Ki-67(20%),VIM(+),CD34(+)。術后診斷為LCA伴髓外造血。患者術后9 d順利出院,術后1個月影像學檢查未見明顯異常,隨訪至2023年11月,恢復良好。
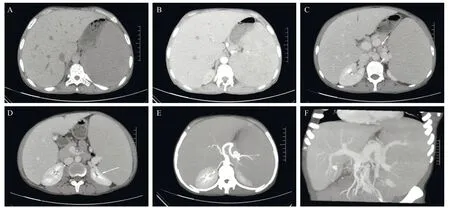
圖1 LCA伴地中海貧血患者的上腹部CT平掃+增強掃描
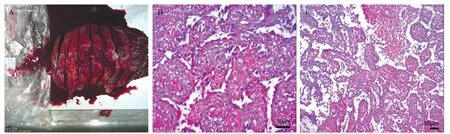
圖2 LCA伴地中海貧血患者的脾臟大體標本和病理圖片
討論
LCA的病因尚不清楚,但最近有研究認為,硫唑嘌呤等免疫抑制劑或生物活性TNF-α引起的免疫異常可能與LCA的發生有關[3-4]。各年齡段均可發生LCA,以50歲居多,男女比例在5∶3左右[5]。目前研究認為,LCA是一種良性腫瘤,原發于脾臟,但不排除潛在惡性的可能性,且有研究表明,LCA患者可并發惡性腫瘤如肝癌、胰腺癌、結直腸癌、腎癌等[2]。本例患者LCA與地中海貧血并發,尚不清楚二者之間的聯系。
影像學檢查對LCA的診斷具有重要價值,大多數LCA以脾彌漫性多發性結節狀病灶為特征,極少數表現為孤立性單發結節。CT在鑒別脾臟腫瘤病變性質、血供、與周圍器官的聯系等方面具有較大的優勢,是目前最有價值的影像學診斷方法之一。本例患者的CT示肝臟、脾臟明顯腫大,胰尾部受壓移位,左腎受壓變形。增強掃描肝臟未見異常強化灶,脾臟內可見多發類圓形低密度影,未見強化。脾動脈明顯增粗迂曲,門靜脈主干增寬、脾靜脈增粗迂曲。LCA的MRI成像取決于竇岸細胞內吞噬沉積的含鐵血黃素,表現為T1 加權成像顯示低信號,T2加權成像強度不定,診斷不具有特異性。本例患者MRI示脾臟明顯增大,其內見多發小斑片狀長T1、稍長及短T2 信號影;肝臟、脾臟明顯增大,肝臟、胰腺、脾臟信號異常,考慮鐵沉積,脾臟多發小結節。
組織病理學檢查是目前診斷LCA最有價值的檢查,也是確診的主要手段。大體標本見脾體積增大,切面灰紅、質軟,有單個或多個結節。組織學特征是病變由類似脾血竇的吻合血管組成,通常伴有乳頭狀或囊性擴張,其中有兩種細胞類型,兩種細胞均缺乏異型性,且免疫組化表現不同。一類與正常脾臟竇岸細胞形態非常相似,排列在乳頭狀擴張的表面,體積較小,具有內皮細胞特性,免疫組化示細胞CD31(+)、FVⅢ(+)、CD34(-);另一類組織細胞體積更大,常與管腔分離,免疫組化示CD68(+)。在光鏡下,腫瘤組織位于邊界清晰的灰質中,腫瘤內部見相通的竇道,周圍是纖維細胞基質,竇道表面覆有單層內皮樣細胞。
LCA臨床上需要與脾血管瘤、脾錯構瘤、血管肉瘤、脾竇岸細胞血管肉瘤等進行鑒別,僅靠影像學難以區分,尚需病理組織學檢查結果。脾血管瘤是最常見的脾臟良性腫瘤,可分為毛細血管瘤及海綿狀血管瘤兩種類型,常呈膨隆或裂隙狀,內層為平坦的內皮細胞,在各發育時期的管腔中易形成微血栓,常有內皮分子標志物CD31、CD34 及FVⅢRAg等。其影像學特征為“快進慢出的向心性強化”,也就是在動脈期,從瘤緣到中心不均勻強化,再到門脈期和延緩期進一步增強的向心強化[6-8]。血管肉瘤大體病理可發現在脾臟實質中有大量的紫紅色小結節,常伴有出血、壞死和囊性變[9],表現為迷宮狀血管腔,內襯為多形性和上皮性紡錘形結構,內皮細胞異常,常表現為核分裂,腫瘤細胞沿血管壁呈巢狀或乳頭狀發展。硬化性血管瘤樣結節轉化是一種特有的脾臟紅髓非腫瘤性病變,樹枝狀的纖維分割對診斷具有一定的價值。CD34、CD31和CD8聯合應用能鑒別病灶內三種不同的血管,其三種血管成分及多個模糊結節是鑒別本病的重要依據[10]。竇岸細胞血管肉瘤病理組織見血管吻合,內皮細胞呈片狀增生,常伴出血壞死及核分裂。與LCA相比,竇岸細胞血管肉瘤中CD8、CD34呈陽性,而CD21、FVⅢ RAg呈陰性,Ki-67增殖指數更高[5]。脾錯構瘤是一種罕見的良性血管增生性病變,由無組織的竇狀通道組成,內襯有豐滿或扁平的內皮細胞,其特征在于襯里細胞的CD8陽性的免疫表型。
目前LCA的治療方法以外科手術為主,可采用腹腔鏡/開腹全脾切除。對于病灶范圍較小、單個病灶較小的單一病灶,在全面評估后,可施行脾部分切除術。近年來,腹腔鏡下脾切除已成為LCA的主要治療方法。本例患者因“乏力1 個月、腹瀉7 d”入院,影像學檢查提示巨脾且多個臟器受壓變形,行開腹全脾切除術,術后復查受壓迫臟器已無明顯異常;患者入院時血細胞分析示重度貧血,地中海貧血基因檢測示CD17和βE突變,住院期間嚴密監測血象的同時給予輸血治療,但患者血紅蛋白等指標升高并不明顯,行脾臟切除術后患者血紅蛋白短期內快速恢復。術后7 d復查血常規,提示紅細胞較前升高、血紅蛋白指標恢復至輕度貧血狀態,凝血功能指標較前好轉,患者術后恢復良好。綜合既往文獻報道的病例分析,LCA患者的血象可表現為正常、白細胞和血紅蛋白降低或三系減低等多種形式;但血紅蛋白異常的患者僅報道了相關檢驗指標,忽略了患者的貧血類型、貧血程度,也未進一步探討貧血類型是否與該疾病相關。LCA患者多種血象表現是否可以反映疾病進程,有待后續更多研究論證。

