注射用氨芐西林鈉質量評價
劉旭春?姚羽?付曉麗?王丹?張玲變?周曉溪

摘要:目的 對注射用氨芐西林鈉的質量進行評價。方法 采用法定標準結合探索性研究對95批次注射用氨芐西林鈉進行檢驗,并與往年的兩次國抽結果進行縱向比較,評價本品的質量狀況。結果 按法定標準檢驗,95批次樣品全部符合規定。原料為冷凍干燥和溶媒結晶工藝的產品在堿度、有關物質、水分、含量等方面存在明顯差異。表現為冷凍干燥工藝的產品堿度相對較低,含量(按無水物計算)相對較低,雜質量、水分相對較高。探索性研究表明,在加速試驗條件下放置,隨著時間的增長,原料為冷凍干燥工藝的產品顏色加深,雜質增大;而溶媒結晶工藝的產品顏色和雜質變化較小。結論 注射用氨芐西林鈉總體質量較好,采用溶媒結晶工藝為原料的產品質量相對更優,原料是影響本品質量的主要因素。
關鍵詞:注射用氨芐西林鈉;質量評價;生產工藝
中圖分類號:R978.1文獻標志碼:A
Quality evaluate of ampicillin sodium for injection
Abstract Objective To evaluate the quality of ampicillin sodium for injection. Methods The quality of this product was assessed by conducting tests on 95 batches of samples using both the statutory standard procedures and exploratory research methods. Additionally, the product's quality was reviewed by comparing its results with three national random drug testing outcomes over a period of time. Results According to the statutory standards, 95 batches of samples all met the requirements. There were obvious differences in alkalinity, related substances, water and the content of samples between freeze-drying and solvent crystallization processes. The alkalinity and content calculated by anhydrous substance of freeze-dried products were relatively low. The impurities and moisture of freeze-drying products were relatively high. Under the condition of the accelerated test, the exploratory study showed that the color of raw materials with the freeze-drying process was deepened and the impurities increased, with the passage of time. However, the color and impurity of the products changed little in the process of solvent crystallization. Conclusions The quality of ampicillin sodium for injection was generally of good quality. The quality of products using the solvent crystallization process as the raw material was relatively better. The production process of the raw material was the main factor affecting the quality of the product.
Key words Ampicillin sodium for injection; Quality evaluation; Production process
氨芐西林鈉為廣譜半合成青霉素類抗生素,主要用于治療敏感細菌所致的呼吸道感染、泌尿系統感染、消化道感染、耳鼻喉感染、皮膚及軟組織感染等[1-2]。注射用氨芐西林鈉由氨芐西林鈉無菌原料直接分裝得到。目前,氨芐西林鈉原料和注射用氨芐西林鈉均收載于《中國藥典》2020年版。氨芐西林鈉原料的生產工藝包括溶媒結晶法和冷凍干燥法,其生產工藝對產品質量的影響已受到關注 [3-4]。
2022年注射用氨芐西林鈉被列為國家藥品抽檢品種。本文依據現行質量標準檢驗并結合探索性研究,對國內注射用氨芐西林鈉的關鍵質量屬性進行分析,并對2009、2011和2022年的抽檢結果進行縱向比較,探討產品存在的主要質量問題,明確提高產品質量的方向。
1 儀器與試藥
1.1 儀器
戴安U3000高效液相色譜儀(Thermo Fisher Scientific);賽多利斯CPA225D電子天平(Sartorius);梅特勒V30水分滴定儀(Mettler Toledo);戴安U3000/QE液質聯用儀(Thermo Fisher Scientific);Agilent 6890N氣相色譜儀(Agilent);Malvern 2000激光粒度分析儀(Malvern Panalytical));超純水機(ELGA)。
1.2 試藥
氨芐西林對照品(批號:130410-201908,含量:85.6%)、氨芐西林系統適用性對照品(批號:130618-201202)、頭孢拉定(批號:130427-201708)均購自中國食品藥品檢定研究院。乙腈為色譜純;磷酸二氫鉀、冰醋酸為分析純;水為超純水。
9個生產企業的95批次注射用氨芐西林鈉均為2022年國家藥品抽檢樣品,涉及19個批準文號和2個執行標準(《中國藥典》2020年版和國家藥品監督管理局標準YBH03372021)。其中,原料為冷凍干燥工藝的樣品有15批次,溶媒結晶工藝的有80批次。
2 試驗方法
2.1 法定標準檢驗
按照法定標準[5-6],對注射用氨芐西林鈉進行檢驗。主要項目包括有關物質、堿度、水分、含量測定等。
2.2 探索性研究
根據法定檢驗中出現的問題,通過文獻檢索[7-13]、
企業調研等,對產品的雜質譜、原料藥對制劑質量的影響、加速穩定性試驗等方面進行研究。
2.2.1 雜質譜研究
國家藥品監督管理局標準YBH03372021為制劑企業Z1通過一致性評價后的執行標準,參照此標準并結合國內原料多來源的實際情況,通過篩選色譜柱、調整流動相比例等對有關物質分析方法進行優化。
采用Waters Spherisorb ODS2色譜柱(4.6 mm×
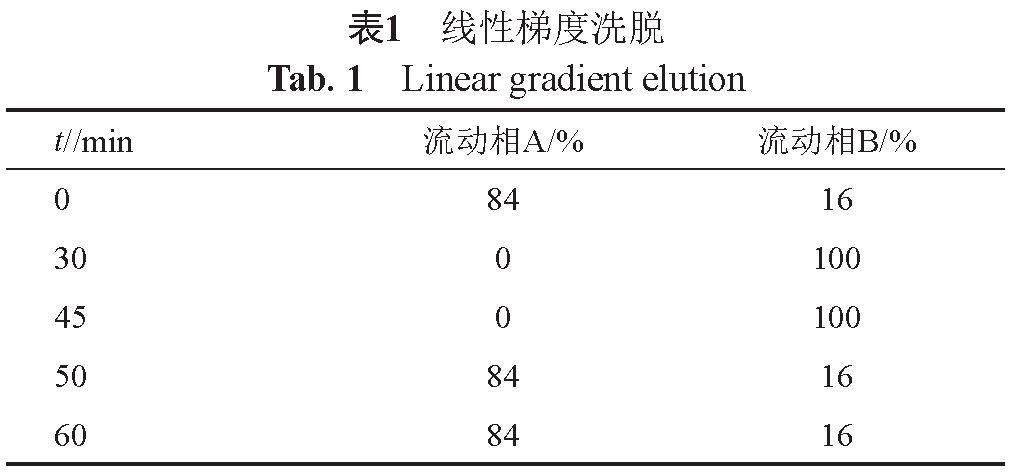
250 mm, 5 μm);流動相見《中國藥典》2020年版二部氨芐西林鈉項下,先以流動相A-流動相B(84:16)等度洗脫,待氨芐西林峰洗脫完畢后立即按表1進行線性梯度洗脫;柱溫為30 ℃;流速為0.6 mL/min;檢測波長為254 nm;進樣體積為20 μL。
2.2.2 原料藥對制劑質量的影響
選擇4家不同企業的氨芐西林鈉原料各1批,①采用粉末X-射線衍射法測定樣品的晶型;②依據《中國藥典》2020年版四部通則0861,測定上述原料中的殘留溶劑;③依據《中國藥典》2020年版四部通則0873,測定樣品中殘留的2-乙基己酸;④依據《中國藥典》2020年版四部通則0982,采用激光粒度分析儀對樣品的粒度分布進行測定。⑤選取不同原料來源的注射用氨芐西林鈉,參照國家藥品監督管理局標準YBH03372021,測試其復溶時間。
2.2.3 加速穩定性試驗
選取4家不同企業的注射用氨芐西林鈉共6批,于溫度40 ℃、相對濕度75%的條件下放置,分別于0、20、40和60 d進行測定,比較其性狀、水分、溶液的顏色、堿度、雜質等的變化情況。
3 結果與討論
3.1 法定標準檢驗結果
按照現行法定標準檢驗,95批次樣品均符合規定,合格率100%。
3.1.1 有關物質
對95批次樣品測定結果進行統計,氨芐西林閉環二聚體的量為0.24%~3.10%,其他總雜質的量為0.49%~3.23%。按原料工藝比較樣品中的雜質量,冷凍干燥工藝樣品閉環二聚體的量為1.50%~3.10%,其他總雜質的量為1.04%~3.23%;溶媒結晶工藝樣品閉環二聚體的量為0.24%~1.16%,其他總雜質的量為0.49%~1.45%。冷凍干燥工藝樣品閉環二聚體和其他總雜質的量明顯大于溶媒結晶工藝樣品。
3.1.2 堿度
95批次樣品的堿度在8.79~9.64之間。按原料工藝比較樣品的堿度,冷凍干燥工藝樣品的堿度為8.79~9.24,溶媒結晶工藝樣品的堿度為9.33~9.64,冷凍干燥工藝樣品堿度明顯低于溶媒結晶工藝樣品。
3.1.3 水分
采用費休氏法測定,95批次樣品的水分為0.04%~1.28%。按原料工藝比較樣品的水分,冷凍干燥工藝樣品的水分為0.80%~1.28%,溶媒結晶工藝樣品的水分為0.04%~0.24%,冷凍干燥工藝樣品水分明顯高于溶媒結晶工藝樣品。
3.1.4 含量測定
95批次樣品按無水物計算,含量在86.01%~93.71%之間;按平均裝量計算,含量在95.67%~106.29%之間。按原料工藝比較樣品氨芐西林(按無水物計算)的含量,冷凍干燥工藝樣品的含量為86.01%~90.91%,溶媒結晶工藝樣品的含量為88.49%~93.71%,冷凍干燥工藝樣品含量(按無水物計算)明顯低于溶媒結晶工藝樣品。
3.1.5 質量縱向比較
按法定標準檢驗,注射用氨芐西林鈉的合格率從2009年的98.61%到2022年的100%,質量呈現向好趨勢。其中,產品的水分和雜質量明顯下降,含量明顯增高(表2),說明該品種關鍵質量指標的控制水平顯著提升。
3.2 探索性研究結果
3.2.1 雜質譜研究
在《中國藥典》2020年版二部注射用氨芐西林鈉有關物質系統適用性溶液的基礎上增加系統適用性溶液2(原系統適用性溶液命名為系統適用性溶液1)。系統適用性溶液2為樣品經過熱破壞定位雜質O[6],使氨芐西林閉環二聚體和雜質O峰的分離度大于1.5,典型的色譜圖見圖1。
通過優化有關物質檢測方法,共檢出19個雜質(圖2),雜質確認情況詳見表3。
其中,3、8、10、13、17號雜質與氨芐西林系統適用性對照品比較,分別對應為氨芐西林噻唑酸、2', 5'-二酮哌嗪-2(R)氨芐西林、氨芐西林開環二聚體、氨芐西林閉環二聚體、氨芐西林開環三聚體;4號和14號雜質參考國家藥品監督管理局標準YBH03372021有關物質系統適用性溶液1、2的色譜圖分別確認為氨芐西林噻唑酸和雜質O(命名參照YBH03372021,結構式見圖3)。
3.2.2 原料藥對制劑質量的影響
(1)晶型研究? ? 4家不同企業的氨芐西林鈉原料X-射線衍射圖有明顯差異(圖4)。A1企業和A2企業的氨芐西林鈉均為結晶性粉末,粉末X-射線衍射圖中顯現有多個特征衍射峰,且圖譜基本一致;B1企業和B2企業提供的冷凍干燥工藝生產的氨芐西林鈉,粉末X-射線衍射圖中均無明顯的衍射峰,為無定型粉末。
(2)殘留溶劑? ? 原料中的殘留溶劑均在《中國藥典》2020年版四部通則0861規定的限度范圍內。B1和B2兩家企業冷凍干燥工藝的氨芐西林鈉原料均未檢出異丙醇,A1企業、A2企業的最大殘留溶劑分別為正丁醇和異丙醇(表4)。
(3)2-乙基己酸? ? 2家溶媒結晶工藝的氨芐西林鈉原料藥檢出2-乙基己酸,A1企業的量為0.18%,A2企業的量為0.28%;2家冷凍干燥工藝的氨芐西林鈉原料因生產過程中未用到2-乙基己酸,均未檢出。
(4)粒度分布? ? B1和B2企業為冷凍干燥工藝,原料粒徑相差較小;A1和A2企業為溶媒結晶工藝,原料粒徑相差較大,A2企業的粒徑明顯比A1企業的大(表5)。
(5)復溶時間? ? 冷凍干燥工藝樣品的復溶時間明顯較短。溶媒結晶工藝樣品中,來自A1企業的原料藥復溶時間更長。A2企業的原料粒徑更大,復溶時間反而較短,可能是粒徑較大能避免藥品加水后的粘連,減少其復溶時間(表6)。
通過對95批次樣品的堿度、水分、雜質、含量等測定結果和原料藥生產工藝等進行多因素相關分析,表明原料藥生產工藝與樣品的堿度、水分、雜質、含量(按無水物計算)等均顯著相關(P<0.01)。說明氨芐西林鈉原料藥的生產工藝是影響本品質量的主要因素。
3.2.3 加速穩定性試驗
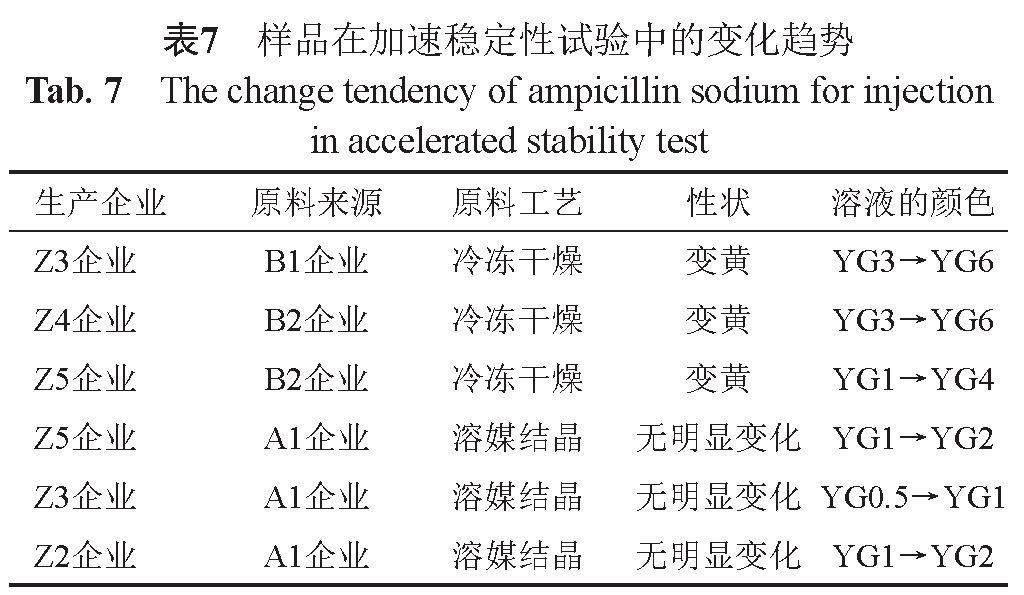
按《中國藥典》2020年版二部檢測樣品的性狀、水分、溶液的顏色和堿度,按優化后的色譜條件檢測樣品有關物質。結果顯示,樣品的堿度和水分無明顯變化;性狀和溶液的顏色變化與原料工藝相關(表7),原料為冷凍干燥工藝的樣品變化明顯,溶媒結晶工藝的樣品變化較小。
進一步比較樣品中閉環二聚體及其他總雜質的變化趨勢,二者均呈現增大趨勢(圖5)。其中,原料來源為B1和B2企業的樣品增大趨勢更加明顯。可見,原料為溶媒結晶工藝的樣品較冷凍干燥的更穩定。
通過對3年國抽結果的縱向比較發現,氨芐西林鈉原料藥生產工藝中,質量及穩定性最差的噴霧干燥工藝已被淘汰,冷凍干燥工藝所占的比例也不斷下降,質量及穩定性最好的溶媒結晶工藝所占的比例大幅增長(圖6)。
4 結論
本次國家藥品抽檢結果顯示,國內注射用氨芐西林鈉總體質量較好,合格率100%。
通過標準檢驗和探索性研究發現,影響本品質量的主要因素為原料藥的生產工藝。原料藥生產工藝不同,制劑質量存在差異。溶媒結晶工藝的產品水分和雜質量均小于冷凍干燥工藝產品,且穩定性也優于冷凍干燥工藝的產品。
通過縱向比較發現,氨芐西林鈉原料藥生產工藝有大幅改進,噴霧干燥工藝產品已被淘汰,冷凍干燥工藝產品所占的比例也不斷下降,質量及穩定性較好的溶媒結晶工藝產品所占的比例大幅增長。
參 考 文 獻
中華醫學會, 中華醫院管理學會藥事管理專業委員會, 中國藥學會醫院藥學專業委員會. 抗菌藥物臨床應用指導原則[J]. 中華醫學雜志, 2004, 84(23): 2026-2056.
岑海燕, 吳建國, 陳燕, 等. 老年性尿路感染的流行病學及診治現狀[J]. 國外醫藥(抗生素分冊), 2023, 44(6): 379-382.
周曉溪, 李青翠, 郭景文, 等. 注射用氨芐西林鈉質量研究[J]. 藥物分析雜志, 2011, 31(5): 875-878.
李一蘭, 周曉溪, 姚羽, 等. 注射用氨芐西林鈉氯唑西林鈉質量評價[J]. 中國抗生素雜志, 2019, 44(3): 295-299.
國家藥典委員會.中華人民共和國藥典[S]. (2020年版二部). 北京: 中國醫藥科技出版社, 2020: 1373.
國家食品藥品監督管理局. 國家食品藥品監督管理局標準[S]. YBH03372021.
胡昌勤. 對抗生素藥品評價性抽驗基本思路與方法的思考[J]. 中國抗生素雜志, 2013, 38(1): 1-11.
周曉溪, 郭景文, 鄭臺, 等.國產注射用氨芐西林鈉雜質譜與其生產工藝的相關性研究[J]. 藥物分析雜志, 2013, 33(3): 486-489.
國家食品藥品監督管理局. 國家食品藥品監督管理局標準[S]. YBH01412022.
薛晶, 尹利輝, 鄒文博, 等. 生產工藝對氨芐西林鈉質量的影響[J]. 中國藥物雜志, 2011, 46(23): 1833-1839.
黃婕, 滕鈺, 徐洪, 等. 國產氨芐西林膠囊質量評價[J]. 中國抗生素雜志, 2018, 43(3): 296-302.
石秀梅, 朱全讓, 王希敏, 等. 氨芐青霉素鈉合成的研究[J]. 山東科學, 1990, 3(1): 55-58.
黃小璧, 李子熊. 氨芐西林質量分析[J]. 廣東藥學, 2004, 14(2): 23-25.

