脫氫膽酸調控OPG/RANK和TRAF3抑制破骨細胞分化
朱禹潼 張曉楠 關溪 尚東,3*
1.大連醫科大學附屬第一醫院中西醫結合臨床重點學科實驗室,遼寧 大連 116011
2.大連醫科大學中西醫結合研究院(學院),遼寧 大連 116044
3.大連醫科大學附屬第一醫院普外三科,遼寧 大連 116011
骨質疏松癥是一種代謝性骨病,以骨量丟失和結構退化為特征,易發生脆性骨折[1]。骨質疏松癥影響著全球2億多人[2]。在中國,骨質疏松癥和老齡化的速度都在上升。中國男性和女性老年人大于50歲的骨質疏松患病率分別為6.46%和29.13%[3]。在全球范圍內,骨質疏松及其相關的脆性骨折給患者帶來了巨大的健康和經濟負擔,一直是主要的健康問題[4-5]。目前治療骨質疏松的藥物有雙膦酸鹽、降鈣素、選擇性雌激素受體調節劑和地諾單抗[6]。然而,大多數藥物有嚴重的副作用或不適合長期使用。
骨骼經過不斷的重塑以保持礦化平衡和結構完整性。骨重建過程中,成骨細胞(骨形成)與破骨細胞(骨吸收)相互作用導致骨穩態[7]。過度骨吸收引起的骨穩態紊亂可導致骨質疏松[8]。來自單核巨噬細胞的破骨細胞(osteoclasts,OCs)促進骨吸收。巨噬細胞集落刺激因子(macrophage colony-stimulating factor,M-CSF)和核因子κB受體活化因子配體(receptor activator of nuclear factor-κB ligand,RANKL)共同誘導破骨細胞分化[9]。NF-κB受體活化因子(receptor activator of NF-κB,RANK)與RANKL結合,通過激活一系列下游靶向因子激活OCs[10]。
脫氫膽酸(dehydrocholic acid,DHCA)是一種人工合成的膽汁酸衍生物。DHCA作為一種利膽藥,用于治療急性膽源性胰腺炎,可抑制胰腺組織水腫和壞死[11]。也用于治療膽管功能障礙、膽囊結石等疾病。然而,DHAC在骨質疏松癥中的作用尚不清楚。有研究首次報道了正常人血清中DHCA含量顯著高于骨質疏松患者[12]。因此,DHCA可能是用于治療骨質疏松的一種新方法,本文研究了DHCA在體外對OCs分化和功能的影響。
1 材料與方法
1.1 材料
粒細胞-巨噬細胞集落刺激因子(美倫公司);RANKL(MedChemExpress公司);Phalloidin-iFluor 594(Abcam公司);OPG和β-actin單克隆兔抗小鼠抗體(Abcam公司);RANK單克隆兔抗小鼠抗體(Zenbio公司);TRAF3單克隆兔抗小鼠抗體(Proteintech公司);TRAP染色試劑盒(Genmed scientific公司);RNA提取試劑盒、Evo M-MLV逆轉錄試劑盒和SYBR?Green Pro Taq HS預混qPCR試劑盒(艾科瑞公司);DHCA(CAS編號81-23-2,Panphy Chemicals公司)。
1.2 方法
1.2.1骨髓巨噬細胞的分離與培養:由大連醫科大學實驗動物中心提供雄性C57BL/6小鼠(6~8周齡,體重20 g左右)用于研究(許可證號:AEE19001)。所有小鼠麻醉后頸椎脫位處死。將脛骨和股骨置于無菌超凈實驗臺上,去除脛骨和股骨上的肌肉后,將骨骼置于PBS中。剪斷骨骺,用PBS輕輕沖洗股骨和脛骨的髓腔,直至骨變成半透明。將細胞懸液離心(1 000 r/min,5 min),加入5 mL紅細胞裂解液重懸細胞,4 ℃靜置10 min后離心。在DMEM培養基(10%FBS+20 ng/mL GM-CSF)中培養3 d獲得BMMs。
1.2.2破骨細胞的分化:BMMs在DMEM(10% FBS+20 ng/mL GM-CSF+50 ng/mL RANKL)完全培養基中分化為OCs。DHCA(10、50、100、150、200 μmol/L)與BMMs共培養至OCs分化成熟。培養4 d后采用TRAP染色法對OCs進行計數,顯微鏡下觀察≥3個細胞核被視為OCs[13]。
1.2.3細胞活力測定:將細胞懸液接種于96孔板(2×103細胞/孔),孵育3 d。在第4天,實驗組每孔分別加入10、50、100、200、500、1 000 μmol/L DHCA,每組6個復孔,孵育4 d后,加入CCK8孵育2 h后在波長450 nm,測定各孔的吸光度值。
1.2.4破骨細胞F-肌動蛋白(F-actin)染色:DHCA作用培養4 d采用F-actin染色。取出細胞培養皿,PBS沖洗細胞3次。4%多聚甲醛固定,0.5% Triton X-100溶液透化處理。加入Phalloidin-iFluor 594對F-actin染色。使用DAPI對細胞核進行復染,共聚焦顯微鏡下進行熒光觀察。
1.2.5qRT-PCR:Trizol法提取總RNA。使用Evo M-MLV逆轉錄試劑盒進行逆轉錄反應。最后,采用SYBR?Green Pro Taq HS預混qPCR試劑盒檢測OCs形成和分化相關基因。采用2-△△Ct法對結果進行分析。引物序列見表1。

表1 引物序列
1.2.6Western blot:培養至OCs分化成熟后,提取細胞蛋白。SDS-PAGE跑膠,轉移到PVDF膜上,然后用5%脫脂牛奶封閉1 h,按照說明書稀釋TRAF3、OPG、RANK(1∶2 000)和β-actin(1∶5 000),4 ℃孵育過夜。二抗(1∶10 000)于次日室溫孵育1 h。采用ECL系統(Tanon-5200)進行印跡檢測。根據灰度值數據(ImageJ 1.8.0)分析各蛋白的相對表達量。
1.3 統計分析
使用GraphPad Prism 8.4.3對所有數據進行分析,用t檢驗分析兩組間的顯著性差異。P<0.05為差異有統計學意義。
2 結果
2.1 DHCA抑制破骨細胞形成
為探討DHCA抑制OCs分化的有效濃度,首先檢測DHCA的細胞毒性,結果顯示當DHCA濃度≥500 μmol/L時,細胞活力下降(圖1A)。隨后分別用10、50、100、150、200 μmol/L DHCA干預OCs分化。TRAP染色顯示,與未使用DHCA的對照組相比,DHCA處理后TRAP陽性細胞(紅色區域)數量呈劑量依賴性減少。DHCA在200 μmol/L時對OCs分化的抑制率最大(圖1B、1C)。
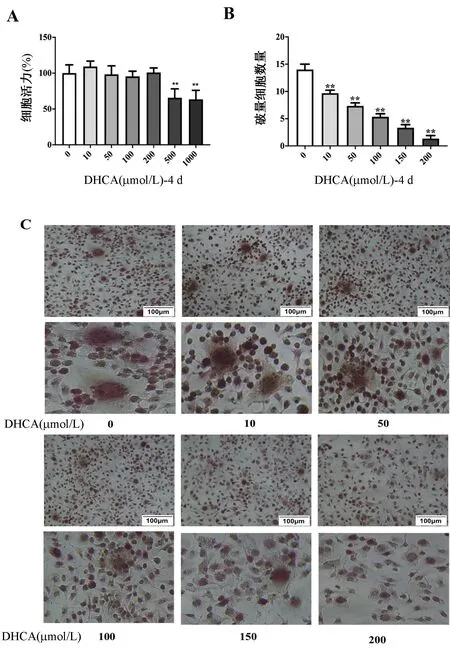
圖1 DHCA抑制破骨細胞分化
2.2 DHCA抑制破骨細胞F-actin環的形成
采用破骨細胞F-actin染色,以觀察成熟的破骨細胞F-actin的形成。與對照組(未使用DHCA)相比,DHCA能抑制F-actin環的形成,見圖2。

圖2 DHCA抑制破骨細胞F-actin環的形成
2.3 DHCA抑制破骨細胞形成與分化功能相關基因表達
用200 μmol/L DHCA干預OCs分化,qRT-PCR檢測OCs特異性基因ACP5、CTSK和MMP9的表達水平。如圖3所示,與對照組(未使用DHCA)相比,DHCA顯著抑制了與OCs分化成熟相關的ACP5 mRNA,以及與骨吸收功能相關的CTSK和MMP9 mRNA的表達。
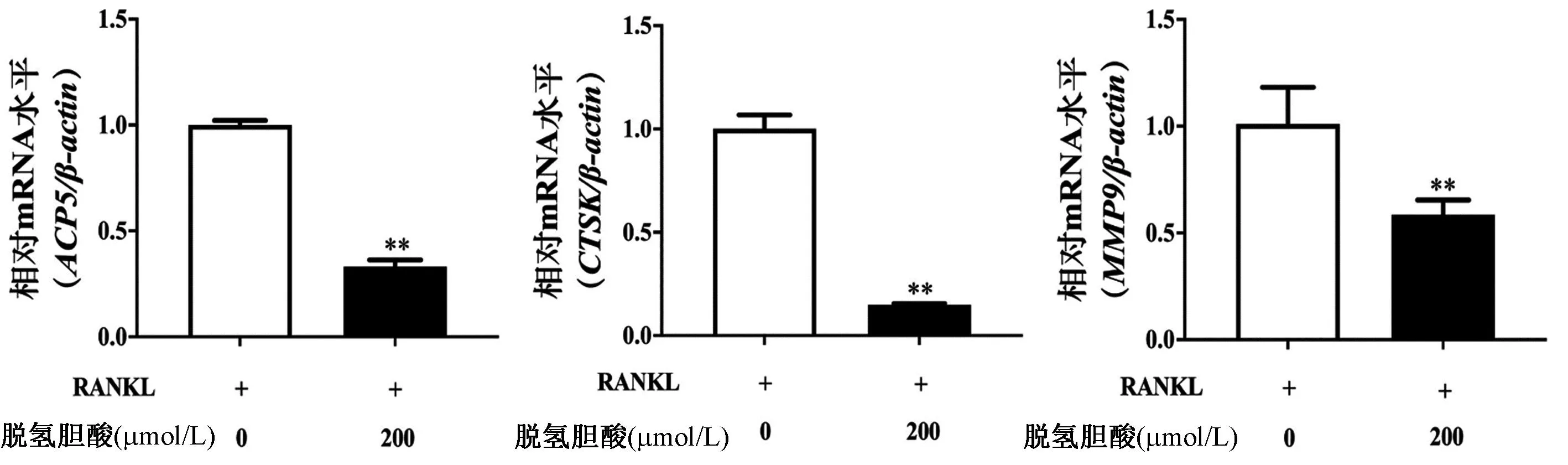
圖3 DHCA抑制破骨細胞特異性基因表達
2.4 DHCA通過OPG/RANK和TRAF3抑制破骨細胞分化
Western blot結果顯示,與對照組(未使用DHCA)相比,DHCA顯著增加OPG水平,降低RANK水平,見圖4。結果表明,DHCA通過抑制OPG/RANK/RANKL信號通路抑制OCs分化。RANKL刺激后,TRAF3蛋白水平降低,DHCA可逆轉該作用。DHCA可通過抑制TRAF3蛋白降解從而抑制OCs分化。
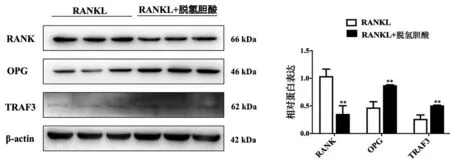
圖4 DHCA通過OPG/RANK和TRAF3抑制OCs分化(DHCA體外作用4 d)
3 討論
骨重建功能穩態依賴于成骨細胞的骨形成和OCs的骨吸收的共同維持。OCs的過度激活導致骨量丟失和骨微結構破壞,導致骨質疏松性骨病。抑制OCs的活化、分化和功能是目前公認的治療骨質疏松的有效方法。目前尚無DHCA用于治療骨質疏松或其他骨代謝疾病的報道。根據代謝組學分析,骨質疏松患者血清中DHCA含量較正常人明顯降低,為骨代謝疾病藥物的開發提供了拓展思路。在OC和OC前體細胞中,RANKL與其配體RANK結合,通過激活下游通路,包括NF-κB和絲裂原活化蛋白激酶,刺激OC相關下游因子的表達,導致OC的分化、活化和成熟[14-15]。本研究中,TRAP染色顯示DHCA以劑量依賴性方式抑制RANKL誘導的OCs形成。ACP5在活化的OCs中高表達,是OCs分化的特異性基因。CTSK是OCs中最重要的細胞因子,對骨組織具有特異性降解活性,反映了OCs的骨吸收功能[16]。MMP參與了骨的發育、修復以及細胞外基質的重塑。OCs分化過程中MMP9的表達上調,進而刺激骨吸收[17-18]。本研究發現DHCA通過下調ACP5、CTSK和MMP9基因的表達來抑制OCs分化和骨吸收。
OPG/RANK/RANKL信號通路在調控成骨細胞和OCs的成熟和分化,維持成骨細胞和OCs的動態平衡中發揮重要作用[19]。OPG/RANKL/RANK信號的異常調控是骨質疏松發生的前提。OC前體細胞或OC表面RANK與RANKL結合,介導信號激活OC前體細胞分化為成熟OC,抑制OC凋亡[20-21]。OPG是一種分泌型糖蛋白,屬于TNF受體超家族。OPG可與RANKL競爭性結合,從而抑制RANKL與RANK結合,抑制OCs分化和骨吸收活性[22-23]。DHCA可上調OPG蛋白的表達,下調RANK蛋白的表達,表明DHCA通過OPG/RANK/RANKL信號通路抑制OCs分化。
TNF受體相關因子(TNF receptor-associated factors,TRAF)是OCs中RANK激活所必需的[24]。RANK通過招募TRAFs啟動下游信號級聯[25]。TRAFs由多種亞型組成,TRAF2、TRAF3和TRAF6在OCs分化的研究中常見。TRAF3使cIAP1/2介導K48-link泛素化,導致蛋白酶體中TRAF3降解,激活非經典NF-κB信號通路[26-28]。TRAF3抑制衰老中破骨細胞的生成[29]。此外,一項研究表明氯喹可以通過阻止TRAF3降解來減少破骨細胞的生成[30]。本研究結果表明TRAF3是OCs形成的重要負調控因子,表明DHCA可以通過阻斷TRAF3的降解來抑制OCs的形成。
綜上所述,本研究表明DHCA抑制OCs形成與分化,可能是通過抑制OPG/RANK/RANKL信號通路及阻斷TRAF3降解,抑制OCs形成與分化。

