肝炎病毒感染導致肝細胞癌發生的免疫機制研究進展
徐令東,徐逸帆,張 飛,4,徐平龍,4,5,6,汪 洌
1. 浙江大學實驗動物中心,浙江 杭州 310058
2. 浙江大學醫學院,浙江 杭州 310058
3. 浙江大學生命科學研究院,浙江 杭州 310058
4. 浙江大學杭州國際科創中心智能醫藥研究所,浙江 杭州 311200
5. 浙江大學生命系統穩態與保護教育部重點實驗室 浙江省癌癥分子細胞生物學重點實驗室,浙江 杭州 310058
6. 浙江大學癌癥研究院,浙江 杭州 310058
肝細胞癌占原發性肝癌的90%。由于其早期診斷困難,往往出現明顯癥狀時已經是中晚期,最終影響治療的有效性[1]。臨床統計數據表明,病毒性肝炎持續性感染導致的慢性肝炎和肝硬化是引發肝細胞癌的主要因素[2]。在五種不同的肝炎病毒中,HBV和HCV在肝細胞癌的致病因素中最為重要[2-3]。全球范圍內,由HBV感染導致的肝細胞癌占45%[4];在我國,由HBV所致的肝細胞癌更是占到了84%[5]。由于受到免疫微環境的壓力篩選,隨著HBV感染時間的推移,其基因序列突變也隨之增加,這不僅增加了癌癥發生的相關風險,同時也增加了HBV 感染預防和治療的難度[6]。我國HCV 慢性患者約450 萬人,其中有20%左右的患者會發展為肝硬化甚至肝細胞癌[7]。HAV感染不會直接導致肝細胞癌的發生,但其對免疫細胞的影響是多方面的,包括影響免疫細胞的侵襲、干擾信號轉導和誘導凋亡等,從而削弱免疫應答,增加肝細胞癌發生風險[8]。HDV 可以與HBV 共感染,加劇肝臟損傷,使肝炎更易呈慢性化發展,因此HDV的潛在危害不可忽視[9]。HEV是導致急性肝炎的主要病原體。近些年,免疫缺陷人群中HEV慢性感染造成肝硬化的病例日益增多,其感染導致肝細胞癌發生的潛在風險也日益增大[10]。此外,肝炎病毒急性感染會間接促進肝細胞癌的發生,肝炎病毒急性感染介導的組織損傷可能進一步發展為自身免疫性肝炎,并隨后發展為肝硬化甚至肝細胞癌,這是一個病毒和宿主動態互作的過程[11]。“癌癥進化發育學”為肝炎病毒感染導致肝癌的機制給出了完整的理論框架:以HBV為代表的肝炎病毒在感染宿主的過程中,一方面,病毒會在宿主的免疫微環境壓力下發生突變以適應宿主;另一方面,宿主會在病毒誘導下使體內原來沉默的原癌基因再次表達[12]。肝炎病毒感染在宿主細胞內觸發一系列分子事件,如表觀遺傳修飾、介導NF-κB、Wnt和p53等信號通路的激活與肝細胞癌的風險密切相關[13]。本文對五種肝炎病毒直接誘導肝細胞癌或通過調控宿主因子導致肝細胞癌的相關研究進展進行總結,以期為肝炎病毒感染導致肝細胞癌發生的臨床和基礎研究提供參考。
1 甲型肝炎病毒感染導致肝細胞癌發生的免疫機制
HAV 為小RNA 病毒科嗜肝病毒屬,是單股正鏈RNA 病毒,基因組大小為7.8 kb,病毒呈二十面體立體對稱結構,直徑約27 nm,存在無囊膜和類囊膜兩種病毒形式[14]。HAV 基因組編碼的結構蛋白為組成病毒顆粒的主要成分,包括VP1、VP2、VP3 和VP4;非結構蛋白參與病毒的復制和轉錄過程,主要包括聚合酶和其他輔助蛋白[14]。
過去一直認為HAV 感染與肝細胞癌的發展無關[15],但統計結果顯示,感染HAV 會削弱患者的抵抗力,從而增加感染HCV 的概率,而HCV 與肝細胞癌密切相關[16]。此外,HAV 能介導組織損傷,這意味著其可能可以間接促進肝細胞癌的發生[16]。研究顯示,HAV 相關性組織損傷并非由病毒本身直接導致,而是通過引發強烈的CD8+T 細胞免疫反應介導,非HAV特異的CD8+T細胞、NK細胞和NKT 細胞等其他免疫細胞也參與其中[8]。此外,在HAV 感染小鼠模型中,由MAVS 激活信號介導的固有凋亡似乎是肝炎的原因之一[17]。宿主和病毒因子的遺傳變異也可以影響HAV 感染的嚴重程度,如T 細胞免疫球蛋白1 和IL-18 結合蛋白的基因變異與HAV 感染的嚴重程度有關[8]。此外,HAV 急性感染患者可能發展為自身免疫性肝炎,進而發展為肝硬化和肝細胞癌[18-19]。這些機制并不是相互排斥的,而是能單獨或共同作用,導致患者肝臟損傷,增加肝細胞癌發生的潛在風險。
綜上所述,HAV 感染導致免疫失調或肝臟損傷對肝細胞癌的發病、進展和預后產生潛在影響,需要進行更大規模的研究以深入了解這一過程。
2 乙型肝炎病毒和丁型肝炎病毒感染導致肝細胞癌發生的免疫機制
2.1 HBV感染
HBV 為嗜肝DNA 病毒科正嗜肝DNA 病毒屬,病毒顆粒直徑約為42 nm,是一種能引發慢性肝炎的常見病原體[20]。HBV 慢性感染是肝細胞癌發生的主要誘因,超過50%的肝細胞癌患者是HBV攜帶者。并且,HBV攜帶人群其終生肝細胞癌發病風險比非感染人群高25~37倍[21]。
HBV 慢性感染引發持續性炎癥反應導致的肝細胞損傷和修復是肝細胞癌發展的基礎。此外,HBV 的基因組可以整合到肝細胞的基因組中,該過程可能會導致基因組的變異和不穩定,進而導致肝細胞的惡性轉化[22]。臨床上,與其他肝炎病毒感染的肝細胞癌患者比較,更多HBV感染的肝細胞癌患者在沒有肝硬化的情況下表現出肝細胞癌的癥狀[23]。與其他非病毒因素肝細胞癌患者比較,HBV 感染的肝細胞癌患者肝硬化比例較低,表明HBV可能通過直接激活細胞中某些信號通路來影響細胞增殖或抑制細胞凋亡,從而影響肝細胞癌進展。
HBV 通過激活NF-κB、Wnt/β-catenin 和p53等細胞信號轉導通路來促進細胞增殖或抑制凋亡[22]。來源于病毒X 基因的HBx 在HBV 感染的發病機制和病毒轉錄過程中扮演著關鍵角色,其與肝細胞癌的發生具有一定相關性[24],見圖1。NF-κB 在炎癥和免疫反應中發揮著關鍵作用,其過度活化會導致炎癥性細胞損傷和細胞生存信號的失衡[25-26]。有研究顯示,HBx 可能通過激活NF-κB 信號通路促進肝細胞惡性增殖,最終導致肝細胞癌[27]。Wnt/β信號通路在肝炎病毒感染過程中也扮演著重要角色。該通路在正常情況下調控細胞的增殖和分化,但其異常激活與多種癌癥類型相關。有研究發現,HBx 可以通過激活NF-κB 上調β-catenin 的表達,最終激活Wnt 信號通路[27-28],從而促進肝細胞癌形成。p53 是重要的腫瘤抑制蛋白,其對DNA損傷的監測和修復起著關鍵作用。當DNA 受到損傷時,p53 會激活細胞內的一系列基因,這些基因可以促進細胞凋亡或使細胞停止分裂,并進行DNA 修復[29]。HBx通過與p53 結合干擾其功能,阻止p53 與DNA 的結合,從而抑制其對DNA 損傷的監測和修復功能,同時還促進p53 的降解[30]。研究顯示,HBx 能與甲基化CpG 二核苷酸結合,促進甲基化過程并調節基因表達[31]。HBx 可以促進血管生成,即形成新血管,從而幫助肝癌細胞生長和擴散[32]。HBx還可以抑制NK 細胞活性,并下調MHCⅠ類分子的表達,使肝癌細胞不易被T 淋巴細胞識別和攻擊[33]。此外,HBx 參與調控Ras 蛋白和TP53 等多種癌癥發生相關蛋白[34]。HBx 在HBV 相關肝癌發病中起著核心作用,是肝細胞癌抑制治療極具潛力的靶點。
此外,HBV 感染引發的炎癥因子會刺激APOBEC3B 顯著上調[35]。與APOBEC3A 比較,APOBEC3B 誘發基因變異的能力相對溫和,其誘導的變異水平仍然在細胞耐受范圍內而不會導致細胞凋亡,因此促進APOBEC3B 上調的遺傳多態性會增加肝細胞癌在內的多種癌癥的發生風險[36]。
總的來說,一方面,HBV 感染會導致肝硬化,增加肝細胞癌發生風險;另一方面,HBV 感染可調控NF-κB、Wnt/β 和p53 等多個信號通路,且這些信號調控并不是獨立的,其復雜互動導致了細胞失去正常的生長控制和DNA損傷修復機制,最終推動肝細胞癌發展。
2.2 HDV與HBV共感染
HDV 為小核糖核酸病毒,病毒顆粒呈球形,直徑約36 nm;其基因組為環狀單股負鏈RNA,全長1679 bp,編碼核心蛋白和包膜蛋白;其復制需要借助HBV 的包膜蛋白才能完成裝配[37]。HBV對HDV 的組裝、釋放、保護和吸附等多方面均有輔助作用[38]。HDV 主要通過輸血、注射及性接觸進行傳播。據估計,全球乙型肝炎表面抗原攜帶合并HDV 感染者有2000 萬例[39]。在臨床上,如果檢測到HDV 感染,一定伴有HBV 感染。因臨床上HBV 感染較為多見,常掩蓋或漏診HDV 感染,故臨床HDV感染診斷率不高。當病情較重或突然加重,應警惕HDV 與HBV 的共感染[40]。研究顯示,HDV 和HBV 共感染會促進肝硬化形成[41]。同時,肝硬化是否發展為肝細胞癌與患者體內HDV血癥水平相關[41]。
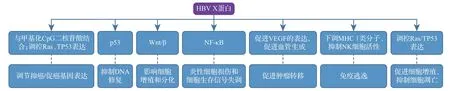
圖1 HBV X蛋白誘導肝細胞癌發生的機制及靶點示意圖Figure 1 The mechanism and target of hepatocellular carcinoma induced by HBV X protein
目前,HDV 在肝細胞癌發生中的作用仍存在爭議,更多人認為HDV 與HBV 共感染加重了HBV 相關臨床癥狀或促進了肝硬化進程,從而間接導致了肝細胞癌發生。HDV 是否可以獨立誘導肝細胞癌的產生,及其在肝癌發生中的潛在作用仍需進一步研究。
3 丙型肝炎病毒感染導致肝細胞癌發生的免疫機制
HCV是單股正鏈RNA病毒,基因組長度約為9.5 kb,屬于黃病毒科,由Houghton團隊于1989年發現[42]。HCV基因組編碼三種結構蛋白(core、E1和E2)和六種結構蛋白(NS2、NS3、NS4A、NS4B、NS5A和NS5B)[43]。HCV 是RNA 病毒,較易變異,不同地區的分離株只有68.1%~91.8%的核苷酸相同[44]。HCV 主要通過母嬰、血液和性接觸等進行傳播。全球HCV 慢性感染者有1.3 億~1.7 億[45]。HCV 感染者中有60%~80%會發展為慢性感染,后者中15%~30%在20年內出現肝硬化,一部分患者可能進一步發展為肝細胞癌[46]。與非HCV 感染人群比較,HCV 感染者中肝細胞癌的發病率增加15~20倍[47]。HCV感染與酒精、吸煙以及伴隨糖尿病的肥胖癥共同作用,通過促進肝纖維化及肝硬化進程增加肝細胞癌的風險[48-51]。HBV 或HIV與HCV共同感染增加了HCV慢性感染患者發生肝細胞癌的風險[13,52]。
HCV 感染或病毒編碼的毒力蛋白導致免疫細胞對肝細胞的持續性損傷、改變肝細胞凋亡信號以及TGF-β 誘導的肝纖維化等潛在因素在HCV 慢性感染進展為肝細胞癌的過程中發揮了重要作用(圖2)。通常情況下,由于天然免疫及細胞免疫(炎癥反應)作為一種機體自我保護機制,可以抵抗病毒感染,其對宿主是有益的。然而,HCV 對人體免疫系統來說非常狡猾。一方面,先天免疫中由于HCV NS3蛋白質通過切割負責誘導Ⅰ型干擾素的MAVS 來抑制天然免疫的激活[53]。這是HCV 難以被先天免疫清除從而產生慢性感染的重要原因之一。另一方面,在HCV感染過程中,特異性T 細胞會攻擊HCV 陽性細胞,且招募的肝巨噬細胞分泌的TGF-β 會促進肝纖維化發生[54]。這意味著HCV 慢性感染導致的肝細胞損傷在很大程度上是由于針對病原體及其特異性抗原的免疫反應引起的[55-56]。此外,HCV E2 蛋白通過抑制NK 細胞促進免疫逃避和慢性感染的建立[57]。
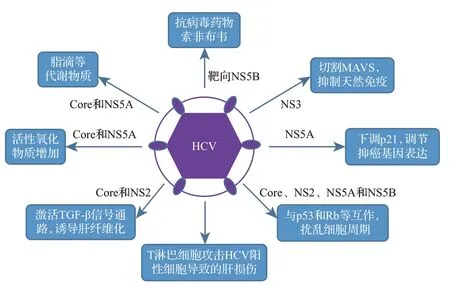
圖2 HCV誘導肝細胞癌發生的機制及靶點示意圖Figure 2 Mechanism and targets of HCV induced hepatocellular carcinoma occurrence
HCV 可以通過調控多種與細胞增殖和凋亡密切相關的細胞信號轉導通路導致肝細胞癌發生。其中,NS5A 蛋白作為轉錄因子激活劑,與包括細胞周期/凋亡、脂質代謝在內的各種信號通路相互作用[58-59]。NS5A 通過阻止Smad 蛋白核轉位抑制TGF-β 信號傳導,導致肝癌細胞系中腫瘤抑制因子p21 表達下調[60-61]。Rb 和p53 蛋白對細胞周期的調控具有重要作用,是重要的抑癌蛋白。HCV Core、NS2、NS5A 和NS5B 與腫瘤抑制蛋白p53 和Rb 相互作用,導致其功能紊亂[62-65]。這些相互作用可以促進HCV 感染的肝細胞增殖和腫瘤形成,從而增加肝硬化和肝癌風險。HCV 感染除了通過調節細胞增殖和凋亡外,還通過調節細胞代謝、活性氧產生和影響DNA修復等途徑誘導肝細胞癌發生[66-68]。
4 結 語
肝炎病毒是誘導肝細胞癌發生的主要致病因素。肝炎病毒感染導致肝細胞癌的發生在機制方面存在一些共性,如病毒性肝炎慢性感染導致肝臟的纖維化和肝硬化,誘發肝細胞癌的產生。同時,不同肝炎病毒在誘發肝細胞癌方面也有各自的特點,如HBV 和HCV 分子通過各自的病毒蛋白,通過影響細胞的凋亡和增殖,從而誘發肝細胞癌。多種肝炎病毒感染導致肝細胞癌發生的過程中存在著許多共性。一方面,肝病患者常伴隨持續性的肝臟炎癥、肝纖維化以及肝細胞異常再生,這些異常的生理過程不僅導致了肝硬化的形成,還在TP53等基因和表觀遺傳學層面上引發了一系列的改變。這些變化最終導致異常增生結節(腫瘤癌前病變)的形成,進而發展為肝細胞癌[4]。以HBV 為例,在病毒長期慢性感染導致肝細胞癌的過程中,伴隨著肝炎病毒突變積累,病毒自身的突變使得病毒能夠更好地在人體內生存和繁殖;肝細胞也會發生一系列基因組變化,包括基因擴增、缺失、重排等。這些變化使得肝細胞失去了正常的生長控制和分化能力,進而形成肝癌[69]。癌癥進化發育學通過建立完整的理論體系解釋了肝炎病毒慢性感染過程中病毒突變和肝癌發生的進程,認為肝癌的發生是一個多階段、多步驟的過程。在病毒感染初期,免疫系統會識別并攻擊病毒,但病毒會通過突變不斷逃逸。隨著時間的推移,不僅病毒基因組的突變會累積,肝細胞癌發生密切相關基因變異同樣會積累,如TP53、CTNNB1、AXIN1等。這些基因變異影響了細胞生長、分化和凋亡的調控,促進了肝細胞癌的發展[70]。另一方面,病毒通過其自身的蛋白(如HBV 的HBx 以及HCV 的Core 和NS2 等)調節與細胞增殖和凋亡密切相關的細胞信號轉導通路,使異常增生細胞獲得增殖、侵襲性和生存優勢,并最終完成到成熟肝細胞癌的轉變[22,29,62-65]。這些病毒蛋白對細胞信號轉導通路的改變促進肝細胞的惡性轉化,從而加速了肝細胞癌的發展。
同時,不同的肝炎病毒感染導致肝細胞癌發生的過程也存在一些差異。如在HBV 感染患者中,肝細胞癌也可以發生于不存在肝硬化或明顯炎癥的慢性肝病患者中,這表明HBV感染有直接致癌作用[23]。然而,在HCV 感染者中,如果不伴有重度肝纖維化,則肝細胞癌很少發生[46]。此外,相較于其他肝炎病毒,HCV還可導致脂肪性肝炎,從而加速肝纖維化和肝硬化的進程[58-59]。HEV在器官移植和獲得性免疫缺陷綜合征等免疫缺陷人群中的慢性感染是其特殊的臨床問題[71-72]。盡管鮮有HEV 感染導致細胞增殖和凋亡相關的細胞信號通路激活從而誘導肝細胞癌發生的報道,已有流行病學和臨床研究提示HEV 慢性感染可能是導致肝細胞癌發生的因素之一[73]。
這些共性和差異反映了各種肝炎病毒感染導致肝細胞癌發生的特征和風險因素,對理解和管理這些疾病具有重要意義。
志謝研究得到浙江省自然科學基金(LQ22H190003,LQ22C070001)、國家自然科學基金(31830052)、國家重點研發計劃(2021YFA1301401)支持. 浙江大學生命科學研究院尚衛娜老師在本文修改中提供幫助
AcknowledgementsThis work was supported by the Natural Science Foundation of Zhejiang Province (LQ22H190003,LQ22C070001), National Natural Science Foundation of China (31830052) and National Key R&D Program of China(2021YFA1301401). SHANG Weina from the Life Sciences Institute, Zhejiang University, provided assistance in the revision of this article
利益沖突所有作者均聲明不存在利益沖突
Conflict of InterestsThe authors declare that there is no conflict of interests
?The author(s) 2024. This is an open access article under the CC BY-NC-ND 4.0 License (https://creativecommons.org/licenses/by-nc-nd/4.0/)

