腫瘤免疫微環(huán)境中cGAS-STING信號通路的細胞間信號傳遞
王夢秋,徐平龍,2,3,4,吳芑柔
1. 浙江大學生命科學研究院,浙江 杭州 310058
2. 浙江大學生命系統(tǒng)穩(wěn)態(tài)與保護教育部重點實驗室 浙江省癌癥分子細胞生物學重點實驗室,浙江 杭州 310058
3. 浙江大學杭州國際科創(chuàng)中心智能醫(yī)藥研究所,浙江 杭州 311200
4. 浙江大學癌癥研究院,浙江 杭州 310058
腫瘤免疫微環(huán)境包括腫瘤細胞、內(nèi)皮細胞、多種類型的免疫細胞和復雜的細胞外基質(zhì)等,是腫瘤與免疫相互作用的關(guān)鍵因素。與正常細胞比較,腫瘤細胞通常存在異常的細胞質(zhì)DNA,其來源主要包括基因組不穩(wěn)定性形成的包裹染色質(zhì)片段的微核釋放[1]、DNA 損傷修復和細胞周期失調(diào)引起的胞質(zhì)內(nèi)異常dsDNA 的積累[2]。此外,氧化應激和線粒體功能障礙也可能導致線粒體DNA 泄露到細胞質(zhì)中[3]。DNA 作為一種免疫刺激因子,具有PAMP和DAMP 的雙重特性,被模式識別受體識別,參與調(diào)控微生物感染、自身免疫、炎癥、器官退化等多種病理過程[4]。
cGAS-STING 通路是識別胞質(zhì)DNA 的重要途徑。cGAS 可以識別細胞質(zhì)中游離的dsDNA,其同源二聚體以高親和力結(jié)合不同來源的dsDNA,形成四聚體復合物,并通過液-液相分離促進聚集[5]。cGAS對dsDNA的識別是序列非依賴的,在靜息狀態(tài)下cGAS 為自抑制狀態(tài),其在結(jié)合dsDNA 后發(fā)生構(gòu)象變化,激活并催化第二信使cGAMP 的合成[6]。cGAMP 結(jié)合內(nèi)質(zhì)網(wǎng)跨膜蛋白STING 的細胞質(zhì)配體結(jié)合域,使STING 發(fā)生構(gòu)象變化后活化,在COP-Ⅱ和ARF GTP酶等調(diào)節(jié)蛋白的協(xié)助下,從內(nèi)質(zhì)網(wǎng)轉(zhuǎn)移到內(nèi)質(zhì)網(wǎng)-高爾基體中間體以及高爾基體[7]。STING 在轉(zhuǎn)位過程中招募TBK1/IKKε 激酶,后者經(jīng)磷酸化活化后招募IRF3 形成經(jīng)典的STING 信號體。隨后,磷酸化并二聚化的IRF3 進入細胞核,促進Ⅰ型干擾素和大量ISG 產(chǎn)生,并協(xié)同活化的NF-κB 誘導促炎性細胞因子產(chǎn)生。除了介導天然免疫應答之外,cGAS-STING 信號的非經(jīng)典功能也受到了廣泛的關(guān)注,在細胞衰老、自噬、信使RNA翻譯和能量代謝等多種生理過程中具有重要的調(diào)控功能[4]。
cGAS-STING 通路在腫瘤免疫調(diào)控中扮演著重要的角色,是連接天然免疫和適應性免疫的關(guān)鍵橋梁,已成為腫瘤免疫治療中備受關(guān)注的靶點[8]。cGAS-STING 通路的下游信號誘導細胞凋亡和細胞周期停滯,從而阻礙了早期腫瘤發(fā)展[9-11],介導抗原提呈細胞激活以及促炎性細胞因子產(chǎn)生,促進腫瘤免疫循環(huán)并重塑腫瘤免疫微環(huán)境[12-13],并促使樹突狀細胞、T 淋巴細胞、NK 細胞等免疫細胞招募和激活,增強了免疫監(jiān)視以及免疫系統(tǒng)對腫瘤細胞的攻擊能力[14]。cGAS-STING通路的細胞間信號傳遞有多種方式,包括基于膜系統(tǒng)細胞外囊泡運輸、膜融合和吞噬作用等,基于膜蛋白介導的轉(zhuǎn)運和縫隙連接等[12],深入研究腫瘤免疫中cGAS-STING 通路的細胞間信號傳遞,有助于更深入地理解細胞之間的相互作用,腫瘤微環(huán)境的動態(tài)變化以及免疫細胞的協(xié)同作用,同時為癌癥治療和免疫療法的發(fā)展提供潛在的靶點和策略。本文將深入探討cGAS-STING 通路在鄰近細胞之間的細胞間信號傳遞,涵蓋不同的介質(zhì)和傳遞方式,從信號傳遞的角度探討其在腫瘤免疫治療中的生物學意義。
1 cGAS-STING信號通路對腫瘤微環(huán)境的調(diào)控
在腫瘤中,cGAS-STING通路的作用具有兩面性。一方面,STING 的激活上調(diào)了腫瘤細胞中的多種炎癥基因,誘導細胞凋亡和細胞周期停滯,從而阻礙了早期的腫瘤發(fā)展[9-11]。同時,腫瘤來源的dsDNA、cGAMP 以及活化的STING 蛋白可以通過細胞間轉(zhuǎn)移激活樹突狀細胞、NK 細胞等中的STING 信號級聯(lián),促進腫瘤免疫循環(huán)并重塑腫瘤免疫微環(huán)境[12-13]。此外,STING介導的自噬具有非免疫性抗腫瘤的功能[15]。另一方面,cGAS-STING通路促進一些腫瘤的發(fā)生發(fā)展,如STING 誘導的調(diào)節(jié)性B 細胞限制腫瘤免疫中NK 細胞功能[16],STING上調(diào)PD-L1促進宮頸癌進展[17]等。
腫瘤免疫微環(huán)境中cGAS-STING 通路的細胞間信號傳遞涉及多種復雜的介質(zhì)和機制,具有深遠的生物學意義。該信號的細胞間傳遞促進了信息共享,來自受損或癌變細胞的關(guān)鍵信息可以傳遞給免疫細胞,這有助于維持免疫監(jiān)視的高度敏感性。同時,這一過程介導了腫瘤微環(huán)境的動態(tài)變化,cGAS-STING通路通過產(chǎn)生干擾素和促炎性細胞因子,形成炎癥微環(huán)境,使腫瘤細胞更容易被免疫系統(tǒng)識別和攻擊[18]。此外,cGAS-STING通路在樹突狀細胞、T 淋巴細胞、NK 細胞等不同類型免疫細胞間的通信加強了免疫系統(tǒng)的協(xié)同作用,有助于有效識別、定位和清除腫瘤細胞[12]。研究表明,宿主細胞可以將PAMP 以及cGAS-STING通路的信號因子轉(zhuǎn)移到旁觀者細胞中,并促進旁觀者細胞中該信號的激活[19]。
隨著cGAS-STING 通路調(diào)控腫瘤免疫機制的深入研究,STING 激動劑的研發(fā)受到了極大的關(guān)注。STING 激動劑能有效促進腫瘤消退,在臨床前試驗中獲得了不錯的結(jié)果。但是,由于STING激動劑的臨床應用存在穩(wěn)定性差、跨膜性差以及腫瘤精確性不足等問題[20],其臨床試驗結(jié)果不容樂觀[21-22](附表1)。
利用細胞外囊泡或病毒包被等可對STING 激動劑進行包裝,這在腫瘤治療中具有巨大的潛力。細胞外囊泡是天然的載體,具有較高的生物相容性,不易引起免疫反應或毒副作用,因此在藥物遞送中安全性更高[23]。在穩(wěn)定性上,細胞外囊泡以及病毒的膜結(jié)構(gòu)在很大程度上保護了其負載物質(zhì),使藥物能夠在血液中較長時間內(nèi)保持穩(wěn)定,提供了更長的治療窗口。在跨膜性能上,細胞外囊泡能夠穿越細胞膜、組織屏障和血腦屏障等生物屏障,將藥物傳遞到腫瘤組織等目標部位[24]。在精確性上,細胞外囊泡作為藥物遞送領(lǐng)域的一種前沿技術(shù),可以通過特定的表面分子與目標細胞選擇性相互作用實現(xiàn)藥物的精確遞送[25]。cGAS-STING 通路的細胞間信號傳遞為STING 激動劑等藥物的遞送提供了潛在的機制,可用于精確遞送藥物以及擴大藥物影響范圍等,能克服STING 激動劑在臨床應用中的不足。
2 cGAS-STING基于膜系統(tǒng)的細胞間通信
在腫瘤免疫微環(huán)境中,膜介導的細胞間通信是cGAS-STING 通路信號在不同類型細胞間傳遞的重要機制之一,包括細胞外囊泡運輸、吞噬作用和細胞膜融合等(圖1)。這些基于膜系統(tǒng)的細胞間通信能傳遞dsDNA、cGAMP 和活化的STING蛋白等重要的免疫分子,從而加強免疫監(jiān)視和炎癥應答。
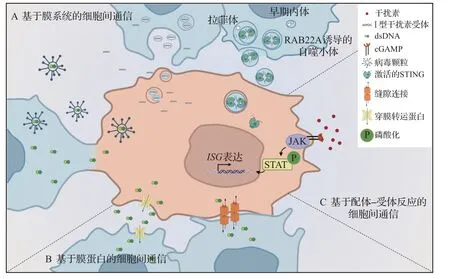
圖1 cGAS-STING通路的細胞間信號傳遞Figure 1 The cell-to-cell communications of cGAS-STING pathway
2.1 細胞外囊泡運輸
細胞外囊泡是從細胞膜突起產(chǎn)生的脂質(zhì)雙層結(jié)構(gòu)的囊泡小體,可以被細胞釋放和捕獲,廣泛存在于各種體液中,通過自分泌和旁分泌方式參與抗原提呈、細胞遷移和細胞分化等[26]。細胞外囊泡中包裹的功能分子包括蛋白質(zhì)、脂質(zhì)、遺傳物質(zhì)、氨基酸和代謝產(chǎn)物等。在腫瘤免疫中,細胞外囊泡對受體細胞的影響主要由其內(nèi)容物決定,cGAS-STING 通路的dsDNA 和活化的STING 蛋白能通過細胞外囊泡轉(zhuǎn)運至旁觀者細胞。
在感染、炎癥和惡性腫瘤等情況下,dsDNA存在于直徑小于200 nm 的小型細胞外囊泡中,包含有外源dsDNA 的細胞外囊泡是PAMP 在細胞間傳遞的重要方式[27]。在克羅恩病中,攜帶dsDNA 的細胞外囊泡從炎癥部位釋放,隨后激活cGAS-STING 通路,增強巨噬細胞的先天免疫反應,從而加重疾病[28]。在腫瘤中,細胞向外分泌包含有dsDNA 的細胞外囊泡,調(diào)節(jié)腫瘤免疫微環(huán)境,細胞外囊泡到達受體細胞后引起多種響應,如線粒體DNA 結(jié)合蛋白Lon 的上調(diào)能夠誘導攜帶線粒體DNA 和PD-L1 的細胞外囊泡的分泌,進一步誘導干擾素和IL-6的產(chǎn)生并減弱T淋巴細胞的免疫能力[29],從而調(diào)控腫瘤的進展和轉(zhuǎn)移。
細胞外囊泡也能夠攜帶cGAMP,但其是否具有功能還有待進一步研究。與細胞外囊泡類似,病毒感染的細胞中包含cGAMP 的病毒顆粒將胞質(zhì)DNA 識別信號傳遞到下一個被感染的細胞中[30]。研究顯示,cGAMP是能包被進病毒顆粒內(nèi)的一種小分子,且包裹進病毒顆粒內(nèi)cGAMP 的量足以激活細胞質(zhì)中的STING,從而引發(fā)抗病毒免疫應答[31]。基于cGAMP 結(jié)構(gòu)的STING 激動劑是腫瘤免疫中極具發(fā)展前景的藥物靶點,以病毒顆粒或細胞外囊泡的方式遞送STING 激動劑為腫瘤免疫治療提供了實驗基礎和研發(fā)方向。
值得注意的是,活化的STING 蛋白被封裝到由RAB22A 介導的細胞外囊泡中,通過非經(jīng)典自噬機制在細胞間傳遞[32]。STING是一種位于內(nèi)質(zhì)網(wǎng)的跨膜蛋白,當與cGAMP 結(jié)合時,其與cGAMP的連接區(qū)域結(jié)構(gòu)會重組,進而導致STING的活化,進一步被定向運輸?shù)礁郀柣w,并通過自噬和溶酶體降解[4]。RAB22A 與PI4K2A 結(jié)合產(chǎn)生PI4P,PI4P招募形成Atg12-Atg5-Atg16L1復合體,從而誘導內(nèi)質(zhì)網(wǎng)中RAB22A 介導的非經(jīng)典自噬體形成,該自噬體包裹了激活的STING 蛋白。隨后,活化的STING蛋白被包裝進拉菲體(rafeesomes),這是由內(nèi)質(zhì)網(wǎng)來源RAB22A 介導的非經(jīng)典自噬小體與RAB22A 陽性的早期內(nèi)體融合形成的細胞器。在此過程中,RAB22A 使RAB7 失活,從而抑制了拉菲體與溶酶體的融合,并使這些內(nèi)含活化STING 的小囊泡以細胞外囊泡的形式分泌出來。內(nèi)吞體轉(zhuǎn)運復合體ESCRT 的元件STAM 同樣參與結(jié)合活化的STING 寡聚體,并將其轉(zhuǎn)運至細胞外囊泡中[33]。旁觀者細胞接受含有STING 的細胞外囊泡,促使其釋放β 干擾素到腫瘤微環(huán)境中,從而促進抗腫瘤免疫[32]。在受體細胞中,STAM 還通過協(xié)助STING 降解負向調(diào)控STING 信號,以達到精準調(diào)控的目的[33]。盡管在STING 蛋白中尚未發(fā)現(xiàn)分泌信號肽,但在Ⅰ型單純皰疹病毒感染產(chǎn)生的細胞外囊泡中檢測到了宿主來源的STING 蛋白[34],從側(cè)面證明STING 通過細胞外囊泡進行細胞間傳遞,為理解功能膜蛋白的細胞間遷移提供了新的視角。通過拉菲體將活化STING 分泌到細胞外能夠重塑腫瘤微環(huán)境,增強抗腫瘤免疫的療效,可能成為以STING 為靶點的免疫治療策略。
2.2 吞噬作用和細胞膜融合
巨噬細胞、樹突狀細胞和中性粒細胞等免疫細胞通過吞噬作用攝取DAMP,包括凋亡細胞、損傷相關(guān)碎片和代謝產(chǎn)物等。腫瘤細胞與免疫細胞之間的dsDNA 轉(zhuǎn)移通常通過吞噬作用發(fā)生在腫瘤微環(huán)境中。免疫細胞感知腫瘤細胞來源的dsDNA,觸發(fā)cGAS-STING 信號的激活,促進抗原提呈以及獲得性免疫反應[35]。此外,在HIV-1 感染中,病毒融合蛋白HIV-1 Env在供體T淋巴細胞中表達介導了其與內(nèi)源性表達HIV受體CD4的未感染巨噬細胞發(fā)生膜融合反應,cGAMP通過融合位點的細胞間轉(zhuǎn)移增強了巨噬細胞干擾素反應[36],這表明細胞與細胞間接觸依賴的膜融合事件是抵御病毒感染的一部分。吞噬作用和膜融合發(fā)生均能介導cGAS-STING 信號通路在不同類型細胞間傳遞,這對于免疫系統(tǒng)的協(xié)同至關(guān)重要。
3 cGAS-STING基于膜蛋白的細胞間通信
基于膜蛋白的細胞間通信是細胞間實現(xiàn)物質(zhì)和信號傳遞的另一種重要機制。這些膜蛋白允許離子、小分子、蛋白質(zhì)等通過細胞膜或亞細胞膜結(jié)構(gòu)進行傳遞,從而影響細胞的功能。cGAMP能通過縫隙連接、膜轉(zhuǎn)運蛋白等方式在鄰近細胞間傳遞,而dsDNA 能通過膜轉(zhuǎn)運蛋白在鄰近細胞間傳遞,這對免疫調(diào)節(jié)和炎癥反應至關(guān)重要(圖1、2)。
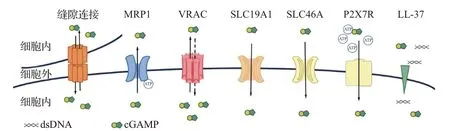
圖2 cGAS-STING基于膜蛋白的細胞間通信Figure 2 The cell-to-cell communications of cGAS-STING pathway based onmembrane protein
3.1 縫隙連接
縫隙連接是一種細胞間通道,允許相鄰細胞進行離子和小分子的直接交換。cGAMP 不能直接穿過細胞膜,其在細胞間的傳遞需要轉(zhuǎn)運蛋白協(xié)助,cGAMP可以通過縫隙連接在兩個相鄰細胞間自由傳遞。最先在病毒感染的細胞中發(fā)現(xiàn)cGAMP通過縫隙連接在細胞間傳遞[37],連接蛋白connexin 43 和45 介導了病毒感染的內(nèi)皮細胞和巨噬細胞之間的cGAMP 傳遞,這種跨細胞類型激活的cGAS-STING 通路加強了抗病毒免疫應答[38]。體內(nèi)實驗證實,將cGAMP 包被在脂質(zhì)體中,并涂布在肺表面活性物質(zhì)上,其可以被肺泡巨噬細胞吸收,并通過縫隙連接轉(zhuǎn)移到肺泡上皮細胞[39]。此外,在腦轉(zhuǎn)移腫瘤中,腫瘤細胞通過protocadherin 7 和connexin 43 介導的縫隙連接將cGAMP傳遞給星形膠質(zhì)細胞,加強干擾素和腫瘤壞死因子等細胞因子的分泌,從而促進腫瘤轉(zhuǎn)移[40]。因此,破壞這種旁分泌環(huán)路的縫隙連接調(diào)節(jié)因子可能成為治療該類腦轉(zhuǎn)移腫瘤的靶點。
3.2 穿膜轉(zhuǎn)運蛋白
與縫隙連接不同,基于膜轉(zhuǎn)運蛋白的信號傳遞涉及出現(xiàn)在細胞外基質(zhì)中的信號分子,參與調(diào)控腫瘤免疫微環(huán)境中的細胞外基質(zhì),并能將信號分子傳遞到更遠處的受體細胞中。腫瘤細胞死亡會釋放大量dsDNA 到細胞外基質(zhì)中,通常這些dsDNA 會被DNA 酶快速降解,因此失去免疫原性。內(nèi)源性抗菌肽LL-37是中性粒細胞的重要效應分子,具有廣譜殺菌及抗腫瘤活性,能與細胞外基質(zhì)中的dsDNA形成復合體,介導dsDNA轉(zhuǎn)運到單核細胞中,以Toll 樣受體非依賴的方式介導Ⅰ型干擾素的產(chǎn)生,調(diào)節(jié)腫瘤免疫微環(huán)境,從而調(diào)控NK細胞等免疫細胞的功能[41]。
細胞外基質(zhì)中的cGAMP受到其唯一水解酶ENPP1 的調(diào)控[42-43],并且能在多種膜轉(zhuǎn)運蛋白的協(xié)助下穿過細胞膜進入受體細胞的胞質(zhì)中,激活并傳遞cGAS-STING 信號通路。轉(zhuǎn)運cGAMP的膜轉(zhuǎn)運蛋白可以分為向細胞外輸出和向細胞內(nèi)攝取兩種類型。 MRP1,也稱為ABCC1,其結(jié)構(gòu)包含17 個跨膜結(jié)構(gòu)域形成的孔洞,是依賴ATP的直接輸出cGAMP的轉(zhuǎn)運蛋白[44]。MRP1 通過向外輸出cGAMP 阻止細胞質(zhì)中的cGAMP 與STING 的結(jié)合,從而負向調(diào)控cGAS-STING 通路介導的干擾素的產(chǎn)生[45]。VRAC是響應細胞外滲透壓變化的離子通道,能根據(jù)cGAMP 化學濃度梯度介導cGAMP 的輸出和輸入,其組成蛋白LRRC8A 的遺傳學敲除可以抑制VRAC 通道活性并抑制各種原代和培養(yǎng)細胞中50%~70% 的cGAMP 攝取[19,46]。SLC 家族中的SLC19A1 是介導包括cGAMP 在內(nèi)的多種相似環(huán)狀二核苷酸攝取的蛋白,結(jié)構(gòu)分析顯示cGAMP 的攝取需要反向的陰離子濃度梯度提供驅(qū)動力[47-48]。SLC19A1 在THP-1和U937人單核細胞系中發(fā)揮作用,其同家族的SLC46A 作為陽離子交換劑在CD14+單核細胞中被鑒定為調(diào)控cGAMP 攝取的主要蛋白[49]。ATP 門控蛋白P2X7R 是傳遞cGAMP 的另一種蛋白質(zhì),作為非選擇性陽離子通道在免疫細胞中高表達,開放其通道需要細胞外高濃度的ATP。在細胞損傷或死亡時,細胞外存在高濃度ATP,允許cGAMP 等納米級分子通過[50]。LL-37 除了能介導dsDNA 的細胞間傳遞,也可介導cGAMP 的傳遞從而增強cGAS-STING 通路的激活[51],但其機制還有待進一步研究。綜上,基于膜轉(zhuǎn)運蛋白的cGAMP 細胞間傳遞需要結(jié)合細胞外基質(zhì)以及離子濃度發(fā)揮作用,并受到ENPP1的調(diào)控。
4 cGAS-STING 基于配體-受體反應的細胞間通信
在腫瘤免疫微環(huán)境的調(diào)控中,cGAS-STING通路下游的效應因子如干擾素發(fā)揮著關(guān)鍵而復雜的作用(圖1)。干擾素是一類高活性、多功能的分泌型糖蛋白,具有廣泛的生物學活性,通過配體-受體反應調(diào)節(jié)適應性免疫、病原體感染、抗腫瘤免疫應答和炎癥反應等。Ⅰ型和Ⅲ型干擾素是Toll 樣受體、RIG-Ⅰ樣受體和cGAS 下游的重要分泌蛋白,其在細胞間的傳遞主要通過與受體蛋白(如α 干擾素受體1 和α 干擾素受體2)結(jié)合,并以旁分泌的方式激活JAK-STAT 信號通路[52]。這個基于配體-受體的干擾素信號傳遞過程促使多個ISG 的產(chǎn)生,從而調(diào)節(jié)和影響免疫應答。干擾素在腫瘤免疫中的作用是多方面的。首先,干擾素能夠激活樹突狀細胞,后者在免疫系統(tǒng)中充當信息傳遞的樞紐。激活的樹突狀細胞能夠捕獲和提呈腫瘤相關(guān)抗原,隨后激活適應性免疫細胞,干擾素通過增加CD8+T 細胞數(shù)和活性來加強免疫系統(tǒng)對于腫瘤的攻擊力[53]。值得注意的是,干擾素也可以通過PD-L1 調(diào)控免疫監(jiān)視。PD-L1與T 淋巴細胞表面上的PD-1 受體相互作用,抑制T 淋巴細胞的活性[54],從而允許腫瘤細胞逃脫免疫攻擊。而干擾素通過減少PD-L1 的表達,恢復T 淋巴細胞的殺傷功能,進一步增強抗腫瘤免疫反應[55]。干擾素在腫瘤免疫中發(fā)揮著復雜而關(guān)鍵的作用,其激活了免疫細胞,提高了抗腫瘤免疫反應,同時也有助于克服腫瘤細胞的免疫逃逸策略。因此,研究cGAS-STING 通路下游的效應因子如干擾素的細胞間傳遞對于更好地理解和利用免疫系統(tǒng)來對抗腫瘤具有重要意義。
5 結(jié) 語
cGAS-STING 通路在增強先天免疫和激活適應性免疫方面具有重要功能,其信號的激活通常有助于提高抗腫瘤免疫,且STING 激動劑是極具潛力的腫瘤免疫治療藥物[56]。值得注意的是,cGAS-STING 通路不僅在細胞內(nèi)發(fā)揮作用,還可以通過基于膜系統(tǒng)的細胞外囊泡運輸、吞噬作用和細胞膜融合,基于蛋白質(zhì)通道的縫隙連接、膜轉(zhuǎn)運蛋白,以及配體-受體反應等多種途徑,作為一種可傳遞的信號傳播到旁觀者細胞中(圖1)。cGAS-STING 通路在細胞間的傳遞擴大了感知PAMP和DAMP的影響范圍,增強了天然免疫。
然而,cGAS-STING 通路信號在細胞間傳遞的精確機制及其在多種疾病特別是腫瘤中的免疫治療方案仍須進一步研究。調(diào)節(jié)cGAS-STING信號的細胞間傳遞是一種有前景的可治療腫瘤的新策略。細胞外基質(zhì)中的cGAMP 被認為是腫瘤的免疫刺激因子,注射cGAMP 在多種腫瘤臨床前研究中顯示有效,這表明高水平的細胞外cGAMP 可以促進免疫反應。而細胞外基質(zhì)中的cGAMP 生理濃度受到cGAMP 水解酶ENPP1的控制,這使得ENPP1 成為干預cGAS-STING 信號傳遞的潛在靶點[57]。不透膜的ENPP1 抑制劑可以顯著增加血漿中的cGAMP 濃度增強免疫反應,從而減輕腫瘤的負擔,目前已有相關(guān)藥物進行臨床試驗[58]。此外,在抗腫瘤藥物治療的過程中,dsDNA 的細胞間傳遞有助于腫瘤的治療,腫瘤細胞釋放的細胞外囊泡中包含有dsDNA,能夠激活樹突狀細胞,并且細胞外囊泡通過傳遞活化的STING 誘導β 干擾素的產(chǎn)生,促進抗腫瘤免疫[28,32]。進一步開發(fā)和研究cGAMP 轉(zhuǎn)運蛋白如LRRC8A的激活劑和抑制劑也將為調(diào)控腫瘤免疫提供新的靶標。反之,抑制縫隙連接阻礙cGAMP從腫瘤細胞傳遞到星形膠質(zhì)細胞,這也是限制腫瘤腦轉(zhuǎn)移的策略之一[40]。值得注意的是,由于cGAS-STING信號能夠引起細胞因子風暴[59],期望相關(guān)藥物增強效應的同時,還要避免cGAS-STING通路長期激活導致的慢性炎癥。
研究表明,cGAS-STING 通路不僅在誘導干擾素響應中發(fā)揮作用,還介導非經(jīng)典信號調(diào)控蛋白質(zhì)翻譯[60]、細胞代謝[61]、細胞衰老[2]和細胞死亡[62]等多種生理過程。最近有研究報道STING蛋白的新功能——作為氫離子通道介導高爾基體內(nèi)氫離子的外流導致細胞內(nèi)酸堿度值上升,從而參與非經(jīng)典自噬和NLRP3炎癥小體的激活[63],這加深了我們對DNA 識別信號調(diào)控和傳遞的理解。DNA 識別信號在不同的生理過程和治療策略中激活不同的下游通路,其信號傳遞的復雜性及其對腫瘤免疫的調(diào)控作用需要進一步的研究。cGAS-STING 通路中STING 的激動劑是一種極具治療潛力的腫瘤免疫療法,而cGAMP 以及基于環(huán)狀二核苷酸結(jié)構(gòu)研發(fā)的STING 激動劑在腫瘤中的應用具有局限性。利用cGAS-STING 通路在細胞間傳遞的不同方式可以將STING 激動劑或者活化的STING 以細胞外囊泡或病毒顆粒包被的方式,通過特定的表面分子選擇性地與目標細胞相互作用遞送至特定的細胞中,從而達到精準治療的目的[25]。同時,細胞外囊泡等包被結(jié)構(gòu)有利于生物屏障的穿透,并提高了藥物遞送的穩(wěn)定性和安全性[24]。綜上,DNA 識別信號在細胞間傳遞的機制探索將為腫瘤等各種疾病的治療提供新的策略。
本文附表見電子版。

志謝研究得到國家自然科學基金(31725017,31830052)、國家重點研發(fā)計劃(2021YFA1301401)支持
AcknowledgementsThis work was supported by the National Natural Science Foundation of China (31725017,31830052) and National Key R&D Program of China (2021YFA 1301401)
利益沖突所有作者均聲明不存在利益沖突
Conflict of InterestsThe authors declare that there is no conflict of interests
?The author(s) 2024. This is an open access article under the CC BY-NC-ND 4.0 License (https://creativecommons.org/licenses/by-nc-nd/4.0/)

