產蛋雞子宮部鈣離子轉運及調控的研究進展
郭妍婷,周建民,王 晶,齊廣海
(中國農業科學院飼料研究所 農業農村部動物產品質量安全飼料源性因子風險評估實驗室(北京) 農業農村部飼料生物技術重點開放實驗室,北京 100081)
蛋殼是禽類進化過程中為保護繁衍而形成的一種特殊結構,是蛋內物質與外界環境的交流通道,能夠為胚胎發育提供物理保護,并防止微生物入侵。雞蛋蛋殼由大約95%的碳酸鈣(CaCO3)、3.5%的有機基質和1.5%的水組成[1]。鈣是蛋殼礦化過程中最為關鍵的礦物元素,直接影響蛋殼品質[2],蛋殼中的鈣主要來自飼糧和骨骼。飼料是蛋殼礦化中Ca2+的主要來源,經過消化道吸收進入體液,再由體循環運送到子宮部參與蛋殼礦化。在蛋殼礦化形成時,髓質骨破骨作用加劇,向子宮部提供了部分Ca2+。無機礦化離子[主要為Ca2+和碳酸氫根離子(HCO3-)]和有機基質蛋白相互作用并運輸至子宮部礦化位點是蛋殼礦化的關鍵環節[3]。礦化離子在子宮部的跨膜轉運主要有主動運輸和被動運輸。被動運輸主要是靠膜兩側的離子濃度差,是無需耗能的擴散過程。Ca2+的跨膜轉運系統包括跨細胞途徑(主動運輸)和旁細胞途徑(被動運輸),這一直以來是子宮部鈣吸收和轉運研究的重點。近年來隨著對胞外囊泡研究的深入,其對子宮部Ca2+轉運和蛋殼礦化的作用成為新的研究熱點[4]。此外,轉錄組學和蛋白組學的成熟應用正鑒定出越來越多參與了蛋殼礦化的Ca2+轉運相關基因和蛋白,為理解Ca2+轉運在蛋殼礦化發生和調節中的作用提供了新視角[1,5-6]。因此,以蛋殼礦化期的Ca2+轉運為靶點,通過營養干預的方式改善生產中蛋殼品質下降的問題具備可行性。本文綜述了蛋殼礦化期子宮部Ca2+的來源和轉運途徑,Ca2+轉運對蛋殼礦化和蛋殼品質的影響及其營養調控措施,旨在為生產中雞蛋蛋殼品質的改善提供科學依據。
1 蛋殼的礦化
蛋殼的形成是一個周期性、時序性的動態過程,大約需要24 h。蛋殼的礦化主要發生在蛋雞輸卵管子宮部,是在子宮部分泌的有機基質的精密調控下,由多種離子參與交換和沉積,形成以CaCO3為主要組成的生物礦化物[7]。蛋殼超微結構中乳突層的形成是礦化初始階段,一般發生在排卵后5~10 h,礦化速度相對較慢。排卵后10~22 h,卵到達子宮部中部,在子宮液充足、持續的離子供應下,蛋殼的礦化進入快速沉積期,形成超微結構中最厚的一層——柵欄層。排卵后22~24 h,進入礦化末期,形成垂直晶體層、膠護膜等,礦化停止[8-9]。
2 蛋雞子宮部鈣離子的轉運
蛋殼礦化形成所需的大量Ca2+和HCO3-,并不在子宮部貯存,而是由血液持續供應[10]。因此子宮部Ca2+轉運是指血液中的Ca2+跨過子宮上皮細胞,到達子宮液中蛋殼(或殼膜)礦化位點的過程。目前報道的子宮部Ca2+轉運方式有三種:跨細胞途徑、細胞旁途徑和細胞外囊泡途徑[3-4]。
2.1 鈣離子的跨細胞和細胞旁轉運途徑
跨細胞轉運是蛋雞子宮上皮細胞Ca2+轉運的經典途徑。Ca2+從血液進入到子宮上皮細胞需依賴瞬時受體電位陽離子通道蛋白(TRPV6),在細胞內與鈣結合蛋白d28k(CaBP-d28k)結合,完成貯存或運輸。除CaBP-d28k外,子宮上皮細胞的內質網對Ca2+穩態也具有調控作用[11]。細胞內Ca2+過量時,通過肌漿網/內質網Ca2+-ATP酶(ATP13A5、ATP2A2/3)運輸至內質網儲存;當胞內Ca2+濃度不足時,又通過Ca2+儲存庫——肌醇1,4,5-三磷酸受體(ITPR1/2/3)從內質網釋放補充[12]。Ca2+從子宮上皮細胞排出到子宮液的過程則需質膜Ca2+-ATP酶(plasma membrane calcium ATPase,PMCA)和Ca2+/Na+交換器的參與[13]。因此,子宮上皮細胞Ca2+的跨細胞轉運主要有3步:Ca2+首先通過Ca2+通道或Ca2+轉運體進入子宮上皮細胞一側的頂膜;其次,Ca2+進入細胞質與Ca2+結合蛋白結合轉運到基底側膜;最后,Ca2+由子宮上皮細胞進入子宮液。為維持子宮上皮細胞內的離子平衡,Ca2+在子宮部轉運的同時也伴隨Na+、K+、Mg2+、H+和Cl-的轉運[6](圖1),因此涉及多種離子轉運體的參與(表1),包括Na+通道(SCNN1α/2β/3γ)、Na+/K+交換器(ATP1A1、ATP1B2、NKA1N4)、K+內流通道(KCNJ2/15/16、KCNMA1、KCNH1)、Cl-通道(CLCN2/5)、H+泵(ATP6V1B2、ATP6V1C2、ATP6V1G3、ATP6V0D2)和Mg2+通道(SLC41A2/3、NIPAL1)(表1),且Ca2+轉運相關基因參與蛋殼的形成,表達隨蛋殼鈣化階段而發生變化[6,14]。此外,血液Ca2+也可直接通過上皮細胞之間的緊密連接蛋白進入子宮液[15],此為細胞旁途徑。緊密連接蛋白包括閉合蛋白、閉鎖蛋白、閉合小環蛋白等[16]。

圖1 蛋雞子宮上皮細胞的離子轉運(參考Broinne等[19]和Zhang等[20])Fig.1 The ion transport in uterine epithelial cells of laying hens (Referring to Broinne et al[19] and Zhang et al[20])
子宮部的HCO3-主要來自血液中的HCO3-和CO2[17]。血HCO3-依賴Na+/HCO3-共轉運體——溶質載體家族4成員4、5、7和10(solute carrier family 4, member 4/5/7/10,SLC4A4/5/7/10)進入子宮上皮細胞。CO2則通過擴散進入上皮細胞,在碳酸酐酶4(CA4)的催化下與水形成HCO3-。子宮上皮細胞內HCO3-的轉出則通過HCO3-/Cl-交換器——溶質載體家族4成員8(solute carrier family 4, member 8,SLC4A8)和溶質載體家族26成員9(solute carrier family 26, member 9,SLC26A9)。轉出的HCO3-隨后與子宮液中游離Ca2+結合形成碳酸鈣前體物質,沉積到蛋殼礦化位點[18]。綜上所述,蛋殼礦化是多種離子轉運(Ca2+、HCO3-、Na+、H+、Mg2+、K+和Cl-)調控的協同過程,在此過程中,Ca2+和HCO3-以及有機質前體分泌到子宮液中相互作用形成蛋殼[8]。因此,這些離子轉運基因和載體與蛋殼礦化和蛋殼品質有密切聯系。
2.2 胞外囊泡轉運途徑
胞外囊泡是由脂質雙分子層包繞形成的球狀膜性囊泡。已發現并證實,蛋雞子宮上皮細胞可通過分泌細胞外囊泡(extracellular vesicles,EV)轉運蛋殼礦化所需的碳酸鈣[4]。有研究在蛋雞輸卵管中鑒定到了胞外囊泡標志物的mRNA,并證實EV參與了蛋殼礦化[4]。Waqas等[21]利用透射電鏡觀察到蛋雞的子宮上皮細胞和子宮液中存在與EV發生有關的多泡小體和包含無定形碳酸鈣(ACC)的EV。Riou等[22]研究了蛋雞子宮液中蛋白質的分子功能,發現有29種蛋白質與多泡小體的生物發生有關,并在EV中檢測到熱休克蛋白家族成員8、熱休克蛋白家族成員90α、含纈酪肽蛋白、膜聯蛋白A(annexin-A1/2/4/5,ANXA-1/2/4/5)、帕金森氏病蛋白7和蘋果酸脫氫酶蛋白1等標志蛋白。根據現有證據,推斷EV轉運Ca2+的模式如圖2所示:在蛋殼礦化開始時,子宮上皮細胞分泌EV到子宮液,EV中的ANXA形成Ca2+通道,Ca2+與ANXA上的色氨酸殘基結合被轉運至EV中,與CA4催化形成的HCO3-作用生成ACC,然后EV包裹著ACC運輸至蛋殼礦化位點開始礦化。此過程中卵清蛋白、溶菌酶和其他EV蛋白共同作用阻止了子宮液的非特異性沉淀。有研究表明EGF樣重復序列和盤狀蛋白I樣結構域3(EGF-like repeats and discoidin I-like domains 3,EDIL3)和重組乳脂球-EGF生長因子8(recombinant milk fat globule-EGF factor 8,MFGE8)可將含有ACC的EV靶向引導到礦化位點[23]。目前對蛋雞子宮部EV轉運途徑的研究仍十分有限,EV在蛋殼礦化過程的作用和調控機制值得深入研究。
3 子宮部鈣離子轉運對蛋殼礦化和蛋殼品質的影響
蛋殼礦化初始期碳酸鈣的平均沉積速度約為0.1 g·h-1,快速沉積期為0.33 g·h-1。子宮部Ca2+的轉運涉及了多個基因及蛋白。Jonchère等[6]通過F-2α前列腺素注射使雞蛋在蛋殼礦化前排出,對比了37個離子轉運基因在礦化和非礦化期的表達情況,篩選到11個過表達的離子轉運基因,包括Ca2+轉運基因(CALB1、ATP2B1,2)、Na+轉運基因(SCNN1G、ATP1A1)、K+轉運基因(KCNJ2、KCNJ15和KCNMA1)、HCO3-轉運基因(CA2、SLC26A9)、Cl-轉運基因(CLCN2,5)、H+轉運基因(ATP6V1B2);Zhang等[24]通過轉錄組篩選出13個呈時序性表達的與離子轉運相關的基因,結果表明,CALB1、CA2、SCL26A9、SCNN1G、NKAIN4、CLCN2,5和KCNJ15不僅在礦化期過表達,且都在產蛋后16~20 h表達量達到最高。研究發現,TRPV6與蛋殼強度和鈣含量呈正相關,而且是調控蛋殼礦化的關鍵通道,隨著蛋殼礦化其表達量在快速沉積期達到最大[25];Khan等[26]對比了礦化初始期(排卵后5 h)和線性沉積期(排卵后15 h)的子宮轉錄組結果,發現與囊泡定位和分子合成相關的基因在礦化初始期上調,而與Ca2+轉運及離子和分子合成、分泌活動相關的基因在線性沉積期表達上調,進一步,篩選和鑒定了影響蛋殼礦化和力學特性的離子轉運基因[6,27]。高、低蛋殼強度((44.57±0.91)Nvs. (26.68±0.38)N)蛋雞在蛋殼礦化期子宮部的轉錄組研究顯示,內質網Ca2+轉運基因(ATP13A5)和HCO3-轉運基因(SLC4A1,SLC26A9)的表達水平在高蛋殼強度組中顯著上調[20];Zhang等[28]比較了高、低強度蛋殼蛋雞基因組,也鑒定出10個與Ca2+轉運相關的差異表達基因,其中包括Na+/Ca2+共轉運載體基因(SLC8A1)。另有研究報道,內質網Ca2+轉運基因(ATP2A3、ITPR1)、Na+/HCO3-共轉運基因(SLC4A5)和Na+/K+交換器基因(SLC8A3)顯著影響蛋殼強度、蛋殼厚度和蛋殼重量[26];內質網Ca2+泵(ITPR2)與蛋殼強度和蛋殼厚度有關,并通過其通道開放時間和時長控制Ca2+分泌,從而調節蛋殼厚度[28-29]。可見,蛋雞子宮部Ca2+轉運相關基因的表達與蛋殼品質密切相關,并且在蛋殼礦化過程中呈時序性表達。
除上述離子轉運基因,離子轉運體對蛋殼礦化及品質也有重要影響。鈣結合蛋白(CALB)不僅負責胞內Ca2+的貯存和運輸,還具有促進CaCO3晶體沉積和形態調控的作用[30];PMCA作為子宮上皮細胞基底側膜的Ca2+泵,在子宮部的差異表達會影響蛋殼品質[11];CA能夠促進蛋殼膜上CaCO3晶體的生長并加速其沉積,在高蛋殼強度產蛋雞體內表現出更高的活性[31]。

表1 蛋雞子宮上皮細胞的離子轉運載體及功能Table 1 Ion transpoters and their fuctions of uterine epithelial cells in laying hens
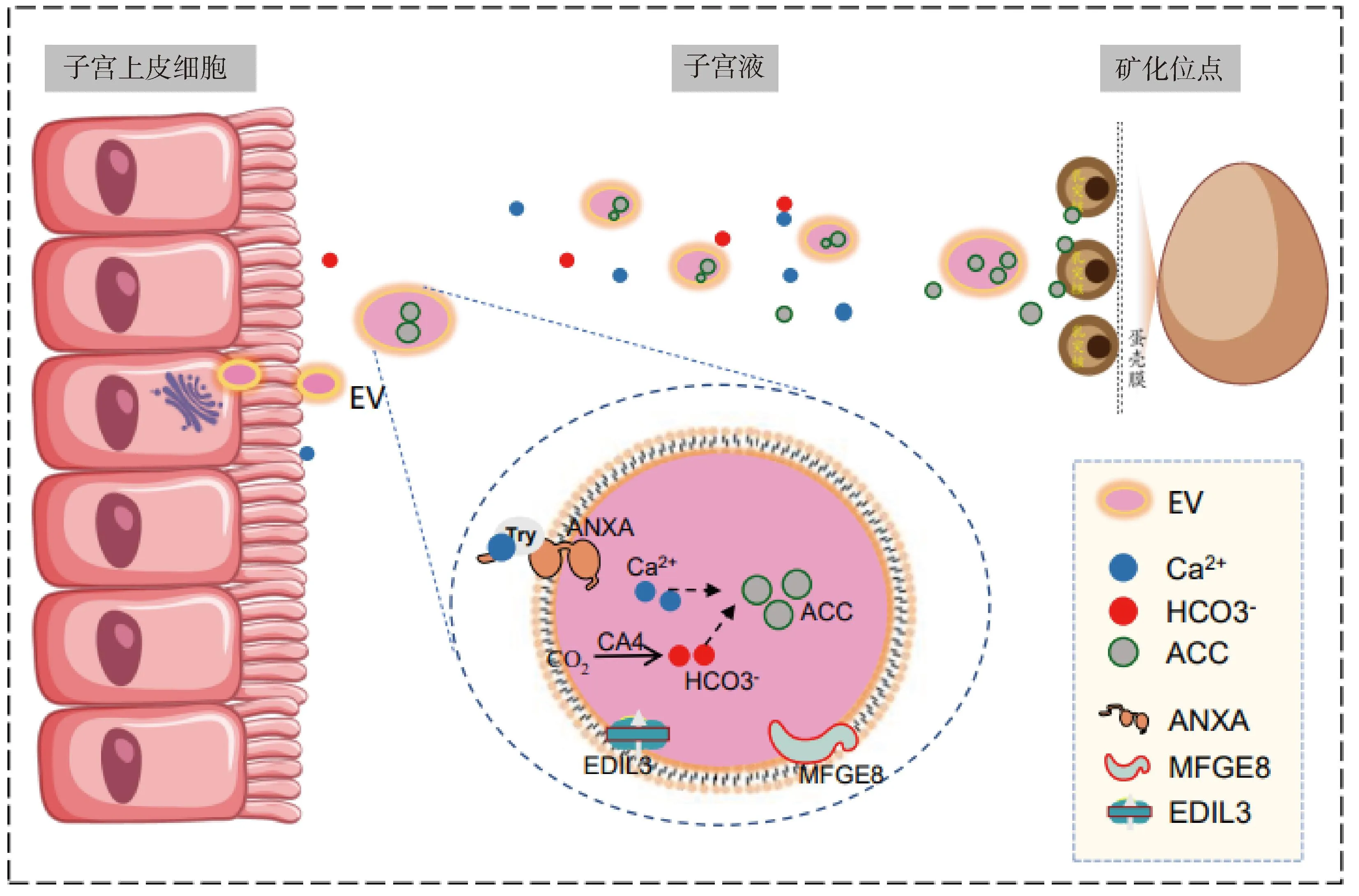
圖2 蛋雞子宮液的胞外囊泡轉運(參考Stapane等[4])Fig.2 Extracellular vesicle transport in uterine fluid of laying hens (Referring to Stapane et al[4])
EV的蛋白質和脂質成分也在蛋殼礦化過程中發揮作用。ANXA是EV中種類最豐富的蛋白質,從不同類型的細胞中共分離出12種不同的ANXA,其中對ANXA5在生物礦化中的作用研究最多[34]。而EV的脂質成分磷脂酰絲氨酸(phosphatidylserine,PS)可提高ANXA5對Ca2+的親和力,并促進CaCO3晶體的生長[33]。蛋雞子宮部免疫熒光結果顯示,EDIL3水平在蛋殼礦化起始期間顯著升高[23],研究表明EDIL3和MFGE8可通過與富含Ca2+的晶體表面選擇性相互作用以促進晶體成核或改變晶體形態[35]。另有研究比較了PS與ANXA5和MFGE8的結合能力,發現PS與MFGE8的親和力更高,推測MFGE8對EV運輸ACC到礦化位點起更強的調控作用[36]。綜上,蛋雞子宮部Ca2+轉運是蛋殼礦化的關鍵過程,以子宮部Ca2+轉運為調節靶點,通過營養干預的方式調節蛋殼礦化過程,可作為解決生產中多種因素(增齡、飼糧和應激水平等)誘發蛋殼品質下降問題的重要方向。
4 影響蛋雞子宮部鈣離子轉運的因素
4.1 激素
Ca2+和HCO3-的離子平衡受下丘腦-垂體-性腺的激素軸調控。黃晨軒等[37]研究發現,飼糧鈣水平對蛋殼品質的影響與甲狀旁腺素水平有關。卵泡刺激素和黃體生成素可以促進雌激素的分泌,而蛋雞子宮部CALB基因的表達受孕酮和雌激素的調節,孕酮通過下調子宮部中Ca2+-ATPase、CALB和PMCA的基因表達抑制蛋殼礦化[38-40],而雌激素在蛋殼礦化期間分泌增加,促進了CALB的表達[41]。Zhang等[42]研究發現,孕酮可以改變蛋殼超微結構,進而影響蛋殼品質,在蛋雞產蛋后2 h注射孕酮,可加速乳突體的早期融合,延長礦化期,從而減少乳突層厚度并增加有效層厚度,其可能的機制是上調了礦化初始期子宮部CaBP-d28k及CA2的表達以增加子宮Ca2+轉運和改善晶體結構,促進CaCO3形成與沉積;而產蛋后5 h注射孕酮卻降低了蛋殼有效層厚度,可能是孕酮抑制了快速沉積期CaBP-d28k的表達使子宮部Ca2+供應不足。此外,激素水平的變化影響因素較多,如何利用營養因素通過調控激素水平間接影響Ca2+轉運是研究的重點和難點。
4.2 維生素
CALB的表達與維生素D3代謝的強弱密切相關,飼糧維生素D3被攝入體內在肝和腎中轉化為1,25-二羥維生素D3(1,25-(OH)2D3),1,25-(OH)2D3是類固醇激素,可促進腸上皮CALB的表達,增加鈣離子的吸收和轉運,進而影響蛋殼形成,提高蛋殼品質。研究發現,飼糧中添加125 μg·kg-1維生素D3和1,25-(OH)2D3增加了乳突密度和柵欄層厚度,提高了蛋殼強度,同時提高了血漿鈣水平[43];350~450 IU·kg-1飼糧維生素D3水平殼顯著改善蛋殼乳突層厚度以及血清鈣、磷含量[44]。飼糧中維生素D3缺乏時,機體吸收鈣的能力下降,蛋雞子宮部CaCO3濃度隨之降低,則會導致薄殼蛋和軟殼蛋的產生[45]。然而,1,25-(OH)2D3是否調節蛋雞子宮部CALB的表達存在爭議[41,46],飼糧1,25-二羥維生素D3對子宮CALB蛋白水平沒有影響[47],而體外培養蛋雞子宮部組織中添加1,25-二羥維生素D3又可以促進CALB蛋白的表達[48]。此外,有研究表明,維生素D3可以增加上皮組織中PMCA的表達[49]。可以確定的是,蛋雞對維生素D3或2,5-羥維生素D3的需求與鈣水平一樣存在上限,過量補充維生素D3雖提高了血鈣濃度,但加重了蛋殼丘疹問題[50]。此外有研究發現,飼糧添加維生素A、維生素C對蛋殼品質也有一定的改善作用[44,51],但是否通過調控Ca2+轉運發揮作用還需進一步研究。
4.3 礦物元素
鈣、磷、銅、鋅、錳、鈉和氯等礦物元素是蛋殼形成所必須的,它們通過維持蛋殼礦化時子宮部的離子穩態來調控Ca2+轉運,并最終影響蛋殼的礦化過程[52-55]。
4.3.1 鈣、磷 鈣、磷來源和水平及鈣的溶解度都會對蛋殼品質產生影響,同時與Ca2+的轉運有密切關系[58]。常見的鈣源有石灰石、蛤殼、牡蠣殼、蛋殼等;磷的來源主要有植酸磷和非植酸磷。Lee等[56]對比了粗、細雞蛋殼、石灰石、蛤殼和牡蠣殼對蛋殼品質的影響,結果表明粗蛋殼相較于其他組可以更好地提高蛋殼品質;粗石灰或牡蠣殼相較于細石灰石在雞胃中停留時間長、溶解速度也較慢,可以更好地為蛋雞供應鈣,在夜間也可以維持血鈣濃度[57]。飼糧中添加非植酸磷可以改善蛋殼品質[58]。隨周齡增加,蛋雞攝入礦物元素的能力逐漸下降,Ca2+轉運活動減弱[59]。飼糧中鈣、磷水平可直接影響產蛋雞子宮腔內CALB1蛋白表達而改變CaCO3的沉積能力[60-61]。研究表明,70周齡產蛋雞飼糧鈣水平升高可線性提高蛋殼強度和厚度,降低蛋殼破損率[62],4%鈣水平顯著降低了子宮部CA活性、提高了子宮部CALB含量,從而改善蛋殼品質[63]。然而,一味地增加飼糧鈣水平并非是蛋殼品質改善的“萬能密碼”,過高鈣水平亦會引發蛋雞子宮部Ca2+轉運紊亂,造成蛋殼礦化異常[64]。Shet等[65]研究發現,飼糧中添加植酸磷降低了蛋雞子宮部中CALB的表達,說明磷的來源和水平也會影響Ca2+轉運基因,但鈣的來源及溶解度對于Ca2+轉運的影響還有待進一步探究。
4.3.2 鋅、錳 研究發現鋅源(硫酸鋅和蛋氨酸鋅)和水平會影響蛋雞子宮部CA、堿性磷酸酶(ALP)、骨橋蛋白(OPN)和蛋殼基質蛋白-116(OC-116)的基因表達及血清中CA和ALP水平,調控蛋殼礦化過程[66-67]。在蛋鴨上,飼糧添加80 mg·kg-1的鋅可促進鴨蛋殼礦化過程中HCO3-的生成,增加蛋殼中的鈣、磷含量,并影響子宮部內CA2、SLC4A4/5和SLC26A9的基因表達[68]。錳源(硫酸錳和氨基酸錳)和水平同樣影響蛋殼礦化過程,飼糧硫酸錳可線性和二次提高蛋殼鈣化層中糖胺聚糖(礦化中Ca2+轉運和沉積的重要調控物質)的含量,而氨基酸錳可同時提高蛋殼鈣化層和基質薄膜中糖胺聚糖含量,二者通過調控蛋殼的礦化過程增加了蛋殼有效層厚度,從而改善蛋殼品質[69],轉錄組與PCR結合分析進一步證實了該過程還涉及錳對子宮蛋白糖基化和糖代謝的調節[70]。
4.3.3 鈉、氯 電解質鈉、氯也是影響蛋殼品質的重要因素。筆者團隊研究發現,利用碳酸氫鈉或硫酸鈉替代氯化鈉降低飼糧氯水平可提高鈣的表觀代謝率和蛋殼中鈣水平,改善蛋殼有效層厚度和蛋殼強度[71]。繼而以硫酸鈉和碳酸氫鈉分別作為鈉源,發現0.71%硫酸鈉(飼糧總鈉0.3%)可提高蛋殼鈣化層的糖胺聚糖水平,并改善蛋殼厚度和比例[72]。進一步地,筆者團隊證實了硫酸鈉通過上調子宮部離子轉運基因SLC8A1、SCNN1α、ATP1BA和KCNMA1的表達,提高峽部ATPS、SULT、DS和CS含量,改善蛋殼礦化結構和品質(數據未發表)。因此,礦物元素在改善蛋殼品質方向上具有巨大潛力,其他微量元素如鐵、硒、碘等對蛋殼子宮部Ca2+轉運的影響有待進一步研究。
4.4 氨基酸
氨基酸對Ca2+轉運的影響主要通過Ca2+轉運相關基因表達和酶活性調控來提高蛋殼品質。研究發現,隨著日糧添加精氨酸-硅酸鹽-肌醇復合物水平的提高,硅酸鹽和肌醇復合使用有利于提高精氨酸生物利用度[73],蛋殼鈣沉積量也相應提高[74]。保持較低水平(約0.57%)的Met+Cys可以維持蛋殼厚度[75]。此外,氨基酸與礦物元素復合物似乎對改善蛋殼品質有更好的效果。飼糧中添加Zn-Met和Mn-Met可以顯著增加蛋殼厚度[76];Abd El-Hack等[77]發現,日糧添加50 mg ZnO和100 mg Zn-Met可以提高蛋雞血清中Zn水平;最新一項研究發現,在蛋雞飼糧中添加一種蛋白質鋅也可以通過提高血清Zn水品顯著提高蛋殼品質[78]。進一步研究表明,飼糧添加80 mg·kg-1Zn-Met顯著提高了血清鈣含量和子宮CA、CaBP-d28k的基因表達,促進蛋殼礦化中Ca2+的沉積而提高蛋殼品質[67];Min等[79]研究發現飼料添加蛋氨酸羥基類似物螯合鋅通過提高肝組織CA活性,促進Ca2+沉積,改善蛋殼品質。
4.5 植物提取物
近年來,植物提取物(類黃酮、精油)被發現可能通過促進鈣、磷等礦物質的吸收或增強Ca2+轉運能力提高蛋殼品質[80-81]。類黃酮主要通過影響機體生長激素釋放激素、促黃體素、孕酮等激素水平而調控Ca2+轉運過程,Xiao等[82]在飼糧中添加大豆苷元與中草藥混合物,發現機體鈣、磷含量、黃體生成素水平顯著提高;4,7-二羥基異黃酮顯著提高機體孕酮、卵泡刺激素、黃體生成素和雌激素水平,從而促進子宮中CaCO3晶體形成相關酶的產生提高蛋殼品質[83-84];桑葉黃酮可以通過提高Ca2+轉運相關基因CALB、KCNA1的表達,提高蛋殼品質等[85];在患有子宮炎癥的蛋雞飼糧中添加植物精油,可以通過提高CALB1、ATP2B1、ATP2B2、SLC26A9的表達來改善蛋殼品質[86]。此外,酚類物質、牛至精油、八角茴香精油等也被證明有提高蛋殼品質的作用[87-89],但對其是否及如何參與蛋雞子宮部蛋殼礦化期的Ca2+轉運調節還有待進一步研究。綜上,植物提取物對礦化調控的作用有待深入研究。
5 總結與展望
近十余年來,中外學者對雞蛋蛋殼礦化過程的認知取得了較大進展。CaCO3作為蛋殼形成的最主要原料,子宮部Ca2+的有效運無疑是蛋殼礦化的關鍵環節和保證。在已知的三條Ca2+轉運途徑中,對跨細胞和細胞旁途徑的認識已取得長足進展,而對胞外囊泡轉運途徑和調控機制的了解仍十分有限,具有很大的創新空間和研究價值。蛋白質組學和轉錄組學等技術的成熟應用使得越來越多的Ca2+轉運相關基因和蛋白與蛋殼礦化過程聯系了起來,這些因子對蛋殼力學特性、化學組成和微觀結構的調控也正被逐漸認知,這對以Ca2+轉運為切入點,從遺傳或營養角度優化蛋殼礦化程序,改善蛋殼品質提供了靶點和可能。從營養的角度看,對蛋殼礦化和品質有實在或潛在調節效應的物質有很多,包括礦物質、激素、氨基酸等常規營養素和植物提取物等飼料添加劑。然而,目前對這些物質如何參與輸卵管子宮部的Ca2+轉運,及調節礦化過程的具體機制的研究仍不夠深入,一定程度限制了其在生產上的廣泛應用。筆者認為,以蛋殼礦化過程的Ca2+轉運為突破口,未來值得深入開展研究的方向有二:一是探索建立成熟的蛋雞子宮上皮細胞培養技術,助力從跨細胞和旁細胞途徑探究Ca2+轉運對蛋殼礦化和受外部調節的影響;二是加強胞外囊泡轉運途徑的深入研究,利用多種新興的技術和儀器開展囊泡形成和分泌機制、形態特征、理化性質、功能特性和調控機制等研究,力求更深入的理解其在蛋殼礦化中的作用和調控潛力。

