基于半胱胺保護(hù)的金納米酶催化光度法測(cè)定痕量亞硝酸根
姚秀琪,韋礱,覃慶婷,何深怡,吳海嬌,凌紹明
(百色學(xué)院 化學(xué)與環(huán)境工程學(xué)院,廣西 百色 533000)
亞硝酸鹽是一種存在于水、土壤和生物體內(nèi)的無(wú)機(jī)化合物,在農(nóng)業(yè)和工業(yè)中常用作防腐劑和添加劑[1]。然而,亞硝酸鹽離子可以作為亞硝胺和亞硝酸化合物的前體,這些物質(zhì)會(huì)致癌和誘變,因此攝入大量亞硝酸鹽會(huì)嚴(yán)重?fù)p害人體健康[2-3]。此外,亞硝酸鹽是氮循環(huán)的活性中間體之一,可作為評(píng)價(jià)氮循環(huán)氧化和還原步驟平衡狀態(tài)的重要指標(biāo)[4]。亞硝酸鹽離子也是水質(zhì)污染程度的一個(gè)指標(biāo),世界衛(wèi)生組織建議[4]雨水中亞硝酸鹽的最高含量為3 mg·L-1。對(duì)飲用水,歐洲監(jiān)管機(jī)構(gòu)[5]將亞硝酸鹽的最大允許含量定為0.1 mg·L-1。因此,亞硝酸鹽的定量分析對(duì)水質(zhì)安全和食品安全監(jiān)測(cè)具有重要的意義。目前,檢測(cè)亞硝酸根的方法主要有液相色譜法[6]、熒光法[7]、分光光度法[8]、化學(xué)發(fā)光法[9]、電化學(xué)法[10-11]、離子色譜法[12-13]、共振瑞利散射光譜法[14]和表面增強(qiáng)拉曼光譜法[15]等。
上述檢測(cè)NO2-方法,各有優(yōu)勢(shì)與不足。如碳量子點(diǎn)熒光法[7]檢測(cè)亞硝酸根借助碳點(diǎn)與NO2-的專一作用機(jī)制,也就是說(shuō)一份分析物只能生成一份信號(hào),靈敏度偏低的問(wèn)題還是存在[16]。對(duì)一對(duì)一檢測(cè)方法而言,催化熒光分析法得到極大關(guān)注,極少量催化劑的引入能夠帶來(lái)較多的生成物,致使熒光信息發(fā)生擴(kuò)增作用,從而較大幅度地提高檢測(cè)靈敏度[17]。廖雪鳳等[18]利用NO2-催化溴酸鉀氧化過(guò)量碘化鉀生成I3-,借助I3-的刻蝕作用導(dǎo)致BSA保護(hù)的納米金熒光減少原理,建立催化熒光法檢測(cè)NO2-。該法靈敏度高、選擇性好,但是熒光材料的制備與純化過(guò)程復(fù)雜,檢測(cè)費(fèi)時(shí)。
近年來(lái),基于納米材料模擬酶的催化活性成為放大檢測(cè)信號(hào)的重要手段,實(shí)現(xiàn)了痕量物質(zhì)的高靈敏測(cè)定。研究發(fā)現(xiàn),金屬及其氧化物、貴金屬納米團(tuán)簇、石墨烯及金屬硫化物納米片等具有過(guò)氧化物酶催化活性,這種納米材料統(tǒng)稱為“納米酶”[19-20]。納米酶在催化活性、表面電荷、形貌和尺寸上與天然過(guò)氧化物酶極為相似,具有價(jià)廉、穩(wěn)定、易合成等優(yōu)點(diǎn),在生物醫(yī)學(xué)檢測(cè)、環(huán)境監(jiān)測(cè)以及食品安全等領(lǐng)域應(yīng)用廣泛。如Wang等[21]基于金屬有機(jī)骨架(MOF)[Cu(PDA)(DMF)]的過(guò)氧化物酶活性,實(shí)現(xiàn)人尿中多巴胺的檢測(cè)。吳亮亮等[22]通過(guò)表面修飾Ag/Pt復(fù)合納米簇,用于調(diào)控納米酶的催化活性,實(shí)現(xiàn)對(duì)環(huán)境水樣中痕量Cu2+的快速測(cè)定。因此,豐富和發(fā)展NO2-的檢測(cè)新技術(shù),降低檢測(cè)成本、提高檢測(cè)速度和靈敏度以及在線檢測(cè)能力已成為急需解決的科學(xué)問(wèn)題。
根據(jù)催化反應(yīng)能夠增強(qiáng)檢測(cè)信號(hào)的作用[17],本工作擬將亞硝酸根的催化氧化反應(yīng)和金納米酶的催化顯色反應(yīng)相結(jié)合,組建“雙催化反應(yīng)體系”以期提高檢測(cè)NO2-的靈敏度,探索建立一種快速、靈敏度高的、操作簡(jiǎn)便的比色分析法。即:利用亞硝酸根催化溴酸鉀氧化過(guò)量的碘化鉀生成I3-,基于I3-對(duì)半胱胺保護(hù)的金納米粒子(cyst-AuNPs)的刻蝕作用,調(diào)控了cyst-AuNPs催化“過(guò)氧化氫與四甲基聯(lián)苯胺(TMB)反應(yīng)”的催化活性,探索建立一種檢測(cè)NO2-的新型比色探針。
1 實(shí)驗(yàn)部分
1.1 主要儀器
日本島津公司生產(chǎn)的2700型紫外可見分光光度計(jì);北京格瑞恩科技發(fā)展公司生產(chǎn)的SY-1220型恒溫水浴箱;上海梅特勒-托利多儀器有限公司生產(chǎn)的ME204電子分析天平;美國(guó)Miliipore公司生產(chǎn)的Driect-55UV型純水機(jī)。
1.2 主要試劑及配制方法
亞硝酸根標(biāo)準(zhǔn)儲(chǔ)備液:0.16 mg·mL-1,準(zhǔn)確稱取0.060 1 g亞硝酸鈉(優(yōu)級(jí)純,上海阿拉丁生化科技股份有限公司),用超純水溶解后定容于250 mL茶色容量瓶,搖勻,冰箱保存;亞硝酸標(biāo)準(zhǔn)工作液:1.0 μg?mL-1,移取62.5 μL亞硝酸根儲(chǔ)備液于10 mL比色管中,加超純水至刻度,現(xiàn)配現(xiàn)用;氯金酸:2.4×10-2mol?L-1;半胱胺鹽酸鹽(cyst):213 mmol?L-1;3,3′,5,5′-四甲基聯(lián)苯胺(TMB)乙醇溶液:10 mmol?L-1;NaAc水溶液:0.20 mol?L-1;HAc水溶液:0.20 mol?L-1;pH值=4.0 NaAc-HAc緩沖溶液:取18.0 mL 0.20 mol?L-1NaAc水溶液和82.0 mL 0.20 mol?L-1HAc水溶液混合而得;過(guò)氧化氫儲(chǔ)備液:0.10 mol?L-1,現(xiàn)配現(xiàn)用;過(guò)氧化氫工作液:1.0×10-3mol?L-1,現(xiàn)配現(xiàn)用;硼氫化鈉水溶液:10 mmol?L-1,現(xiàn)配現(xiàn)用;KBrO3水溶液:0.10 mol?L-1;H2SO4水溶液:0.10 mol?L-1;KI水溶液:0.40 mol?L-1。
1.3 cyst-AuNPs的合成
參照文獻(xiàn)[23]合成,并做些改動(dòng)。向潔凈的三角瓶中加入2.34 mL濃度為2.4×10-2mol?L-1的氯金酸,補(bǔ)加超純水40 mL,放入攪拌子攪拌,向燒杯中加入500 μL濃度為213 mmol?L-1的半胱胺鹽酸鹽溶液,繼續(xù)攪拌20 min后,逐滴加入90 μL濃度為10 mmol?L-1硼氫化鈉水溶液,滴加完畢繼續(xù)攪拌15 min,得酒紅色溶液,無(wú)菌密封冰箱保存。
1.4 實(shí)驗(yàn)方法
在5.0 mL離心管中依次加入NO2-標(biāo)準(zhǔn)工作液、0.10 mol?L-1H2SO4水溶液120 μL、0.10 mol?L-1KBrO3水溶液50 μL、0.40 mol?L-1KI水溶液200 μL,用超純水稀釋至1.0 mL,并做空白試液(A0)。室溫下孵育時(shí)間(t1)30 min后,加入100 μL cyst-AuNPs溶液,預(yù)孵育時(shí)間(t2)15 min,再依次加入550 μL NaAc-HAc緩沖溶液(pH值4.0,0.20 mol?L-1)、300 μL 10 mmol?L-1TMB、200 μL 1.0×10-3mol?L-1過(guò)氧化氫,定容至3.0 mL,于30 ℃水浴中反應(yīng)時(shí)間(t3)30 min,測(cè)定655 nm處吸光度值A(chǔ),計(jì)算ΔA=A0-A。
2 結(jié)果與討論
2.1 cyst-AuNPs的吸收光譜及催化活性
圖1是cyst-AuNPs吸收光譜圖。制得的cyst-AuNPs呈現(xiàn)酒紅色,在521 nm處有強(qiáng)吸收,吸收峰的半峰寬較窄,初步說(shuō)明合成的cyst-AuNPs顆粒均勻,穩(wěn)定性好。
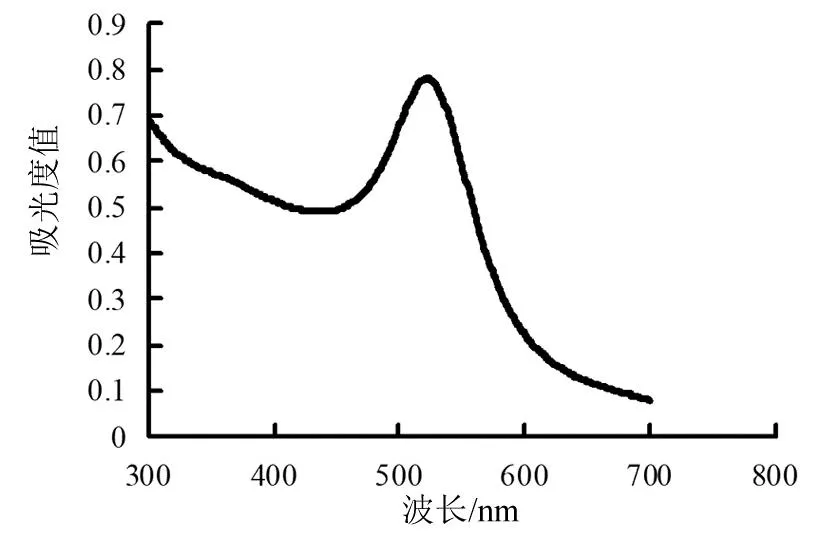
圖1 cyst-AuNPs的吸收光譜圖
圖2是不同體系的吸收光譜圖。TMB獨(dú)立存在時(shí)無(wú)明顯吸收峰(見圖2曲線1),TMB與過(guò)氧化氫反應(yīng)后體系在655 nm處有TMB氧化態(tài)的特征吸收峰,但是強(qiáng)度弱(見圖2曲線2),這是因?yàn)門MB與過(guò)氧化氫反應(yīng)極為緩慢。加入cyst-AuNPs后,體系在655 nm處的吸收值明顯增大(見圖2曲線5),溶液微深藍(lán)色,說(shuō)明cyst-AuNPs能夠有效催化過(guò)氧化氫氧化TMB。當(dāng)體系存在不同質(zhì)量濃度NO2-時(shí),體系在655 nm處的吸收降低,并且隨著NO2-質(zhì)量濃度的增加體系吸收值減小(見圖2曲線3與4)。這是因?yàn)殡S著NO2-質(zhì)量濃度的增加,體系生成的I3-增多,導(dǎo)致有更多的cyst-AuNPs被刻蝕,引起cyst-AuNPs催化活性降低。
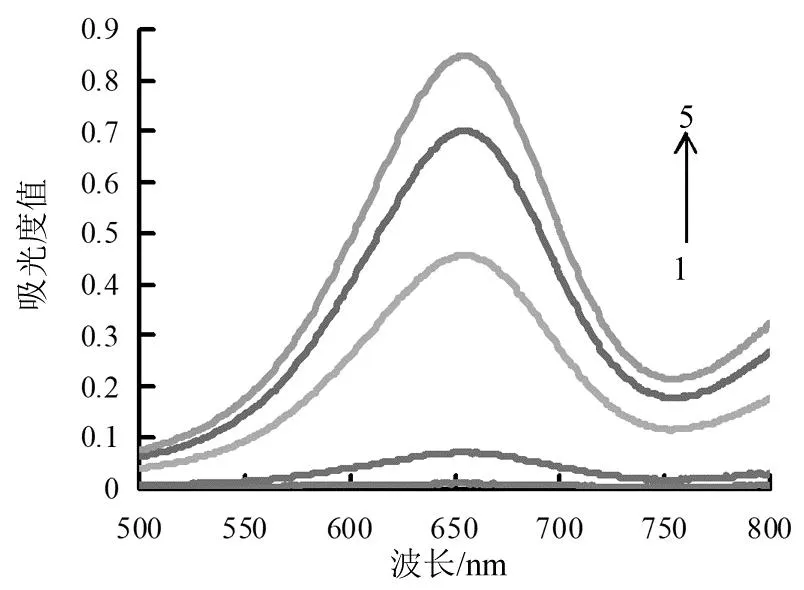
1.TMB;2.H2SO4+KBrO3+KI+NaAc-HAc+TMB+H2O2;3.H2SO4+KBrO3+KI+cyst-AuNPs+NaAc-HAc+TMB+H2O2+0.108 μg?mL-1 NO2-;4.H2SO4+KBrO3+KI+cyst-AuNPs+NaAc-HAc+TMB+H2O2+0.033 3 μg?mL-1 NO2-;5.H2SO4+KBrO3+KI+cyst-AuNPs+NaAc-HAc+TMB+H2O2+0.00 μg?mL-1 NO2-;cyst-AuNPs:100 μL+TMB:1.0 mmol?L-1 +H2O2:0.066 7 mmol?L-1 +pH值4.0
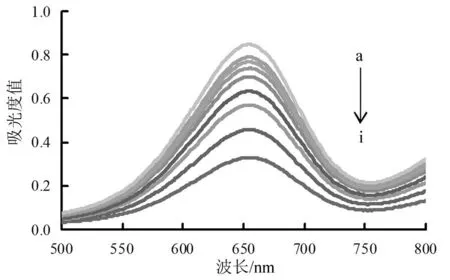
cyst-AuNPs:100 μL+TMB:1.0 mmol?L-1 +H2O2:0.066 7 mmol?L-1 +pH值4.0+NO2-(a到i:0,0.008 33,0.016 7,0.025 0,0.033 3,0.041 7,0.075 0,0.108,0.142 μg?mL-1)
圖3是有不同NO2-質(zhì)量濃度時(shí)體系的吸收光譜圖。由圖3可見,隨著NO2-質(zhì)量濃度增加,體系產(chǎn)生的I3-越多,有更多的金納米粒子被刻蝕,金納米粒子模擬酶催化活性被抑制,TMB被氧化的數(shù)量減少,體系在655 nm處的吸收值減小,體系的吸收值線性下降。實(shí)驗(yàn)選擇655 nm為測(cè)定波長(zhǎng)。
2.2 測(cè)定條件優(yōu)化
研究表明,痕量的NO2-對(duì)溴酸鉀氧化碘化鉀有強(qiáng)烈的催化作用[24],當(dāng)有過(guò)量碘化鉀存在時(shí),體系形成I3-,I3-對(duì)cyst-AuNPs有刻蝕作用,引起cyst-AuNPs模擬酶的催化活性被抑制。本工作主要對(duì)cyst-AuNPs模擬酶的催化反應(yīng)條件進(jìn)行優(yōu)化。
2.2.1 cyst-AuNPs溶液用量影響
固定其他條件,通過(guò)改變cyst-AuNPs溶液用量以考察cyst-AuNPs溶液用量對(duì)測(cè)定體系影響,結(jié)果見圖4。

圖4 cyst-AuNPs溶液用量影響
由圖4可見,隨著cyst-AuNPs溶液用量增加,體系的吸光度差值逐漸增大,當(dāng)用量為100 μL時(shí),吸光度差值達(dá)到最大值,此時(shí)測(cè)定靈敏度最高;隨后吸光度差值增長(zhǎng)比較緩慢,因此實(shí)驗(yàn)選擇cyst-AuNPs溶液用量為100 μL。
2.2.2 緩沖溶液pH值影響
固定其他條件,改變緩沖溶液pH值以考察緩沖溶液pH值的影響,結(jié)果見圖5。

圖5 緩沖溶液pH值影響
由圖5可見,隨著pH值增大,體系的吸光度差值快速增大,但當(dāng)pH值=4時(shí),體系的吸光度差值開始迅速下降。這是因?yàn)樗嵝原h(huán)境能夠保持cyst-AuNPs表面形成大量的正電荷而維持其穩(wěn)定性,pH值增大,cyst-AuNPs表面電荷減少,穩(wěn)定性降低,影響cyst-AuNPs催化活性。所以實(shí)驗(yàn)取緩沖溶液pH值=4比較合適。
2.2.3 緩沖溶液用量影響
固定其他條件,改變緩沖溶液用量以考察緩沖溶液用量的影響,結(jié)果見圖6。

圖6 緩沖溶液用量影響
由圖6可見,用量400~550 μL時(shí),吸光度差值逐漸上升。當(dāng)緩沖溶液的用量大于550 μL時(shí),吸光度差值開始降低,所以緩沖溶液用量取550 μL比較合適。
2.2.4 TMB用量影響
固定其他條件,改變TMB用量以考察其對(duì)體系的影響,結(jié)果見圖7。

圖7 TMB用量影響
由圖7可見,TMB的用量為150~270 μL時(shí),吸光度差值增長(zhǎng)的比較的快,300 μL以后,吸光度差值增加的比較緩慢。所以TMB用量取300 μL比較合適。
2.2.5 H2O2用量影響
固定其他條件,改變H2O2用量以考察其對(duì)體系的影響,結(jié)果見圖8。
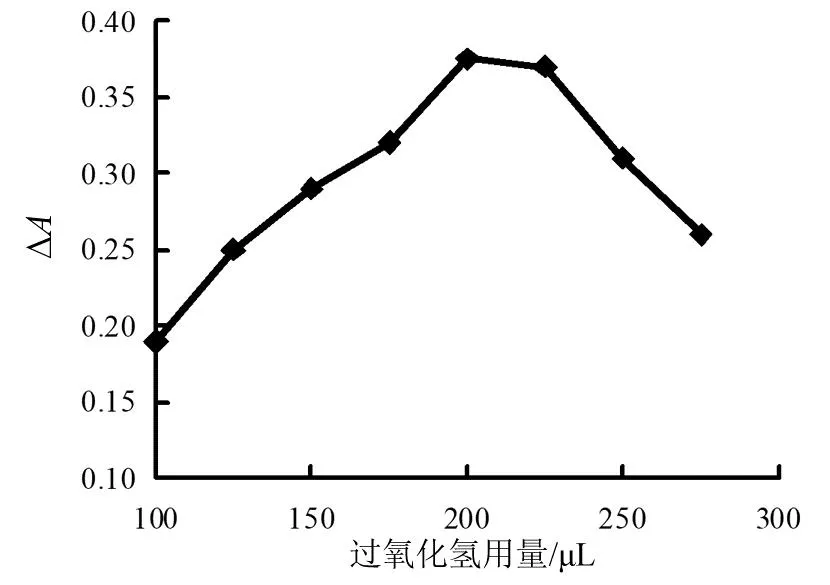
圖8 過(guò)氧化氫用量影響
由圖8可見,過(guò)氧化氫的用量為200 μL之前時(shí),吸光度差值逐漸增長(zhǎng),到200 μL以后,吸光度差值逐漸減小。所以過(guò)氧化氫用量200 μL比較合適。
2.2.6 溫度的影響
固定其他條件,通過(guò)改變納米酶催化反應(yīng)溫度以考察其對(duì)體系的影響,結(jié)果見圖9。
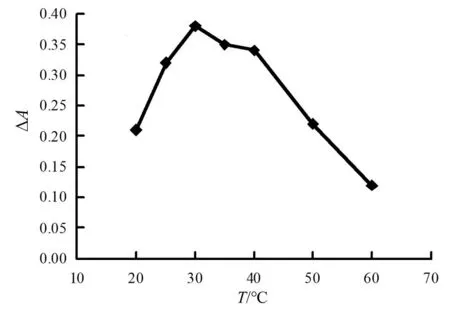
圖9 納米酶催化反應(yīng)溫度的影響
由圖9可見,納米酶催化反應(yīng)溫度為20~30 ℃時(shí),吸光度差值逐漸遞增,到30 ℃以后,吸光度差值開始減小。這是因?yàn)檩^高溫度下會(huì)加快過(guò)氧化氫分解,cyst-AuNPs活性降低。所以實(shí)驗(yàn)取30 ℃比較合適。
2.2.7 時(shí)間(t3)影響
固定其他條件,通過(guò)改變納米酶催化反應(yīng)時(shí)間(t3)以考察其對(duì)體系的影響,結(jié)果見圖10。

圖10 納米酶催化反應(yīng)時(shí)間(t3)影響
由圖10可見,反應(yīng)時(shí)間(t3)30 min之前,吸收光差值逐漸遞增,當(dāng)30 min之后,吸收光差值趨于平緩。隨著反應(yīng)時(shí)間的進(jìn)行,體系生成的I3-增多,導(dǎo)致有更多的cyst-AuNPs被刻蝕,引起cyst-AuNPs催化活性降低。當(dāng)30 min時(shí),反應(yīng)基本完成了。
2.3 線性方程及檢出限
參照實(shí)驗(yàn)方法,分別測(cè)定不同質(zhì)量濃度NO2-(0,0.008 33,0.016 7,0.025 0,0.033 3,0.041 7,0.075 0,0.108,0.142 μg?mL-1),測(cè)定不同質(zhì)量濃度NO2-的吸收值A(chǔ),計(jì)算ΔA,結(jié)果發(fā)現(xiàn)ΔA值與體系不同質(zhì)量濃度NO2-有較好線性關(guān)系,檢測(cè)方法的線性方程為ΔA= 0.024 9 + 3.474ρ,相關(guān)系數(shù)R2為0.987 7,線性范圍為0.008 33~0.142 μg?mL-1,檢出限(3S/K)為0.005 8 μg?mL-1。
2.4 干擾實(shí)驗(yàn)
實(shí)驗(yàn)對(duì)常見共存物質(zhì)進(jìn)行干擾實(shí)驗(yàn)。當(dāng)NO2-含量為0.075 μg?mL-1,相對(duì)誤差在10%以內(nèi)時(shí),1 000倍的K+、Na+、Ca2+、Mg2+、F-、Cl-、Br-、NO3-、CO32-、HPO42-、H2PO4-、Ac-;500倍的Zn2+、Pb2+;300倍的Mn2+、Al3+、Ni2+;100倍的Cd2+;50倍的V(Ⅴ);25倍的Fe3+;10倍的Cu2+;5倍的Hg2+、Ag+不干擾NO2-檢測(cè)。
2.5 樣品測(cè)定
水樣品經(jīng)過(guò)濾后,取適量樣品用本法進(jìn)行測(cè)定,并做加標(biāo)試驗(yàn),結(jié)果見表1。
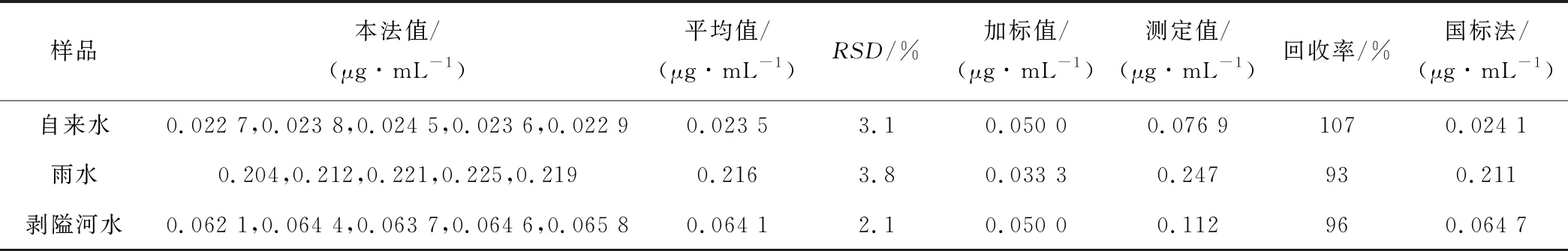
表1 樣品測(cè)定及加標(biāo)試驗(yàn)結(jié)果
本法測(cè)定結(jié)果與國(guó)標(biāo)法[25]基本一致。
3 結(jié)論
基于cyst-AuNPs納米酶催化活性、NO2-的催化氧化反應(yīng)以及I3-刻蝕作用原理,將納米酶催化反應(yīng)與NO2-的催化氧化反應(yīng)相結(jié)合,構(gòu)建高靈敏檢測(cè)NO2-的“雙催化反應(yīng)”體系。在優(yōu)化測(cè)試條件下,NO2-的質(zhì)量濃度與體系吸收變化量ΔA有線性關(guān)系,據(jù)此建立了靈敏檢測(cè)0.008 33~0.142 μg?mL-1NO2-的光度分析法。本法用于測(cè)定環(huán)境水樣品中NO2-的含量,結(jié)果滿足NO2-含量測(cè)定要求。

