用于含酚廢水處理的鐵基載體Fenton催化劑研究進展
張涵,葉卉,呂婧,李泓
(天津工業大學 材料科學與工程學院 省部共建分離膜與膜過程國家重點實驗室,天津 300387)
隨著工業生產的發展和對化學品的不斷需求,大量含酚廢水被排入水體。苯酚主要用于化工生產和石化行業,通常被用作生產烷基酚、甲酚和樹脂等化學品的中間體[1]。此外,染料、紡織工業和爆炸性材料也需要苯酚作為原材料之一[2-3]。這些直接或間接將含酚廢水排入水體的工業活動會造成水污染。苯酚廢水常用的處理方法有蒸餾法、吸附和萃取法、生物降解法等,但這些方法普遍存在工藝復雜、苯酚不能完全去除、成本高、可能產生污染環境的副產物等問題。因此,迫切需要一種高效且成本低廉的處理方法來解決當前的問題。
高級氧化法(AOPs)是一種降低廢水中苯酚濃度的有效方法。這種方法操作條件溫和,試劑用量少。H2O2是一種化學氧化劑,在酸性或堿性介質中都是一種強氧化劑。然而,H2O2作為單獨的氧化劑,其反應活性通常較慢且不完全,因此需要H2O2與均相或非均相催化劑偶聯才能增強其反應活性。傳統的Fenton反應是H2O2與Fe2+在酸性環境中結合生成Fe3+和?OH,用于催化降解有機化合物。
1 傳統Fenton處理苯酚廢水
Fenton過程依賴于活性氧(ROS)的形成[4]。生成的ROS具有高度氧化活性,可以與溶液中的有機物發生反應,導致它們被完全氧化為CO2和H2O,也稱為有機物礦化[5]。Fenton反應依賴于在催化劑存在下H2O2的分解,在反應(1)后產生?OH。當在酸性介質中進行時,Fenton反應也可以發生反應(2)。

(1)

(2)
由于Fe2+作為催化劑的作用,?OH可以不斷地生成和積累。催化循環也包括Fe3+與H2O2反應的均相類Fenton反應(3)。該反應再生Fe2+,并產生較弱的氧化劑,即超氧自由基(HO2?)。盡管HO2?幾乎不會導致有機物礦化,但它可以在反應(4)后再生催化劑。

(3)

(4)
文獻報道Fenton工藝處理苯酚廢水指出苯酚轉化為羥基化芳香族化合物及其氧化衍生物[6-14]。圖1展示了水體中Fenton反應在?OH作用下苯酚礦化的反應路徑[15]。苯酚初始羥基化生成對苯二酚(HQ)、鄰苯二酚(CT)和間苯二酚(RC)的混合物。同時,鄰苯二酚和間苯二酚進一步羥基化得到1,2,3-三羥基苯(THB)。這些芳香烴隨后開環產生羧酸的混合物,再轉化為草酸和甲酸,這兩種酸最終轉化為CO2和H2O。

圖1 水中苯酚的Fenton礦化反應途徑[15]
Fenton氧化法的主要優點是工藝簡單,對廢水中酚類降解效果好。此外,Fe2+和H2O2都很容易獲得,簡單易行,不需要任何額外的能量輸入。然而,傳統的Fenton工藝存在一些缺點,如需要將pH值調整到酸性范圍 (pH值為2.8~3.5),而且會產生大量的鐵污泥,造成處理困難,并可能導致二次污染。
為了解決傳統Fenton存在的缺點并探索Fenton反應(2)拓展至中性或近中性條件下的可能性,近年來研究證明載體Fenton催化劑能夠解決傳統Fenton反應pH值使用范圍窄的缺點。此外,由于固體催化劑可以連續重復使用,大大降低了運行成本。
2 載體Fenton催化劑處理含酚廢水進展
許多類型的載體Fenton催化劑,如沉積在底物的鐵離子[16-17]、鐵氧化物[18-19]和復雜結構[20]的催化劑已被用于苯酚的降解。在此條件下,大部分鐵催化劑仍保持不溶狀態,在其表面存在Fe(Ⅱ)和Fe(Ⅲ)物種誘導下發生非均相Fenton反應(5)和非均相類Fenton反應(6)[18]。非均相Fenton反應生成的?OH在催化劑表面附近破壞有機物。除了直接使用各種鐵礦物作為非均相Fenton催化劑外,還可以負載在各種載體上,如沸石、金屬有機骨架(MOFs)、黏土、氧化石墨烯(GO)等。例如,將α-FeOOH固定在GO-CNTs[21]或沉積在沸石上[22]以及Fe2O3[23]、α-Fe2O3[24]負載在蒙脫土上形成的載體Fenton催化劑。

(5)

(6)
2.1 金屬有機骨架及復合材料
金屬有機骨架(MOFs)是由各種金屬離子與有機配體相互作用而形成的一類組裝體。高孔隙率、優異的表面積等優勢引起了研究人員對MOFs的廣泛關注。在過去的十年中,由于其高效的?OH生成能力,在非均相Fenton反應中使用了含鐵MOFs。目前,Fe-MOFs和半導體復合材料的制備是提高電荷轉移效率的一種成功策略。Niu等[25]將Pd/Fe3O4納米顆粒負載在空心Fe-MOFs上,在pH值4.0的條件下可以實現100%的苯酚降解,并提出通過將電子從Pd轉移到Fe3O4和Fe-MOF上以增強Fe(III)/Fe(II)氧化還原循環來產生?OH。
聚羧酸鹽和氨基聚羧酸鹽可以與Fe(III)形成穩定的配合物,在近紫外和可見光區域可以更有效地吸收光。金屬-羧酸配合物(Me(OOCR)z+)對光敏感,紫外光照射可誘導配體與金屬電荷轉移(LMCT)發生絡合反應[26]。這種光驅動的反應減少了金屬中心,促進了配體的脫羧[27]。當采用光-Fenton反應時,該反應可以使Fenton催化劑再生并誘導礦化。文獻中描述的最常見的反應是Fe(Ⅲ)-草酸根配合物[15],根據反應(7)~(10)進行光脫羧反應。

(7)

(8)

(9)

(10)
2.2 黏土基催化劑
黏土材料在地殼中大量存在,具有比表面積大,熱穩定性好和機械強度高等優點,常被用作Fenton催化劑的載體。Liu等[28]將Ag/AgCl浸漬在海泡石黏土上,并用羥基鐵(Ag/AgCl/Fe-S)修飾。該催化劑具有良好的降解苯酚的活性。Wang等[29]通過改變Cu/Ni比制備了一系列CuNiFe層狀催化劑。實驗證明?OH自由基主要由Cu(Ⅱ)/Cu(I)對的反應(11)和(12)產生,但非均相類Fenton反應(6)形成較弱的HO2?自由基。Ni(III)/Ni(Ⅱ)對分別通過反應(13)和(14)幫助加速Cu(I)和Fe(III)的形成。圖2為該催化劑表面的離子產生和苯酚的氧化反應。

圖2 CuNiFe層狀催化劑上非均相類Fenton法脫除苯酚的反應機理[29]

(11)

(12)
(13)
(14)
Deng等[30-31]認為Fe(II)絡合物與穩定的三聚磷酸鹽(TPP)形成的絡合物可以產生大量的?OH,如下所示:

(15)

(16)

(17)
Fe-海泡石黏土被提出作為一種非均相催化劑懸浮在TPP電解質中[30]在200 mL 1.40 mmol/L苯酚溶液中加入0.050 mol/L TPP,向陰極通入O2產生H2O2。在pH值=6和I=200 mA的條件下,60 min時苯酚完全去除。在這些條件下電解420 min后,TOC的降解率為85%。這些結果遠遠優于使用0.050 mol/L K2SO4和0.40 mmol/L Fe2+的均相電-Fenton (EF)工藝所達到的27% TOC降解率。EF體系的高降解率的原因是Fe-海泡石黏土被腐蝕,向電解液中提供Fe2+離子,形成Fe2+-TPP絡合物。Fe2+-TPP絡合物能夠在較寬的pH值范圍內通過反應(15)~(17)與O2反應,從而產生H2O2和?OH,從而提高EF性能。
Deng等[31]采用了鎳-鐵陰極,其具有從溶解的O2中生成H2O2和通過腐蝕釋放Fe2+離子的能力。圖3說明了在此電解體系中生成?OH的反應,包括化學腐蝕、陰極保護和H2O2生成的途徑。pH值=6時,苯酚在50 min內被完全去除,電解100 mL空氣飽和溶液240 min后,TOC的降解率為74%。

圖3 采用Pt陽極和Pt/Ni-Fe陰極對三聚磷酸鹽(TPP)進行非均相電-Fenton處理的機理概述[31]
2.3 石墨烯及相關材料
碳材料與非均相Fenton催化劑結合,由于其快速的單電子轉移能力,有助于將Fe(III)快速還原為Fe(II)。石墨烯是一種二維單層碳原子,具有優異的電子遷移率、機械穩定性和導電性。石墨烯的存在為Fenton催化劑提供了支撐,增強了Fenton反應的性能。Fe0/Fe3O4納米結構[19]和分散在rGO[32]上的催化能力比Fe3O4大得多。在pH值=3和25 ℃的條件下,使用5 mmol/L H2O2和1 g·L-1的兩種濃度的催化劑處理50 mg·L-1的苯酚。Fe0/Fe3O4-rGO在50 min內可以使苯酚完全礦化,但Fe3O4-rGO在90 min內苯酚的降解率只有75%。作者解釋了Fe0/Fe3O4納米粒子的優越性,認為Fe0被氧化成Fe3+,電子轉移到Fe3O4上,使Fe(Ⅲ)轉化為Fe(Ⅱ),通過非均相Fenton反應(6)加速?OH的生成(見圖4)。

圖4 H2O2存在下Fe0/Fe3O4-rGO催化表面苯酚降解的反應機理[32]
Fe-Cu復合材料是具有協同催化性能的雙金屬非均相類Fenton催化劑。將Fe(II)和Cu(II)吸附在活性炭上或者將Fe-Cu納米粒子嵌入到有序的多孔活性炭中,制備CuFeO2@RGO[33]和Cu2O-CuFe2O4[34]微粒,均可得到較好的苯酚降解效果,但Fe和Cu均有損失。Cu在中性條件下可以和H2O2發生反應(11)(12)。銅在較寬的pH值范圍內具有較高的溶解度,這為中性pH值條件下的類Fenton反應提供了機會。此外,還提出了通過反應(18)還原Fe(III)來提高?OH的產量。
(18)
2.4 沸石基催化劑
沸石是由MO4四面體(M= Si4+,Al3+)連接而成的框架鋁硅酸鹽結構。沸石因其高的比表面積而被選為Fenton催化劑的負載材料。含鐵沸石因其結構均勻性和對不同污染物的高催化活性而被廣泛研究。Yang等[35]通過浸漬法將Fe2O3納米顆粒沉積在Y型沸石上。含鐵9%的沸石催化劑在中性pH值下2 h可降解90%的苯酚。催化劑與H2O2反應生成?OH的過程如圖5所示。
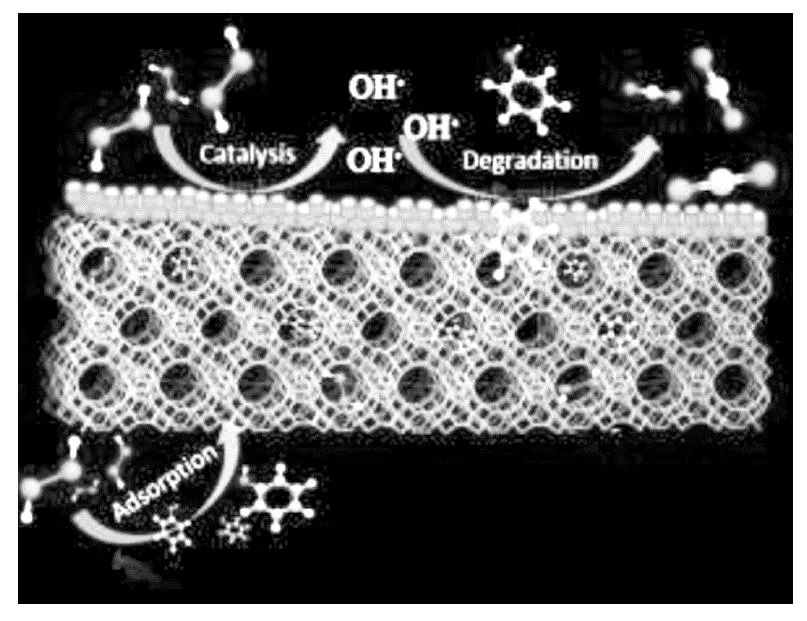
圖5 沸石多孔骨架的結構表征和苯酚降解的可能途徑[35]
在本課題組前期工作中[36],采用冷凍干燥法制備了含有孤立鐵物種(命名為4A-Fe)的Fenton催化劑。催化劑的鐵負載質量分數為8.90%,大部分鐵位點以孤立的鐵物種存在。通過在不同的pH值下降解苯酚,研究了所制備的催化劑的苯酚催化性能[37]。對于4A-Fe催化劑,在pH值=2和16 mmol/L H2O2的條件下,97.15%的苯酚在13.5 min內降解。但是,該催化劑仍只在酸性條件下表現出優異的催化降解性能,在中性和堿性條件下降解效率大大降低,pH值使用范圍依舊很窄。因此,本課題組利用4A-Fe為核心成分,以二維氫氧化銅納米片組件為外殼結構的核殼式分層4A沸石/Fe@Cu類Fenton催化劑,并用于苯酚的降解[37]。結果表明,在接近中性pH條件下,4A沸石/Fe@Cu雙金屬催化劑對H2O2的催化活性和利用效率高于4A沸石/Fe和4A zeolite@Cu單金屬催化劑。在H2O2存在下,在pH值=5條件下,4A沸石/Fe@Cu雙金屬催化劑在4 h后對苯酚的去除率為95.3%,遠高于相同條件下的單金屬催化劑。
3 催化膜/Fenton氧化系統
膜分離與AOPs的結合是廢水處理領域的前沿技術之一。催化劑可以錨定在膜表面或嵌入到主體結構中的孔道中。因此催化膜具有過濾和催化的雙重功能[38]:一方面,表面污染物可以被氧化,實現膜的自清潔;另一方面,與膜相結合的催化劑可以回收和重復使用。
膜表面的鐵基催化劑可以發生類Fenton過程活化H2O2,原位生成的具有強氧化能力的羥基自由基可以分解廢水中的有機污染物。在膜分離耦合Fenton氧化過程中,H2O2濃度、催化劑負載量、反應溫度、溶液pH均會影響降解效率。
Huang等[39]制備了Fe3O4/PVDF催化膜,發現Fe3O4的負載增加了催化膜的親水性和熱穩定性。此外,在100 mg·L-1MB和100 mg·L-1H2O2的混合溶液(pH值=4)中,摻雜質量分數為4% Fe3O4納米粒子的催化膜表現出最佳的催化效果,其純水通量為175.8 L·m-2·h-1,MB去除率為97.6%。Zhang等[40]制備了Fe3O4@SiO2/PES催化膜,并研究了MB降解和Fenton氧化的影響因素。實驗結果表明,在35 ℃下,以H2O2(體積分數30%)和MB (10×10-6)為原料液(50 L·min-1),質量分數20% Fe3O4@SiO2/PES膜對MB的降解率比PES原膜提高了45%。
Sun等[41]制備了由α-FeOOH/Zr/TiO2/α-Al2O3組成的催化膜。SEM圖像顯示α-Al2O3涂層膜被α-FeOOH棒狀催化劑均勻覆蓋。此外,在UV照射下(401 μW·cm-2),對BSA和HA的降解效率相比于沒有光照的催化膜/Fenton體系提高了約50%。α-FeOOH/Zr/TiO2/α-Al2O3催化膜/光Fenton體系幾乎不受溶液pH值的影響,實現了中性條件下對水體污染物的高效降解。
本課題組利用之前制備的4A-Fe催化劑,通過NIPS法制備了4A-Fe/PES混合基質膜作為CNMR,并將其用于動態連續去除苯酚[42]。結果表明,當m(催化劑)∶m(苯酚)為1∶3時,在pH值為2的條件下,反應6 min后,苯酚的轉化率達到99.9%±1.6%。當苯酚溶液初始pH值為6時,反應12 h后,苯酚的降解率為97.2%±3.3%。動態連續催化使過氧化氫與膜內催化劑接觸,加速Fenton反應,使降解效率大幅提升。
4 結語
Fenton工藝因其對環境友好、反應條件溫和、降解效率高等特點,可有效降解含酚廢水。相比于傳統Fenton反應,鐵基載體Fenton催化劑因其廣泛的pH值應用范圍、低污泥形成和可重復使用而顯示出巨大的應用潛力。本文綜述了鐵基載體Fenton催化劑研究進展,并詳細闡述了Fenton反應中的氧化機制。未來可通過開發原位產生H2O2的新型材料或可通過減少H2O2的自分解來提高H2O2利用率,從而大幅降低反應的運行成本,為Fenton反應的應用提供良好的開發思路。這些研究為高效處理含酚廢水奠定了重要的理論基礎,同時也為Fenton工藝的工業化應用提供了參考。

