那他霉素關鍵雜質的制備及其結構鑒定
李曉露?曹鵬然?高月麒?張雪霞?王寧 任風芝 于蘭
摘要:目的 分離純化那他霉素關鍵工藝雜質,并鑒定其結構,為那他霉素工藝和質量控制奠定基礎。方法 采用色譜純化技術,分離制備那他霉素粗品中的關鍵雜質,經LC-MS和NMR分析鑒定雜質結構。結果 建立了那他霉素工藝雜質的分離純化方法,制備得到了3個雜質化合物,并通過波譜分析鑒定了化合物結構,其中雜質1為那他霉素的C2位差向異構體;雜質2為那他霉素的C18位甲氧基取代產物;雜質3為那他霉素三元氧環開環后脫去羥基形成的雙鍵產物。結論 雜質化合物與那他霉素具有相似的骨架結構,均由那他霉素生產過程產生,為那他霉素原料藥的生產工藝開發和質量控制提供了技術參考。
關鍵詞:那他霉素;雜質;分離純化;結構鑒定
中圖分類號:R978.1文獻標志碼:A
Preparation and structure identification of the key impurities of natamycin
Li Xiaolu, Cao Pengran, Gao Yueqi, Zhang Xuexia,Wang Ning, Ren Fengzhi, and Yu Lan
(National Engineering Research Center of Microbial Medicine, Hebei Industry Microbial Metabolic Technology Innovation Centre, New Drug Research & Development Company of NCPC, Shijiazhuang 052165)
Abstract Objective To isolate and purify the key process impurities of natamycin, and to identify their structures, so as to lay a foundation for the process and quality control of natamycin. Methods The key impurities in the natamycin crude product were separated and prepared by chromatographic purification technology, and their structures were identified by LC-MS and NMR analysis. Results A method was established for separation and purification of the process impurities of natamycin. Three impurities were prepared, and their structures were identified by spectral analysis. Among them, Impurity 1 was the C2 epimer of natamycin; Impurity 2 was the C18 methoxy substituent of natamycin; Impurity 3 was the double bond product formed by removing the hydroxyl group after the ring opening of the epoxy three-membered of natamycin. Conclusion These impurity compounds have similar skeleton structure with natamycin, which are produced in the production process of natamycin. This study provides a technical reference for the production process development and quality control of natamycin API.
Key words Natamycin; Impurity; Separation and purification; Structural identification
那他霉素是一種多烯大環內酯類抗生素,不僅能有效抑制霉菌和酵母菌的生長,還能抑制真菌毒素的產生,在食品保鮮和抗真菌治療方面均有很好的應用[1-5]。那他霉素滴眼液由美國Alcon公司研發,1978年在美國上市,商品名為Natacyn?(那特真)。由于其顯著的抑菌和殺菌作用,那他霉素被專家推薦為一線眼部抗真菌藥物,其抗菌機制為同真菌細胞膜上的固醇相結合,轉化為多烯固醇復合物,通過改變細胞膜內外滲透壓導致細胞內容物外溢,造成真菌細胞死亡[6]。由于那他霉素良好的治療效果,它通常也是大多數真菌性角膜炎和角膜潰瘍患者的首選抗生素。
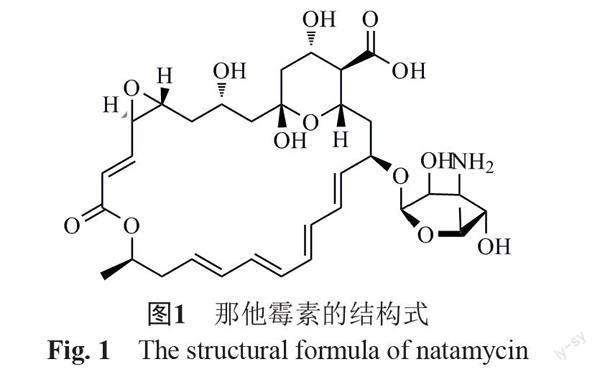
那他霉素來源于微生物發酵,雖然發酵過程主要產生那他霉素,但也會產生許多那他霉素的結構類似物和其他發酵副產物。那他霉素含有堿性和酸性基團(圖1),可溶于冰醋酸,微溶于甲醇,幾乎不溶于乙醇和水[7]。
雜質研究是藥物開發的重要組成部分,不僅可為原料藥及制劑的工藝質量控制提供依據,也有助于提高產品質量標準的可靠性。本文建立了那他霉素關鍵工藝雜質的分離提純方法,制備得到了雜質單體,并鑒定了雜質結構,這對那他霉素相關物質的控制和藥物安全性的保證具有重要意義。
1 儀器與試藥
LC-2030C 3D型高效液相色譜儀(日本島津公司);LC3000型制備液相色譜儀(北京創新通恒科技有限公司);TR026型酸度計(Mettler公司);Loborata 4000型旋轉蒸發器(Heidolph公司);AS-LGJ-18A型冷凍干燥機(鄭州安晟科學儀器有限公司);Xevo TQ質譜儀(Waters公司);Avance III 500型核磁共振波譜儀(Bruker公司)。
那他霉素粗品(色譜純度86.3%)本公司自制;UniSil C18購自蘇州納微科技股份有限公司;色譜純乙腈、甲醇、氘代二甲基亞砜購自美國Merck公司;其他試劑購自天津市科密歐化學試劑有限公司。
2 方法與結果
2.1 色譜條件
參照《中國藥典》2020年版方法[7],進行那他霉素HPLC檢測,色譜柱:Diamonsil C18 (4.6 mm×250 mm,
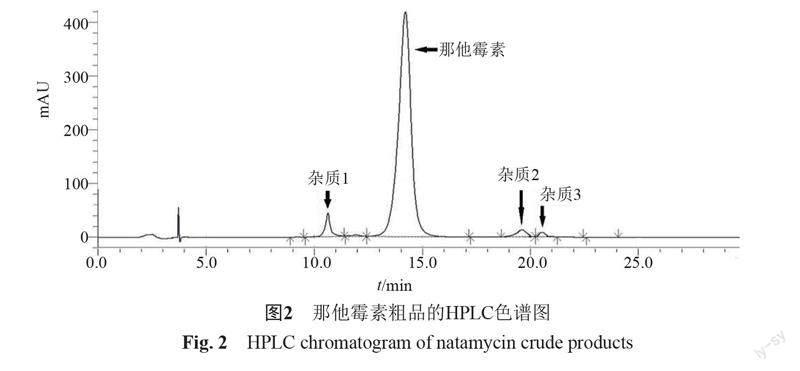
5 μm);以乙酸銨緩沖液-乙腈-四氫呋喃(76:24:0.5)為流動相;流速1.0 mL/min;檢測波長303 nm。那他霉素粗品的HPLC圖譜見圖2。
2.2 雜質富集
稱取那他霉素粗品15 g,加入120 mL甲醇,用2 mol/L鹽酸調pH至3.7~4.2使之溶解,溶解液經0.45 μm濾膜過濾,得到澄清上樣液。
2 L層析柱(反相硅膠C18填料,10 μm),流動相為37%乙腈-63%水(含0.2%乙酸銨),流速為70 mL/min,檢測波長303 nm,平衡1倍柱體積后上樣,采用同樣條件進行洗脫,根據在線圖譜分別進行主峰前雜質和主峰后雜質的收集,收集的洗脫液減壓濃縮后待再次純化。
2.3 雜質單體制備
2.3.1 主峰前雜質的分離制備
制備柱(Kromasil C18,100-10-C18,21.2 mm ×250 mm),流動相為27%乙腈-73%水(含0.2%乙酸銨),流速為14 mL/min,檢測波長303 nm。
平衡制備柱2倍柱體積后,取“2.2”項所得主峰前雜質進樣,根據在線檢測圖譜進行雜質餾分收集。合并HPLC純度大于95%的雜質1餾分,經減壓濃縮后凍干,得到雜質1: 60 mg,色譜純度98.2%。
2.3.2 主峰后雜質的分離制備
制備柱(Kromasil C18,100-10-C18,21.2 mm ×250 mm),流動相為32%乙腈-68%水(含0.2%乙酸銨),流速為14 mL/min,檢測波長303 nm。
平衡制備柱2倍柱體積后,取“2.2”項所得主峰后雜質進樣,根據在線檢測圖譜進行餾分收集。分別合并HPLC純度大于95%的雜質2餾分和雜質3餾分,經減壓濃縮后凍干,得到雜質2:32 mg,色譜純度95.3%;雜質3: 26 mg,色譜純度96.7%。
2.4 雜質結構鑒定
2.4.1 質譜分析
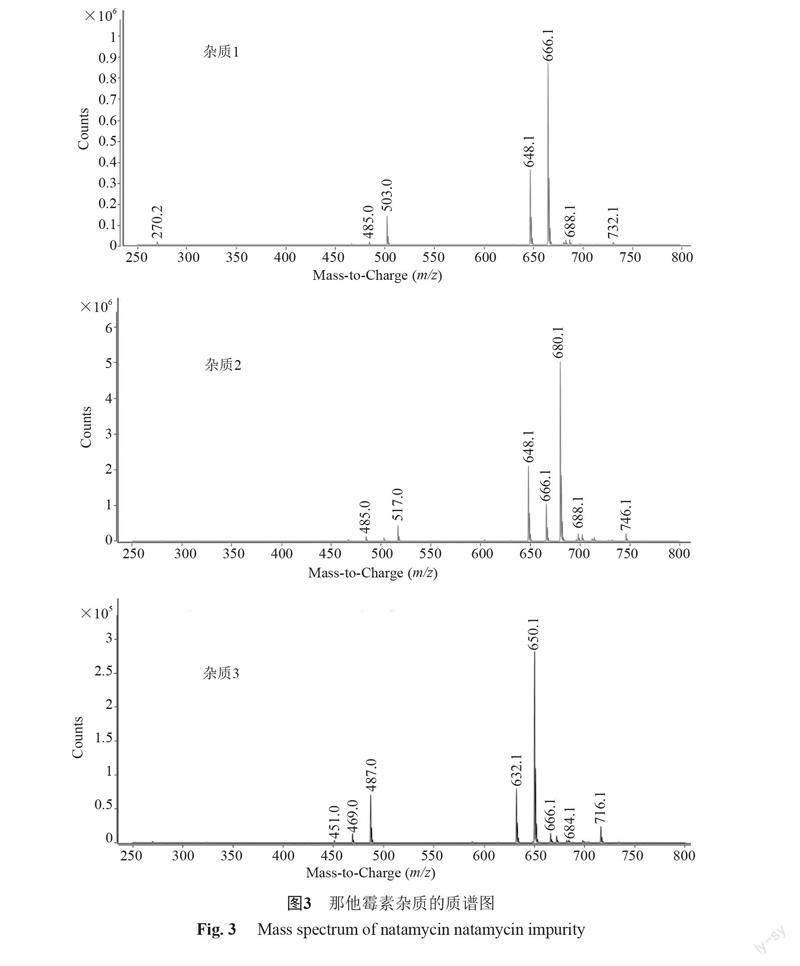
將那他霉素雜質化合物用甲醇溶解,進行質譜分析,其ESI(+)分析結果見圖3。
2.4.2 核磁共振分析
將那他霉素雜質化合物用氘代二甲基亞砜(DMSO-d6)溶解,進行核磁共振波譜分析,其1H NMR和13C NMR數據見表1~2。
2.4.3 結構解析[6]
雜質1:由ESI(+)離子峰圖譜可知,雜質1分子量為665,與那他霉素的分子量相同。由NMR數據可知雜質1與那他霉素C、H的個數相同,因此確定雜質1的分子式與那他霉素相同。比對雜質1與那他霉素的NMR數據,可以發現二者數據基本一致,僅C-3(ΔδC 6.6)化學位移有明顯差別,結合NOESY譜中1-Me與H-4有NOE相關,即雜質1的1-Me朝向與那他霉素相反,可以判斷雜質1為那他霉素的C2位差向異構體。
雜質2:由ESI(+)離子峰圖譜可知,雜質2分子量為679,比那他霉素的分子量多14。由核磁共振波譜數據可知,雜質2含有一個連氧甲基,該甲氧基δC 47.39 ppm,δH 2.97 ppm, s, 結合HMBC,可以發現該甲氧基的氫信號與C18相關。綜合分析HSQC、HMBC、H-H COSY及NOESY,對雜質2的碳信號和氫信號進行了歸屬,可以判斷雜質2為那他霉素的C18位甲氧基取代產物。
雜質3:由ESI(+)離子峰圖譜可知,雜質3分子量為649,比那他霉素的分子量少16。由NMR數據可知雜質3較那他霉素少一個O。比對雜質3與那他霉素的NMR數據,可以發現二者數據基本一致,差異主要為C-22和C-23的化學位移,根據存在差異的H譜裂分情況、C譜的化學位移變化、HSQC以及H-H COSY的相關,可以判斷雜質3是那他霉素三元氧環開環后脫去羥基形成的雙鍵產物。
雜質1~3的結構式見圖4。
3 討論
那他霉素是納塔爾鏈霉菌或褐黃孢鏈霉菌等微生物的次級代謝產物,從發酵液中提取純化后獲得,工藝雜質的研究及控制對于產品質量控制尤為重要。本研究應用制備色譜純化技術,探索了那他霉素粗品中關鍵雜質的分離提純方法,并通過質譜和核磁共振波譜等分析手段,確定了雜質的結構,其中雜質1為那他霉素的C2位差向異構體;雜質2為那他霉素的C18位甲氧基取代產物;雜質3為那他霉素三元氧環開環后脫去羥基形成的雙鍵產物。經檢索,3個雜質未見文獻報道,為首次分離鑒定。
在進行那他霉素雜質流程研究時發現,雜質1~3均為那他霉素發酵代謝產物。其中,雜質2和3在提取精制過程中,所占比例逐漸降低,成品中占比均小于0.1%,對產品質量影響較低。雜質1在粗提過程中占比有波動,堿溶酸沉步驟略有增長,且對pH比較敏感,精制結晶過程可有效去除,成品中未檢出。因此,在那他霉素發酵及提取過程中,避免高pH條件,可減少雜質1的生成。該研究為更加精準控制那他霉素產品質量和指導生產工藝優化提供了可靠的依據。
參 考 文 獻
Welscher Y M, Napel H H, Balague M M, et al. Natamycin blocks fungal growth by binding specififically to ergosterol without permeabilizing the membrane[J]. J Biol Chem, 2008, 283(10): 6393-6401.
Ture H, Eroglu E, Ozen B, et al. Effect of biopolymers containing natamycin against Aspergillus niger and Penicillium roquefortii on fresh kashar cheese[J]. Int J Food Sci Technol, 2011, 46(1): 154-160.
王冬梅, 陳光勝, 黃明漢. 那他霉素在真菌性角膜潰瘍愈合中的治療作用[J]. 國際眼科雜志, 2010, 10(4) :744-745.
忻丹麗, 沈降, 潘飛. 那他霉素聯合伊曲康唑治療真菌性角膜炎的療效分析[J]. 中國現代醫學雜志, 2017, 27(20): 73-75.
鄭振揚, 葉忠強. 那他霉素聯合伏立康唑治療真菌性角膜炎的療效分析[J]. 中國實用醫藥, 2020, 15(30):155-157.
梁景樂. 納他霉素高產菌株空間育種、工藝優化及工業放大研究[D].? 浙江大學博士學位論文, 2007.
國家藥典委員會. 中華人民共和國藥典[S]. (2020年版第二部). 北京: 中國醫藥科技出版社, 2020: 498-499.
收稿日期:2022-12-28
基金項目:河北省科技研發平臺建設專項(No. 22567651H)
作者簡介:李曉露,女,生于1974年,碩士,正高級工程師,主要從事微生物藥物分離純化,E-mail: luncpc@163.com
*通信作者, E-mail: yulan2680@163.com

