影響氯堿生產次氯酸鈉產品質量的因素分析
王 偉
(青海鹽湖海納化工有限公司,青海西寧 811600)
1 氯堿生產次氯酸鈉工藝簡介
氯堿生產次氯酸鈉工藝主要利用氯氣和15%~18%的氫氧化鈉反應生成氯化鈉、次氯酸鈉和水這一反應機理,把來自電解單元,氯氫單元,鹽酸合成單元純度小于98.5%的廢氯氣送往氯氣處理除害吸收系統, 氯氣依次進入除害塔和吸收塔與循環濃度為15%~18%的氫氧化鈉堿液逆流接觸,把有害的廢氯氣完全吸收,最后將非有害合格氣體通過尾氣風機抽負放空。循環液不斷的吸收氯氣最終產出合格次氯酸鈉。
反應機理:2NaOH+Cl2=NaCl+NaClO+H2O
2 影響次氯酸鈉質量的因素分析
2.1 除害系統循環液的溫度
堿循環液在吸收氯氣的過程中會釋放大量的熱,如果不加以控制溫度超過40 ℃會熱分解,有效氯迅速衰減,最終導致有效氯含量低,無法產出合格的次氯酸鈉,還會存在廢料處理難等問題。
次氯酸鈉熱分解反應機理:
2NaClO=2NaCl+O2↑
2NaClO+O2↑=NaClO3
溫度越高,次氯酸鈉分解越快,但常溫下也會緩慢分解。
當溫度過低的時候,循環液的粘度增加,流動性降低,不利于液相均勻分布,從而減小了堿循環液和氯氣的接觸面積,導致氣液兩相反應不充分。而且溫度過低循環液中的鹽的溶解度會降低會造成鹽析出結晶,堵塞管道造成系統無法正常運行。
由此可知,保證次氯酸鈉合格,就必須控制循環液的溫度。該溫度正常工藝指標為25~35 ℃。正常工況下循環液通過板式換熱器與循環水間接傳熱,為了控制循環液溫度指標,可以在循環液出換熱器管線安裝遠傳溫度儀表與換熱器循環水進口調節閥形成設定聯鎖保證溫度的穩定控制。
2.2 進除害系統的氯氣攜帶鐵離子等雜質成分
由鹽酸合成通往廢氯氣管道為碳鋼管道,廢氯氣在與碳鋼管道會發生反應生成鐵銹等物質,在異常工況下,大量廢氯氣會排入除害系統時會攜帶鐵銹進入除害系統,溶入循環液,生成氫氧化鐵微溶物質,生成物為紅褐色,會導致產出次氯酸鈉因鐵超標而變紅。
循環液與鐵離子反應機理:
FeCl3+3NaOH=Fe(OH)3↓(紅褐色)+3NaCl
鐵離子等金屬離子促使次氯酸鈉的分解,起到催化劑作用。所以在次氯酸鈉的生產,運輸和使用過程中避免接觸金屬容器,減少金屬雜質的引入。
故而,防止氯氣中攜帶雜質進入除害系統至關重要。為了解決這一難題,在鹽酸合成的廢氯氣管道進除害前加容積1 m3內置過濾桶的立式過濾器,有效將鐵銹等雜質過濾,定期清理過濾器底部沉積的雜質,保證長期高效運行。我廠未加過濾器前次氯酸鈉變紅率為20%,加裝過濾器后目前再未發生因次氯酸鈉變紅導致的質量事件。
2.3 除害吸收塔的運行狀況
除害吸收系統為兩塔串聯運行,均為填料塔,在長時間運行的過程中,頂部液體分布器可能變形損壞,液體不能均勻分布,存在局部偏流,與氯氣無法充分接觸,吸收不完全。
塔中填料會在異常工況下,溫度驟升導致填料塑性變形甚至過度膨脹破碎,溫度過低會導致循環液在填料層結晶,這些填料疏松狀態不夠,碎填料和鹽結晶堵塞,均會影響氯氣和循環液的充分接觸。
由此可見,生產次氯酸鈉過程中,保證填料塔的液體分布器和填料的完好和疏松狀態尤為重要,所以,建議將原有拉西環(材質CPVC)更換為鮑爾環(材質聚丙烯),鮑爾環是對拉西環的改進,有氣體通量大,傳質效率高的優點。材質方面CPVC脆硬容易破碎,聚丙烯更具有韌性不容易碎裂。同時定期進行檢查更換老化的填料和嚴格控制堿循環液的溫度也可以延長設備的使用壽命。
2.4 次氯酸鈉過飽和
當次氯酸鈉循環液已經飽和,假如繼續和通入的氯氣反應,待堿含量消耗完后,氯氣持續通入,由于沒有可供氯氣反應的堿,氯氣就會開始和水進行反應生成次氯酸和鹽酸,而鹽酸和次氯酸鈉反應會生成氯氣和氯化鈉,該反應為放熱反應,溫度升高,生成的氯氣也會繼續和水反應,會進一步加劇飽和次氯酸鈉分解,次氯酸鈉迅速分解釋放氯氣,最終有效氯幾乎為零,只剩下氯化鈉,氯酸鹽和水存在。
次氯酸鈉過飽和可能涉及反應機理:
NaClO+Cl2+H2O=NaCl+2HClO
NaClO+2HClO=NaClO3+2HCl
NaClO+2HClO=NaCl+H2O+Cl2↑
3NaClO=NaClO3+2NaCl
NaClO+2HCl=Cl2↑+NaCl+H2O
Cl2+H2O=HClO+HCl(可逆)
溶液的pH越小越容易分解,穩定性越差;當pH小于7時反應劇烈進行;pH值高有利于次氯酸鈉的穩定。
故而,要產出合格的次氯酸鈉,必須要準確的判斷飽和次鈉的切槽(飽和次氯酸鈉循環槽和新配的濃度為15%~18%的氫氧化鈉堿液備用槽之間的切換)時機。為解決這一問題,可以安裝ORP在線分析儀作為參考,實時監控,建議切槽時機ORP值為610 mV,以在線分析ORP值為參考指導切槽時機,以質檢實驗室分析檢驗報告單為標準。定期對ORP進行標定更換探頭,保證長期高效運行。

表1 ORP值對應的堿濃度和有效率濃度
2.5 飽和次氯酸鈉的取樣分析
影響次氯酸鈉測定結果主要有取樣過程,有效氯的測定等。
取樣過程:取樣前應充分的混合均勻,防止局部濃度偏高或者偏低。取樣時應置換干凈滯留介質后再取。待分析樣品在運輸和儲存的時候應有遮陽避光措施,避免高溫處存放,防止光照分解和熱分解導致有效氯衰減。
有效氯檢測過程:測定原理利用次氯酸鈉具有強氧化性,能將碘離子氧化為碘分子。游離出的碘在弱酸性溶液內用硫代硫酸鈉標準溶液滴定。次氯酸鈉的有效氯是指次氯酸鈉與酸作用后產生的氯含量,它表示氧化還原反應中的強度。目前常用間接碘量法測定。
反應機理:2H-+ClO-+2I-=I2+Cl-+H2O
檢測過程中如果溫差大,試劑污染,不密封碘逸出都會導致測定結果誤差大。所以,試樣應保持在室溫條件下測定,淀粉指示劑渾濁必須重新配置,測定時應迅速加入鹽酸,并立即加蓋密封,防止碘逸出。
2.6 次氯酸鈉溶液中的氫氧化鈉的含量
圖1為氯堿生產次氯酸鈉日常生產過程中合格次氯酸鈉在不同氫氧化鈉濃度下對應次氯酸鈉濃度的折線圖。
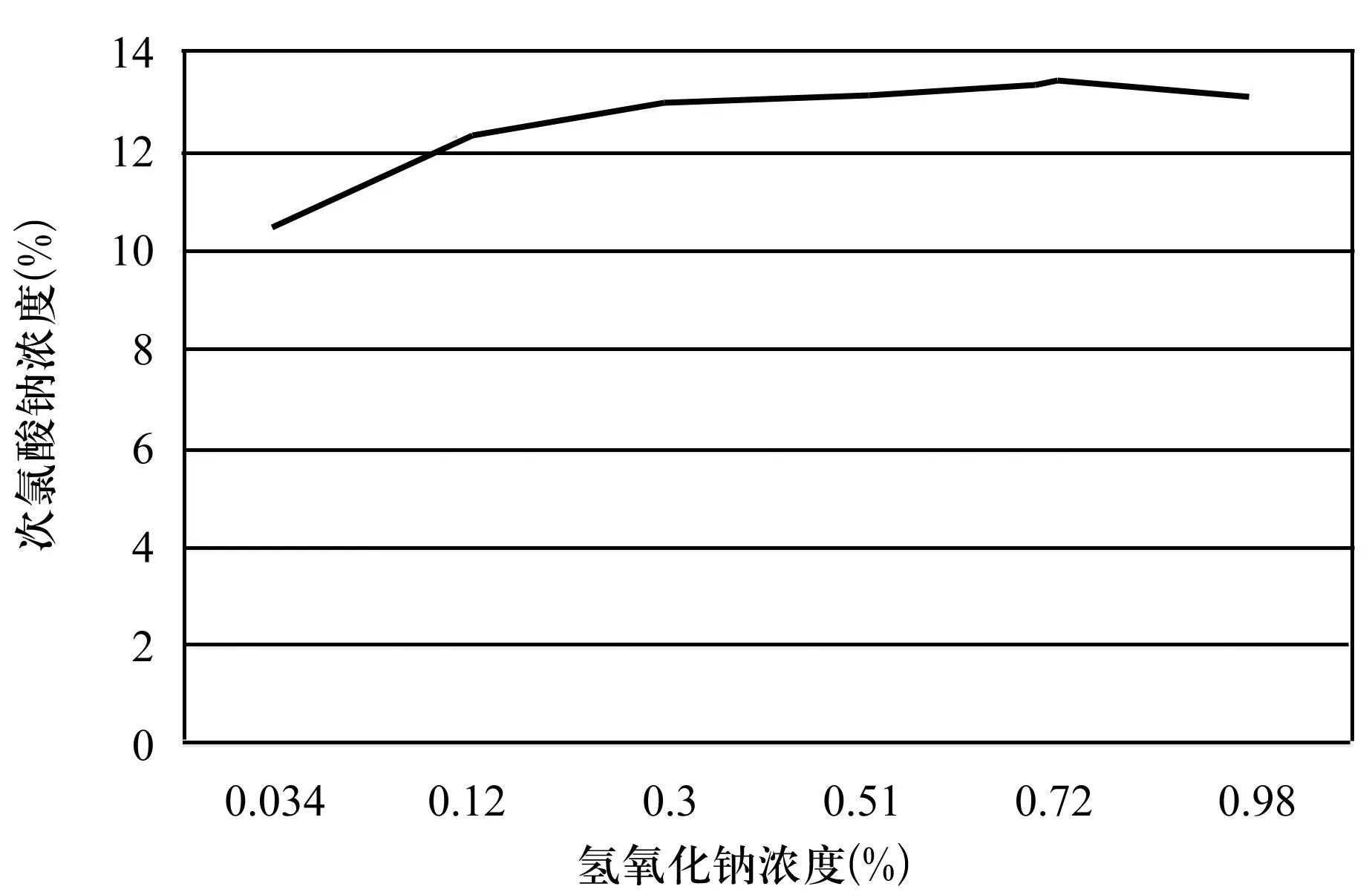
圖1 生產中次氯酸鈉濃度與氫氧化鈉濃度的關系
由圖1可見,當堿濃度小于0.3%,次氯酸鈉的濃度也明顯會隨著堿濃度的降低而降低。當堿濃度高于0.3%,次氯酸鈉濃度趨于穩定。同時可以看出當堿濃度約在0.72%,次氯酸鈉濃度最高。從化學機理上分析,當溶液為強堿性時,主要以NaClO存在,當溶液為弱堿性時,主要以NaClO存在,也會有少量HClO。當溶液為酸性時,主要以HClO形式存在,HClO容易分解或歧化成HCl,NaClO的水解反應:NaClO+H2O=NaOH+HClO是可逆過程,溶液中OH-濃度增大,有利于逆向反應。
由此說明,堿濃度的含量在保證合格(0.1%~1%)的基礎上,堿濃度適度提高,有助于提高次氯酸鈉的濃度,對次氯酸溶液有很好的穩定作用。同時在儲存過程中也能減緩次氯酸鈉的分解。
3 綜 述
由上可知,在氯堿生產次氯酸鈉過程中,不但要控制好循環液的溫度,準確判斷飽和次鈉的切槽時機,還要防止廢氯氣中攜帶的金屬離子等雜質,注意取樣的代表性和測定有效氯的過程注意事項,而且要更換設備內部填料來優化設備運行狀態和定期檢查除害系統中各個設備的運行情況。最后在保證合格的基礎上,適度提高堿濃度增加次氯酸鈉溶液的穩定性。

