以結(jié)構(gòu)化促進素養(yǎng)發(fā)展的教學(xué)研究
——以“常見酸的化學(xué)性質(zhì)”為例
王小文 陳 凱
一、教學(xué)主題內(nèi)容及教學(xué)現(xiàn)狀分析
(一)教學(xué)主題
“常見酸的化學(xué)性質(zhì)”選自滬教版九年級《化學(xué)》下冊第七章第二節(jié),內(nèi)容包括酸與活潑性金屬、金屬氧化物以及鹽的化學(xué)變化,酸與酸堿指示劑作用內(nèi)容位于第七章第一節(jié),酸堿中和內(nèi)容則置于后續(xù)章節(jié)中。這樣的編排有利于知識建構(gòu),對于循序漸進的教學(xué)具有重要意義。但是在實際教學(xué)過程中,解決綜合型生活議題往往需要應(yīng)用酸的各類性質(zhì),同時需要三重表征、論證推理來實現(xiàn)思維升華、觀念建構(gòu),這樣實際拓展的教學(xué)對于資優(yōu)生的培養(yǎng)具有重要意義。
(二)教學(xué)現(xiàn)狀
首先,培養(yǎng)資優(yōu)生的初中化學(xué)教學(xué)研究成果主要集中于初高中銜接的課題,如溶液[1-2]、蠟燭燃燒[3]。其次,通過文獻分析發(fā)現(xiàn),在教學(xué)中將酸的通性的微觀本質(zhì)分析與實驗探究過程割裂[4-5],并不能真正實現(xiàn)宏觀辨識與微觀探析的融合,導(dǎo)致學(xué)生無法針對一類物質(zhì)的化學(xué)性質(zhì)形成廣泛聯(lián)系、有序鏈接的結(jié)構(gòu)化認知體系,所以在紙筆測驗中面對實際問題解決時感到困難。
二、教學(xué)思想與創(chuàng)新點
《義務(wù)教育化學(xué)課程標準(2022 版)》提出基于核心素養(yǎng)的培養(yǎng)要求,加強課程內(nèi)容的內(nèi)在聯(lián)系,突出課程內(nèi)容結(jié)構(gòu)化。內(nèi)容結(jié)構(gòu)化主要有以下三種形式:基于知識關(guān)聯(lián)的結(jié)構(gòu)化、基于認識思路的結(jié)構(gòu)化和基于核心觀念的結(jié)構(gòu)化[6]。
(一)基于知識關(guān)聯(lián)的教學(xué)內(nèi)容結(jié)構(gòu)化
學(xué)生在已有的學(xué)習(xí)經(jīng)歷中對酸的化學(xué)性質(zhì)的認識比較瑣碎,所以將酸的化學(xué)性質(zhì)整合在真實情境中,外顯宏微符相結(jié)合的思維方式,滲透物質(zhì)的組成決定性質(zhì),性質(zhì)決定用途的認識思路,促進知識結(jié)構(gòu)化。知識關(guān)聯(lián)的結(jié)構(gòu)化需要基于已有知識儲備進行建構(gòu),實現(xiàn)事實性知識的結(jié)構(gòu)化建構(gòu),如圖1所示。
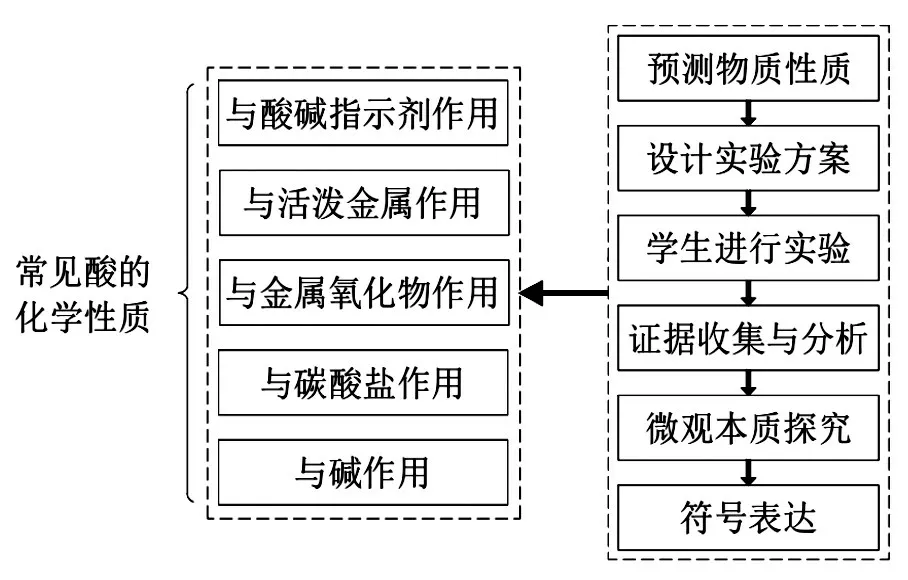
圖1 內(nèi)容結(jié)構(gòu)化建構(gòu)
(二)基于認識思路的教學(xué)內(nèi)容結(jié)構(gòu)化
認識思路的結(jié)構(gòu)化是從學(xué)科本質(zhì)和規(guī)律對物質(zhì)及其變化的認識過程的一種概括,如物質(zhì)“結(jié)構(gòu)、性質(zhì)、應(yīng)用”的關(guān)系[7]。以常見酸的化學(xué)性質(zhì)為例,需要挖掘具體知識背后的本質(zhì)及規(guī)律,凝練出初中化學(xué)認識一類物質(zhì)的一般思路,如圖2所示。
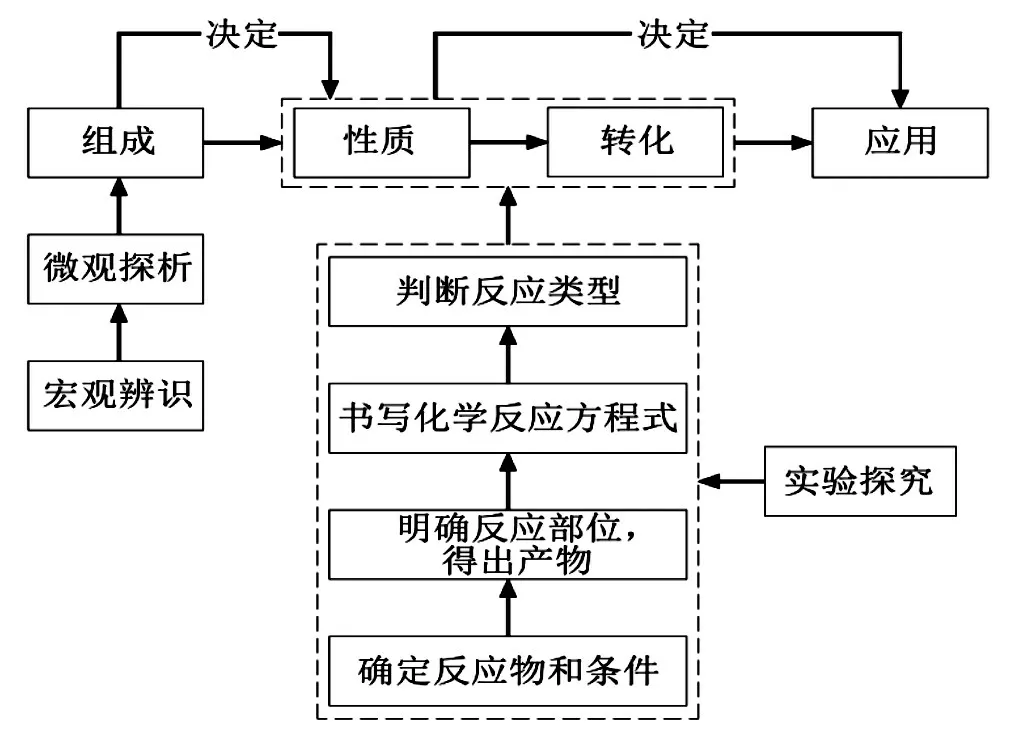
圖2 認識化合物的一般思路
在認識具體物質(zhì)過程中融入從科學(xué)風(fēng)險視角的分析,明確應(yīng)對風(fēng)險議題的決策手段,也是兼顧知識與科學(xué)態(tài)度的一種認識思路。
(三)基于核心觀念的結(jié)構(gòu)化
學(xué)科觀念建構(gòu)的教學(xué)有利于學(xué)生洞悉化學(xué)學(xué)科的本質(zhì)屬性和內(nèi)在規(guī)律,在此基礎(chǔ)上能夠更好地將原來孤立零散的知識聯(lián)系起來,形成有意義的整體。觀念是深藏在知識背后的一種思想,觀念建構(gòu)不能一蹴而就[8],而需要潛移默化、廣泛聯(lián)系、層層推進。通過對酸的各種性質(zhì)、反應(yīng)類型和產(chǎn)物類別的分析,促進變化觀的建構(gòu);以繪制微粒分布圖的方式加深對微粒觀的理解。這些新知建構(gòu)均要應(yīng)用學(xué)生較熟悉的微粒、元素、化學(xué)方程式、質(zhì)量守恒定律等先修知識。學(xué)生在已有知識與問題解決之間進行關(guān)聯(lián),最終實現(xiàn)觀念結(jié)構(gòu)化[8]。
三、教學(xué)目標
1.在實驗探究中了解酸的化學(xué)性質(zhì),從微觀視角分析酸的通性的本質(zhì)原因,逐步建構(gòu)以酸為中心議題的結(jié)構(gòu)化知識體系。
2.能運用研究物質(zhì)性質(zhì)的一般思路與方法,從物質(zhì)類別視角,初步預(yù)測常見酸的性質(zhì),設(shè)計實驗方案,分析、推理、解釋有關(guān)實驗現(xiàn)象。
3.在與酸有關(guān)的科學(xué)風(fēng)險問題分析過程中形成基于風(fēng)險進行決策的科學(xué)思路,提升風(fēng)險決策能力,樹立合理使用日化用品和解決生活問題的科學(xué)態(tài)度。
四、教學(xué)流程
本節(jié)課教學(xué)流程如圖3所示。
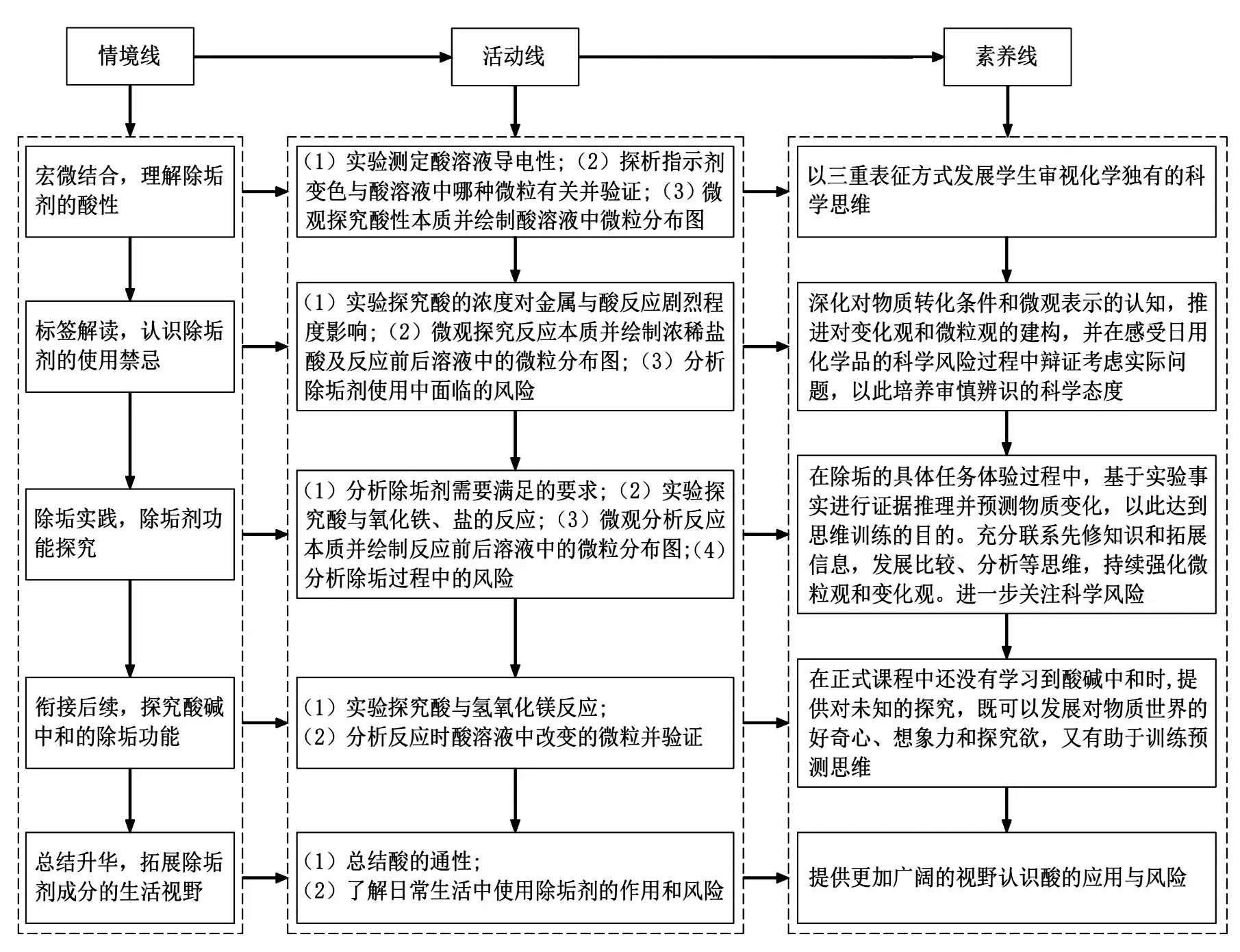
圖3 教學(xué)流程圖
五、教學(xué)實錄
(一)宏微結(jié)合,理解除垢劑的酸性
[師]家中水垢、銹跡等給人帶來煩惱,今天就讓我們一起探究除去這些污垢的方法,讓家變得更干凈衛(wèi)生。
[展示]除垢劑標簽,如圖4所示。

圖4 除垢劑的標簽
[師]從除銹劑標簽可知其呈酸性。如何設(shè)計簡單方案來檢驗這瓶“水垢清潔劑”的酸堿性?
[演示實驗]將紫色石蕊試劑滴入無色除垢劑中。
[師]商場里賣的除垢劑一般呈藍色,需要用吸附法除色或采用pH 計來避免原有顏色對現(xiàn)象觀察產(chǎn)生影響。
[師]紫色石蕊變紅與酸溶液中哪一種離子有關(guān)?請說出理由。
[生]從溶質(zhì)的元素組成看,都有氫元素,所以推測紫色石蕊變紅與H+有關(guān)。
[師]現(xiàn)提供兩個硫酸分子、兩個氯化氫分子,請同學(xué)們分別繪制出稀鹽酸和稀硫酸中離子分布圖。繪圖時注意溶液中陰陽離子電荷總數(shù)相同。
[學(xué)生繪圖]微粒分布示意圖如圖5所示。

圖5 學(xué)生繪制酸分子產(chǎn)生的離子示意圖
[師]溶質(zhì)是分子,溶解之后產(chǎn)生了離子,是不是與溶液中水分子作用有關(guān)呢?完善酸溶液中微粒分布圖。
[學(xué)生繪圖]鹽酸和硫酸中的微粒分布示意圖,如圖6所示。

圖6 學(xué)生繪制的酸溶液中微粒分布示意圖
教師點評:在真實的除垢情境中,通過導(dǎo)電性測定實驗、微粒分布示意圖繪制等活動培養(yǎng)宏微結(jié)合思維,以此幫助理解酸溶液的化學(xué)性質(zhì)與H+有關(guān),為后面進一步理解酸的通性的本質(zhì)奠定基礎(chǔ)。
(二)標簽解讀,認識除垢劑的使用禁忌
[師]使用任何日化用品前,都需要仔細研讀標簽上的注意事項,明確化學(xué)品的使用禁忌。請仔細觀察除銹劑和水垢清潔劑的標簽,你有哪些發(fā)現(xiàn)?金屬和酸反應(yīng)的劇烈程度可能受哪些外界因素影響?利用控制變量法,設(shè)計實驗驗證酸的濃度對反應(yīng)劇烈程度的影響。
[學(xué)生實驗]利用如圖7所示裝置進行分組實驗,觀察現(xiàn)象。
[師]反應(yīng)物的濃度會影響反應(yīng)劇烈程度,適當(dāng)?shù)靥岣啕}酸的濃度可以提高不銹鋼表面的光潔度,但是濃度過高則會降低除銹的效果[9]。鹽酸濃度高,揮發(fā)性強,這會為除垢帶來一定的風(fēng)險。
[師]由金屬離子和酸根離子組成的物質(zhì)是鹽。在實驗室中,利用活潑金屬與酸反應(yīng)生成鹽和氫氣的性質(zhì)來制取氫氣。宏觀現(xiàn)象源于微觀本質(zhì),以鐵和稀硫酸反應(yīng)為例,結(jié)合所給資料,分析反應(yīng)中哪些微粒將發(fā)生改變?請設(shè)計實驗方案并驗證。
[資料]10%硫酸溶液的pH 約為0,10%硫酸亞鐵溶液的pH 約為3.7。SO42-與Ba2+結(jié)合會產(chǎn)生不溶于水和酸的白色沉淀BaSO4。
[學(xué)生分析]根據(jù)溶液顏色的改變,判斷鐵單質(zhì)變成了Fe2+,并猜測酸溶液中改變的是H+。驗證方法為:將鐵加入到少量的硫酸溶液中,測反應(yīng)前后溶液的酸堿性變化。
[學(xué)生實驗]用pH 計測量反應(yīng)前后溶液的pH 值。向反應(yīng)后溶液中滴加氯化鋇溶液,觀察實驗現(xiàn)象,分析得出結(jié)論。
[師]由宏觀現(xiàn)象可知,酸能與活潑金屬反應(yīng)。從微觀視角看,酸溶液中改變的是H+。基于以上分析,繪制出該反應(yīng)前后溶液中的微粒分布示意圖。
[學(xué)生繪圖]學(xué)生繪制的反應(yīng)前后溶液中的微粒分布示意圖,如圖8所示。
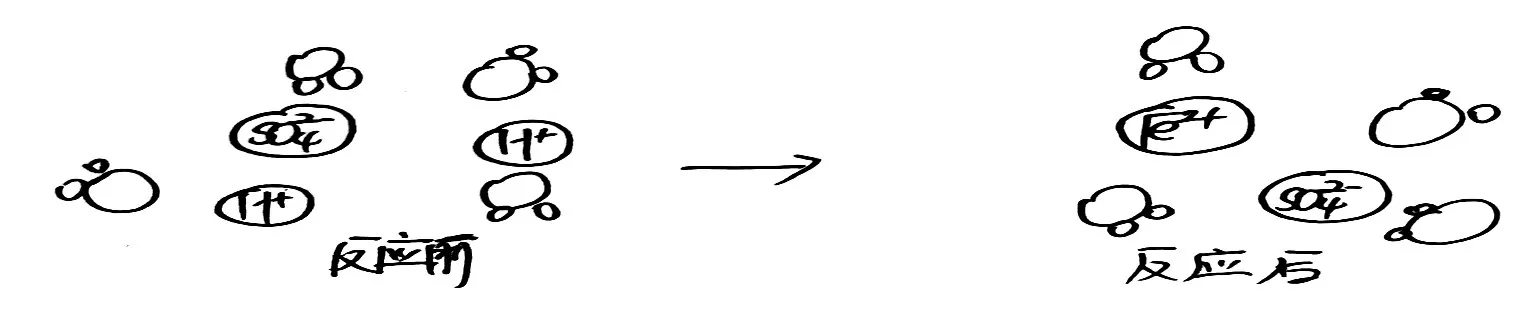
圖8 學(xué)生繪制的硫酸與鐵反應(yīng)前后溶液中的微粒分布示意圖
教師點評:解讀除垢劑標簽,既可以滲透科學(xué)風(fēng)險意識,還能夠揭示酸與活潑金屬反應(yīng)的性質(zhì),以此設(shè)計實驗來探究濃度對反應(yīng)速率的影響,初步了解調(diào)控化學(xué)反應(yīng)的方法。通過實驗探究、分析推理進一步確定酸溶液具有共同化學(xué)性質(zhì)的原因。在方程式書寫、物質(zhì)類別判斷和微觀探析中逐步構(gòu)建結(jié)構(gòu)化認知。
(三)除垢實踐,除垢劑功能探究
[師]鐵銹(主要成分是氧化鐵)質(zhì)地疏松,易吸收水分和空氣,導(dǎo)致鐵生銹越來越嚴重,所以要及時去除。除垢劑需要具備什么性質(zhì)呢?
[學(xué)生討論](1)除垢劑能和氧化鐵反應(yīng)且不產(chǎn)生新的難溶性沉淀。(2)加入的除垢劑要足量。(3)除垢劑和氧化鐵反應(yīng)的產(chǎn)物不能污染環(huán)境。
[師]使用除銹劑時存在潛在的危險,我們需要有防范意識。利用金屬氧化物和酸反應(yīng)生成鹽和水的性質(zhì)除去銹垢。以硫酸和氧化鐵反應(yīng)為例,繪制出該反應(yīng)前后溶液中的微粒分布示意圖。
[學(xué)生繪圖]學(xué)生繪制反應(yīng)前后溶液中的微粒分布示意圖,如圖9所示。
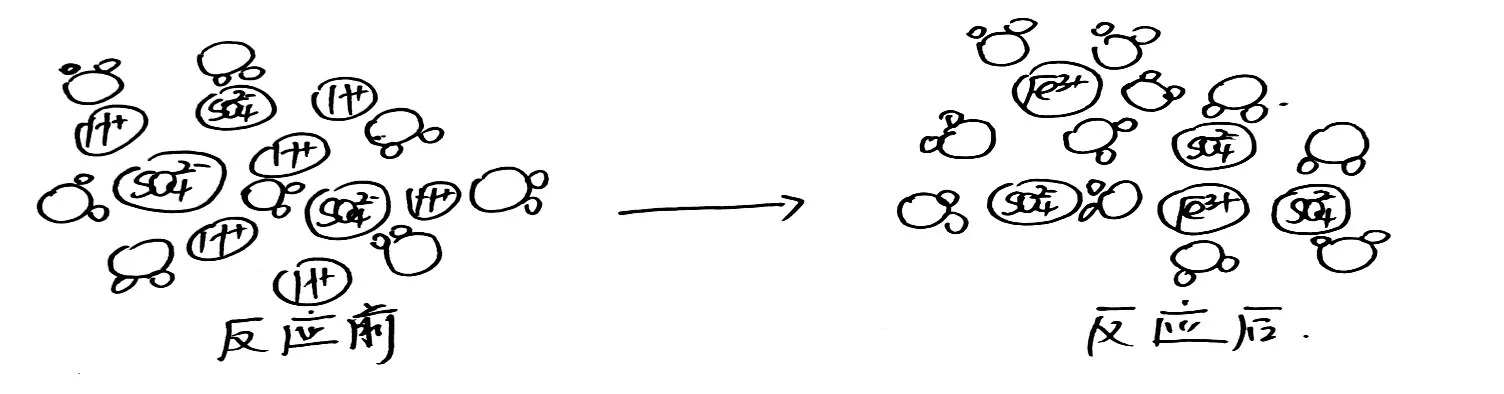
圖9 學(xué)生個案繪制的硫酸與氧化鐵反應(yīng)前后微粒分布示意圖
[師]在第二章學(xué)習(xí)硬水軟化時,我們知道水中可溶性鈣鎂化合物是導(dǎo)致水硬度變化的主要物質(zhì),而煮沸軟化法恰是將這些鈣鎂化合物轉(zhuǎn)變?yōu)殡y溶物質(zhì)。結(jié)合已學(xué)知識,難溶性含鈣化合物最有可能是什么?如何證明這一猜想?
[學(xué)生猜測]碳酸鈣,用鹽酸與之反應(yīng),產(chǎn)生的氣體能使澄清石灰水變渾濁。
[師]以碳酸鈣與稀鹽酸反應(yīng)為例,結(jié)合所給資料,你認為酸溶液中改變的是哪一種離子?如何證明?如何檢驗氯離子是否改變?畫出反應(yīng)前后溶液中的微粒分布示意圖,分析變化異同。
[資料]硝酸銀可用于檢驗鹽酸或在溶液中能產(chǎn)生Cl-的化合物,生成AgCl 白色沉淀。
[學(xué)生繪圖]學(xué)生繪制的CaCO3與鹽酸反應(yīng)前后溶液中的微粒分布示意圖,如圖10所示。
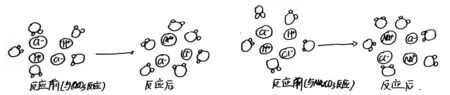
圖10 學(xué)生個案繪制的反應(yīng)前后溶液中微粒分布示意圖
教師點評:將酸與某一種物質(zhì)的反應(yīng)拓展到一類物質(zhì)的反應(yīng)。
(四)銜接后續(xù),探究酸堿中和的除垢功能
[師]水垢的另一種主要成分是氫氧化鎂,運用除垢的一般思路,氫氧化鎂也應(yīng)該和酸反應(yīng)。
[演示實驗]氫氧化鎂分別和稀鹽酸、稀硫酸反應(yīng)。
[學(xué)生觀察]白色固體消失了。
[師]鹽酸、硫酸都能溶解水垢,也是氫離子發(fā)揮了作用。
教師點評:水垢成分復(fù)雜,酸能與金屬、鹽、堿等發(fā)生反應(yīng),將研究物質(zhì)性質(zhì)的思路與方法進行遷移,為后續(xù)探究中和反應(yīng)做鋪墊。
(五)總結(jié)升華,拓展除垢劑成分的生活視野
[師]物質(zhì)的組成決定性質(zhì)。由于酸溶液中都含有氫離子,所以表現(xiàn)出相似的化學(xué)性質(zhì)。但是陰離子不同,不同酸的性質(zhì)也有差異性。請從物質(zhì)類別角度總結(jié)鹽酸、硫酸等酸性物質(zhì)化學(xué)性質(zhì)上的通性,并預(yù)測醋酸的化學(xué)性質(zhì)與用途。
[生]總結(jié)酸的通性,并預(yù)測醋酸也具有酸的通性,可用于除去水垢。
[師]實踐證明用醋酸除垢的時間較長,你們認為是何緣故?
[生]生活中使用的醋酸濃度低、酸性弱。
生活中常見的酸溶液的pH 值,如圖11所示。

圖11 生活中常見酸溶液的pH
[師]酸性強弱與酸的濃度有一定的關(guān)系。酸的濃度對物質(zhì)的性質(zhì)和用途有重要影響,如胃液中的鹽酸,合適的濃度可以促進食物消化,但是濃度過大,身體也會不舒服。生活中一般用檸檬酸作為水垢的清洗劑,檸檬酸做除垢劑的優(yōu)點有哪些?
[學(xué)生討論]檸檬酸酸性較強,除垢速度快;食品級,無害環(huán)保;呈現(xiàn)固態(tài),便于儲存和運輸?shù)取?/p>
[師]酸的化學(xué)性質(zhì)在一定程度上體現(xiàn)了酸的腐蝕性,但是對人類而言并非只有壞處。生活中要能從化學(xué)視角辯證地認識物質(zhì)性質(zhì),要有防范風(fēng)險意識以及規(guī)避風(fēng)險能力。
教師點評:觀念顯性化有助于加深對知識的結(jié)構(gòu)化認知。聯(lián)系生活實際并不只是“知道”,還在于實踐和比較。
六、教學(xué)反思
學(xué)生在課后交流時提及最大收獲就是可以類比酸化學(xué)性質(zhì)的研究思路與方法認識其他類物質(zhì)。一方面,從不同途徑體驗化學(xué)變化的證據(jù),認識調(diào)控化學(xué)反應(yīng)快慢的方法;另一方面,從宏微結(jié)合視角認識物質(zhì)性質(zhì)背后的本質(zhì),在結(jié)構(gòu)、性質(zhì)和用途聯(lián)系的整體架構(gòu)中觸類旁通,解決實際問題。
學(xué)生拓展了認識知識的視角。(1)教科書外知識的適當(dāng)補充,并沒有增加學(xué)生的學(xué)習(xí)負擔(dān),反而有利于對概念的深入理解;(2)課堂上做的實驗都短小精練,非常適合獨立操作;(3)科學(xué)風(fēng)險視角的融入,在知識學(xué)習(xí)之外,增加了對社會和生活的思考。教師在教學(xué)過程中感受到了加強科學(xué)風(fēng)險教育的意義,在本節(jié)課中學(xué)生不僅要面對常規(guī)化學(xué)實驗藥品的危險性和操作不當(dāng)可能帶來的風(fēng)險,還要關(guān)注日化用品、化工生產(chǎn)中的安全隱患[10],在潛移默化中超越知識,逐步構(gòu)建發(fā)現(xiàn)風(fēng)險、認識風(fēng)險、分析風(fēng)險、理解風(fēng)險以及規(guī)避潛在風(fēng)險的結(jié)構(gòu)化認識體系[11]。此外,本課多處拓展的信息、數(shù)據(jù)、知識旨在帶領(lǐng)學(xué)生感受科學(xué)知識的不確定性和復(fù)雜性,這有助于補充完善學(xué)科知識結(jié)構(gòu),對資優(yōu)生發(fā)展意義重大。但是本節(jié)課課堂內(nèi)容容量大,需要學(xué)生對資料進行分析理解,部分學(xué)生有跟不上的現(xiàn)象,需要在后續(xù)教學(xué)中反思改進。
- 中小學(xué)教學(xué)研究的其它文章
- 語篇連貫視域下的邏輯思維品質(zhì)培養(yǎng)路徑探析
——以英語高考題型選句填空教學(xué)為例 - 基于項目式學(xué)習(xí)的小學(xué)語文課本劇“三度”策略探究
——以統(tǒng)編教材六年級上冊小說單元的教學(xué)為例 - 小學(xué)語文教學(xué)滲透勞動教育的策略探究
- 酸、堿、鹽單元復(fù)習(xí)的項目式教學(xué)實錄
——以“健康保‘胃’戰(zhàn)”為例 - 小學(xué)數(shù)學(xué)教學(xué)“比較”運用研究
- 立足化學(xué)史實 聚焦模型建構(gòu)
——以人教版《物質(zhì)結(jié)構(gòu)與性質(zhì)》中“共價鍵”為例

