姜黃素對玉米赤霉烯酮致小鼠肝臟氧化應激和NLRP3炎癥小體活化的影響
宋 超,付長其,皇甫和平,張愛國,王亞鍇,石冬梅,王俊東,彭 巍
(1.河南牧業經濟學院 動物醫藥學院,河南 鄭州 450000;2.青海省畜牧獸醫科學院,青海 西寧 810000)
玉米赤霉烯酮(zearalenone,ZEA)是一種由鐮刀菌屬真菌產生的次級代謝產物,廣泛存在于霉變的谷類作物(如玉米、小麥、大麥、燕麥等)中,其理化性質穩定,在自然條件下降解緩慢,給畜禽養殖業造成嚴重經濟損失[1]。ZEA具有生殖毒性、腎毒性、免疫毒性等[2]。肝臟作為機體內重要的代謝和解毒器官,也是ZEA作用的主要靶器官之一[3]。ZEA誘導的活性氧(ROS)過量產生會導致肝臟氧化應激的發生,是ZEA造成肝毒性的重要原因[4]。此外,NOD樣受體熱蛋白結構域相關蛋白3(NLRP3)炎癥小體的活化也在ZEA引起的機體損傷中發揮關鍵作用[5]。因此,尋找安全有效的天然抗氧化與抗炎物質是有效預防或緩解ZEA肝毒性的一個重要方向。
姜黃素提取自姜科植物姜黃的根莖,是一種二酮類化合物,具有抗炎、抗氧化、免疫調節等藥理作用[6]。近年來的研究指出,姜黃素在治療肝損傷中有良好的應用前景[7]。研究表明姜黃素在體外可有效緩解ZEA誘導的PK-15細胞(豬腎上皮細胞)凋亡[8]。然而,目前有關姜黃素對ZEA致肝損傷保護作用的研究較少。因此,本研究以小鼠為對象,探討姜黃素對ZEA誘導小鼠肝臟氧化應激和NLRP3炎癥小體活化的改善作用,為ZEA中毒的預防及治療提供理論依據與新的治療策略。
1 材料與方法
1.1 實驗動物雄性昆明小鼠(體質量為20~25 g)購自于鄭州大學實驗動物中心,飼養于清潔環境中(室溫(22±2)℃,相對濕度50%~60%)。試驗期間自由采食與飲水。所有動物實驗經過河南牧業經濟學院動物倫理委員會批準。
1.2 主要試劑、抗體及儀器ZEA購自青島普瑞邦生物公司;姜黃素購自北京索萊寶科技有限公司;天冬氨酸氨基轉移酶(AST)、丙氨酸氨基轉移酶(ALT)、丙二醛(MDA)、超氧化物歧化酶(SOD)、過氧化氫酶(CAT)、谷胱甘肽過氧化物酶(GSH-Px)等試劑盒購自南京建成生物工程研究所;蘇木精-伊紅(HE)染液、二氫乙啶(DHE)染液以及透射電鏡固定液等購自武漢賽維爾生物科技有限公司;NLRP3抗體、羊抗兔Fluor488標記熒光二抗、羊抗兔Fluor594標記熒光二抗均購自于江蘇親科生物有限公司;胱天蛋白酶-1(Caspase-1)p20抗體購自北京博奧森生物技術有限公司;反轉錄和熒光定量PCR試劑盒購自北京全式金生物技術股份有限公司;小鼠白細胞介素-1β(IL-1β)ELISA試劑盒購自美國R&D Systems。紫外可見分光光度計(UA-1800,上海翺藝儀器有限公司);透射電子顯微鏡(HT7800,日本Hitachi);酶標儀(Epoch,美國BioTek);熒光定量PCR儀(ABI7500,美國Applied Biosystems);數字切片掃描系統(PANNORAMIC,匈牙利3DHISTECH)。
1.3 分組與干預60只小鼠隨機均分為4組:對照組,姜黃素組,ZEA組,姜黃素+ZEA組,試驗期4周。整個試驗期間,姜黃素組每日灌胃給予150 mg/kg的姜黃素,對照組則給予等體積生理鹽水,1次/d;ZEA組第1周灌胃生理鹽水,從第2周開始每日灌胃40 mg/kg的ZEA,1次/d,持續3周;姜黃素+ZEA組第1周灌胃150 mg/kg姜黃素,后3周每日ZEA灌胃4 h后再次灌胃姜黃素。
1.4 血清ALT和AST水平的測定末次干預后12 h,通過眼球采血來獲取血液樣本,靜置2 h后于3 000 r/min離心15 min收集血清。嚴格按照說明書進行操作,測定D510 nm值,根據標準曲線計算各組血清中ALT和AST水平。
1.5 HE染色4%的多聚甲醛固定肝臟,經過脫水、透明、石蠟包埋。蠟塊切片后進行蘇木精-伊紅(HE)染色觀察肝組織病理變化。
1.6 透射電鏡觀察肝臟超微結構取出的肝組織迅速投入含電鏡固定液的培養皿中,修剪成體積不超過1 mm3的組織塊,后繼續用新鮮的電鏡固定液固定。1%的四氧化鋨固定后用梯度酒精脫水、環氧樹脂滲透、包埋、超薄切片鈾鉛雙染,最后在透射電鏡下觀察拍照。
1.7 DHE染色取新鮮的肝臟組織放入冰凍切片機來制作冰凍切片,加入DHE染液在37℃避光條件下孵育30 min,PBS(1×)洗滌3次后加入DAPI封片液,采用切片數字掃描系統掃描圖片。Image J軟件軟件分析紅色熒光強度。
1.8 氧化應激指標的測定肝臟組織按照1∶9的質量體積比加入生理鹽水,在低溫條件下進行研磨。3 000 r/min離心10 min后收集上清。BCA法測定各組樣品的蛋白濃度。嚴格按照試劑和說明書測定GSH-Px、CAT、SOD活性和MDA含量的變化。
1.9 組織免疫熒光檢測肝臟NLRP3和Caspase-1 p20蛋白表達石蠟切片脫蠟水化,枸櫞酸鈉緩沖液抗原修復,BSA室溫封閉后滴加一抗(NLRP3,1∶100;Caspase-1 p20,1∶100),4℃過夜孵育;PBS洗滌后滴加相應熒光二抗(1∶200),室溫避光孵育1 h;DAPI染液避光染核;滴加抗熒光猝滅劑,封片后進行圖片掃描。高倍視野下(400×)對熒光強度進行分析。
1.10 熒光定量PCR檢測IL-1β mRNA表達Trizol法提取肝臟組織的總RNA,按逆轉錄試劑盒說明書配制逆轉錄體系來合成cDNA,按照說明書來配制熒光定量PCR反應體系,在ABI 7100 PCR儀器上進行反應。引物序列(上海生工合成)為:IL-1β (Forward) 5′-GCAACTGTTCCTGAACTCAAC-T-3′,IL-1β (Reverse) 5′-ATCTTTTGGGGTCCGTCAACT-3′;GAPDH (Forward) 5′- AGGTCGGTGTGAACGGATTTG-3′,GAPDH (Reverse) 5′- TGTAGACCATGTAGTTGAGGTCA -3′。應用2-△△Ct法對數據進行分析。
1.11 ELISA檢測肝臟IL-1β水平按照試劑盒說明嚴格進行操作,測定D450 nm值,根據標準曲線計算肝臟組織中IL-1β水平。
2 結果
2.1 姜黃素對各組小鼠血清中ALT與AST活性的影響如表1,姜黃素組小鼠血清AST和ALT活性與對照組比較無顯著差異(P>0.05);ZEA組小鼠血清中肝臟功能指標AST與ALT活性較對照組均顯著升高(P<0.01);姜黃素+ZEA組小鼠血清中的ALT和AST活性與ZEA組相比降低,有顯著差異(P<0.01)。
表1 姜黃素對ZEA處理小鼠血清中AST和ALT活性的影響 U/L
2.2 姜黃素對各組小鼠肝臟病理變化的影響對照組和姜黃素組小鼠肝臟組織輪廓清晰,結構完整,胞核清晰且肝細胞的大小均一;ZEA組小鼠肝臟可以見到多數肝細胞出現水腫,結構破壞,胞質疏松淡染;ZEA引起的這些肝臟病理變化在姜黃素干預后明顯緩解(圖1)。
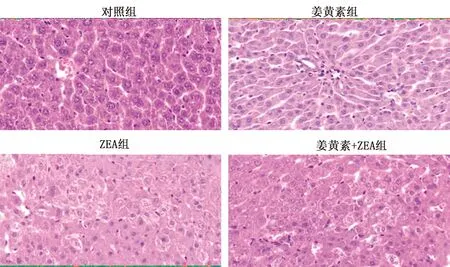
圖1 姜黃素干預緩解了ZEA誘導的肝臟損傷
2.3 姜黃素對各組小鼠肝臟組織超微結構的影響對照組和姜黃素組小鼠肝臟細胞線粒體結構完整,線粒體嵴清晰;ZEA組小鼠肝臟細胞中有較多的線粒體表現出線粒體嵴減少、消失以及空泡化;姜黃素+ZEA組細胞中有受損線粒體的數量減少(圖2)。
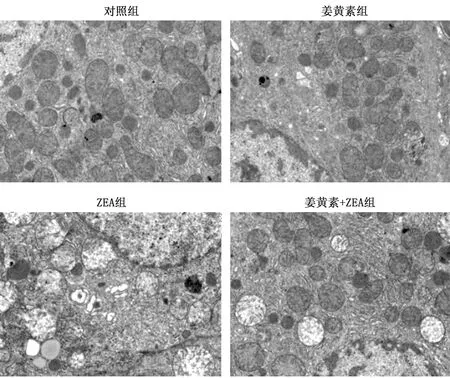
圖2 姜黃素對ZEA處理小鼠肝臟超微結構的影響(6 000×)
2.4 姜黃素對各組小鼠肝臟ROS水平的影響DHE染色結果表明(圖3),姜黃素組小鼠肝臟ROS較對照組沒有顯著差異(P>0.05);ZEA組小鼠肝臟ROS水平與對照組和姜黃素組比較顯著升高(P<0.01);姜黃素+ZEA組較ZEA組ROS水平顯著減少(P<0.01)。
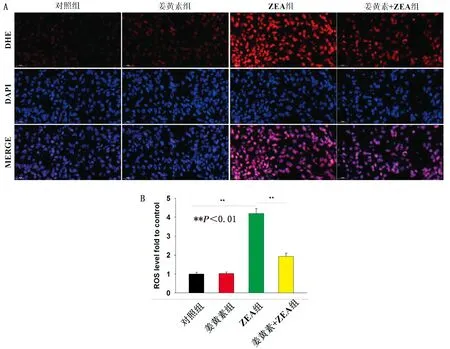
圖3 DHE染色結果(A)與小鼠肝臟ROS水平(B)(標尺:20 μm)
2.5 姜黃素對各組小鼠肝臟GSH-Px、CAT、SOD和MDA變化的影響與對照組相比,ZEA組小鼠肝臟中的SOD、CAT和GSH-Px活性降低(P<0.01),而MDA含量則升高(P<0.01);姜黃素+ZEA組小鼠肝臟中的SOD、CAT和GSH-Px活性較ZEA組升高,MDA含量降低,差異顯著(P<0.01)。結果見表2。
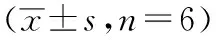
表2 姜黃素對ZEA處理小鼠肝臟氧化應激指標的影響
2.6 姜黃素對各組小鼠肝臟NLRP3和Caspase-1 p20表達水平的影響與對照組比較,ZEA組小鼠肝臟中NLRP3和Caspase-1 p20的蛋白表達水平明顯升高(P<0.01);與ZEA組比較,姜黃素+ZEA組小鼠肝臟中NLRP3和Caspase-1 p20的蛋白表達水平降低,差異有統計學意義(P<0.01)(圖4)。
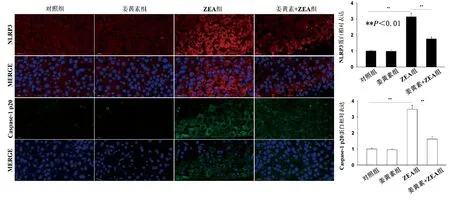
圖4 姜黃素對ZEA處理小鼠肝組織NLRP3和Caspase-1 p20蛋白表達的影響(標尺:20 μm)
2.7 姜黃素對ZEA處理小鼠肝臟組織IL-1β水平的影響與對照組比較,ZEA組小鼠肝組織IL-1β mRNA表達和IL-1β水平顯著升高(P<0.01);姜黃素+ZEA組小鼠肝組織IL-1β mRNA表達和IL-1β水平較ZEA組顯著降低,有統計學差異(P<0.01)(圖5)。
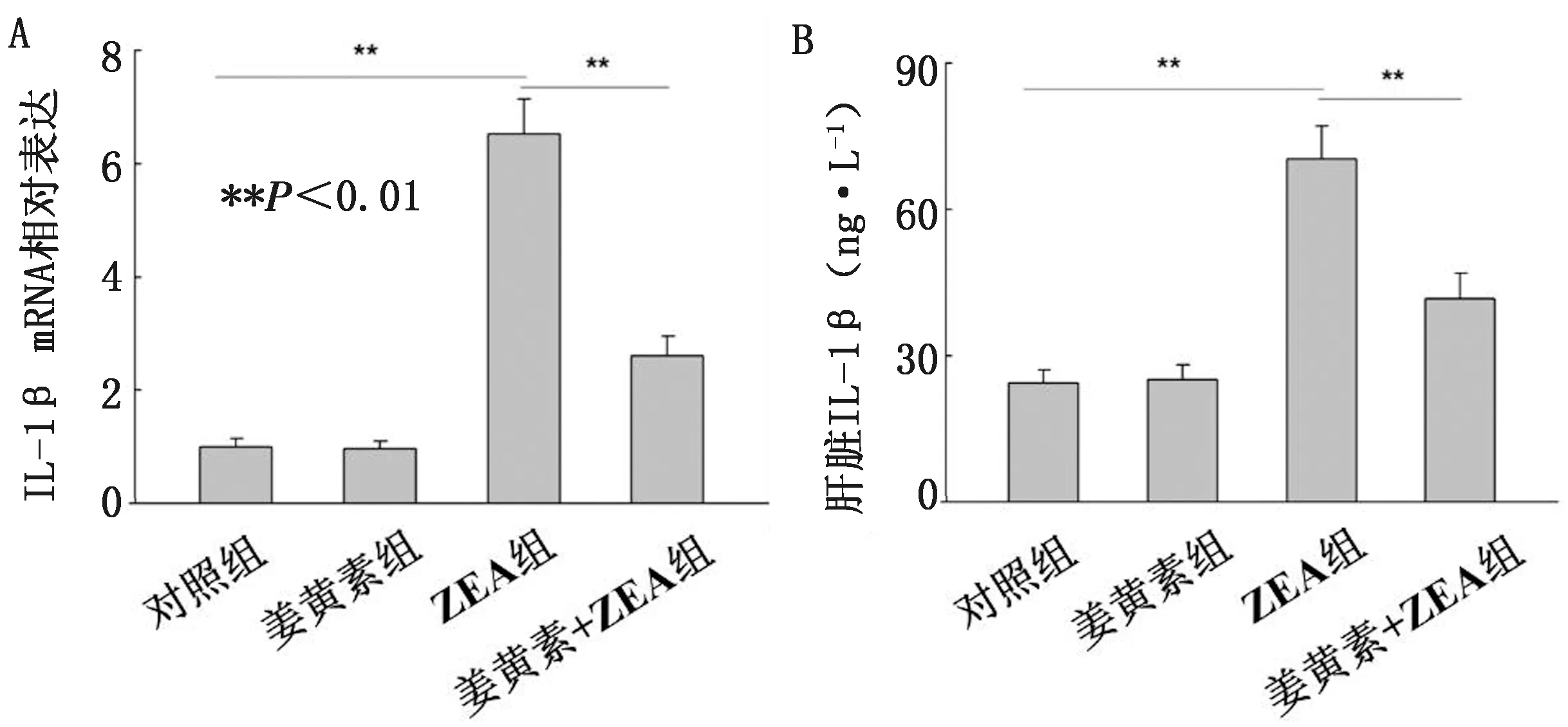
A.各組小鼠肝臟IL-1β mRNA表達;B.各組小鼠肝臟IL-1β 水平
3 討論
前期研究證實,ZEA暴露會導致小鼠肝組織細胞水腫,肝組織結構的完整性遭到破壞[9]。本研究采用HE染色和透射電鏡評價肝臟病理學變化,結果顯示ZEA引起肝組織形態學損傷。姜黃素的干預可顯著改善肝臟組織的病理損傷。此外,血清中AST和ALT水平是評價肝臟功能的生物學指標,當肝細胞膜的通透性改變或這些酶的生物合成發生紊亂,會導致血清中AST和ALT水平的升高[10]。本研究發現ZEA組血清中AST與ALT水平較對照組明顯升高,姜黃素能夠降低ZEA處理小鼠血清AST和ALT水平。這些結果提示,姜黃素可以緩解ZEA誘導的肝臟損傷。
作為天然免疫系統重要組成部分的炎癥小體,同時也是炎癥調節的關鍵因子,與肝疾病的發生有密切關系[11]。NLRP3炎性小體的活化引起Caspase-1前體被切割為具有活性的Caspase-1 p20,導致促炎因子IL-1β的成熟與分泌,最終參與到機體炎癥信號的啟動以及加劇炎癥反應造成的損傷[12-13]。已有研究證實,ZEA可增強肝組織中促炎因子IL-1β的水平[14]。ZEA處理引起INS-1(大鼠胰島細胞瘤細胞)細胞死亡,這與其激活NLRP3介導的細胞焦亡有關[15]。本研究發現,ZEA組小鼠肝臟中NLRP3和Caspase-1 p20蛋白表達水平顯著增加,促炎因子IL-1β水平明顯上升,姜黃素的干預能抑制NLRP3炎性小體活化,降低Caspase-1 p20的產生以及IL-1β的水平,表明姜黃素對ZEA誘導的NLRP3炎性小體活化具有抑制作用。
氧化應激是機體中抗氧化和氧化平衡被打破的一種病理過程。當氧化應激發生時,大量累積的ROS能直接對組織與細胞造成氧化損傷[16-17]。研究發現ZEA發病機制中的關鍵步驟是氧化應激[18]。MDA是脂質過氧化反應的產物,其含量高低可以作為評價組織氧化損傷程度的指標;SOD可以清除細胞內氧自由基,是組織細胞內主要的抗氧化酶,其活性也間接反映了組織的抗氧化能力[19];此外,肝臟中有著高水平的GSH-Px,它與CAT等抗氧化酶一起在清除體內多余自由基中發揮著重要的作用[20]。本研究結果表明,ZEA處理后,肝臟中SOD、CAT、GSH-Px活性降低,而MDA含量升高。經過姜黃素干預后,肝臟中SOD、CAT、GSH-Px活性升高,MDA含量降低,表明姜黃素能夠緩解ZEA誘導的肝臟氧化損傷。前期研究指出,過量的ROS可以激活NLRP3炎性小體,放大機體的炎性反應[21]。ZEA誘導的ROS水平升高在肝NLRP3炎性小體活化中的作用需要進一步的研究。
綜上所述,姜黃素可有效減輕ZEA誘導的小鼠肝臟損傷,其保護作用機制可能與抑制肝臟氧化應激和NLRP3炎癥小體活化有關。

