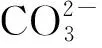伊利石對Sr的反應性吸附及機理表征
蔡偉海, 左銳*, 劉月鵬, 王金生, 杜璨, 徐云翔, 武子一
(1.北京師范大學水科學研究院, 北京 100875; 2.地下水污染控制與修復教育部工程研究中心, 北京 100875; 3.河北省生態環境保護技術服務中心, 石家莊 050051; 4.中國地質調查局發展研究中心, 北京 100037)
核能開發利用所產生的放射性廢物的妥善處置問題不容忽視[1]。90Sr是放射性核廢物中的典型組分之一,具有半衰期長、遷移速率快等特點,且具有生物毒性和化學毒性,容易在環境介質中遷移并通過生物鏈累積[2],已被國際原子能機構認定為高風險放射性核素之一。目前,含Sr廢物的處置方法有化學沉淀法、離子交換法、地質處置法和靜電吸附法等,其中地質處置法是目前世界上公認的處理含90Sr等放射性核素的核廢物最為安全有效的處置方法[3]。
地質體等天然屏障介質對放射性核素的吸附特性是評價處置庫安全性的重要內容之一。目前,相關學者針對不同地質處置介質對Sr的吸附開展了大量研究,如徐東輝等[4]研究了Sr在花崗巖裂隙填充物中的吸附行為,結果表明Sr在該吸附體系中為單分子層吸附;Lihareva等[5]研究了Sr在沸石中的吸附動力學特征,發現顆粒內擴散作用和液膜擴散作用均可影響其吸附過程;Du等[6]研究表明離子交換作用和絡合作用在黏土巖吸附Sr過程中起到重要作用。地質介質對放射性核素的吸附行為研究雖然已經取得一定的進展,但是不同類型的吸附介質對核素的吸附行為特征及機理仍有待進一步探索。黏土礦物具有吸附性強、比表面積大等特點,是一種良好的吸附材料,也是核廢物處置庫圍巖中的常見礦物。前人對不同黏土礦物對Sr的吸附行為開展了相應研究,如高嶺石、蒙脫石、膨潤土和凹凸棒等,研究發現膨潤土和高嶺石對Sr的吸附行為符合準二級動力學模型[7-8],可自發進行;蒙脫石對Sr的吸附作用以表面絡合和離子交換反應為主[9];方沸石對Sr的吸附過程為單分子層吸附,以化學吸附為主[10]。但是,目前國內有關伊利石對Sr的吸附研究較少,關于伊利石對Sr的吸附研究仍不全面[11],對吸附機理的表征刻畫研究仍不夠深入。
現以伊利石為吸附介質,通過靜態吸附實驗探究伊利石對Sr的吸附行為,結合吸附動力學模型分析其吸附過程特征,借助掃描電子顯微鏡(scanning electron microscope,SEM)、X射線衍射(X-ray diffraction,XRD)、傅里葉變換紅外光譜儀(Fourier transform infrared spectrometer,FTIR)和X射線光電子能譜(X-ray photoelectron spectroscopy,XPS)等多種表征分析方法探究和刻畫伊利石對Sr的吸附機理。
1 材料與方法
1.1 實驗材料
蘇宏圖地處內蒙古高原西部,行政區劃屬內蒙古自治區阿拉善盟阿拉善左旗管轄,是中國高放廢物備選場址之一[12]。該地區黏土巖分布廣泛,對其間的黏土巖X射線衍射分析(表1),可知黏土巖樣品中的主要黏土礦物為伊利石[13],因此選取伊利石為吸附介質。

表1 黏土巖樣品中黏土類礦物XRD結果分析表Table 1 Analysis of XRD results of clay minerals in clay rock samples
1.2 實驗方法
依據參照廢物處置場中的含Sr廢水濃度和已有實驗研究[6,14],靜態吸附實驗中Sr的濃度設定為20 mg/L。此外,由于蘇宏圖處置場所在區域地下水的pH為6~9,且在溫度10~40 ℃時,地下水中成分的變化不大。因此,實驗初始條件設置為pH=7,溫度為25 ℃。
采用恒溫震蕩批處理方法進行吸附實驗:向錐形瓶(250 mL)中加入反應介質(2.50 g)、250 mL Sr儲備液(20 mg/L),搖勻后待用。用忽略體積的NaOH溶液(0.1 mol/L)和HCl溶液(0.1 mol/L)調節pH為7左右。將錐形瓶放置于恒溫搖床內,相關參數設置為25 ℃、200 r/min。根據預實驗結果將吸附時間設置為4 320 min。吸附結束后取上清液離心,收集樣品,采用電感耦合等離子體發射光譜法(inductively coupled plasma atomic emission spectrometry,ICP-AES)檢測Sr的吸附溶液濃度。
1.3 數據分析方法
1.3.1 數據計算分析方法
借助于吸附質的質量濃度隨時間的變化關系分析吸附發生的過程,主要采用的吸附動力學模型主要為:準一級動力學模型[15]、準二級動力學模型[16]、Elovich模型[17]和顆粒內擴散模型[18]。
單位吸附量公式為
(1)
式(1)中:Qt為吸附量,mg/g;C0為含Sr溶液的初始濃度,mg/L;Ct為吸附后含Sr溶液的濃度,mg/L;V為吸附溶液的體積,L;m為吸附介質的質量,g。
吸附率公式為
(2)
式(2)中:R為吸附率,%。
Pseudo-first-order (PFO)公式為
qt=qe(1-e-kft)
(3)
式(3)中:qt為t時刻的吸附量,mg/g;qe為平衡時的吸附量,mg/g;kf為速率常數,min-1。
Pseudo-second-order (PSO)公式為
(4)
式(4)中:ks為速率常數,g/(mg·min)。
Elovich公式為
(5)
式(5)中:α為初始階段的吸附率,mg/(g·min);β為與化學吸附活化能和表面覆蓋度均相關的系數,g/mg。
Intra-particle Diffusion公式為
(6)
式(6)中:Kp為速率常數,mg/(g·min1/2);C為常數,mg/g,由邊界層厚度控制。
1.3.2 微觀表征分析方法
使用掃描電子顯微鏡(SEM,Hitachi SU8010)觀察伊利石樣品在吸附前后的表面形態結構變化;利用多功能X射線衍射儀(TTR Ⅲ,日本理學)測定吸附前后樣品在礦物組成上的變化;使用傅里葉紅外光譜儀(IRAffinity-1)測定吸附前后樣品在官能團方面的變化;通過光電子能譜儀(Thermo Scientific K-Alpha)測定實驗前后元素種類及化學價態的變化。
2 結果與討論
2.1 吸附動力學過程分析
根據伊利石對Sr的吸附率和單位吸附量隨時間的變化(圖1)可知,伊利石對Sr的吸附性較強,在實驗初始階段,吸附率迅速增加,當吸附時間為1 h時達到最大值為77.15%,此時單位吸附量為1.543 mg/g;隨后,吸附率和單位吸附量略有下降后逐漸趨于穩定,于240 min時達到吸附平衡狀態,吸附率為76.65%。

圖1 伊利石對Sr的吸附率和單位吸附量隨時間的變化Fig.1 Adsorption percentage and unit adsorption amount of Sr on illite changes over time
為進一步探究伊利石對Sr的吸附行為與吸附機制,用準一級動力學模型、準二級動力學模型、Elovich模型、顆粒內擴散模型4種模型對實驗數據進行擬合,擬合結果如表2所示。

表2 伊利石對Sr的吸附動力學擬合結果表Table 2 Table of fitting results of adsorption kinetics of Sr on illite
分析可知,準一級(PFO)、準二級(PFO)和雙曲正切模型對伊利石吸附Sr的數據擬合效果最好,相關系數R2>0.998,且根據這3個模型求得的qe與實驗所得的平衡吸附容量誤差最小,殘差平方和為0.003 9。據此推測,伊利石對Sr的吸附行為受到擴散作用控制,且物理吸附作用和化學吸附作用并存,這一過程與Sr在凹凸棒土、膨潤土和蒙脫土中的吸附行為類似[19]。結合伊利石對Sr的吸附百分數隨時間的變化,可知伊利石對Sr的吸附可分為兩個階段:在實驗初期(≤ 60 min)黏土巖表面有大量的吸附位點,因而吸附速率較快,在短時間內大量Sr被吸附到黏土巖表面,這一階段的主要的驅動力為液膜擴散作用,以物理吸附作用為主[20];隨吸附時間的增加,伊利石表面的吸附位點減少,因而吸附速率降低,Sr與黏土巖表面發生離子交換、絡合反應等,這一階段主要以化學吸附為主[21]。此外,由擬合結果可知顆粒內擴散模型并不能將實驗數據很好地擬合,因此伊利石對Sr的吸附行為不遵循顆粒內擴散模型,即黏土巖中對Sr的吸附限速步驟并非顆粒內擴散作用。
2.2 微觀表征分析
2.2.1 微觀結構分析
利用掃描電子顯微鏡觀察伊利石在吸附前后的微觀結構變化如圖2所示。吸附開始前,伊利石微觀形貌是由粒徑較小的顆粒物質、粒度較大的塊狀構造和不規則的片層結構組合而成的復雜結構,表面松散,為典型的微孔材料,有孔隙發育且數量較多,其粗糙多孔的結構為吸附Sr提供了大量的吸附點位。

圖2 伊利石吸附Sr前后的SEM圖譜特征Fig.2 SEM characteristics of illite before and after adsorption of Sr
對比伊利石吸附Sr前后的樣品微觀形態可知,吸附作用使伊利石表面發生顯著變化。吸附反應結束后,伊利石仍以塊狀構造和片層結構為主但表面的粗糙多孔結構明顯減少,小顆粒構造減少或消失,表面更加光滑。究其原因,主要為伊利石在與Sr溶液反應過程中發生了溶解和沉淀作用,吸附的Sr占據了其表面的吸附點位,使得伊利石表面的小顆粒物質減少,結構更為光滑。
2.2.2 礦物種類變化分析
利用X射線衍射儀測定伊利石的礦物組成,并將得到的相關數據通過MDI Jade9處理,所得吸附前后伊利石的XRD圖譜如圖3所示。XRD圖譜表明伊利石中的主要礦物種類為石英(SiO2)、伊利石[KAl(Mg0.2Al0.8)(Al0.42Si3.28)O10(OH)2]和斜長石[Na0.98Ca0.02(Al1.02Si2.98O8)]。其中石英特征衍射峰2θ分別為20.86°、26.64°、36.544°、39.465°、45.793°、59.960°、68.318°,對應的晶面分別為(100)、(101)、(110)、(102)、(201)、(211)、(301);伊利石對應的衍射峰位置為21.771°(021面)、24.479°(112面)、29.379°(112面);斜長石含量較少,對應的特征衍射峰2θ為27.912°和42.463°,晶面分為(040)和(060)。
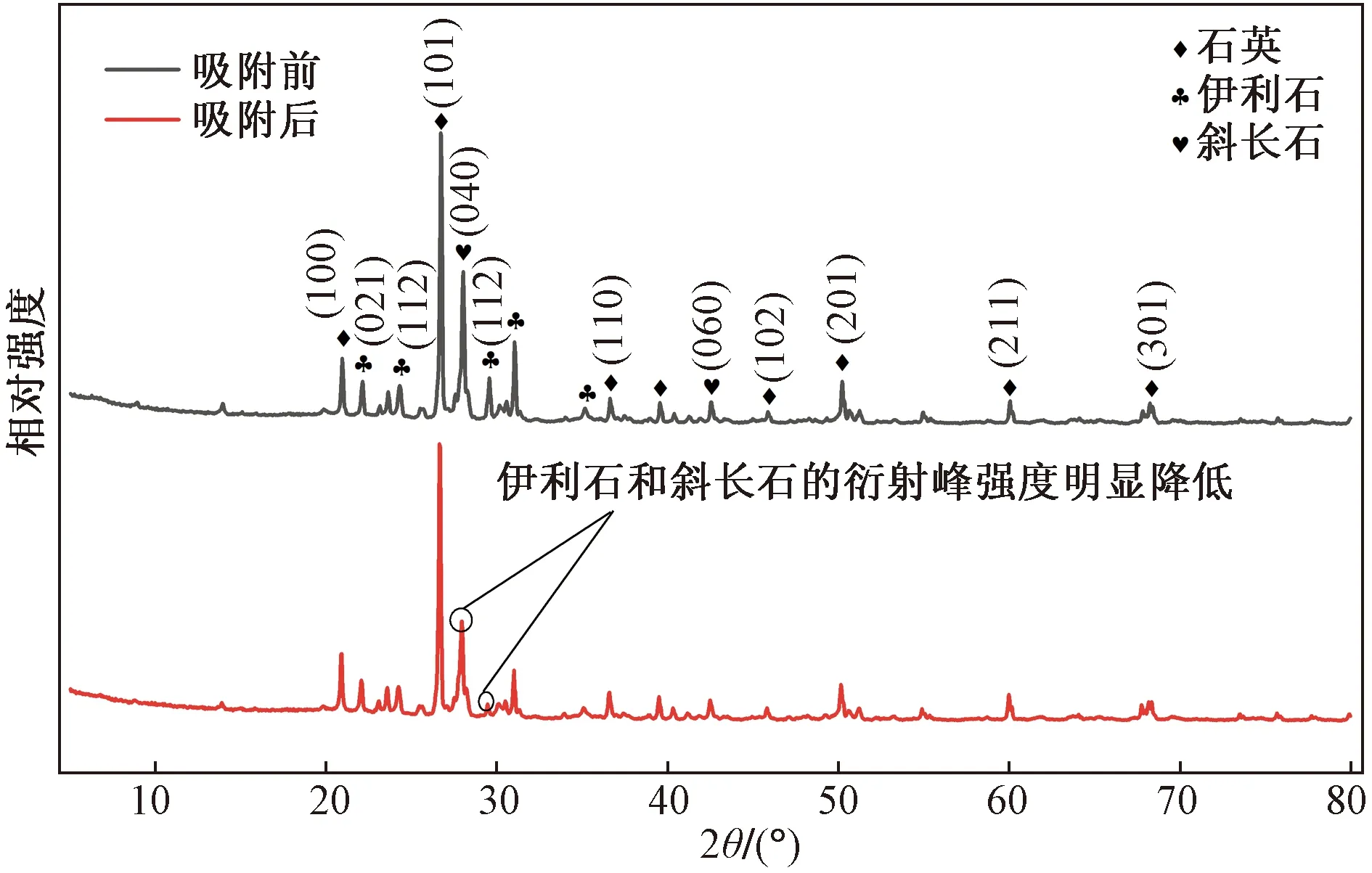
圖3 伊利石吸附Sr前后的XRD圖譜特征Fig.3 XRD patterns of illite before and after adsorption of Sr
對比吸附前后的XRD圖譜可知伊利石吸附Sr后,主衍射峰的位置向高衍射角方向移動,且強度均有不同程度的減弱,其中晶面結構為(040)的斜長石和晶面結構為(112)的伊利石衍射峰強度減弱明顯。據此推測,伊利石吸附Sr后,其礦物中的Ca2+、Mg2+等離子會與Sr發生陽離子交換反應[22-23],致使礦物的晶胞中摻入離子半徑較小的Sr,晶格常數減小,晶胞結構發生改變,主衍射峰強度下降并向高角度方向移動。
2.2.3 官能團變化分析
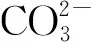

圖4 伊利石吸附Sr前后的FTIR圖譜特征Fig.4 FTIR spectra of illite before and after adsorption of Sr
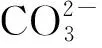
2.2.4 化學鍵變化分析
伊利石吸附Sr前后的XPS全譜特征如圖5所示,可以看出,伊利石中主要的元素有O、C、Ca、Mg、Na、Si、Al等,吸附Sr后全譜中有Sr出現,表明Sr已吸附在伊利石表面,并改變了其化學環境。為進一步探究伊利石吸附Sr過程發生的作用,對元素C和O圖譜進行分峰擬合,如圖6和圖7所示。
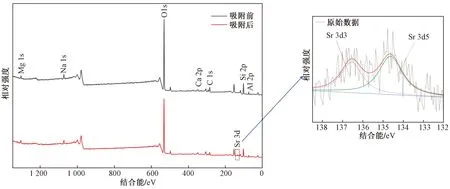
圖5 伊利石吸附Sr前后的XPS全譜特征Fig.5 XPS spectrum characteristics of illite before and after Sr adsorption
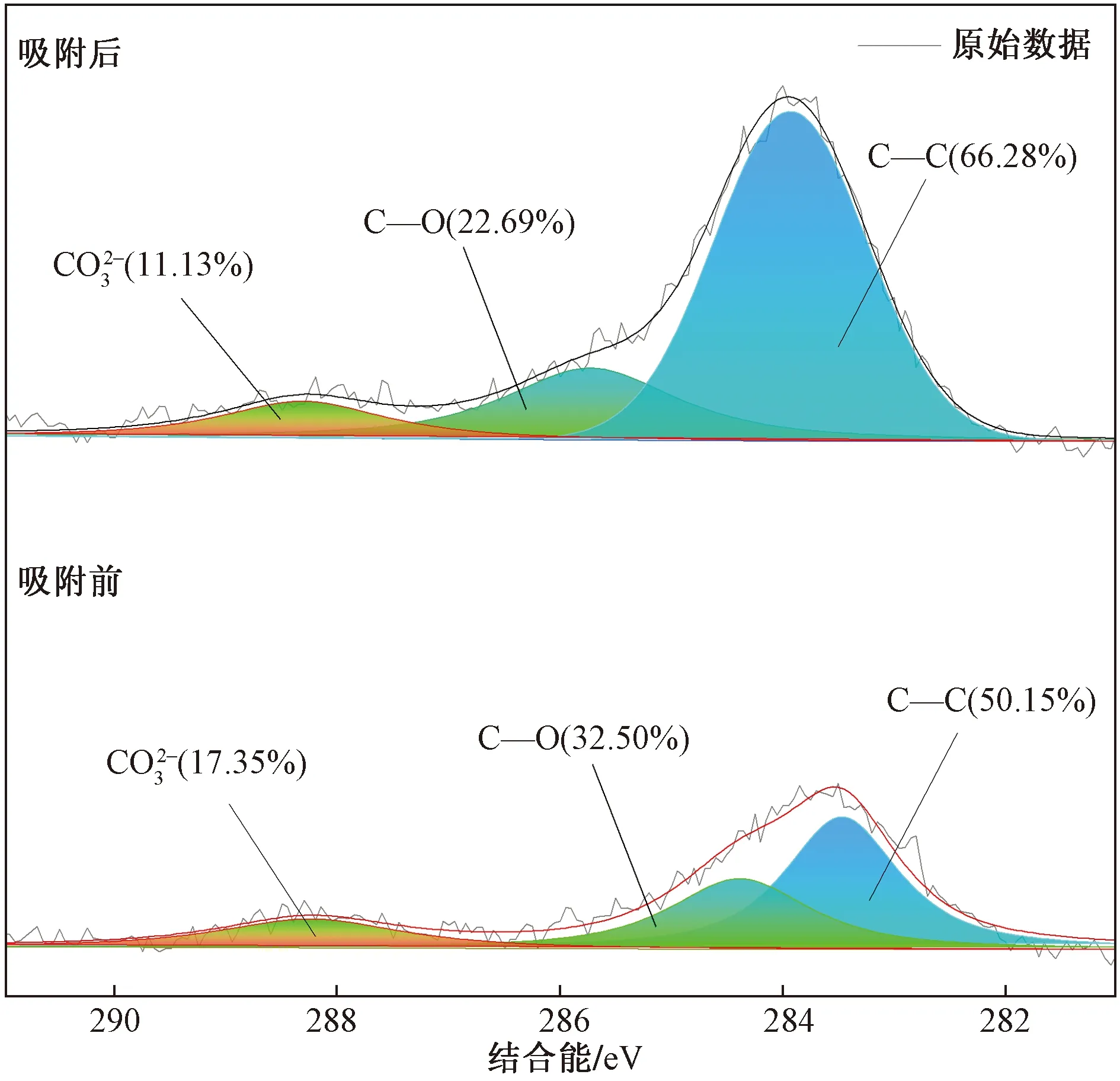
圖6 伊利石吸附Sr前后C 1s XPS圖譜Fig.6 C 1s XPS spectra of illite before and after Sr adsorption
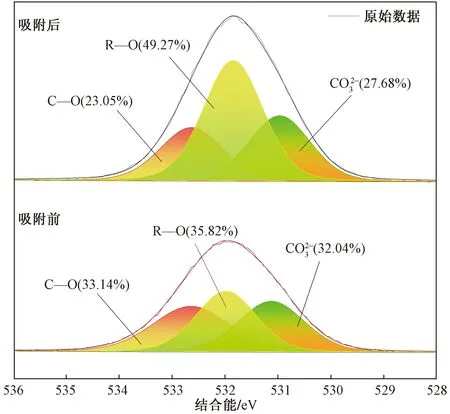
圖7 伊利石吸附Sr前后O 1s XPS圖譜Fig.7 XPS spectra of O 1s before and after adsorption of Sr by illite
2.3 基于表征的吸附反應機理分析
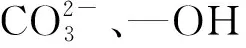

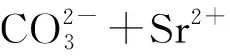


3 結論