噬菌體在食品微生物安全領域中應用的局限性和挑戰
惠瀟然,黃振華,劉 靜,吳 倩,許天明,段為旦,潘迎捷,2,3,張昭寰,*,趙 勇,2,3,*
(1.上海海洋大學食品學院,上海 201306;2.農業農村部(上海)水產品貯藏保鮮質量安全風險評估實驗室,上海 201306;3.上海水產品加工及貯藏工程技術研究中心,上海 201306)
噬菌體是侵襲細菌的病毒,寄生于活菌體內,在自然界中廣泛分布,于1916年由D’Hérelle首次分離[1],其主要通過吸附到宿主細胞上,將遺傳物質注入宿主細胞內,導致宿主細胞裂解并釋放子代噬菌體,從而殺死宿主細菌[2],可用于預防和治療各種細菌感染[1]。將噬菌體合理地應用于食品工業中,能夠專一地殺滅包括耐藥菌在內的特定菌株,而不對其他細菌造成任何影響[3]。此外,研究者們還可根據不同需求分離出針對特定致病菌的噬菌體[4]。綜上,噬菌體可彌補傳統抗生素及殺菌技術的不足,在控制食源性致病菌的污染方面具有良好的應用前景[3]。
在“農場-餐桌”的食品供應鏈中,大量研究報告了噬菌體能夠有效抑制食源性致病菌的生長[5-9],且不會影響食品的感官特征[10]。但噬菌體在食品工業中的實際應用相對較少,其原因主要包括一些技術的限制和消費者的接受程度,如噬菌體應用于食品時如何確保其覆蓋于食品表面達到最佳抑菌效果,噬菌體生物防治的廣泛應用可能會引起對噬菌體有耐藥性細菌的出現,以及消費者可能不愿意購買不熟悉技術加工的食品等[3,11]。因此,需要進一步評估噬菌體的安全性和有效性,以確保它們在食品工業中安全、高效的使用[12]。
本文系統地綜述了限制噬菌體在食品領域中廣泛應用的原因,涵蓋了噬菌體在食品工業中應用的可接受程度、潛在耐藥傳播風險、細菌的噬菌體抗性問題、復雜的食品基質對其作用效果的影響,并對噬菌體在食品工業中的應用方式提出了科學合理的建議,以推動噬箘體的基礎研究走向食品工業的實際應用。
1 噬菌體在食品工業中應用的可接受程度
噬菌體在食品及食品相關環境中的殺菌效果得到了廣泛的研究[13],可抑制多種食物中的致病菌和腐敗菌,如水果[5]、蔬菜[6]、肉制品[7]、乳制品[8]和水產品[9]等。2006年,美國食品和藥品管理局(Food and Drug Administration,FDA)推出第一款可用于食品工業的噬菌體產品ListShieldTM,用于即食食品肉類和家禽產品中單核細胞增生李斯特菌(以下簡稱單增李斯特菌)(Listeria monocytogenes)的控制[14]。國內對噬菌體的研究主要集中在臨床醫學[15]和農業方面[16]。在食品工業中,對噬菌體的應用研究主要集中在對肉質品中的食源性致病菌的控制,如牛肉中大腸埃希菌O157:H7(Escherichia coliO157:H7)的防控[17]、雞肉中沙門氏菌(Salmonella)的防控[18]、冷卻羊肉中產堿假單胞菌(Pseudomonas alcaligenes)的防控[19]。目前我國還未批準相關應用于食品的噬菌體產品,這與消費者對噬菌體應用于食品的可接受程度密切相關。
相對于新興技術加工的食品而言,多數消費者更加傾向于傳統技術加工的食品[20]。盡管利用噬菌體殺菌是一種綠色、安全和靶向的抗菌手段,但其作用方式是在食品表面噴灑“病毒活體”,導致廣大消費者對這種殺菌技術的接受程度較低。病毒在普通大眾的固有觀念中是有害的,所以消費者很難接受應用噬菌體技術加工的產品[12]。盡管噬菌體技術背后的科學原理十分明確,但消費者對于未知事物的不了解甚至誤解,某種程度上限制了噬菌體在食品工業中的應用。
2 噬菌體傳播耐藥性的潛在風險
近年來,人們在農業生產過程中抗生素的濫用問題,促使大量抗生素通過農業廢棄物釋放到環境中,對微生物群落造成選擇性壓力,從而導致了耐藥菌和耐藥基因的選擇和傳播[21]。目前,來源于各類水體、土壤、畜禽以及人體糞便分離的噬菌體中,均檢測出不同種類的抗生素耐藥基因(antibiotic resistance genes,ARGs),如β-內酰胺類、喹諾酮類、四環素類、甲氧西林、磺胺類等。如表1所示,噬菌體攜帶了較高水平的β-內酰胺類耐藥基因(主要集中于blaTEM和blaCTX類)和喹諾酮類耐藥基因qnrA、qnrB和qnrS,以及一些其他的耐藥基因,如磺胺類耐藥基因sul1和sul2、四環素類耐藥基因tetA、tetW和tetM以及萬古霉素耐藥基因vanA等。隨著測序手段的進步,研究人員利用宏基因組學的方法同樣也檢測到了噬菌體攜帶各種ARGs,這表明噬菌體可以被視為一種ARGs的儲存庫。
研究發現,大約20%的細菌基因組是通過噬菌體樣元件而獲得[21],其介導細菌間基因轉移的主要方式為轉導或溶源轉變。轉導是通過噬菌體介導外源DNA轉移的過程[21,39],攜帶耐藥基因的噬菌體感染細菌后,可能會將耐藥基因重組到感染細菌的基因組中,從而使其獲得新的遺傳特性[39-40]。如噬箘體EC10通過轉導的方式將大腸桿菌(E.coliNBRC 12713 KEN1)中的耐藥基因bla轉移到大腸桿菌(E.coliC600RK2/HB101/NBRC 12713/W3110)中[41];噬箘體P24通過轉導的方式將海德堡沙門氏菌(S.heidelbergS25)中的耐藥基因blaCMY-2、tetA和tetB轉移到鼠傷寒沙門氏菌(S.TyphimuriumMZ1262)中[42]。溶源性轉變是指溫和型噬菌體基因組在宿主基因中的整合[43],當溫和型噬菌體感染細菌細胞時,噬菌體DNA整合到宿主細胞染色體上,此時原噬菌體基因的表達將導致宿主表型的變化,形成的溶原細胞可以在不產生噬菌體顆粒或有害噬菌體蛋白的情況下生存[43-44]。如溫和噬菌體TEM123通過溶源轉變的方式將β-內酰胺類抗生素耐藥基因轉移到金黃色葡萄球菌(Staphylococcus aureus)基因組上[45]。因此,噬菌體能夠在ARGs的傳播中發揮重要的作用,造成細菌耐藥性傳播的風險,限制了其在食品工業中的實際應用。
3 細菌的噬菌體抗性問題
在噬菌體應用研究中發現,細菌的噬菌體抗性問題使得噬菌體在食品工業的生物防治效果明顯降低。尤其是在控制食源性致病菌方面,在噬菌體與細菌不斷進化的過程中,細菌抵抗噬菌體的能力也在不斷地提升,從而導致噬菌體用于抑制細菌的效果并不理想,這大大限制了噬菌體在食品工業中的應用。
有無局部現澆的墩柱在節段底部與承臺之間的相對滑移上也有很大差異,如圖10所示,圖10(a)為無耗能鋼筋的2個墩柱,圖10(b)為有耗能鋼筋的2個墩柱.從圖10中可以看出,局部有現澆混凝土的墩柱在節段墩柱底部的相對滑移較大,說明墩柱節段通過局部現澆的連接方式會使墩柱各個節段有很好的整體性,在實際施工中只需對墩柱底部進行細部處理即可.
3.1 難以徹底殺滅細菌
噬菌體生物防治只能在短期內抑制食源性致病菌的生長,不久之后細菌可恢復生長(表2)。理論上,一個噬菌體從感染一個細菌細胞開始,到復制周期結束時,該細胞中會產生100~200 個子代噬菌體,子代噬菌體持續裂解細菌細胞,導致細菌數量會顯著減少[11],但實際情況并非如此。Guenther等[46]用10 mL SM緩沖液(50 mmol/L Tris-HCl,pH 7.5,100 mmol/L NaCl、8 mmol/L MgSO4)稀釋噬菌體顆粒,在15 ℃條件下用3×108PFU/g的噬菌體FO1-E2處理接種103CFU/g沙門氏菌的熱狗、雞胸肉、牛奶和蛋黃等食品,觀察噬菌體處理對沙門氏菌的控制效果。結果發現,除蛋黃外,其他食物中的活菌數量均下降了2(lg(CFU/g)),但是2 d后沙門氏菌能夠再次生長,證明噬菌體處理并不能完全抑制沙門氏菌的繁殖。Spricigo等[47]用3 種噬菌體組成的噬菌體制劑處理豬皮、雞胸肉、雞蛋等食品,結果發現,雞胸肉中腸炎桿菌UA1894在處理后5 d活菌數量減少1.4(lg(CFU/g)),但在第7天時活菌數量僅減少0.9(lg(CFU/g))。Kang等[48]分離出一種強效噬菌體wksl3,將其涂抹于雞皮上觀察噬菌體的抑菌活性,結果發現,在1 d后沙門氏菌數量降低了3(lg(CFU/mL)),但在7 d后細菌數量又有所增加。很多研究均報道了噬菌體只可短期內有效降低食品中致病菌的數量,而不能夠完全清除。產生這一現象的原因可能是出現了抗噬菌體突變株,使噬菌體無法徹底殺滅細菌。
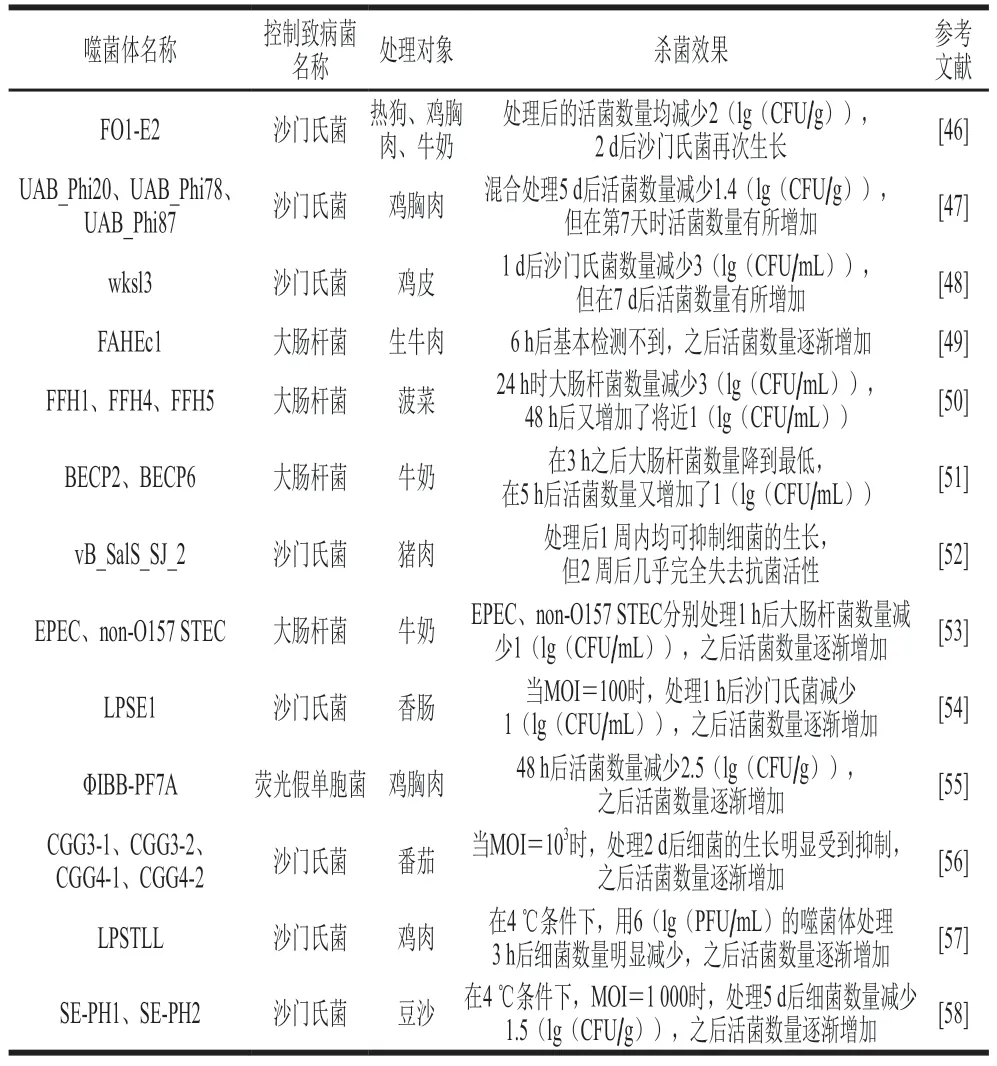
表2 噬菌體在食品殺菌中應用的研究Table 2 Recent studies on the application of phages in food sterilization
3.2 細菌對噬菌體的抗性機制
在應對噬菌體侵襲的過程中,食源性致病菌進化了各種免疫系統來抵御噬菌體的感染,主要有吸附抑制(adsorption inhibition,AI)系統、超感染排斥(superinfection exclusion,Sie)系統、限制修飾(restriction modification,RM)系統、CRISPR-Cas系統、流產感染(abortive infection,Abi)系統和毒素-抗毒素(toxin-antitoxin,TA)系統(圖1)。

圖1 細菌對噬菌體的抗性免疫系統Fig.1 Bacterial immune systems for phage resistance
3.2.1 阻止噬菌體的吸附(AI系統)
噬菌體的吸附是噬菌體感染細菌的第一步(圖1)。噬菌體感染成功的關鍵是噬菌體與細菌表面受體特異性結合,因此受體變異就會使噬菌體無法吸附,從而導致噬菌體感染失敗[59]。在長期進化中,細菌已經進化出許多表面結構來阻止噬菌體的吸附,這一阻斷機制主要包括:噬菌體受體基因突變或修飾、競爭性抑制劑的競爭抑制、胞外基質的覆蓋、噬菌體自身編碼的蛋白與其受體蛋白結合。如霍亂弧菌分泌的OMV可作為噬菌體受體的誘餌蛋白,從而保護細菌免受噬菌體的感染[60],OMV還能夠不可逆地與噬菌體結合,噬菌體一旦附著在OMV上,感染能力就會大大降低[61]。銅綠假單胞菌IV型菌毛糖基化使噬菌體無法識別,從而阻止以菌毛為特異性受體噬菌體的感染[62]。大腸桿菌以及其他革蘭氏陰性菌可通過產生過量的胞外多糖,使噬菌體無法進入宿主細胞[63]。十一烯基磷酸葡萄糖-1-磷酸轉移酶是噬菌體117吸附肺炎克雷伯菌KP36完成裂解過程中的關鍵功能酶,控制該酶的編碼基因WcaJ突變能夠阻斷噬菌體117的吸附[64]。糞腸球菌OG1RF中受體蛋白的編碼基因突變,阻斷了噬菌體的吸附,從而增加了細菌對噬菌體的抗性[65]。假單胞菌噬菌體DMS3編碼的蛋白Aqs1可以與菌毛組裝蛋白PilB結合,從而阻止同類噬菌體與細菌受體結合[66]。假單胞菌噬菌體D3112編碼的蛋白Tip也可以與菌毛組裝蛋白PilB特定區域相互作用并阻斷其活性,從而阻止同類噬菌體的吸附[67]。
3.2.2 阻斷噬菌體DNA的侵入(Sie系統)
噬菌體DNA的侵入是噬菌體感染細菌的第二步(圖1)。Sie系統最初在溫和噬菌體中被發現[68],是阻止噬菌體DNA進入宿主細胞的主要機制,當宿主細胞被噬菌體感染后,同一類噬菌體再次感染宿主細胞時,這種多為膜錨定蛋白或與膜成分相關蛋白就會發揮作用,從而阻止同類噬菌體的再次感染[69]。
在革蘭氏陰性菌中,大腸桿菌T4噬菌體有兩個由imm和sp編碼的Sie系統,T4噬菌體編碼的imm蛋白通過與另一種膜蛋白結合來改變注射位的構象從而阻止噬菌體DNA的進入[69-70],T4噬菌體編碼的sp蛋白抑制了由gp5編碼的溶菌酶的活性,阻止了細胞壁肽聚糖的降解,從而阻斷噬菌體DNA的侵入[69]。在革蘭氏陽性菌中,最具有特征的系統Sie2009發現于溫和型噬菌體乳球菌(Lactococcus lactis)噬菌體Tuc2009的基因組中,可以在不影響噬菌體吸附的情況下阻止936噬菌體組中某些噬菌體DNA的侵入[71];溫和型嗜熱鏈球菌(Streptococcus thermophilus)噬菌體TP-J34編碼的ltp蛋白可通過抑制噬菌體DNA進入細菌細胞質中,從而阻止嗜熱鏈球菌的重復感染[72]。
3.2.3 切割噬菌體DNA(RM系統和CRISPR-Cas系統)
噬菌體的生物合成是噬菌體感染細菌的第三步(圖1),RM系統普遍存在于細菌與古細菌的噬菌體防御機制中,該系統主要由MTase和REase組成[63]。在噬菌體在完成吸附和侵入后,RM系統作為免疫系統攻擊進入細胞的噬菌體DNA,其中REase主要識別并切割特異DNA序列,當噬菌體DNA進入宿主細胞后,REase會識別并切割特定的位點,破壞噬菌體DNA,而宿主細胞DNA上的相同位點則被MTase甲基化,以保護自身DNA不被REase切割。RM系統根據作用機制和亞基可成分為4 種類型,即I~IV型[73-74]。I型和III型RM系統相似,REase都沿著DNA移位,并從識別位點切割,在II型RM系統中,REase在DNA識別位點內部或附近進行切割,IV型系統由于缺乏MTase,只能切割修飾過的DNA[74-75]。最近發現的一種新的防御系統——限制-修改相關的防御島系統(defence island system associated with restrictionmodification,DISARM)能限制噬菌體的DNA進入,類似于RM系統,是一種新型的多基因限制性修飾模塊[76]。
CRISPR-Cas系統是由一個含有短且保守的重復序列的CRISPR基因組位點以及由Cas編碼的Cas蛋白組成[75]。到目前為止,CRISPR-Cas系統一共可分為兩大類(一類是由多個蛋白組成的效應蛋白模塊;另一類是單個蛋白效應模塊),共有6 種類型(I~VI型)和33 種亞型[77]。噬菌體在完成吸附和侵入后(圖1),該系統通過識別和切割外源的DNA或RNA,以一種序列特異性發揮作用,其行使功能分為3 個階段:獲取間隔序列、crRNA的生物合成和目標干擾[78]。當噬菌體DNA第一次進入細菌細胞時,兩種蛋白質Cas1-Cas2復合物會選擇一部分外源DNA序列(原間隔序列)納入CRISPR序列中,形成一段新的間隔序列,這一過程使宿主細胞記住噬菌體的DNA。隨后這段間隔序列就會被轉錄成一個長前體crRNA(pre-crRNA),該前體crRNA進一步加工成含有噬菌體序列的成熟crRNA。最后在成熟的crRNA引導下,Cas核酸酶利用crRNA通過互補堿基配對來識別和切割噬菌體的DNA[78-79]。
3.2.4 阻止噬菌體顆粒釋放(Abi系統和TA系統)
噬菌體的組裝和釋放是噬菌體感染細菌的第四步(圖1),當噬菌體DNA成功入侵后,Abi系統能夠干擾噬菌體復制周期的各個環節,阻止子代噬菌體的釋放,同時導致宿主細胞的死亡[80]。該系統主要是由單一蛋白質或蛋白質復合物組成,通常在噬菌體侵入后被活化,是單個細菌為保護周圍細菌的一種自我犧牲的過程,主要通過干擾細菌細胞DNA的復制、轉錄和翻譯來實現[73,75]。Abi系統種類較多,在乳酸乳球菌中發現有20 種Abi系統(AbiA~AbiZ)[81]。2006年,Lossouarn等在表皮葡萄球菌中也發現了Abi系統,噬菌體表達的蛋白會激活噬菌體防御激酶Stk2,誘導Abi的發生,從而阻止噬菌體向其他細菌種群的繁殖[82]。最近研究人員在糞腸球菌中發現了一種新的Abi系統(Abiα),由原噬菌體編碼的Abiα基因能夠引起糞腸球菌的提前裂解,具有典型的Abi表型[83]。
TA系統廣泛存在于細菌中,主要依靠一個毒素和一個抗毒素組成的防御系統。該系統的基本特點是抗毒素具有不穩定性,必須連續表達才能與毒素保持適當的化學計量比。TA系統中的毒素包括脫氧核糖核酸酶(DNase)和核糖核酸酶(RNase),可以抑制DNA復制、ATP合成[16,75]。以植物致病菌萎縮果膠桿菌為例(圖1),ToxI和ToxN組成了一個TA系統,其中ToxN可以抑制細菌生長,在噬菌體感染后導致ToxN釋放并降解細菌細胞RNA,導致噬菌體和細菌細胞死亡[84]。
4 復雜食品基質對噬菌體作用效果的影響
在噬菌體應用于食品工業的過程中,復雜的食品基質也是影響噬菌體作用效果的重要因素,主要包括食品的pH值、溫度、化學成分等[85]。這些因素往往是食品自身的固有屬性,很難通過工藝優化的方式進行消除,限制了噬菌體在此類食品環境中的實際應用。
4.1 食品pH值對噬菌體作用效果的影響
食品p H 值是影響噬菌體殺菌效果的重要參數之一[85],研究表明,噬菌體在蜜瓜上的應用效果優于蘋果[86-88],Leverent等[86]用噬菌體分別處理蜜瓜(pH 5.8)和蘋果(pH 4.2),結果發現5 ℃和10 ℃下貯藏168 h后蜜瓜上沙門氏菌數量均減少了約3.5(lg(CFU/g)),但蘋果片上沙門氏菌的數量未顯著減少。之后Leverentz等[87]發現,用噬菌體混合物可使蜜瓜(pH 5.5~6.5)中單增李斯特菌的數量降低2.0~4.6(lg(CFU/g)),而對蘋果(pH 3.8~4.2)中單增李斯特菌僅能殺滅0.4(l g(C F U/g))。Oliveira等[88]用噬菌體Listex P100處理密瓜、梨和蘋果4 h后,結果發現蜜瓜和梨中單增李斯特菌的數量分別減少了1.5(lg(CFU/mL))和1.0(lg(CFU/mL)),而在蘋果片上的效果較差。Leverentz等[87]認為噬菌體的感染可能受到蘋果酸性的影響。
4.2 食品溫度對噬菌體作用效果的影響
食品的溫度是影響噬菌體作用效果的另一因素,例如,在4、10 ℃和20 ℃條件下,用噬菌體P100處理接種4(lg(CFU/cm2))單增李斯特菌的干腌火腿片,結果發現在4 ℃條件下噬菌體的殺菌效果最好[89]。用商業噬菌體混合制劑處理奶酪時,觀察到不同溫度對噬菌體的影響效果不同,在22 ℃下噬菌體殺滅單增李斯特菌的效果最好,比6 ℃條件下多殺滅0.79(lg(CFU/g))單增李斯特菌,但22 ℃不適合貯存奶酪,這種條件下會促進霉菌和其他腐敗菌的生長[90]。
4.3 食品中化學成分對噬菌體作用效果的影響
食品中的蛋白質、脂質等化學成分會干擾噬菌體與特定宿主細胞受體之間的相互作用,從而影響噬菌體的作用效果[91]。Gill等[92]發現牛乳中的乳清蛋白因吸附在細菌細胞表面,阻斷了噬菌體的結合,從而影響噬菌體對金黃色葡萄球菌的抗菌活性。Garcia等[93]在半脫脂牛奶和全脂牛奶中檢測了噬菌體對金黃色葡萄球菌的抑菌作用,結果發現噬菌體ΦH5和ΦA72混合處理后,半脫脂牛奶中的金黃色葡萄球菌數量下降了2(lg(CFU/mL)),而對全脂牛奶中的金黃色葡萄球菌幾乎沒有抑制作用。
5 結語
噬菌體在食品工業中應用的可接受程度較低,其本身還具有潛在傳播耐藥性的風險,在控制食源性致病菌時,細菌對噬菌體產生的抗性問題以及復雜的食品基質對其作用效果的影響等諸多問題限制了噬菌體在食品工業中的實際應用。但是,噬菌體具有易于分離、資源豐富、特異性強等優勢,若對其進行合理的開發、提高應用效率、控制潛在風險,能夠有助于突破其在食品工業應用中的局限性。基于此,本文進一步對噬菌體在食品工業中的發展及應用提出以下三點建議。
5.1 推動噬菌體的基礎研究走向食品工業化應用
基于大量關于噬菌體的基礎研究,向食品行業以及廣大消費者進行噬菌體的科普宣傳,使其充分了解噬菌體具有高效、安全、靶向等優勢,并通過微信、短視頻等新興媒體,科學合理地普及噬菌體相關信息,提高噬菌體在食品工業應用中的可接受度。此外,可根據每種噬菌體的最佳條件優化食品工藝,在不影響食品風味的情況下,使噬菌體在食品中發揮作用,從而推動噬菌體的基礎研究走向食品工業化應用。
5.2 基于多組學技術嚴格篩選可用于食品加工的優質噬菌體菌種
噬菌體在自然界中普遍存在,將其作為生物防控劑應用于食品時必須嚴格篩選,從基因組學、蛋白組學等多組學技術上嚴格把控,篩選出不攜帶耐藥基因、毒力基因等風險因素的優質噬菌體菌種,為噬菌體在食品領域中的應用提供科學依據和數據基礎,研發安全、高效的噬菌體類食品添加劑,從而為食品安全的切實保障提供可靠的防控策略。
5.3 采用噬菌體裂解酶擴大適用范圍
大部分噬菌體都能編碼相應的裂解酶,具有裂解活性強、安全性高、易于改造等優勢,在食品實際生產過程中,可以使用噬菌體裂解酶代替噬菌體活體,其不僅具備噬菌體的特異性優勢,而且不易改變食品的質地和口感,能夠較好地克服噬菌體應用的局限性。因此,今后可以將噬菌體裂解酶作為研究目標,發掘出裂解活性高、穩定性強、宿主譜廣的噬菌體裂解酶,以應用于食品工業領域。

