向日葵果膠鋅的制備及其結構表征
京晶,劉國強,楊凱斌,李寶毅,翟麗軍,白雪麗*
(1.太原工業學院 化學與化工系,山西 太原 030008;2.南開大學 化學學院 先進能源材料化學教育部重點實驗室,天津 300071 )
鋅是維持生命必不可少的一種微量元素,在人體正常細胞功能和新陳代謝中發揮著重要作用。鋅元素具有降低血糖水平、促進骨骼的生長和形成、提高機體免疫力等功能[1]。缺乏鋅元素會導致身體生長缺陷、神經功能障礙、性腺機能減退、阻礙骨骼生長等一系列疾病[2]。據世界衛生組織報道,缺鋅是一種普遍存在的現象。人體自身對鋅元素的儲存能力較低,因此通常情況下人類通過外界來獲取鋅元素。然而受經濟水平和飲食文化的影響,無法保證每個人都具有合理的膳食結構。無機鋅補充劑(硝酸鋅、硫酸鋅、氯化鋅)中鋅的生物利用度低、容易對人體消化道造成刺激;有機鋅(葡萄糖酸鋅口服液)長期服用會產生對人體有害的物質且仍對消化道有一定的刺激作用[3]。近年來,多糖鋅因具有穩定性高、生物利用率高、副作用較小等特點而被廣泛研究。目前國內外研究的多糖鋅有生姜皮多糖鋅[4]、羅耳阿太菌多糖鋅[5]、南瓜皮多糖鋅[6]等。
向日葵是全球重要的油料作物之一,在收獲種子后,向日葵盤被作為垃圾丟棄在田地里或者直接進行焚燒,造成環境污染。而向日葵盤中含有大量的低酯果膠,是一種陰離子多糖,主鏈由α-1,4-半乳糖醛酸組成,側鏈中含有大量的羥基和羧基[7],與金屬離子具有較強的結合能力。果膠在食品方面可被用作膠凝劑、添加劑、穩定劑[8];在生物醫學方面也有很廣泛的應用,如:抗氧化劑和治療糖尿病、胃腸疾病、高血壓、癌癥的藥物等[9]。但對于向日葵果膠和微量元素的制備及結構表征的報道較少。
以向日葵果膠和硫酸鋅為原料制備向日葵果膠鋅,通過單因素和響應面試驗法確定向日葵果膠鋅的最佳制備工藝,并對其結構進行初步的表征,為多功能新型補鐵劑的開發提供一定的理論依據。
1 材料與方法
1.1 材料與儀器
向日葵果膠,南京鑫越源生物科技有限公司;硫酸鋅、檸檬酸鈉、氫氧化鈉、鋅標準溶液(1 000 mg/L),上海阿拉丁試劑有限公司。
BSD-TX27臺式恒溫搖床,上海博迅醫療生物儀器股份有限公司;LG10-2.4A高速離心機,北京醫用離心機廠;DHG-9145A電熱鼓風干燥箱,上海一恒科學儀器有限公司;Tensor 27傅里葉紅外光譜儀,瑞士布魯克公司;Bruker D8 Advance X射線衍射儀,瑞士布魯克公司。
1.2 實驗方法
1.2.1 向日葵果膠鋅的制備工藝
采用硫酸鋅法制備向日葵果膠鋅。在50 mL 10 g/mL向日葵果膠溶液加入0.25 g檸檬酸鈉,再加入一定體積的硫酸鋅溶液混合,設計不同的反應時間、反應pH值和反應溫度將混合液置于恒溫搖床中進行反應,反應結束后,趁熱將溶液放入離心機進行分離(6 000 r/min,10 min),待上清液降到室溫,倒入2倍體積的95%乙醇溶液中進行醇沉24 h,將固體放入電熱鼓風干燥箱中干燥24 h,研成粉末,最后得到向日葵果膠鋅粉末。
1.2.2 向日葵果膠鋅的單因素實驗
在反應pH值為7,溫度為80 ℃的條件下,考察反應時間分別為20,50,80,110 min,對果膠鋅螯合率的影響;在反應時間為70 min,溫度為80 ℃的條件下,考察pH值分別為5,6,7,8,9對果膠鋅螯合率的影響;在反應時間為70 min,反應pH值為7的條件下,考察反應溫度為40,60,80,100,120 ℃對果膠鋅螯合率的影響。按“1.2.1”步驟進行操作,每組實驗重復3次。
1.2.3 響應面試驗
在單因素實驗的基礎上,采用3因素3水平的響應面試驗,以反應時間(A)、反應pH值(B)、反應溫度(C)為影響因素,以螯合率(Y)為響應值,用Design 8.0.6軟件,以Box-Behnken設計響應面試驗方案,對向日葵果膠鋅的制備工藝參數進行優化,設計因素及水平見表1。

表1 響應面試驗因素水平表
1.2.4 螯合率的計算
將1 000 mg/L的鋅標準溶液分別稀釋成質量濃度為5,10,20,50,100,200,500 μg/L的鋅溶液,用ICP-MS測定,其標準曲線方程為:y= 254.369 4x+ 196.866 7,R2= 1.000 0。用5%硝酸溶液稀釋上清液,用ICP-MS測定鋅離子的含量,并計算螯合率。
1.2.5 FTIR分析
將樣品粉末與溴化鉀按質量比1∶300混合,在研缽中研磨,壓成薄片,用傅里葉紅外光譜儀在波長為4 000~400 cm-1,分辨率為2 cm-1條件下進行掃描,并記錄譜圖。
1.2.6 XRD分析
用X射線衍射儀(XRD)對樣品進行測定,掃描范圍為5°~80°,掃描速度為5°/min。
2 結果與分析
2.1 單因素實驗結果
2.1.1 反應時間對螯合率的影響
不同反應時間對螯合率的影響如圖1所示。由圖1可知,隨著時間的延長,螯合率先逐漸增大又緩慢下降,當到達90 min時達到最大值。反應時間過短果膠與鋅元素反應不徹底,導致螯合率下降;反應時間過長,可能會出現一些副產物從而使得螯合率下降。因此選擇90 min為響應面試驗中心點。

圖1 反應時間對螯合率的影響
2.1.2 pH值對螯合率的影響
不同pH值對螯合率的影響如圖2所示。由圖2可知,在pH值5~8范圍內,螯合率隨pH值呈先上升后下降的趨勢。當pH值=8時,螯合率達到最大值,當pH值>8時,螯合率開始下降,可能是因為在堿性條件下,Zn2+與OH-會生成沉淀,影響反應的進行使得螯合率下降。因此選擇pH值=8為響應面試驗中心點。
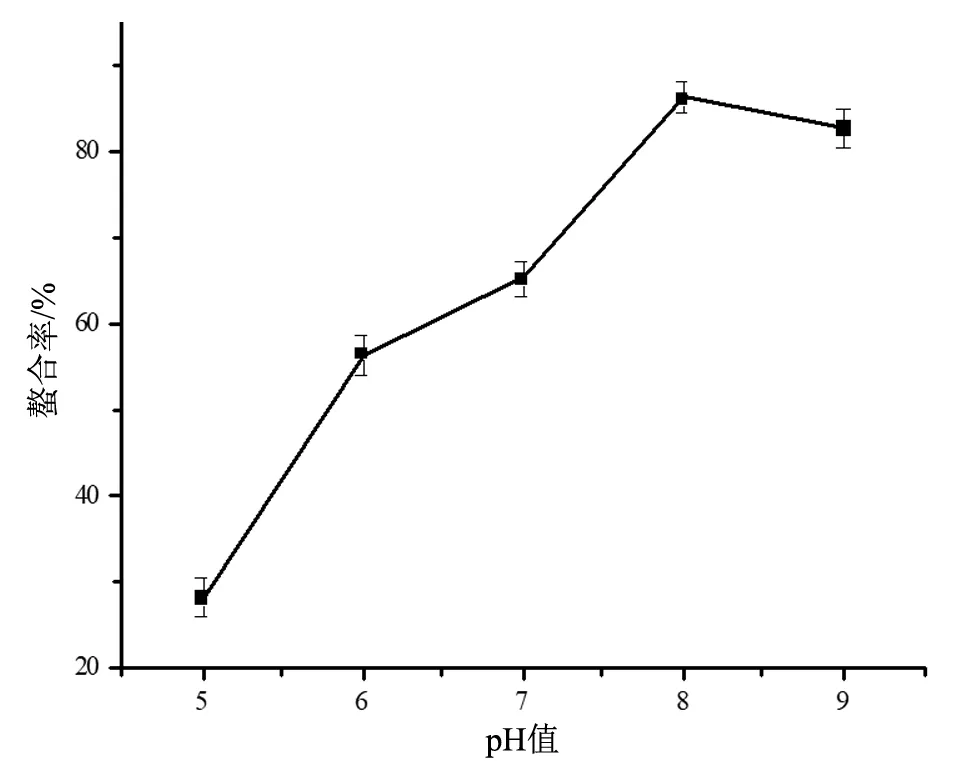
圖2 pH值對螯合率的影響
2.1.3 溫度對螯合率的影響
不同反應溫度對螯合率的影響如圖3所示。由圖3所知,螯合率隨著溫度的增加先上升后下降,當溫度達到100 ℃時,螯合率達到最大值,當溫度大于100 ℃時螯合率開始降低,可能是因為溫度的升高會促進溶液中離子的運動,使更多的結合位點暴露在溶液中,加快螯合的速度,但是溫度過高,溶液中的離子振動劇烈,不利于反應的進行,導致螯合率又發生下降。因此選擇100 ℃為響應面試驗中心點。

圖3 反應溫度對螯合率的影響
2.2 響應面試驗結果
2.2.1 響應面模型的建立
在上述單因素實驗優化的基礎上,選擇反應時間(A)、pH值(B)、溫度(C)為自變量,螯合率(Y)為響應值,并用Design-Expert8.0.6軟件進行分析,試驗設計方案及結果見表2。對實驗結果進行回歸擬合分析,得到的二次回歸方程為:Y=92.52-0.91A-4.92B-1.86C+3.67AB-0.40AC+4.43BC-3.29A2-7.41B2-5.48C2。

表2 響應面試驗設計方案及結果


表3 回歸模型方差分析表
由表3可知,各因素對螯合率影響的順序為:B(pH值)> C(溫度)>A(時間),其中B達到極顯著水平;二次項B2和C2均為極顯著,A2為顯著;交互項因素BC為極顯著,AB和AC達到顯著水平。
2.2.2 響應面圖分析
各因素之間相互作用的等高線圖和響應面曲線圖見圖4。通過等高線圖和響應面圖可直觀地判斷出各交互因素之間對響應值的影響程度,交互項因素對響應值的影響程度越大,等高線圖趨于橢圓形,響應面曲線圖較陡;交互項因素對響應值的影響程度越小,等高線圖趨于圓形,響應面曲線圖較平緩。由圖4可知,C中等高線圖呈橢圓形,響應面曲線圖較陡,因此,BC的交互作用影響最顯著,這與表3分析結果一致。


圖4 各交互因素對向日葵果膠鋅螯合率的等高線圖和響應面曲線圖
2.2.3 響應面模型的驗證試驗
由軟件Design 8.0.6預測得到的最佳工藝參數為:反應時間81.51 min,pH值7.45,溫度92.41 ℃,螯合率為94.41%。為了考慮實際操作方便,選擇反應時間85 min,pH值8,溫度95 ℃為制備條件進行三次平行驗證實驗,在該條件下得到螯合率為93.8%±0.41%,與預測值接近,說明該模型可靠。
2.3 結構分析
2.3.1 紅外光譜分析
圖5為向日葵果膠和向日葵果膠鋅的紅外光譜圖。圖中3 422 cm-1附近為-OH伸縮振動吸收峰,在向日葵果膠鋅圖中-OH吸收峰減弱,2 925 cm-1處為C-H伸縮振動吸收峰,1 757和1 612 cm-1分別為酯基和羧基中的C=O伸縮振動吸收峰,而在向日葵果膠鋅譜圖中1 757 cm-1處的吸收峰明顯消失,有可能是因為果膠中的-OH和C=O與鋅離子發生了螯合;1 170~988 cm-1為C-O的伸縮振動吸收峰,向日葵果膠鋅與果膠紅外譜圖中相比明顯減弱,復合物中857 cm-1附近出現新的峰可能是Zn-O彎曲振動吸收峰[10];向日葵果膠鋅在800~400 cm-1峰形與果膠譜圖中比較發生了明顯的改變,可能是因為果膠和鋅發生螯合所導致的。這些變化表明已成功制備向日葵果膠鋅。

圖5 向日葵果膠和向日葵果膠鋅的紅外光譜圖
2.3.2 XRD分析
圖6為向日葵果膠和向日葵果膠鋅的XRD譜圖,向日葵果膠鋅在5°~40°處有較多尖銳的衍射峰,表明向日葵果膠鋅呈結晶型;而向日葵果膠沒有明顯的衍射峰,說明向日葵果膠呈無定型。兩種物質在XRD譜圖中這些明顯的變化表明向日葵果膠鋅已被成功制備。

圖6 向日葵果膠和向日葵果膠鋅的XRD圖
3 結論
1)通過響應面實驗結果可知:單因素對螯合率的影響順序為B(pH值)> C(溫度)>A(時間);交互項因素對螯合率的影響順序為BC>AB>AC。
2)制備向日葵果膠鋅的最佳制備工藝條件為反應時間85 min,pH值8,溫度95 ℃;在該條件下向日葵果膠鋅的螯合率為93.8%±0.41%。
3)FTIR、XRD分析結果表明向日葵果膠鋅中Zn-O鍵的形成且呈結晶型,證明了向日葵果膠鋅成功制備,為開發一種新型鋅補充劑提供了理論依據。

