PICC相關性血栓風險預測模型的系統評價
蘇效添,紀 錚,王秋舟,胡小霞,陳虹秀,付 嵐,張曉霞,3,4*
1.四川大學華西醫院,四川 610041;2.四川大學華西護理學院;3.四川大學華西醫院護理創新研究中心;4.護理學四川省重點實驗室
經外周置入中心靜脈導管(PICC)具有操作安全簡單、維護方便、成本效益低、留置時間長、可輸注高濃度刺激性藥物等優點,目前已廣泛應用于臨床[1]。PICC相關性血栓(peripherally inserted central catheter-related thrombosis, PICCRT)是最常見和最嚴重的并發癥之一,研究報道其發病率為1.9%~71.9%[2-6],是導致PICC 非計劃拔管的首要原因[7-9],可影響病人正常治療的進行和增加病人醫療費用支出。對PICCRT 的管理,關鍵在于對PICCRT 的發生風險進行評估,并根據發生風險分層采取針對性和個體化的預防措施[10-14]。目前,臨床應用較多的Caprini 量表和Autar 量表更適用于篩查下肢靜脈血栓,其針對PICCRT 的發生風險評估缺乏敏感性和特異性[15-17]。因此,近年來國內外越來越多的研究者開始針對PICCRT 開發專門的風險預測模型[10,18-26]。然而,對這些PICCRT 風險預測模型的構建過程、模型性能、內外部驗證情況等缺乏全面系統的了解和比較。因此,本研究旨在全面檢索國內外有關PICCRT 風險預測模型的研究,對其基本特征、構建過程、預測性能和驗證方法等進行評價和分析,為臨床工作者選擇合適的PICCRT 風險預測模型提供科學的參考。
1 資料與方法
1.1 文獻檢索 系統檢索國內外數據庫,包括PubMed、EMbase、Web of Science、萬方、維普和知網,檢索時限為建庫至2021 年8 月30 日。中文數據庫以萬方為例,檢索詞包括:中心靜脈導管、中心靜脈置管、經外周靜脈置入中心靜脈導管、PICC、預測模型、風險分層、風險評分、評估量表、評分量表、靜脈血栓、靜脈栓塞、肺動脈栓塞、肺動脈血栓、VTE(靜脈血栓栓塞癥)等;英文檢索詞包括:peripherally inserted central catheter,central venous catheter,central venous catheterization,central vein catheter,central line,central vascular catheter,central venous access,CVC,PICC,clinical prediction model,clinical prediction rule,risk prediction model,predictive model, risk score, predictive score, risk assessment score,scale,venous thrombosis,venous thromboembolism,deep vein thrombosis, thromboembolic disease, VTE等;檢索策略為主題詞結合自由詞。此外,通過手工檢索,閱讀檢索文獻的參考文獻以尋找符合納入標準的研究。本研究已在PROSPERO 網站注冊,注冊號為:CRD42021283761。
1.2 文獻納入與排除標準
1.2.1 納入標準 ①研究對象為PICC 置管病人;②研究內容為PICC 置管病人靜脈血栓或肺動脈栓塞臨床預測模型的構建和/或驗證;③相同內容重復發表的研究選擇發表時間更近或內容更全的研究。
1.2.2 排除標準 ①研究對象包含置入其他類型中心靜脈導管(頸內靜脈、鎖骨下靜脈或股靜脈置管或輸液港)的病人;②只分析了PICCRT 危險因素,未進行風險預測模型構建的研究;③通過定性研究構建PICCRT風險預測模型的研究;④會議摘要或無法獲得全文而無法提取有效信息的研究。
1.3 文獻篩選與資料提取 首先,由2 名研究者根據納入、排除標準閱讀題目和摘要進行文獻初篩;再仔細閱讀全文,確定完全符合標準的研究。根據Moons等[27]制定的專門用于風險預測模型系統評價資料提取的CHARMS 清 單(checklist for critical appraisal and data extraction for systematic reviews of prediction modelling studies),預先制定本研究的資料提取表格,由2 名研究者獨立進行資料提取。提取資料包括研究基本特征(第一作者、發表年份、國家、研究設計、研究類型、研究對象、樣本量、隨訪時間)、預測模型具體情況(建模方法、預測變量篩選方法、缺失值處理方法、模型預測性能、模型呈現方式、預測因子及個數)、模型驗證情況等。在文獻篩選和資料提取過程中,若2 名研究者間存在分歧,則討論解決,必要時由第3 名研究者判斷并達成一致。
1.4 文獻質量評價 采用Wolff 等[28]開發的針對個體預后或診斷多因素預測模型研究的偏倚風險評估工具(Prediction Model Risk of Bias Assessment Tool,PROBAST)對納入文獻進行質量評價。PROBAST包含4 個方面共20 個條目,主要從研究對象(2 個條目)、預測因子(3 個條目)、結果(6 個條目)和統計分析(9 個條目)等方面對預測模型進行質量評價。由2 名研究者獨立對所有納入分析的研究進行質量評價,意見存在分歧時則討論解決,必要時由第3 名研究者判斷并達成一致。
1.5 統計學方法 由于納入的研究異質性較大且結果的報告存在較大差異,無法進行定量合成分析。因此,本研究只進行定性分析,通過描述性統計分析對納入的研究進行總結、分析和比較。
2 結果
2.1 文獻檢索結果 本研究最終納入13 篇文獻,其中中文文獻8 篇[18,20-25,29],英文文獻5 篇[11-14,30],具體文獻篩選流程見圖1。
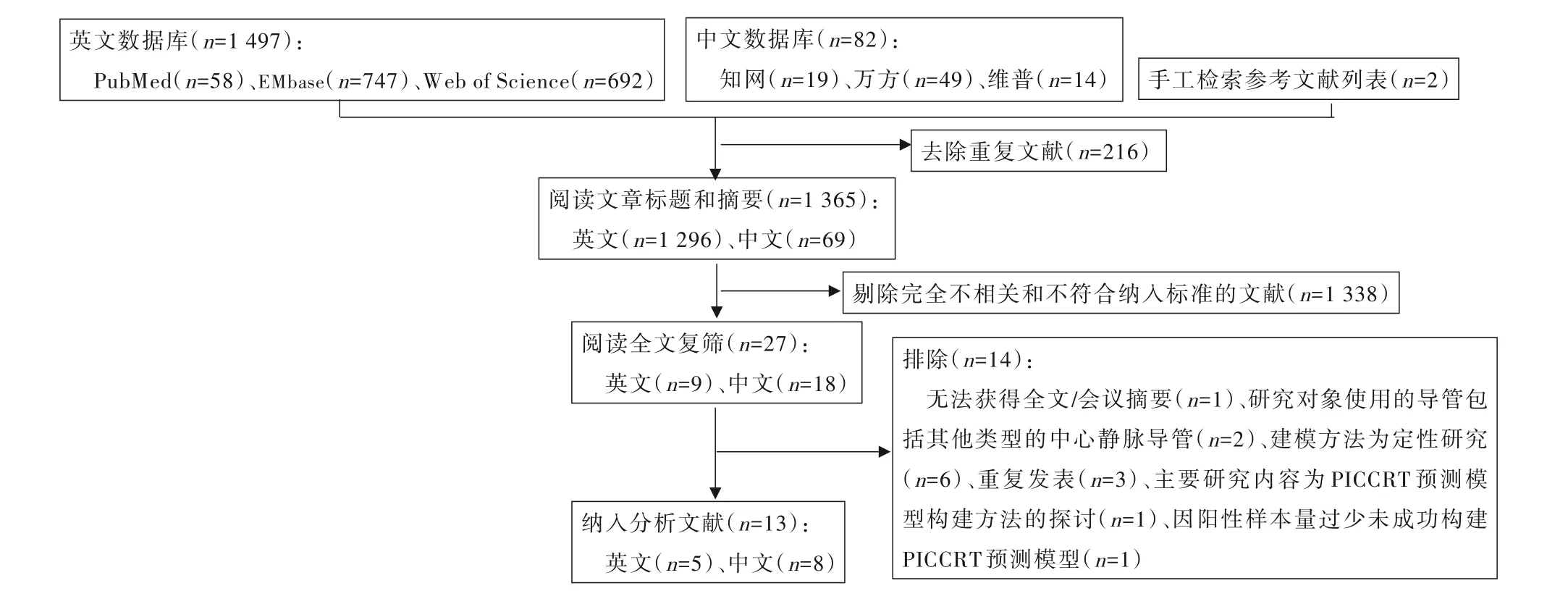
圖1 文獻篩選流程
2.2 納入文獻基本特征 53.8%(7/13)的PICCRT風險預測模型發表在近5 年內,發表國家主要為中國(n=11)和美國(n=2)。5 篇[12,20,24-25,29]研究為模型開發,8 篇[11,13-14,18,21-23,30]為模型開發及內部或外部驗證;6 篇[14,18,20,22-23,29]研究采用的是前瞻性隊列研究設計,5 篇[11-13,25,30]為回顧性隊列研究設計,2 篇[21,24]為系統評價;研究人群以腫瘤病人(n=7)為主,其余涉及老年病人、內科和重癥監護室(ICU)病人等;研究樣本量為233~47 090 人。基本特征詳見表1。
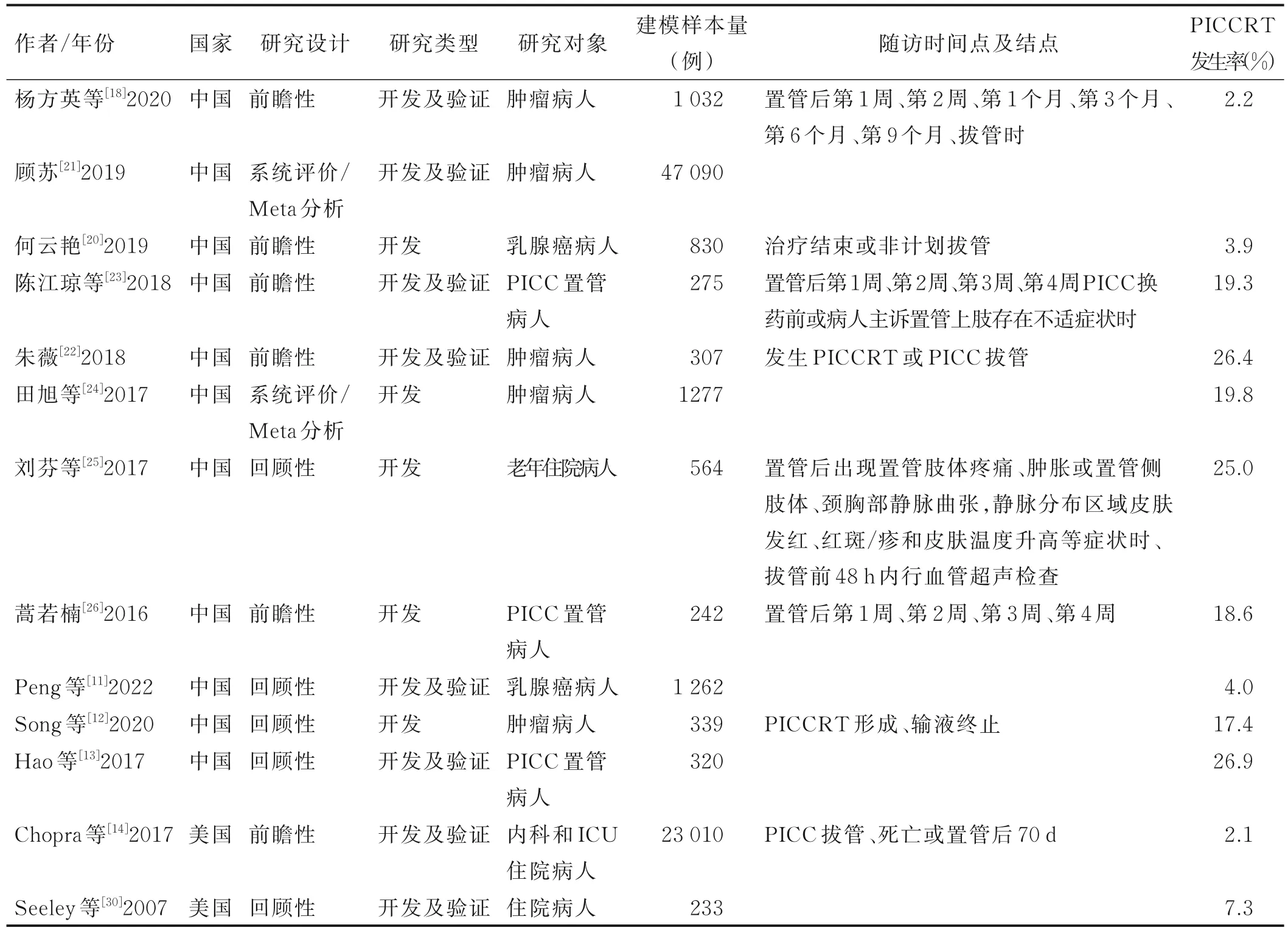
表1 納入研究基本特征
2.3 建模方法、模型呈現、預測性能及驗證情況 建模方法主要為Logistic 回歸(n=11)和Cox 回歸(n=2)。模型呈現形式以評分量表為主(n=9),其余呈現形式包括列線圖(n=2)、回歸方程式(n=2)。11 個模型報道了其預測性能,其中5 個模型[11,13-14,18,20]同時報道了其預測準確度和校準度。在報道了模型準確度的研究中,ROC 曲線下面積(area under curve,AUC)或C 指數為0.64~0.89,靈敏度為62.96%~88.20%,特異度為72.20%~89.04%。具體信息見表2。5 項研究對報道了預測模型內部驗證的具體方法[11,13-14,18,23],主要為Bootstrap 重抽樣或樣本拆分。4 個模型進行了外部驗證[13,21-22,30],其中僅Hao 等[13]的模型在外部驗證中同時評估了模型的區分度與校準度,其余均只評估了模型的區分度。朱薇[22]、顧蘇[21]、Hao 等[13]構建的預測模型在外部驗證中AUC 值或C 指數大于0.7,Seeley 等[30]構建的模型在我國腫瘤化療病人人群中的驗證結果較差,AUC 值小于0.7。具體信息見表3。
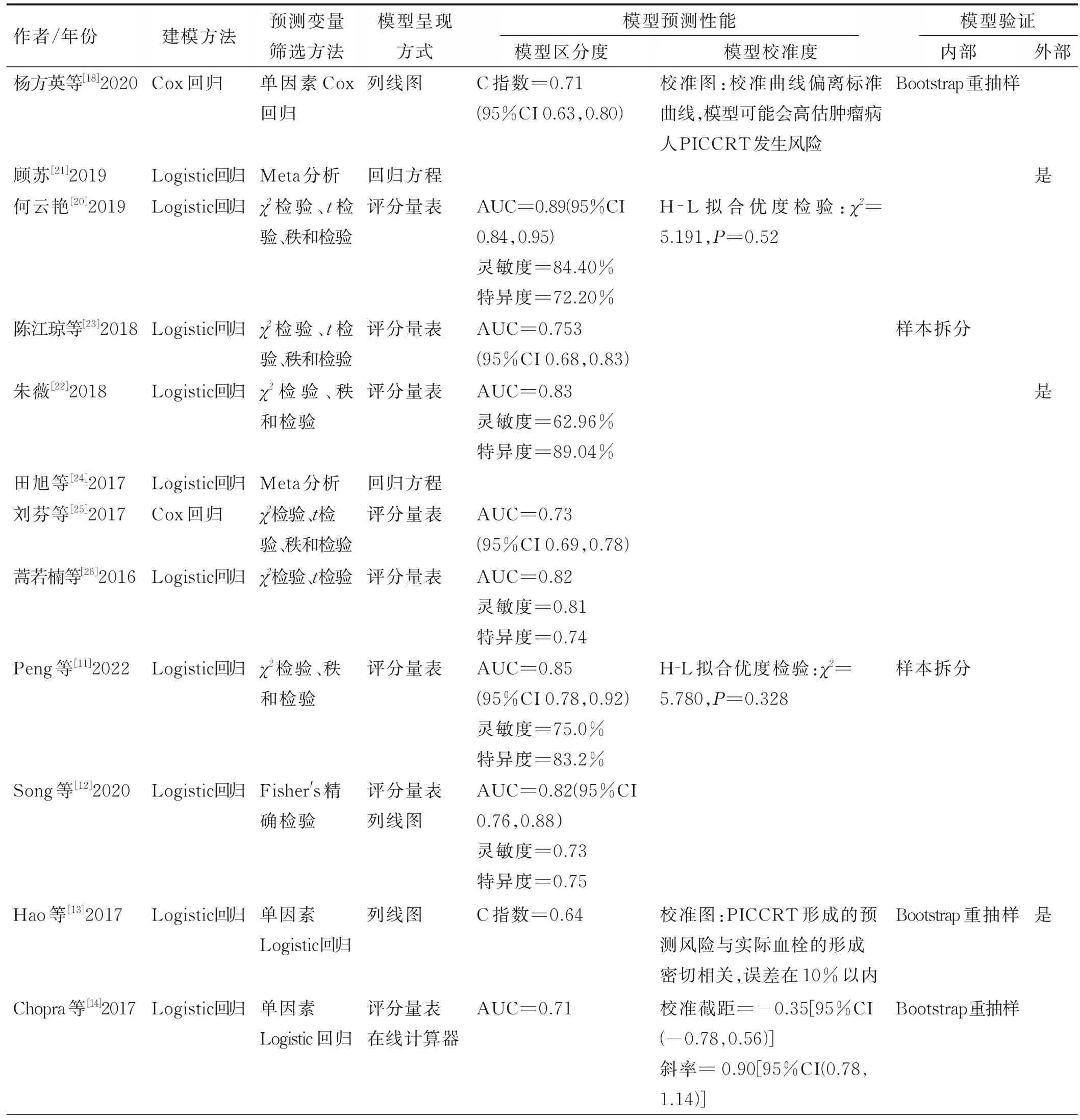
表2 PICCRT 風險預測模型建模方法、模型呈現及預測性能情況
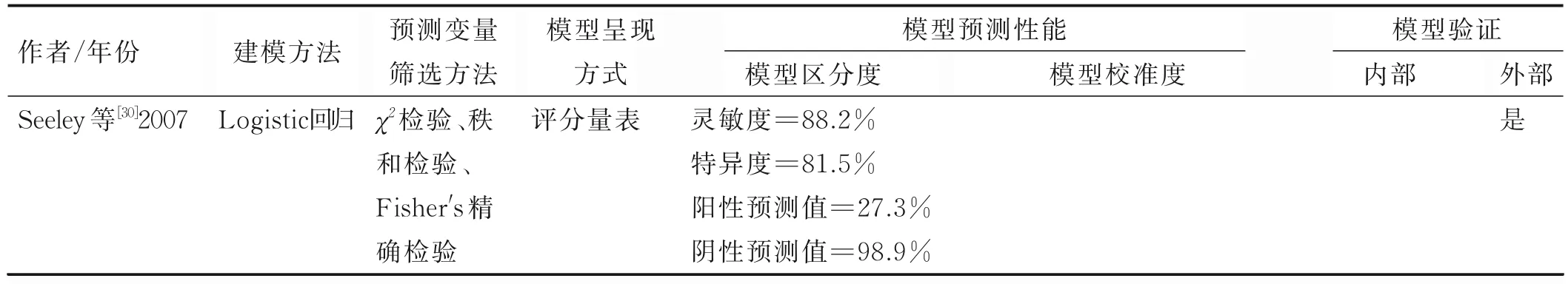
(續表)
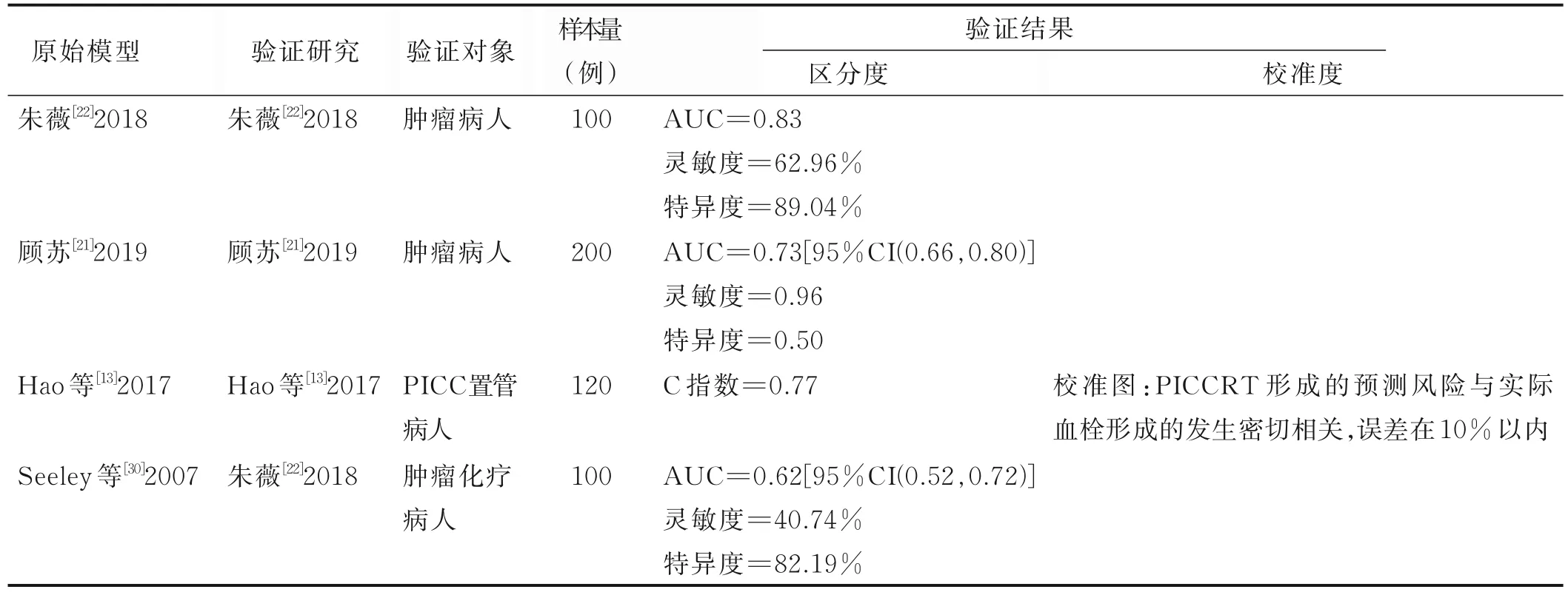
表3 PICCRT 風險預測模型外部驗證研究情況
2.4 模型預測因子及賦值情況 最終納入預測模型的預測因子個數為2~13 個,出現頻次最高的預測因子包括D-二聚體、化療史、血栓史、糖尿病、肥胖或體質指數(BMI)≥25 kg/m2、導管尖端位置異位/非最佳位置以及白細胞計數升高;賦值較高的預測因子包括化療史、血栓史、白細胞計數升高、導管尖端異位/非最佳位置、肥胖或BMI≥25 kg/m2、糖尿病、導管相關性感染、活化部分凝血活酶時間(activated partial thromboplastin time,APTT)、體力狀況評分(PS)>1 分、使用3 腔或4 腔導管、因骨髓炎置管等。76.9%(10/13)的模型[11-12,14,20-23,25,29-30]可根據病人的評分情況,將其劃分為PICCRT 發生低危、中危或高危組等。詳見表4。
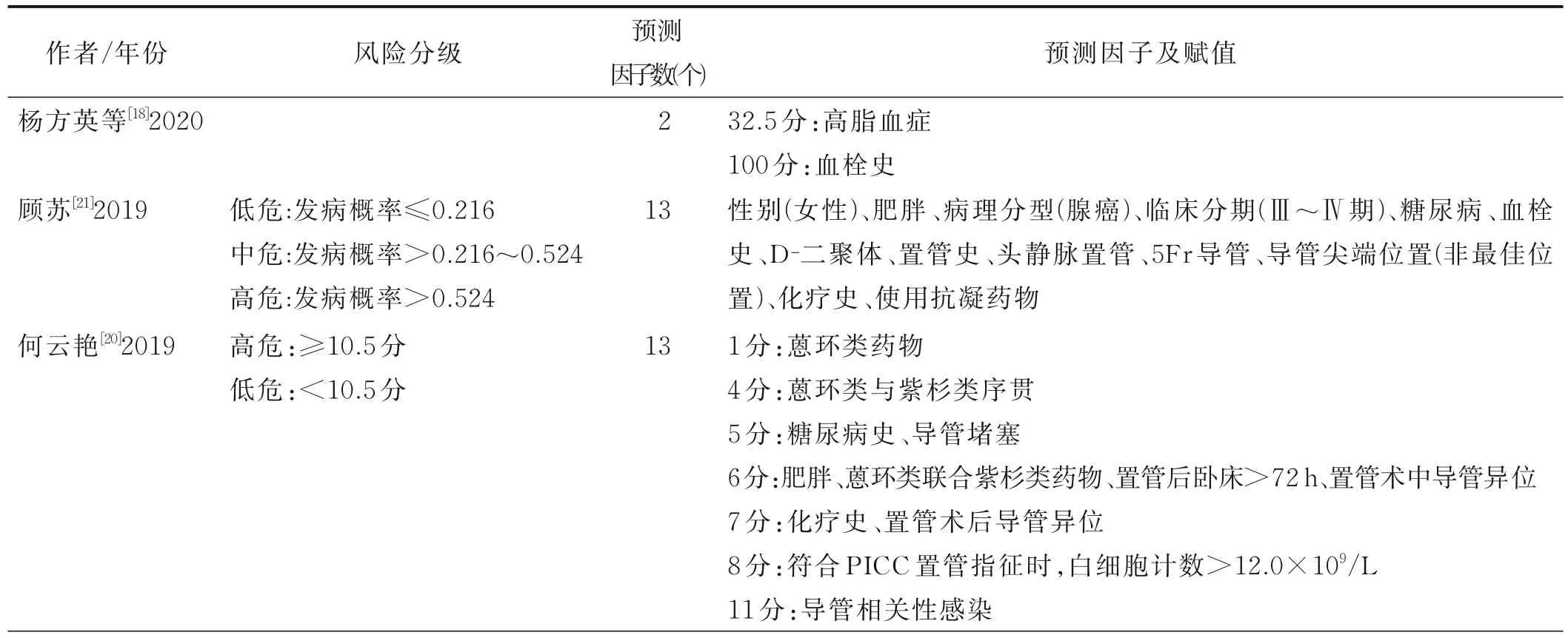
表4 PICCRT 風險預測模型預測因子及賦值情況
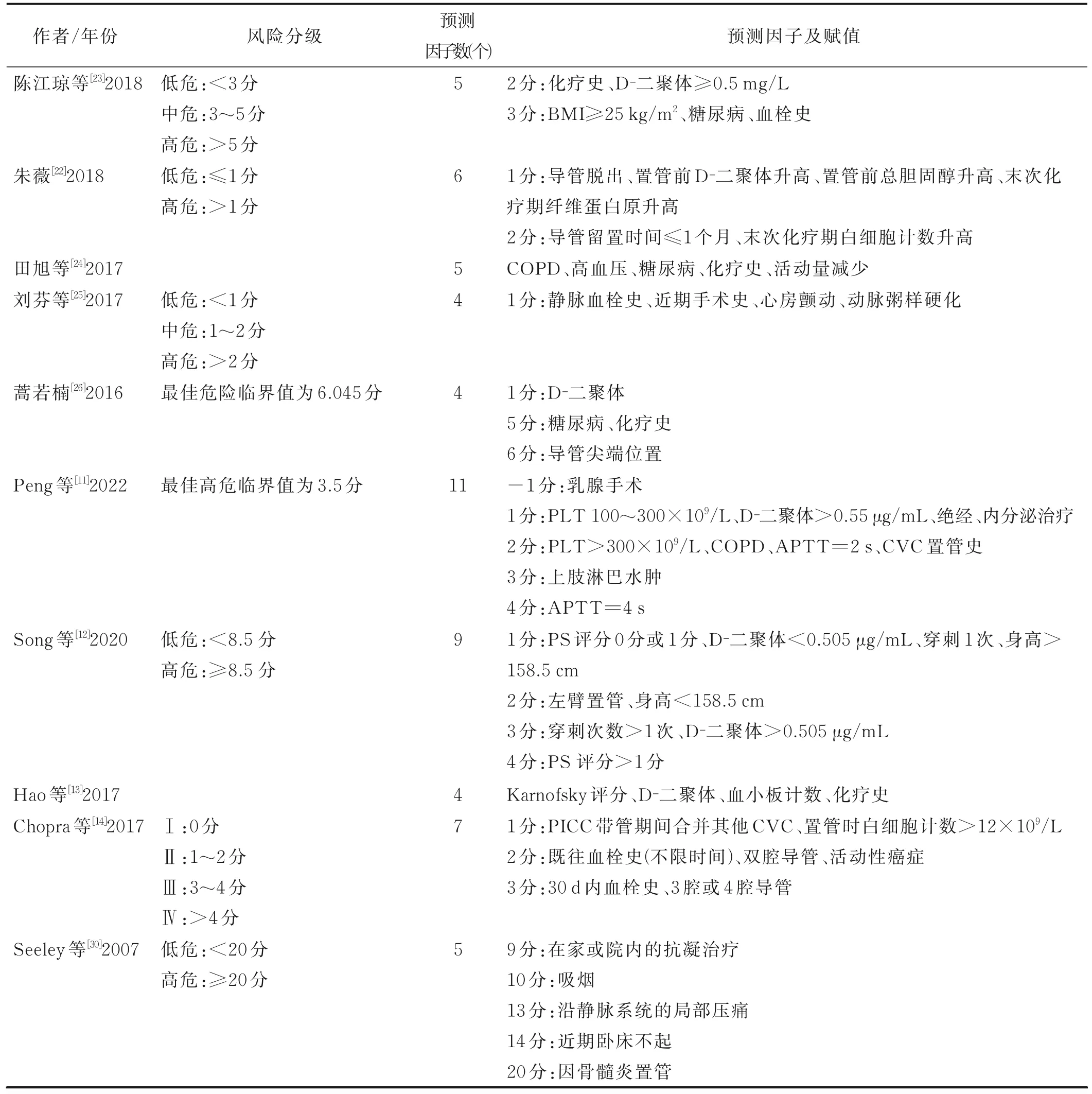
(續表)
2.5 納入分析研究質量評價 采用PROBAST 對納入研究進行質量評價。在研究對象領域,8 篇研究為高偏倚風險或偏倚風險不清楚,主要是由于這8 篇研究數據來源于回顧性隊列研究或未報告研究對象來源;其余5 篇研究為低偏倚風險。在預測因子領域,7 篇研究為偏倚風險不清楚,主要是由于這7 項研究未說明評估者是否是在不了解結果信息的情況下評估的預測因子。在結果領域,7 篇研究為偏倚風險不清楚,主要是由于這7 項研究未說明評估者在確定結果時是否清楚預測因子情況或未報告預測因子評估和結果確定的時間間隔信息。在統計分析領域,13 篇研究均為高風險,主要是由于在模型開發中每個自變量的事件數(events per variable,EPV)小于10、未報告缺失值的情況及其處理方法、基于單因素分析法篩選預測因子或未對校準度和區分度進行評估。整體評估結果顯示,Chopra 等[14]構建的Michigan 預測模型偏倚風險低,其余研究偏倚風險較高。見表5。
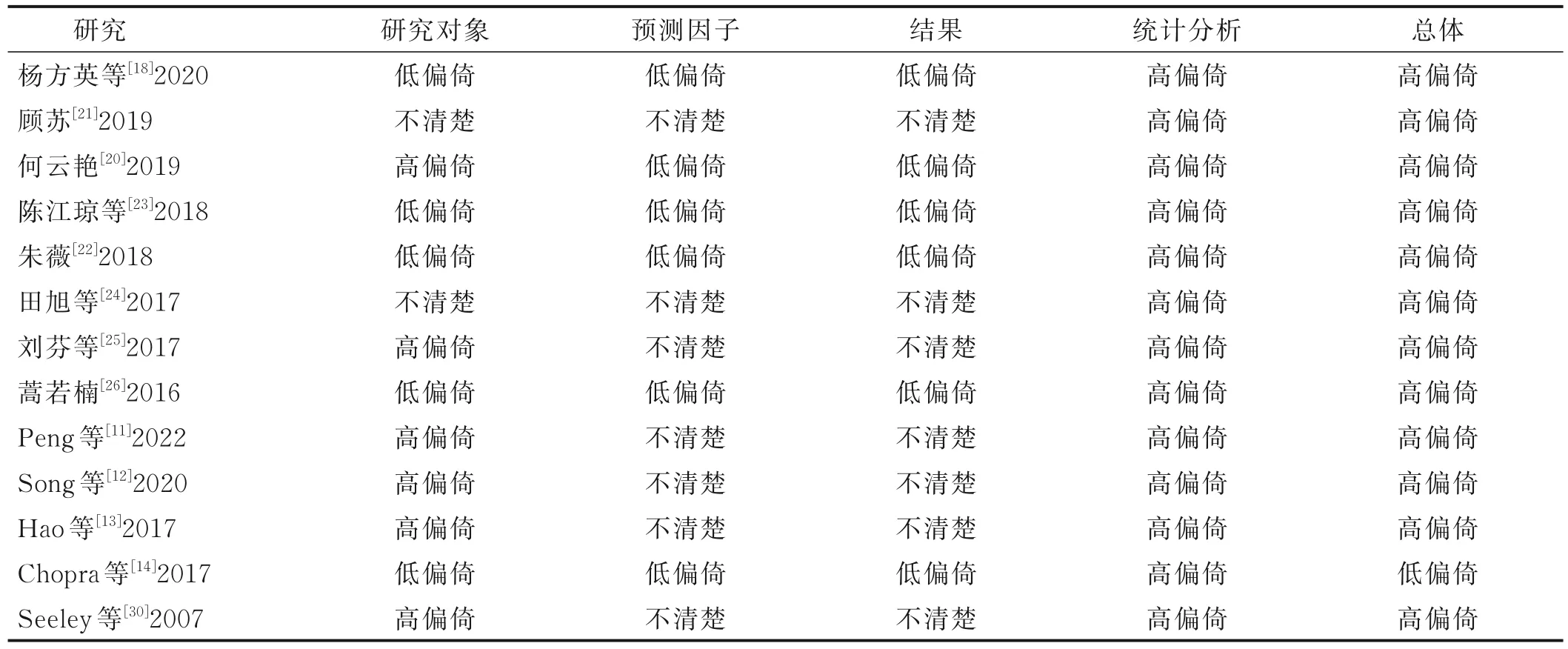
表5 納入文獻質量評價結果
3 討論
PICCRT 發生率高、臨床后果嚴重,采用PICCRT風險評估工具可早期識別高風險人群,進而及早采取預防措施,降低PICCRT 發生率。本系統評價共納入13 個PICCRT 風險預測模型進行分析,其建模人群主要為腫瘤病人,建模方法以Logistic回歸為主,模型呈現形式主要為評分量表,最常見且賦值較高的預測因子包括化療史、血栓史、糖尿病、肥胖或BMI≥25 kg/m2、導管尖端位置異位/非最佳位置及白細胞計數升高等;大部分模型的區分度較好(AUC 或C 指數>0.7),但缺乏對模型校準度的評估及模型外部驗證。
3.1 PICCRT 風險預測模型對臨床工作的指導意義 研究顯示,早期、精準識別血栓高危病人并采取相應措施,可使其發生風險降低50%~60%[31-33]。本研究納入的13 個預測模型中,有9 個預測模型的AUC 值或C 指數大于0.7,說明這9 個預測模型的預測準確度高,能夠準確識別出PICCRT 高危人群。一個好的預測模型,除了需要較高的預測準確性外,其使用便捷性也非常重要。本研究納入的預測模型的預測因子個數為2~13 個,且大部分預測因子可客觀測量、易收集、檢測成本低,相較于傳統的評估量表,這些預測模型使用時更省時、省力,且獲得的結果更客觀可靠。此外,有10 個預測模型進行了風險劃分,評估者可根據病人得分情況將其劃分到低危、中危、高危組等,這在臨床實踐中有助于醫護人員根據病人所處風險等級制訂和采取相應的防治措施。
進一步分析預測模型納入的預測因子可發現,最常見且在各預測模型中賦值較高的預測因子包括化療史、血栓史、糖尿病、肥胖或BMI≥25 kg/m2、導管尖端位置異位/非最佳位置及白細胞計數升高,這些預測因子已被眾多研究證實是導致PICCRT 形成的重要危險因素[3,34-38]。因此,在臨床工作中,醫務人員需更加重視伴有以上危險因素的PICC 置管病人。從危險因素是否可干預這一角度分析以上這些重要的預測因子,除導管尖端位置異位/非最佳位置是PICC 操作者可控制和干預的預測因子外,其余均為病人在置管前就已攜帶的因素,因此,醫務人員難以針對這些因素采取干預措施,只能采取普適性措施,如多運動、多飲水等來預防PICCRT。一項研究將PICCRT 的危險因素劃分為系統性和局部危險因素2 個方面,且證實了在導致PICCRT 形成的過程中,局部危險因素的作用效應大于全身性危險因素[39]。系統性危險因素主要是指病人相關危險因素,如高凝狀態、肥胖、高齡等,這些也是難以進行干預的危險因素;局部危險因素主要是指與PICC 置管技術相關的危險因素,如置管靜脈血流速度、導管血管直徑比值、穿刺次數等。與系統性危險因素相比,局部危險因素的可干預性更強,醫務人員更易根據病人情況制訂相應的干預措施,如針對置管靜脈血流速度慢的病人,可通過加強置管側手臂的鍛煉來加快局部血流速度[40-41];針對血管較細的病人,可通過選擇直徑更小的導管使導管血管直徑比值控制在0.45以內來降低PICCRT的發生風險[42]。現有的PICCRT預測模型幾乎未將局部危險因素納入建模的候選預測因子當中,因此,在今后優化現有預測模型或開發新的PICCRT 風險預測模型時,研究者可考慮將局部危險因素作為預測因子納入預測模型,有望進一步提高預測模型的準確性和臨床實用性。
3.2 PICCRT 風險預測模型建立過程、模型驗證及結果報告情況分析 雖然本研究納入的大部分PICCRT風險預測模型的預測準確性高、使用便捷,但其建立過程、模型驗證和結果報告還需進一步完善和探討。模型的初步建立過程包括確定研究問題、選擇數據來源、篩選預測變量、處理預測變量和擬合預測模型等步驟。在確定研究問題上,本系統評價納入的研究涉及人群包括腫瘤、老年及ICU 病人。Chopra 等[43]的一項系統評價顯示,在PICC 置管人群中,ICU、腫瘤和老年病人的血栓發生風險最高,且不同病種或人群的PICCRT危險因素具有一定的特異性,因此,非常有必要針對這些高危人群構建專門的PICCRT 風險預測模型。本研究結果顯示,關于腫瘤人群的PICCRT 風險預測模型已非常多,而針對ICU 和老年病人的預測模型較少,因此,在今后的研究中研究者可更多地開發針對ICU 和老年PICC 置管病人的血栓風險預測模型。
在數據來源上,來自前瞻性研究的數據代表性好且可靠,回顧性研究可能存在信息偏倚,因此,在建立預后模型時來自前瞻性研究的數據是最推薦的[44-45]。本研究納入的預測模型中,僅6 個模型是在來自前瞻性隊列研究的數據基礎上構建的,其余采用的是回顧性研究的數據。因此,建議今后在開發或優化模型時,盡量采用前瞻性隊列研究、病例對照研究或巢式病例-對照研究,以盡量降低信息偏倚對模型構建的影響。在篩選預測變量上,大部分研究都采用的單因素分析。目前一些新的預測變量篩選方法,如LASSO 回歸,受到越來越多研究的重視,應用逐漸廣泛[44]。與單因素分析相比,LASSO 回歸具有降低備選預測因子多重共線性的優點,適用于備選預測因子多的情況[46]。在今后PICCRT 風險預測模型建立的研究中,可根據實際應用情況考慮使用該方法來篩選預測因子。在處理預測變量上,缺失值的處理和不同類型變量的處理是最常見的問題,這直接影響著模型的建立。在處理缺失值時,統計學專家推薦采用多重插補法;在處理連續性變量時,不推薦在模型構建初期就將其轉換為分類變量,因為這會損失大量的信息[44]。然而,本系統評價納入的研究中,除Chopra 等[14]的研究外,均未報道缺失值的處理方法,連續性變量也幾乎在模型構建初期就已轉化為分類變量。
在預測模型性能評估上,本研究納入的大部分預測模型表現出了良好的預測效能,且大部分是基于我國人群構建的,說明其具有良好的應用潛能,但存在模型性能評價不完整、缺乏外部驗證或外部驗證范圍小等問題。評價模型性能的指標主要包括區分度和校準度,其中區分度常用AUC 值或C 指數來表示,AUC 值或C 指數大于0.7 時,可認為模型區分度較好;校準度常用Hosmer-Lemeshow 擬合優度檢驗、Brier 得分等方法來評價[47]。一個好的預測模型需同時具備較好的區分度和校準度。在本系統評價納入的研究中,有11篇研究評價了模型的區分度,但其中僅5 篇研究同時評價了校準度,這使得模型性能的評價不夠完整,在一定程度上限制了其推廣和應用。在模型驗證上,5 個預測模型進行了內部驗證,4 個模型進行了外部驗證,僅有1 個模型同時進行了內部和外部驗證,模型驗證的范圍也較局限。這是目前整個預測模型研究領域存在的一個共性問題,即模型開發類研究蓬勃發展,模型驗證卻存在滯后[47]。因此,為了促進預測模型開發向臨床應用轉化,在今后的研究中需要進一步對這些預測模型進行優化和外部驗證,全面評估其預測性能,促進其在臨床的推廣和應用。
此外,在結果報告方面,幾乎所有納入的研究都未按照《個體預后與診斷的多變量預測模型透明報告》(TRIPOD)進行報告,這使得大部分預測模型構建的具體過程不夠透明,影響了這些研究的文獻質量評價結果。因此,建議研究者參考TRIPOD 對所構建的預測模型進行報告,以提高預測模型構建過程的透明性。
3.3 本研究的局限性 本系統評價存在以下局限性:①本研究僅納入分析了以中文和英文發表的PICCRT風險預測模型;②由于納入的研究在研究設計類型、模型構建方法、結局指標隨訪時間等方面存在較大異質性,因此只進行了定性分析;③由于本研究系統評價內容不夠具體,未對研究對象、預測因子與結果評估的時間間隔等進行明確的界定,因此未對納入的研究進行適用性風險評估。
4 小結
本系統評價共納入13 個PICCRT 風險預測模型,大部分預測模型預測準確度較高,但整體研究質量偏低,仍需從模型構建過程、模型驗證和結果報告等方面進一步優化,以構建預測性能優良、使用便捷的PICCRT風險預測模型,為臨床醫務工作者早期識別PICCRT 高危人群提供可靠、科學的工具。

