例談中考化學“工藝流程題”熱點題型


摘 要:工藝流程題常以“生產工藝”或“實驗操作流程”為素材,將化工生產過程或實驗操作過程中的主要步驟以流程圖的方式呈現出來,考查考生對化學知識的掌握,以及分析問題和解決問題的能力.據此,文章對中考工藝流程題的考查內容及其常見題型進行了分類和總結.
關鍵詞:題型;工藝流程;中考化學
中圖分類號:G632?? 文獻標識碼:A?? 文章編號:1008-0333(2023)35-0137-03
工藝流程試題是近年來中考化學試題的特色之一.此類試題就是將化工生產過程中的主要生產階段即生產流程用框圖形式表示出來,并根據生產流程中有關的化學知識步步設問,形成與化工生產緊密聯系的化工工藝試題[1].
1 分離、提純和除雜流程
例1 (2023·廣東廣州)制鹽在我國有著悠久的歷史.某鹽湖水樣品含有NaCl、Na2SO4及少量MgSO4和CaSO4,某小組從中獲取NaCl和Na2SO4的主要過程如圖1所示.
(1)“除雜1”應依次加入的兩種試劑是_______、_______,“除雜2”應加入的試劑是_______.[除雜限選試劑:HCl、HNO3、Na2CO3、Ca(OH)2]
(2)將“溶液A”在80 ℃蒸發濃縮,至有少量固體析出.①該小組分析溶解度曲線(如圖2所示),推測析出的少量固體是NaCl,但檢驗后卻發現是Na2SO4.請做出合理解釋:_______.
②該小組停止蒸發濃縮,經_______、過濾得到大量Na2SO4固體及母液;將母液中的NaCl分離出來,操作是_______.
(3)設計由硫黃(單質硫)生產Na2SO4的轉化路徑,依次寫出反應的化學方程式:_______.(提示:常見+4價硫的化合物可與O2化合生成+6價硫的化合物)
解析 (1)樣品中含有的雜質是硫酸鎂和硫酸鈣,可將硫酸鎂或硫酸鈣轉化為氯化鈉和硫酸鈉.從雜質含有硫酸根離子可知,轉化為硫酸鈉較為容易,只需除去鎂離子和鈣離子,引入鈉離子即可.根據給出藥品,可以先加入過量氫氧化鈣,氫氧化鈣和硫酸鎂反應生成硫酸鈣和氫氧化鎂沉淀,之后加入碳酸鈉,碳酸鈉和硫酸鈣反應生成碳酸鈣沉淀和硫酸鈉,氫氧化鈣和碳酸鈉反應生成碳酸鈣沉淀和氫氧化鈉.過濾濾液中有氯化鈉、硫酸鈉、碳酸鈉、氫氧化鈉.雜質碳酸鈉、氫氧化鈉可以加入鹽酸轉化為氯化鈉,鹽酸和碳酸鈉反應生成氯化鈉、水和二氧化碳,氫氧化鈉和鹽酸反應生成氯化鈉和水.
(2)①80 ℃硫酸鈉的溶解度大于氯化鈉的溶解度,如氯化鈉和硫酸鈉的質量相等則氯化鈉先析出,但硫酸鈉先析出,則說明溶液中硫酸鈉的含量比氯化鈉高,硫酸鈉先達到飽和析出.②硫酸鈉的溶解度隨溫度變化較大,40 ℃后隨溫度的降低溶解度降低較多,氯化鈉的溶解度隨溫度的變化改變較小.所以開始經降溫結晶,過濾得到大量硫酸鈉固體與母液.然后可以通過蒸發結晶的方法從母液中將氯化鈉分離出來,操作時加熱蒸發溶劑至有較多晶體析出(溫度較高時硫酸鈉的溶解度又升高,不會因為低溫時飽和蒸發水而析出),趁熱過濾,洗滌,干燥.
(3)使用硫單質生產硫酸鈉,初中常見的硫單質的反應是硫和氧氣點燃生成二氧化硫,化學方程式為S+O2點燃SO2.根據堿的通性,氫氧化鈉可以和二氧化硫反應生成亞硫酸鈉和水,化學方程式為SO2+2NaOHNa2SO3+H2O.根據提示常見+4價硫的化合物可與O2化合為+6價硫的化合物,則亞硫酸鈉和氧氣反應可生成硫酸鈉,化學方程式為2Na2SO3+O22Na2SO4.
答案:略
2 混合物成分確定流程
例2 (2023·天津)某氯化鈉固體樣品中可能含有硫酸鈉、硝酸鋇、氯化鎂、硫酸銅和碳酸鈣中的一種或幾種.為確定其成分,取40 g固體樣品,按如圖3所示流程進行實驗.
回答下列問題:
(1)白色沉淀A的化學式為_______;
(2)寫出生成白色沉淀B的化學方程式_______;
(3)固體樣品中除氯化鈉外,還一定存在_______;
(4)已知實驗中得到2 g白色沉淀A,2.33 g白色沉淀B,5.8 g白色沉淀C,則固體樣品中氯化鈉的質量分數為_______.
解析 分析流程可知,取40 g固體樣品,加入足量水溶解,過濾,得到白色沉淀A和無色溶液1,向白色沉淀A中加入過量稀鹽酸,沉淀全部溶解;碳酸鈣難溶于水,能和鹽酸反應生成氯化鈣、水和二氧化碳,則白色沉淀A是碳酸鈣,原固體中一定有碳酸鈣;向無色溶液1中滴加氯化鋇溶液恰好完全反應,過濾,得到白色沉淀B和溶液2,向白色沉淀B中加入過量稀鹽酸,沉淀不溶解;硫酸鈉和氯化鋇反應生成不溶于酸的硫酸鋇沉淀,則白色沉淀B是硫酸鋇,原固體中一定有硫酸鈉;硫酸鈉和硝酸鋇不能共存,則原固體中一定沒有硝酸鋇;向溶液2中加入過量氫氧化鈉溶液,過濾,得到白色沉淀C和溶液3;過量氫氧化鈉和氯化鎂反應生成氫氧化鎂沉淀和氯化鈉,則白色沉淀C是氫氧化鎂,溶液3中有過量的氫氧化鈉;向溶液3中加入過量的稀鹽酸,稀鹽酸和剩余的氫氧化鈉反應生成氯化鈉和水,再通過蒸發、結晶,過量的鹽酸揮發,得到氯化鈉固體.(1)由分析可知,白色沉淀A是碳酸鈣,化學式為CaCO3;(2)由分析可知,生成白色沉淀B的反應是氯化鋇和硫酸鈉反應生成硫酸鋇沉淀和氯化鈉,反應的化學方程式為BaCl2+Na2SO4BaSO4↓+2NaCl;(3)由分析可知,固體樣品中除氯化鈉外,還一定存在CaCO3、Na2SO4、MgCl2;(4)白色沉淀A是碳酸鈣,白色沉淀B是硫酸鋇,白色沉淀C是氫氧化鎂,實驗中得到2 g碳酸鈣,2.33 g硫酸鋇,5.8 g氫氧化鎂,反應的化學方程式和質量關系如下:
Na2SO4+BaCl2BaSO4↓+2NaCl
142233
1.42 g2.33 g
MgCl2+2NaOHMg(OH)2↓+2NaCl
9558
9.5 g5.8 g
則固體樣品中氯化鈉的質量分數為
40 g-2 g-1.42 g-9.5 g40 g×100%=67.7%.
答案:略
3 廢氣處理及空氣的利用
例3 (2023·湖北宜昌)2023年5月30日,我國“神舟十六號”載人航天飛船成功發射.為保證宇航員正常的生命活動,空間站內的空氣需與我們周圍的空氣組成相近,主要采用如圖4所示循環系統.
(1)空間站內空氣中含量最多且不會被宇航員消耗的氣體是_______(填化學式,下同),補充氧氣的化學反應有_______(填序號).空間站用活性炭凈化空氣,是利用它的_______性.
(2)反應④的化學方程式是_______;此系統中循環利用的物質有_______.
解析 (1)空間站內的空氣需與我們周圍的空氣組成相近,所以空間站內空氣中含量最多且不會被宇航員消耗的氣體是氮氣.反應①水的電解會生成氧氣,反應③二氧化碳與超氧化物反應也會生成氧氣.活性炭具有疏松多孔的結構,常利用活性炭的吸附性凈化空氣.(2)二氧化碳與氫氣在催化劑的催化下生成甲烷和水,反應化學方程式為CO2+4H2催化劑CH4+2H2O.反應①中水被消耗,反應④中水生成,水屬于循環利用物質;反應①中氧氣生成,反應③中氧氣消耗,氧氣屬于循環利用物質;反應①中氫氣生成,反應④中氫氣消耗,氫氣屬于循環利用物質;反應②中二氧化碳生成,反應③中二氧化碳消耗,二氧化碳屬于循環利用物質.
答案:略
4 工業生產流程
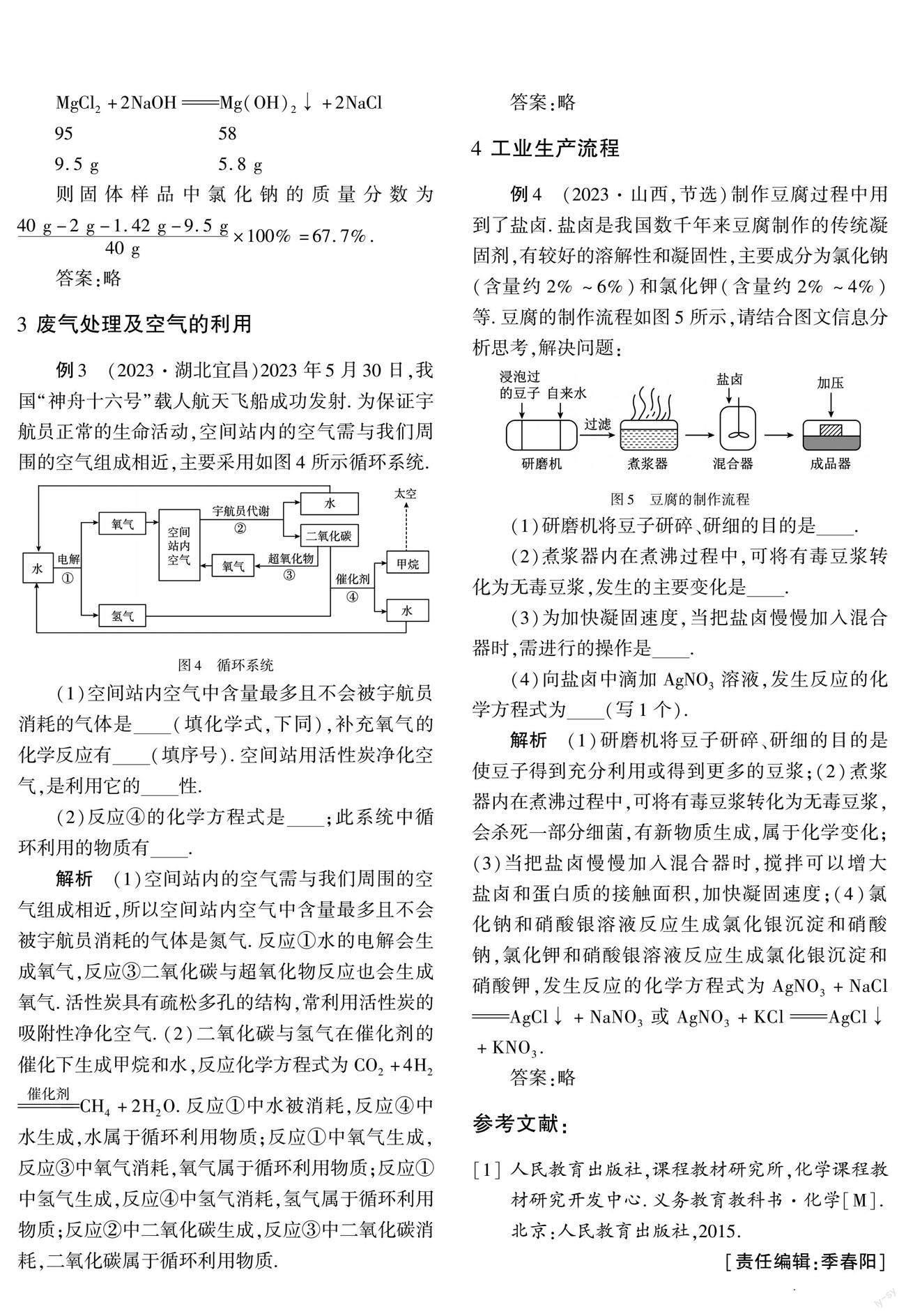
例4 (2023·山西,節選)制作豆腐過程中用到了鹽鹵.鹽鹵是我國數千年來豆腐制作的傳統凝固劑,有較好的溶解性和凝固性,主要成分為氯化鈉(含量約2%~6%)和氯化鉀(含量約2%~4%)等.豆腐的制作流程如圖5所示,請結合圖文信息分析思考,解決問題:
(1)研磨機將豆子研碎、研細的目的是_______.
(2)煮漿器內在煮沸過程中,可將有毒豆漿轉化為無毒豆漿,發生的主要變化是_______.
(3)為加快凝固速度,當把鹽鹵慢慢加入混合器時,需進行的操作是_______.
(4)向鹽鹵中滴加AgNO3溶液,發生反應的化學方程式為_______(寫1個).
解析 (1)研磨機將豆子研碎、研細的目的是使豆子得到充分利用或得到更多的豆漿;(2)煮漿器內在煮沸過程中,可將有毒豆漿轉化為無毒豆漿,會殺死一部分細菌,有新物質生成,屬于化學變化;(3)當把鹽鹵慢慢加入混合器時,攪拌可以增大鹽鹵和蛋白質的接觸面積,加快凝固速度;(4)氯化鈉和硝酸銀溶液反應生成氯化銀沉淀和硝酸鈉,氯化鉀和硝酸銀溶液反應生成氯化銀沉淀和硝酸鉀,發生反應的化學方程式為AgNO3+NaClAgCl↓+NaNO3或AgNO3+KClAgCl↓+KNO3.
答案:略
參考文獻:
[1] 人民教育出版社,課程教材研究所,化學課程教材研究開發中心.義務教育教科書·化學[M].北京:人民教育出版社,2015.
[責任編輯:季春陽]
收稿日期:2023-09-15
作者簡介:尹莉娟(1990.2-),女,江蘇省泗洪人,本科,中學一級教師,從事初中化學教學研究.

