發(fā)展證據(jù)推理水平的主題教學實踐與思考*
——以氯化銅和氨水反應為例
何銀華 肖中榮
(1.杭州市余杭第二高級中學 浙江 杭州 311100;2.杭州市基礎教育研究室 浙江 杭州 310000)
《普通高中化學課程課標(2017版)》要求教師積極開展素養(yǎng)為本的課堂教學實踐,主動探索素養(yǎng)為本的有效課堂教學模式和策略,[1]“我們已經(jīng)確定了8項核心素養(yǎng),目前的關鍵是如何評價它們,這方面的工作還很薄弱”[2]。證據(jù)推理是化學學科核心素養(yǎng),其內(nèi)涵如何解構(gòu),如何基于主題教學發(fā)展學生證據(jù)推理水平,本文以氯化銅和氨水反應為例進行研究。
一、證據(jù)推理的內(nèi)涵解構(gòu)
證據(jù)推理的內(nèi)涵為具有證據(jù)意識,能基于證據(jù)對物質(zhì)組成、結(jié)構(gòu)及其變化提出可能的假設,通過分析推理加以證實或證偽;建立觀點、結(jié)論和證據(jù)之間的邏輯關系。[3]本文從上述描述抽提出關鍵詞:證據(jù)意識、提出假設、分析推理、邏輯關系。“證據(jù)意識”是科學的循證思維,指說話辦事不能主觀臆測,要講事實、有根據(jù)。“提出假設”是發(fā)現(xiàn)問題的意識、提出觀點的能力。“分析推理”是由一個或幾個已知的判斷,推導出一個未知結(jié)論的思維過程。“邏輯關系”指事物或活動間的依賴關系,“觀點、結(jié)論和證據(jù)之間的邏輯關系”是指觀點、證據(jù)、結(jié)論之間要相互支持,形成關聯(lián)規(guī)則和因果機制,[4]符合科學論證的“相關性、充分性和可接受性的論證評價三角標準”[5]。
總之,化學學科核心素養(yǎng)證據(jù)推理是基于證據(jù)進行推理,本質(zhì)是科學論證,涉及識別、篩選證據(jù),轉(zhuǎn)換、形成證據(jù),應用、評價證據(jù),推理、形成結(jié)論的高級思維過程,[6]它強調(diào)收集證據(jù)的必要性、突出分析推理的過程性,彰顯觀點、結(jié)論和證據(jù)之間的邏輯性。
二、證據(jù)推理的水平解構(gòu)
研究表明,證據(jù)、推理和結(jié)論都具有復雜性。[7]證據(jù)的復雜性表現(xiàn)為熟悉與陌生、顯性與隱性等,證據(jù)呈現(xiàn)的方式越陌生越隱性,對思維能力要求越高。推理的復雜性表現(xiàn)為推理前提的多少、推理步驟的長短,推理前提越多、步驟越長,對思維能力要求越高。證據(jù)推理形成結(jié)論的過程具有科學性、準確性、充分性和相關性。證據(jù)來源應該科學、準確,收集過程應體現(xiàn)“科學性和準確性”;要收集不同類型的證據(jù)、從不同的角度證明結(jié)論,體現(xiàn)證明的“充分性”;推理過程要體現(xiàn)證據(jù)和結(jié)論的緊密關系、因果關系等“相關性”。
《普通高中化學課程課標(2017版)》將證據(jù)推理劃分為4級水平,本文基于收集證據(jù)的類型、推理形成結(jié)論的過程,從操作性角度解構(gòu)證據(jù)推理的4級水平,如表1。

表1 證據(jù)推理的4級水平
本文將收集證據(jù)類型分為如下水平:熟悉宏觀→熟悉宏觀和陌生微觀→顯性定性和隱性定量→多元證據(jù)、解釋證據(jù)。推理形成結(jié)論過程分為如下水平:一步推理,科學地得出結(jié)論→多步推理,科學地、準確地得出結(jié)論→多步推理,科學地、準確地、充分地得出結(jié)論→多步推理,科學地、準確地、充分地得出結(jié)論,解釋證據(jù)和結(jié)論的相關性。低級的證據(jù)推理水平主要側(cè)重某個角度和能力,高級的證據(jù)推理水平包含低級的水平要求。
三、發(fā)展證據(jù)推理水平的主題教學實踐——以氯化銅和氨水反應為例
主題教學活動指課堂教學以項目式探究形式或問題解決形式統(tǒng)整書本知識和現(xiàn)實生活、生產(chǎn)和社會中的學科問題,以教學主題為樞紐,在系統(tǒng)內(nèi)各要素相互聯(lián)系、作用和運行中達成學習主體心理結(jié)構(gòu)的完善和自我實現(xiàn)的整體性教學設計。[8]如何判斷物質(zhì)發(fā)生了化學反應、為什么發(fā)生化學反應,這是化學研究的中心問題。本文以氯化銅和氨水反應為教學主題,以判斷化學反應是否發(fā)生為教學背景,以學科方法逐漸深化為教學線索,設置4個關聯(lián)的教學環(huán)節(jié),發(fā)展學生從低級到高級的證據(jù)推理水平。
【環(huán)節(jié)1】收集宏觀證據(jù)推理發(fā)生反應
【教師】演示實驗1:將5mL0.1mol/LCuSO4溶液和10mL0.1mol/LNH3·H2O混合,生成藍色絮狀沉淀,久置后上清液幾乎為無色。CuSO4和NH3·H2O發(fā)生了化學反應嗎,證據(jù)是什么?
【學生】觀察、回答:因為溶液混合生成藍色沉淀、溶液顏色變淺,證明發(fā)生了化學反應,方程式為:CuSO4+2NH3·H2O=Cu(OH)2↓+(NH4)2SO4
【總結(jié)】化學反應常常伴隨發(fā)光、放熱、產(chǎn)生氣體、生成沉淀、變色等現(xiàn)象,可以根據(jù)上述宏觀現(xiàn)象判斷是否發(fā)生了化學反應。
設計意圖:本環(huán)節(jié)中,學生收集熟悉的宏觀證據(jù)證明硫酸銅和氨水發(fā)生化學反應。推理路徑為:觀察藍色絮狀沉淀,證明硫酸銅和氨水發(fā)生化學反應。學生分析顯性的宏觀證據(jù),經(jīng)過一步推理,科學地證明發(fā)生化學反應,發(fā)展水平1。
【環(huán)節(jié)2】收集微觀證據(jù)推理發(fā)生反應
【教師】提問:實驗1硫酸銅溶液和氨水混合,溶液為什么由淺藍色褪為無色?反應前后體系離子濃度如何變化,如何設計實驗證明?
【學生】討論、回答:因為生成氫氧化銅沉淀導致c(Cu2+)減小、溶液褪為無色。根據(jù)方程式判斷反應前后不變增大。證明不變的方案:向濾液中加入足量BaCl2溶液,稱量生成的m(BaSO4),證明反應前后溶液中m()不變。證明c(N)增大的方案:向濾液中加足量NaOH溶液并加熱、收集生成的NH3,證明增大。教師分別測如下溶液的電導率:取25mL0.1mol/LNH3.H2O于50mL小燒杯中,磁力攪拌下逐滴加入蒸餾水,溶液電導率變化如圖1所示(注:蒸餾水體積約為16mL)。

圖1 氨水稀釋電導率的變化
取25mL0.1mol/LCuSO4溶液于50mL小燒杯中,磁力攪拌下逐滴加入蒸餾水,溶液電導率變化如圖2所示(注:蒸餾水體積約為16mL)。

圖2 硫酸銅溶液稀釋電導率的變化
取25mL0.1mol/LNH3.H2O于50mL小燒杯中,磁力攪拌下逐滴加入0.1mol/LCuSO4溶液,溶液電導率變化如圖3所示(注:CuSO4溶液體積約為16mL)。

圖3 氨水和硫酸銅溶液混合電導率的變化
【學生】分析解釋:圖1說明氨水稀釋電導率減小、圖2說明硫酸銅溶液稀釋電導率減小,圖3說明硫酸銅和氨水混合后溶液發(fā)生化學反應,c(N)增大是電導率增大的主要原因,查閱離子的摩爾電荷電導率(描述物質(zhì)中電荷流動難易程度的參數(shù)):

【總結(jié)】溶液中發(fā)生離子反應,參與反應的某些離子濃度會發(fā)生變化(增加或減少),可以比較反應前后離子濃度變化判斷是否發(fā)生了化學反應。
設計意圖:本環(huán)節(jié)中,學生收集陌生的微觀證據(jù)證明硫酸銅和氨水發(fā)生化學反應。學生需要將可觀察的溶液藍色褪去與c(Cu2+)減小建立關聯(lián),將看不見的轉(zhuǎn)化為可稱量的硫酸鋇沉淀、將看不見的轉(zhuǎn)化為可測的電導現(xiàn)象,推理路徑為:溶液顏色變淺→c(Cu2+)減小;混合前后m(BaSO4)不變不變;設計對照實驗、分析溶液電導率變化變大。學生分析顯性宏觀證據(jù)和隱性的微觀證據(jù),經(jīng)過多步推理,科學地、準確地證明離子濃度變化可以作為化學反應發(fā)生的證據(jù),發(fā)展水平2。
【環(huán)節(jié)3】收集定量證據(jù)推理發(fā)生反應
【教師】演示實驗2:向1000mL蒸餾水分別加一滴0.0001mol/LCuSO4溶液、0.0001mol/LNH3·H2O,無沉淀生成,思考為什么。設1滴液體體積約為0.04mL、溶液總體積為1000mL,KspCu(OH)2=2.2×10-20,KbNH3·H2O=1.75×10-5。
【學生】討論,當Q>KspCu(OH)2生成沉淀;Q=KspCu(OH)2建立沉淀溶解平衡;Q<KspCu(OH)2不生成沉淀。估算如下:c(Cu2+)=0.0001×0.04/1000=4×10-9mol/L,c(OH-)2=[(0.0001×0.04×kb/1000)]=[(0.0001×0.04×1.75×10-5/1000)]=7×10-14mol/L,Q=c(Cu2+)×c(OH-)2=2.8×10-22<KspCu(OH)2,實驗2不能生成Cu(OH)2沉淀。
實驗1中,將5mL0.1mol/LCuSO4溶液和10mL 0.1mol/LNH3·H2O混合,c(Cu2+)=0.1×5/15=0.03mol/L,c(OH-)2=[(0.1×10×Kb/15)]=[(0.1×10×1.75×10-5/15)]=0.12×10-5mol/L,Q=c(Cu2+)×c(OH-)2=3.6×10-8>KspCu(OH)2,所以能生成Cu(OH)2沉淀。
【總結(jié)】CuSO4與NH3·H2O能否反應生成沉淀Cu(OH)2,需要通過定量計算、比較Q與KspCu(OH)2大小進行判斷。溶液中生成沉淀的條件遵守溶度積規(guī)則,當難溶物的濃度商大于溶度積才能生成沉淀,發(fā)生化學反應。
設計意圖:本環(huán)節(jié)中,學生需要通過收集隱性的定量證據(jù)證明硫酸銅和氨水能否發(fā)生化學反應。學生根據(jù)硫酸銅和氨水混合c(Cu2+)、c(OH-)計算濃度商,充分證明實驗1能生成沉淀、實驗2不能生成沉淀。推理路徑為:計算混合溶液的c(Cu2+),估算稀氨水中的c(OH-)→計算Q=c(Cu2+)×c(OH-)2→比較Q和KspCu(OH)2大小→解釋能否發(fā)生反應。學生收集定量證據(jù),經(jīng)過多步推理,科學地、準確地、充分地證明溶度積規(guī)則可以作為化學反應發(fā)生的證據(jù),發(fā)展水平3。
【環(huán)節(jié)4】收集多元證據(jù)推理發(fā)生反應
【教師】演示實驗3:將2mol/LNH3·H2O逐滴加入0.5mol/L5mLCuSO4溶液,生成藍色沉淀,滴加過量氨水、振蕩試管沉淀不消失,如何解釋現(xiàn)象呢?
【教師】演示實驗4:向0.5mol/L5mLCuSO4溶液加入氯化銨固體,再滴加2mol/LNH3·H2O,生成藍色沉淀,滴加過量氨水、振蕩試管,沉淀消失,最終生成深藍色溶液。[9]如何解釋現(xiàn)象呢?
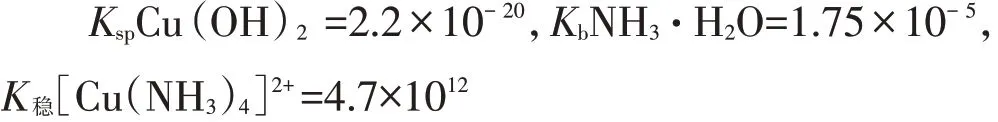
【學生】討論,分析如下:實驗3中,淺藍色溶液→藍色沉淀,證明氫氧化銅不溶于氨水。實驗4中,淺藍色溶液→藍色沉淀→深藍色溶液。兩個實驗現(xiàn)象為什么不同?學生計算實驗3中反應①的平衡常數(shù)K:

K很小,從限度上判斷氫氧化銅不能溶于氨水(實際上溶解速率很慢)。
實驗4涉及如下反應:

則①+②=反應③:
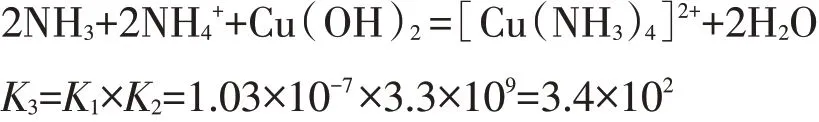
向氨水、氫氧化銅加入足量銨鹽,NH4+耦合OH-,使平衡常數(shù)增加3.24×109倍,有效促進了氫氧化銅的溶解、生成更穩(wěn)定[Cu(NH3)4]2+,減少c(Cu2+)。
【總結(jié)】Cu(OH)2與NH3·H2O不能反應生成銅氨絡離子,向溶液中加入足量的銨鹽,銨鹽和OH-反應耦合,極大增加化學反應平衡常數(shù),生成深藍色、更穩(wěn)定的銅氨絡離子。沉淀能否有效轉(zhuǎn)化為絡離子,可以通過耦合反應等條件調(diào)控增大反應常數(shù)、發(fā)生化學反應。
設計意圖:本環(huán)節(jié)中,學生需要收集多元證據(jù)判斷氫氧化銅和氨水能否發(fā)生化學反應。學生要根據(jù)宏觀證據(jù)判斷氫氧化銅不能溶于氨水、加入銨鹽可以生成銅氨絡離子,然后收集微觀證據(jù)書寫氫氧化銅和氨水、銨鹽反應的離子方程式,最后通過定量計算解釋原因。推理路徑為:沉淀顏色是否變化→基于多重平衡規(guī)則計算簡單反應和復雜反應的平衡常數(shù)→比較K的變化→解釋能否發(fā)生反應→基于“N和OH-耦合”解釋氫氧化銅與氨水發(fā)生反應的原因。學生收集多元證據(jù),經(jīng)過多步推理,科學地、準確地、充分證明耦合反應可以拉動化學反應,解釋證據(jù)對結(jié)論形成支撐的因果關系,發(fā)展水平4。
【課堂作業(yè)】
問題1將0.1mol/L5mLCuSO4溶液和0.1mol/L 10mLNH3·H2O混合,生成藍色沉淀常含有堿式硫酸銅CuSO4·Cu(OH)2,如何證明沉淀中含有硫酸根?
問題2[Cu(NH3)4]2+是穩(wěn)定存在的絡離子,你能否從結(jié)構(gòu)的角度收集證據(jù)說明原因?
設計意圖:問題1基于沉淀的復雜性,培養(yǎng)學生設計實驗方案、收集熟悉證據(jù)的能力:加足量鹽酸溶解、再加氯化鋇檢驗。問題2培養(yǎng)學生收集結(jié)構(gòu)證據(jù)理解[Cu(NH3)4]2+穩(wěn)定存在原因:基于晶體場理論知Cu2+形成的八面體場,失去能量較高、z軸方向的2個配體水分子,4個氨分子在x軸和y軸方向成平面正方形,獲得更多的晶體場穩(wěn)定化能(John-Teller效應)。上述2個問題是主題教學內(nèi)容的延伸,培養(yǎng)學生從實驗探究、文獻查閱的角度進行科學論證的能力,發(fā)展學生證據(jù)推理的綜合素養(yǎng)。
四、結(jié)束語
證據(jù)推理是重要的學科思維方法,本文解構(gòu)了證據(jù)推理的內(nèi)涵,從收集證據(jù)的類型、推理形成結(jié)論的過程劃分證據(jù)推理的水平。教學中以氯化銅和氨水反應為例,基于真實的實驗情境,以學生活動為主體,采取多樣的教學活動,基于宏觀沉淀顏色變化、微觀粒子濃度變化、溶度積規(guī)則、耦合反應等證據(jù)判斷化學反應是否發(fā)生,促進學生認識思路的結(jié)構(gòu)化發(fā)展,提升學生的證據(jù)推理水平。

