曲司氯銨合成工藝研究進展
*李博 李洪發 常樂 莫洪虎 趙玉佳
(牡丹江醫學院 黑龍江 157011)
曲司氯銨(1)是抗膽堿藥物,化學名為為螺環[8-氮陽離子二環[3,2,1]辛烷-8,1‘-吡咯烷]-3-[(羥二苯基-乙酰基)-氧]氯(1α,3β,5α)-(9C1),分子式是C25H30ClNO3,是由美國Indevus醫藥公司(Indevus Pharmaceuticals,Inc.Lexington,MA USA)研制開發成功,并由德國Madaus AG(Madaus AG,Troisdorf,Germany)生產上市的抗膽堿藥物[1]。分子結構式見圖1。

圖1 曲司氯銨結構式
2004年,美國食品藥品管理局(FDA)批準曲司氯銨上市。曲司氯銨對M1、M2和M3型抗膽堿能受體的高親和力,并且曲司氯銨作為化學結構是一個親水的極性的季胺結構的抗毒蕈堿劑,極少通過肝細胞色素P450進行代謝,而是直接隨尿液排出體外,保證了藥物本身的有效性和耐受性[2]。對于因脊髓損傷而導致的逼尿肌過度活動也可起到明顯的治療效果,對于因內臟平滑肌痙攣而造成的絞痛,曲司氯銨亦有治療效果;此外,曲司氯銨可以促進壁內段輸尿管結石的排出,并且減少因此而產生的尿頻、尿急癥狀[3-4]。曲司氯銨作為重要的OAB治療藥物,關于該化合物合成工藝的綜合性評估文獻鮮有報道,因此本文對其合成工藝的研究進展進行綜述。
1.曲司氯銨及中間體的概述
曲司氯銨作為季銨鹽類化合物在臨床上應用于治療膀胱過動癥在有著其獨特的優勢。目前在臨床上主要有三種類型的藥物用于治療膀胱過度活動癥分別為M受體阻滯劑、β3受體激動劑、α1受體阻滯劑,其中,M受體阻滯藥作用機制是抑制突觸后的沖動傳遞來對膀胱肌壁(逼尿肌)受體與乙酰膽堿的結合進行阻斷,減低膀胱尿道不主動萎縮的幅度,提高膀胱尿道容積[5]。但是,因M受體阻滯要是通過M受體對乙酰膽堿的調節從而調節中樞神經系統的興奮作用[6],致使其在調節膀胱過度活動癥的同時也會產生一些副作用[7]。尤其是因年齡的增長導致人體的血腦屏障通透性增加,致使M受體阻滯劑的中樞神經系統的副作用會在老年患者身上越發明顯,進而為治療膀胱過動癥并消除中樞神經系統的副作用就顯得格外重要[8-9]。曲司氯銨作為季銨鹽類化合物難以通過血腦屏障,在腦脊液檢測中甚至不能檢測到曲司氯銨的存在[10]。
合成曲司氯銨的關鍵中間體是二苯羥乙酸去甲托品酯,對與中間體合成曲司氯銨的反應只需要簡單的與1,4-二氯丁烷發生成環反應即可得到曲司氯銨。在曲司氯銨的合成當中,因為其中間體在臨床上應用不多以及原料價格上漲,導致其中間體的研究成本在不斷地提升,因此,要加強對中間體的研發,構建高效、低成本的中間體合成工藝,為中間體的生產的企業提供合理利潤保障。因為藥物中間體并未受到專利法的保護,但是合成中間體的技術路線可以獲得保護,推動合成中間體的技術不斷創新,可以不斷提高曲司氯銨的合成工藝,也能為其他藥物的合成提供思路[11]。
2.曲司氯銨合成技術及分析
目前的關于曲司氯銨的合成研究當中,主要有兩種合成策略:一是由α-托品醇與二苯羥乙酸進行酯化反應,得到中間體3,隨后經過一系列反應脫去N-甲基,得到關鍵中間體二苯基羥乙酸去甲托品酯(2),最終由中間體2與1,4-二氯丁烷進行環合得到目標產物;二是由前期工作合成氯化(3α-去甲托品醇)-8-螺-1’-吡咯銨鹽中間體9,再與二苯羥乙酸類衍生物經酯化得到目標產物(見圖2)。
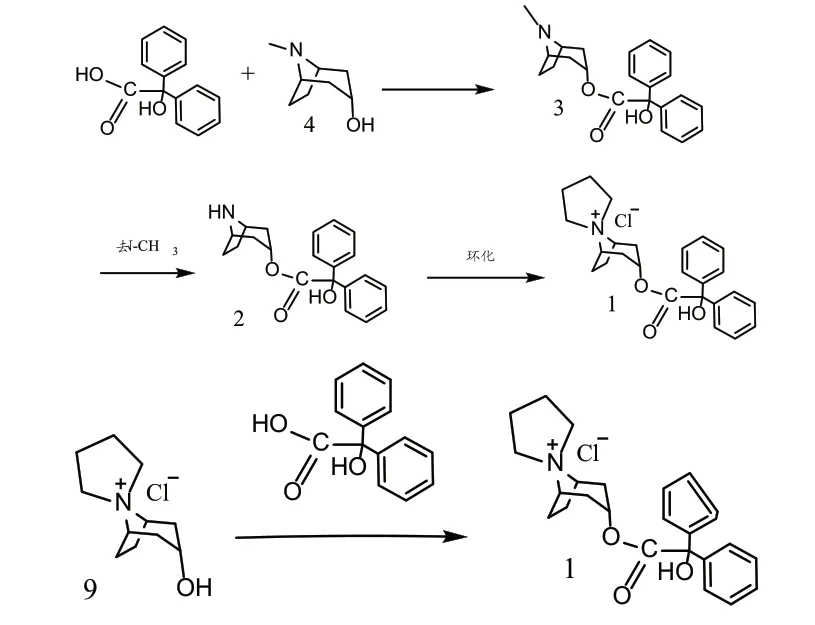
圖2 合成曲司氯銨的兩種方式
(1)經關鍵中間體二苯基羥乙酸去甲托品酯制備曲司氯銨
通過對已發表的曲司氯銨的合成文獻進行分析,現如今曲司氯銨合成的主流方式是由α-托品醇為原料,經酯化化得到二苯基羥乙酸去甲托品酯中間體,再與1,4-二氯丁烷發生環合制得曲司氯銨。劉素云等[12]以α-托品醇(4)和二苯基羥乙酸(5)經酰化反應得到二苯基羥乙酸托品酯(3),此步反應收率為80%。3與三苯膦混合在光照的作用下通入氧氣經去甲基反應脫去托品醇中醇環上的N-甲基可得到二苯基羥乙酸去甲托品酯(2),此步反應收率為79%。2與1,4-二氯丁烷經環合反應即可得終產物曲司氯銨(1),此步反應收率為46%。路線總收率約為19%。但是該合成路線具有兩個較為明顯的缺點:①在第二步去N-甲基反應中,所需要的反應時間非常長,并且底物轉化不完全;②也是在第二步反應,此步反應采用三苯磷混合在光照的作用下通入氧氣脫去N-甲基,此反應在光照條件下進行導致生產成本在無形中提高,因在工業化生產當中整個生產環節是采用大量的原料進行生產以平均生產成本,而光照并不能對整體而大量的原料均勻的照料到,難以進行大規模生產。
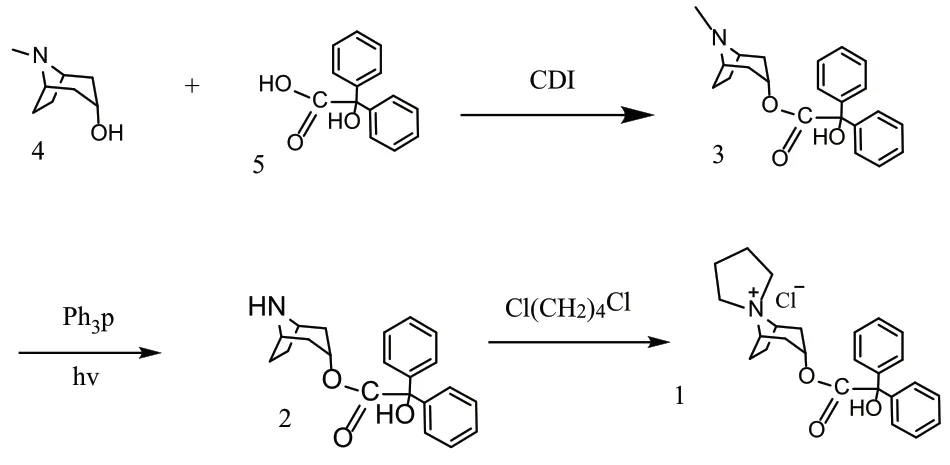
圖3 劉素云等合成曲司氯銨工藝
宋偉國,楊大偉等[13-17]以α-去甲托品醇(6)為原料,與氯甲酸乙酯發生酰化反應制得N-乙氧羰基托品醇(7),此步反應收率為95%。二苯羥乙酸(5)與化合物7經酰化反應制得N-乙氧羰基二苯羥乙酸托品酯(8),此步反應收率為80%。8在甲酸銨/鈀-炭催化氫轉移還原體系中經還原反應除去乙氧羰基得到二苯羥乙酸去甲托品酯(2),此步反應收率為85%。2與1,4-二氯丁烷經環合反應制得目標產物曲司氯銨(1)。路線總收率為52%。此方法操作簡單,使用用綠色環保的催化氫轉移還原體系去除乙氧羰基,有利與生產企業降低成本,總體來說此路線適合工業化生產。

圖4 宋偉國,楊大偉等曲司氯銨合成工藝
(2)經中間體氯化(3α-去甲托品醇)-8-螺-1’-吡咯銨鹽中間體合成曲司氯銨
在現有的曲司氯銨的合成工藝中,與先將底物酯化,制備二苯羥乙酸托品酯關鍵中間體的方式進行相比,采用多種路徑首先制備中間體氯化(3α-去甲托品醇)-8-螺-1’-吡咯銨鹽,后進行酯化也可以作為一種較為優秀的替代方案。
趙文鏡等[18]以α-托品醇(4)為原料經酰化、水解生成去甲托品醇(6),此步反應收率53.3%。6再與1,4-二氯丁烷經環合反應生成氯化(3α-去甲托品醇)-8-螺-1’-吡咯銨鹽(9),此步反應收率為39%。9與二苯乙醇酸咪唑(10)經酰化反應生成曲司氯銨(1),此步反應收率為57.2%,路線總收率為約48.6%。此方法通過不同于主流的合成路線該合成方法避過了對關鍵中間體生成,盡管不采用主流的合成關鍵中間體2的方法,有著思路上的創新。但此方法的工藝路線較其他的路線長,然而此路線的反應條件較為溫和,反應對環境污染小,并且收率較高,具有較好的工業化生產價值。

圖5 趙文鏡等合成曲司氯銨工藝
張晶等[19]以二苯羥乙酸(5)原料與氯化亞砜經鹵置換反應得到二苯羥乙酰氯(11),此步反應收率為93%。以α-托品醇(4)為原料采用Pd/C催化劑催化氫化脫去甲基得到去甲托品醇(6),此步反應收率為66%。6與1,4-二氯丁烷發生環合反應生成氯化(3α-去甲托品醇)-8-螺-1-吡咯銨鹽(9),此步反應收率為68%。9與11發生酰基化反應生成曲司氯銨(1),此步反應收率為65%。此路線反應需要兩種反應環境,對于生產企業而言需要多鍵另一條生產線,致使生產成本較其他路線明顯升高,雖然其中采用的Pd/C的催化試劑在試驗階段以及工業生產階段均可以重復利用。但相較與生產設備而言實驗耗材量較小。
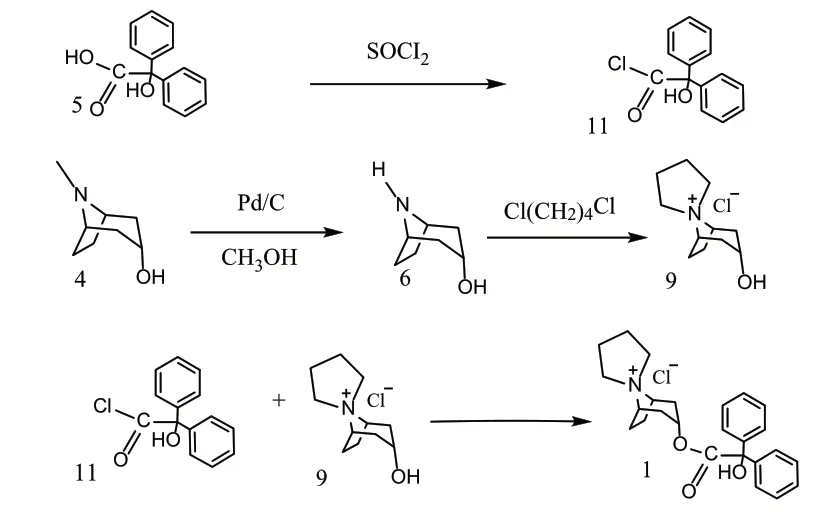
圖6 張晶等合成曲司氯銨工藝
(3)合成工藝分析
通過對合成路線進行分析,合成曲司氯銨的路線可以經由關鍵中間體2二苯羥乙酸去甲托品酯合成,也可以經由另一中間體9氯化(3α-去甲托品醇)-8-螺-1-吡咯銨鹽進行合成。劉素云采用的合成工藝雖原料價廉易得,但在其合成路線當中采用Ph3P光照法進行脫甲基化反應導致整體反應時間增加,生產周期加長且轉化不完全,并最終造成生產效率低下,不適合工業化生產;宋偉國,楊大偉等采用的合成工藝操作簡單,采用用綠色環保的催化氫轉移還原體系去除乙氧羰基,符合綠色化學的理念,適合工業化生產;趙文鏡的合成方法原料易得,反應條件較為溫和,反應對環境污染小,并且收率較高,具有較高工業化生產潛力;張晶的合成路線反應步驟短,同時Pd/C催化氫化脫去甲基,可使催化劑多次套用,減少污染,無繁瑣的反應后處理過程,適合工業生產。
3.結語
本文對國內外已發表的曲司氯銨的合成路線進行了綜述,通過采取不同的反應底物、反應條件合成曲司氯銨的兩種方式都具有其獨特的優勢以及各自的缺點,但是主流的合成曲司氯銨的工藝仍是α-托品醇酯化后合成關鍵中間體二苯羥乙酸去甲托品酯再經環化得到目標產物曲司氯銨。在現如今這個原料價格飛漲,制藥成本居高不下的年代,國內的制藥企業還需要面對來自同行的越發激烈的商業競爭,而它們需要更加努力做到在不影響藥物質量的前提下,提高目標產物的收率以及降低制藥工藝的生產成本。隨著時代的發展,綠色化學越來越受到大眾的關注,因此對于制藥工藝的優化過程當中,如何開發出對環境友好的生產工藝來合成曲司氯銨,并且能夠滿足工業化生產,具有極為重大的現實意義。

