鋰離子電池三元正極材料殘堿測試影響因素
王裕生,柳春月,吳珊珊,孫偉麗
(寧波容百新能源科技股份有限公司,浙江 寧波 315400)
鋰離子電池三元正極材料(LiNixCoyMn1-x-yO2)的能量密度高,倍率性能好,循環壽命長,廣泛應用于電動汽車、消費電子和儲能等領域,但存在一定的安全問題[1]。
在高溫煅燒過程中,三元正極材料中的Li會蒸發損失,實際生產過程中需加入適當過量的Li,導致最終合成的材料中部分Li殘留,主要為Li2CO3和LiOH,即殘堿。殘堿是三元正極材料生產過程中的一項重要控制指標。殘堿含量越高,電池制作勻漿和涂覆過程越容易吸水,使漿料呈果凍狀,導致電池極片出現廢品[2]。此外,Li2CO3會在充放電過程中生成CO2,造成電池脹氣,惡化材料的性能[3]。
本文作者通過電位滴定法系統研究了三元正極材料中殘堿測試的影響因素。
1 實驗
1.1 試劑與材料
實驗用水的制備:用VE-20LH-A型純水機(深圳產)制備純水;按GB/T 603-2002《化學試劑 試驗方法中所用制劑及制品的制備》[4]的要求,煮沸純水并冷卻,制備去CO2純水;用HDNRO-750型純化水設備(溫州產)制備去離子水。
0.05 mol/L HCl標準溶液的配制及標定,參照GB/T 601-2016《化學試劑 標準滴定溶液的制備》[5]進行。
使用本公司研發實驗樣及量產的三元正極材料,包括LiNi0.5Co0.2Mn0.3O2(NCM523)、LiNi0.6Co0.2Mn0.2O2(NCM622)和LiNi0.8Co0.1Mn0.1O2(NCM811)。
1.2 實驗方法
基礎實驗:用JY20002型電子天平(上海產)稱取30 g三元正極材料,置于干凈的250 ml錐形瓶中,加入100 ml純水及磁力攪拌子(直徑8 mm×長度50 mm,上海產),塞上橡膠塞。將錐形瓶置于磁力攪拌器上,以(400±10) r/min的轉速攪拌30 min。之后,將濾紙墊在干凈的燒杯上,倒入攪拌后的上清液,過濾。過濾完成后,移取10 ml濾液于100 ml燒杯中,加入60~70 ml純水,置于預先設定好的905型自動電位滴定儀(瑞士產)上,進行測試,滴定參數詳見表1。研究各影響因素時的實驗條件詳見表2。
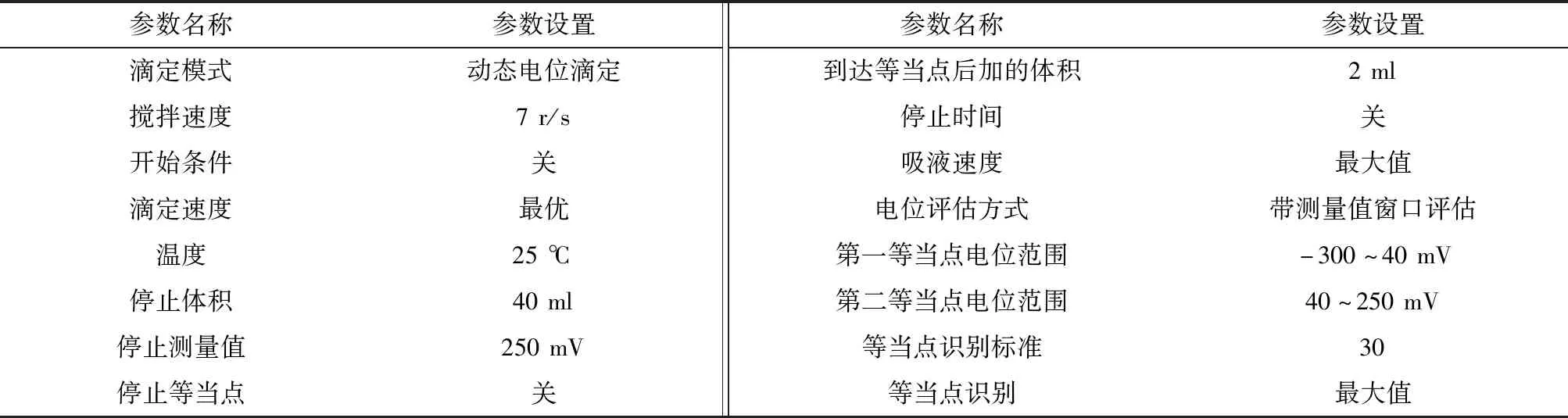
表1 自動電位滴定儀滴定參數 Table 1 Titration parameters of automatic potential titrator
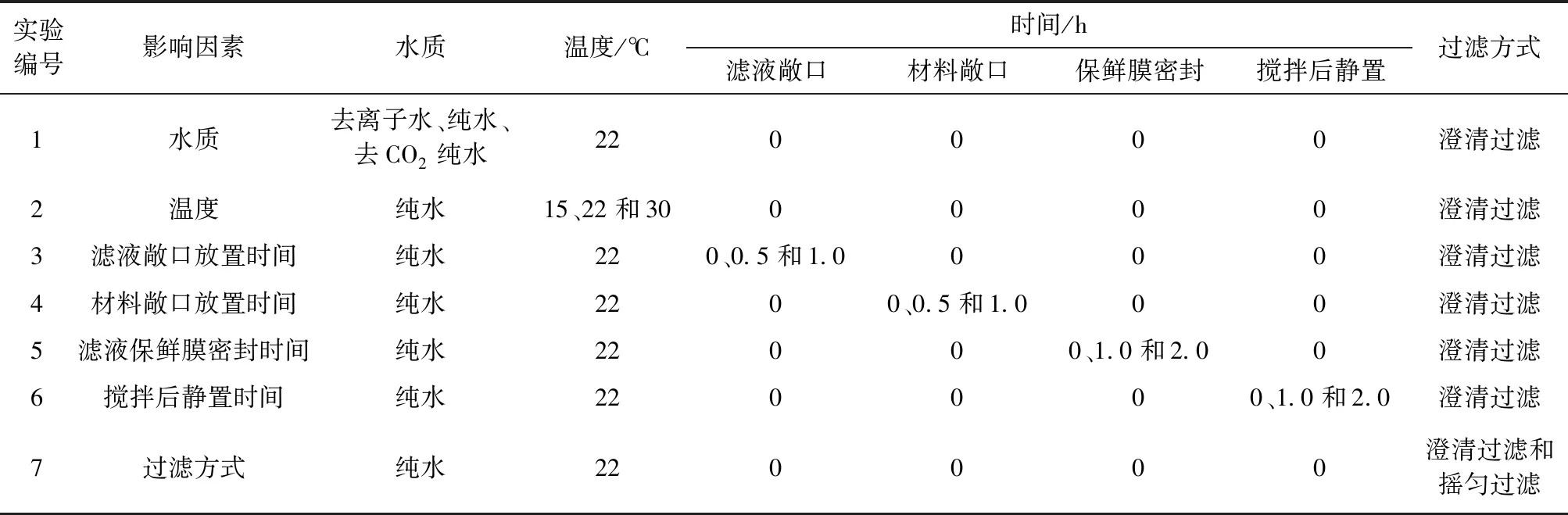
表2 研究各影響因素時的實驗條件 Table 2 Experimental conditions for studying influencing factors
1.3 殘堿計算
Li2CO3的質量分數(ωLi2CO3)、LiOH的質量分數(ωLiOH)和Li的質量分數(ωLi),分別按式(1)-(3)計算:
(1)
(2)
(3)
式(1)-(3)中:V1為第一滴定終點HCl耗量,ml;V2為第二滴定終點HCl耗量,ml;cHCl為HCl的濃度,mol/L;V水為加入純水的體積,ml;V移為移液體積,ml;m為稱取材料的質量,g;Li2CO3、LiOH和Li的分子量為73.89、23.95和6.94。
2 熱力學分析
2.1 標準狀態下的熱力學參數
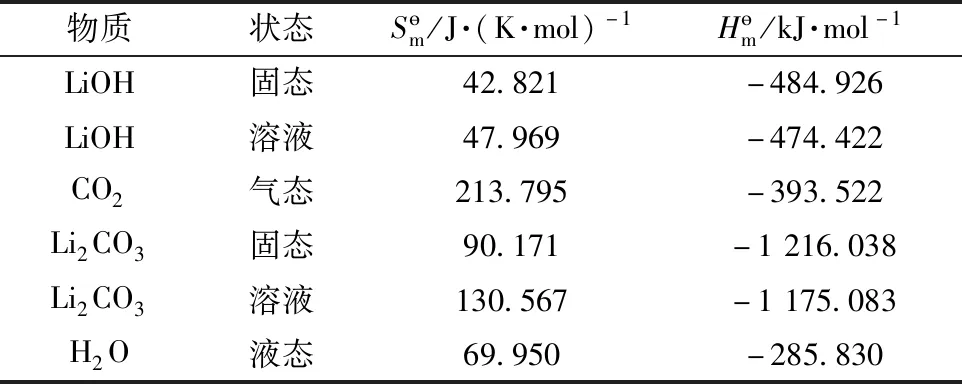
表3 標準熱力學性質表Table 3 Standard thermodynamic properties table
2.2 標準狀態下反應可行性熱力學分析

(4)
(5)
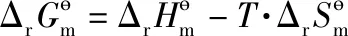
(6)
式(4)-(6)中:T為溫度,298.15 K;P、R分別代表產物、反應物。
相關化學反應式,如式(7)-(8)所示:
2LiOH(s)+CO2(g)=Li2CO3(s)+H2O(l),
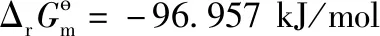
(7)
2LiOH(aq)+CO2(g)=Li2CO3(aq)+H2O(l),
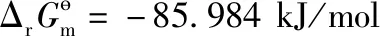
(8)
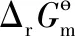
3 結果與討論
3.1 水質的影響
選取兩種殘堿含量不同的三元正極材料,按表2實驗1進行測試,結果見表4。
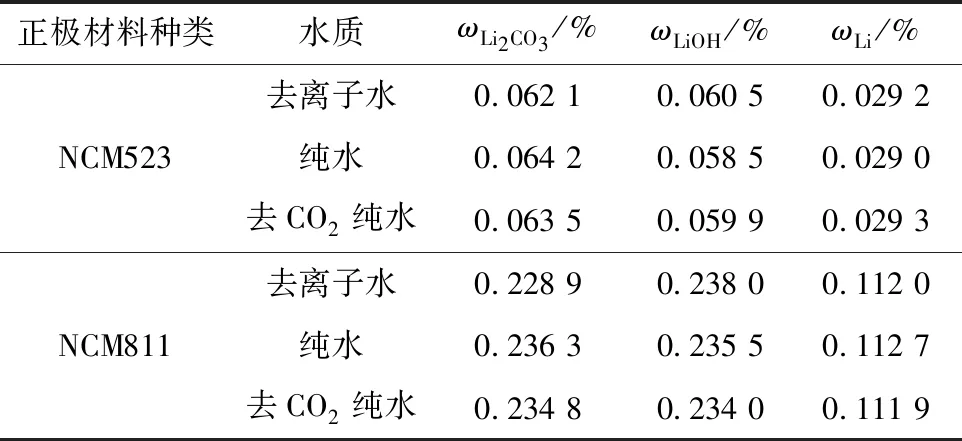
表4 不同水質殘堿測試結果Table 4 Test results of residual alkali with different water
從表4可知,不同水質下,測得同一材料的Li2CO3、LiOH、Li含量的相對極差不高于3.4%,說明水質對測試結果的影響很小,因此,純水和去離子水都可用于殘堿測試。
3.2 溫度的影響
選取兩種殘堿含量不同的三元正極材料,按表2實驗2進行測試,結果見表5。

表5 不同溫度殘堿測試結果Table 5 Test results of residual alkali with different temperatures
從表5可知,不同溫度下,測得同一材料的Li2CO3、LiOH、Li含量的相對極差不高于2.9%,說明溫度對測試結果的影響很小。
3.3 濾液敞口放置時間的影響
選取兩種殘堿含量不同的三元正極材料,按表2實驗3進行測試,結果見表6。
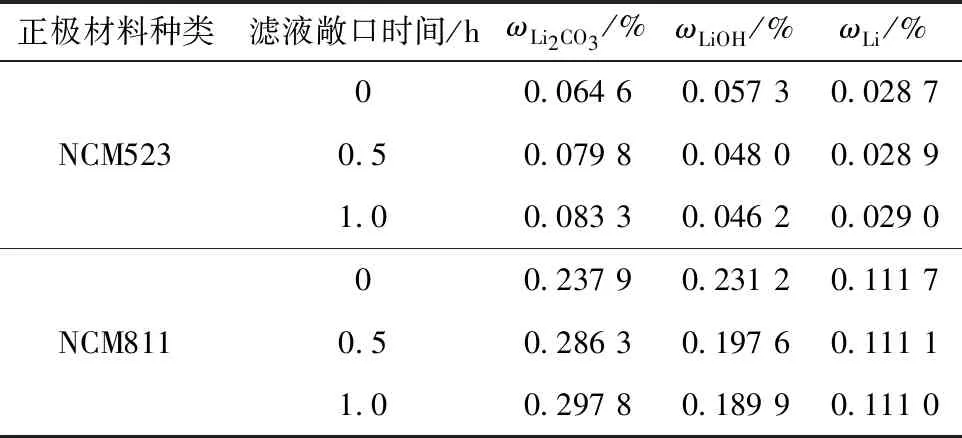
表6 濾液敞口放置不同時間殘堿測試結果Table 6 Test results of residual alkali with different exposure time of filtrate
從表6可知,兩種材料的濾液敞口放置0.5 h后,Li2CO3含量較未敞口放置分別升高23.5%、20.3%,LiOH含量分別降低16.2%、14.5%,Li含量變化小于1.0%。這是由于空氣中的CO2與溶液中的LiOH反應生成了Li2CO3。兩種材料的濾液敞口放置1.0 h后,Li2CO3含量較0.5 h分別升高4.4%、4.0%,LiOH含量分別降低3.8%、3.9%,Li含量變化小于1.0%,說明空氣中CO2與溶液中OH-的反應速率隨敞口時間增大而降低。實際測試過程中,應減少濾液在空氣中的暴露時間,減弱LiOH與Li2CO3的轉化。
3.4 材料敞口放置時間的影響
選取兩種殘堿含量不同的三元正極材料,按表2實驗4進行測試,結果見表7。
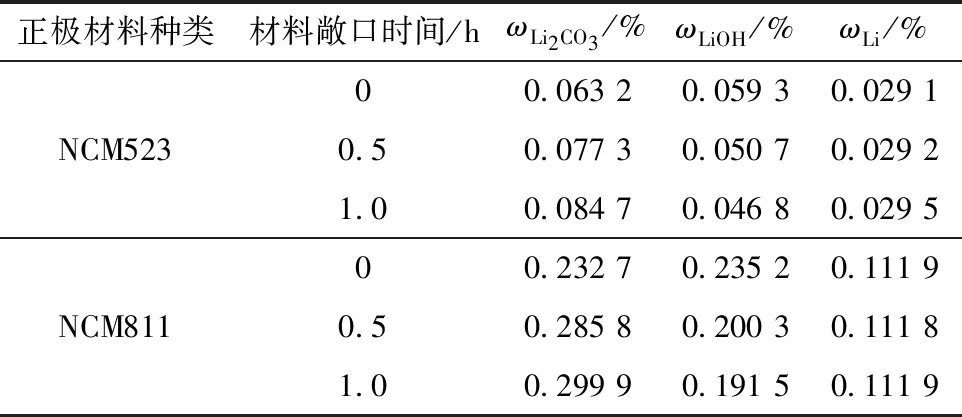
表7 材料敞口放置不同時間殘堿測試結果Table 7 Test results of residual alkali with different exposure time of materials
從表7可知,兩種材料敞口放置0.5 h后,Li2CO3含量較未敞口放置分別升高22.3%、22.8%,LiOH含量分別降低14.5%、14.8%。兩種材料敞口放置1.0 h后,Li2CO3含量較0.5 h分別升高9.6%、4.9%,LiOH含量分別降低7.7%、4.4%,Li含量變化均小于1.0%。測試結果與濾液敞口放置實驗類似,說明三元正極材料暴露在空氣中,也容易吸收CO2,導致LiOH轉化為Li2CO3。
3.5 濾液保鮮膜密封時間的影響
選取兩種殘堿含量不同的三元正極材料,按表2實驗5進行測試,結果見表8。
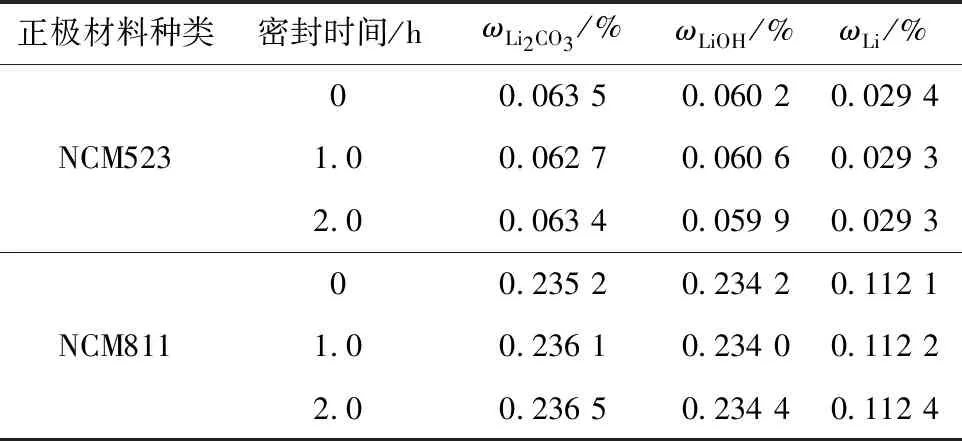
表8 濾液保鮮膜密封不同時間殘堿測試結果Table 8 Test results of residual alkali of filtrate sealed with plastic wrap at different time
從表8可知,兩種材料的濾液用保鮮膜密封2.0 h,測得的Li2CO3、LiOH、Li含量的相對極差不高于1.3%,說明保鮮膜能在2.0 h內隔絕空氣中的CO2,避免LiOH轉化為Li2CO3。
3.6 攪拌后靜置時間的影響
選取兩種殘堿含量不同的三元正極材料,按表2實驗6進行測試,結果見表9。
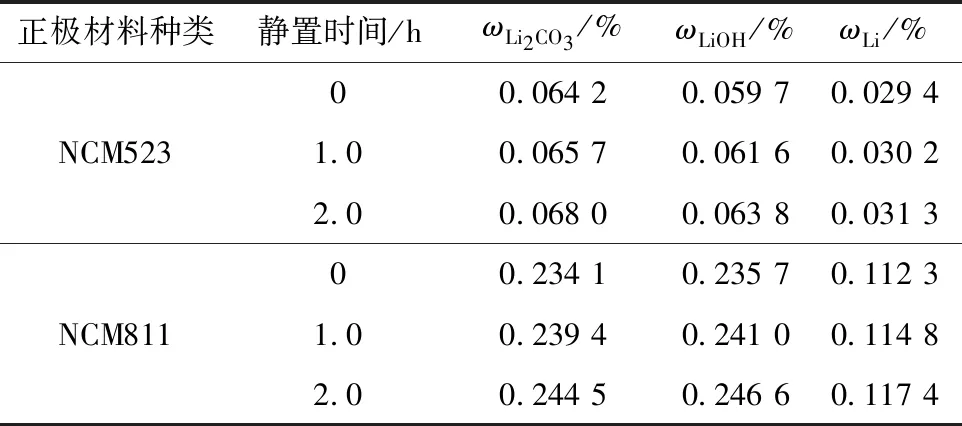
表9 攪拌后靜置不同時間殘堿測試結果Table 9 Test results of residual alkali with different standing time after stirring
從表9可知,兩種材料攪拌結束后靜置,測得的Li2CO3、LiOH、Li含量均升高,靜置2.0 h,Li含量分別升高6.5%、4.6%。殘堿中的Li包括三元正極材料表面殘留的Li及材料體相內的Li,靜置時間過長,材料體相內的Li會不斷溶出,使殘堿含量升高[6]。攪拌后,應盡快測試或過濾到燒杯中,用保鮮膜密封,避免長時間靜置導致的測試結果偏高。
3.7 過濾方式的影響
選取5種殘堿含量不同的三元正極材料,按表2實驗7進行測試,結果見表10。
從表10可知,5種材料搖勻過濾測得的Li2CO3、LiOH、Li含量均比澄清過濾的高,其中,Li2CO3偏高0.4%~3.6%,LiOH偏高1.0%~5.6%,Li偏高1.8%~4.0%,因此,需要規定過濾方式。
4 結論
通過電位滴定法系統地研究了三元正極材料中殘堿測試影響因素。空氣中的CO2對殘堿測試的影響最大,三元正極材料及殘堿溶液敞口放置0.5 h后,Li2CO3含量升高約22%,LiOH含量降低約15%,說明材料暴露在空氣中極易吸收CO2,導致LiOH轉化為Li2CO3,因此,測試殘堿的材料應密封包裝,測試過程中也應減少材料及殘堿溶液與空氣的接觸時間。攪拌結束后,應盡快測試或過濾到燒杯中用保鮮膜密封,避免長時間靜置,導致殘堿測試結果偏高。此外,澄清過濾和搖勻過濾的測試結果存在顯著性差異,需要規定過濾方式,減小測試誤差。水質及溫度對殘堿測試的影響較小。
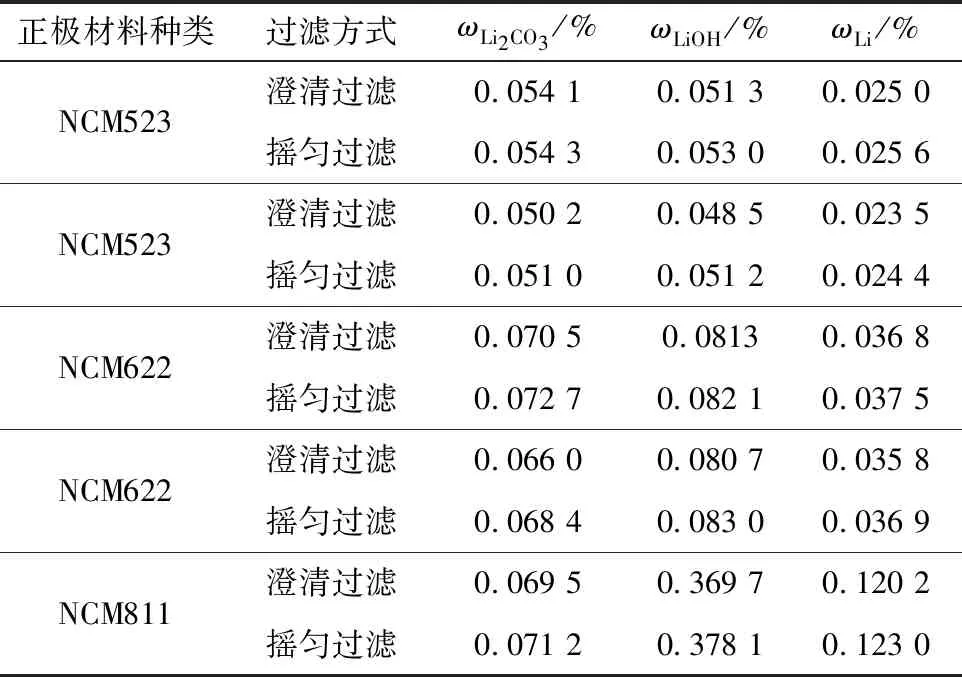
表10 不同過濾方式殘堿測試結果Table 10 Test results of residual alkali with different filtration methods
影響殘堿測試的因素主要有兩個:①空氣中的CO2,導致LiOH轉化為Li2CO3;②材料體相內的Li不斷溶出,導致殘堿含量升高。由于上述因素影響面較廣,三元正極材料中殘堿的測試過程需要嚴格控制,包括未提及的稱樣、加水等步驟,需要快速而準確。

