5,5′-肼基雙四唑二羥胺鹽的合成與性能
劉亞靜,劉浩然,葛瑞榮,趙寶東,劉衛孝,高福磊,張 萌
(1.西安近代化學研究所,陜西 西安 710065;2.中國國際工程咨詢有限公司,北京 100000;3.安徽紅星機電科技有限公司,安徽 合肥 231135;4.陸裝駐西安地區航空軍事代表室,陜西 西安 710065)
引 言
富氮含能離子化合物是一種高氮含量的離子型含能化合物,它既具有富氮化合物的高生成焓、高密度、高氧平衡等特點,也具有含能離子鹽極性強、不揮發、毒害性小、對環境較友好等優點,可用于氣體發生器、低特征信號推進劑、煙火藥和高能低感炸藥等,因此受到廣泛的研究和關注[1-4]。唑環類化合物以其高氮含量、高生成焓、高產氣量、既可作陽離子又可作陰離子和爆轟產物清潔等特點,常用于合成富氮離子鹽[5],目前常用的唑類富氮含能離子化合物有氨基四唑肼鹽、偶氮四唑氨基胍鹽、5,5′-二氨基-3,3-聯-1,2,4-三唑氨鹽等[6-8]。
5,5′-肼基雙四唑(HBT)是典型的四唑類富氮化合物,晶體密度為1.844g/cm3(實測值),氮含量83.3%,爆速9463m/s,爆壓36.7GPa,熱分解溫度242.1℃,撞擊感度遠低于RDX和HMX,在固體推進劑、高能炸藥、煙火藥等領域具有潛在應用前景[7,9]。HBT具有活潑H,有較強的酸性,在溶劑中可脫氫得到HBT2-,后者可與富氮陽離子生成含能離子鹽。因此,國內外研究人員設計合成了5,5′-肼基雙四唑銨鹽、5,5′-肼基雙四唑肼鹽、5,5′-肼基雙四唑氨基胍鹽等含能鹽,并對其熱分解溫度、生成焓、感度等性能進行了研究[7]。其中,5,5′-肼基雙四唑肼鹽具有氮含量高、生成焓高的特點,但其熱穩定性較差,熱分解溫度僅為182℃;而5,5′-肼基雙四唑胍鹽熱分解溫度高達214℃,但生成焓較低,這些缺陷限制了HBT型離子鹽的潛在應用。
羥胺陽離子是一種常用于合成離子型含能化合物的陽離子,其代表物1,1′-二羥基-5,5′-聯四唑二羥胺鹽(HATO),具有高密度、高爆速、熱分解溫度較高等特點[3-4]。本研究結合前期研究,以5-氨基四唑(5-AT)為原料,經過氧化還原和中和反應合成了新型富氮含能離子鹽5,5′-肼基雙四唑二羥胺鹽(HBT-HA),通過核磁、紅外、元素分析進行結構表征,并進行了工藝優化。測試了HBT-HA密度,通過Gaussian軟件預測了爆轟性能,并使用差示掃描量熱(DSC)技術研究了其熱分解特性、熱分解動力學及與改性雙基推進劑組分的相容性,為其工藝安全控制及進一步應用提供理論支撐。
1 實 驗
1.1 儀器與試劑
5-氨基四唑(5-AT),分析純,質量分數大于99%,山東西亞化學工業有限公司;氫氧化鈉、高錳酸鉀、50%羥胺水溶液、無水乙醇、四氫呋喃,均為分析純,質量分數大于99%,成都市科龍化工試劑廠;鎂粉,分析純,天津市科密歐化學試劑有限公司;濃鹽酸,分析純,質量分數35%~37%,國藥集團化學試劑有限公司。
NEXUS 870型傅里葉變換紅外光譜儀,美國熱電尼高力公司;AV 500型(500MHz)超導核磁功能共振儀,瑞士BRUKER公司;VARIO-EL-3 型元素分析儀,德國EXEMENTAR公司;Q-200型差示掃描量熱儀,美國TA公司;耐馳TG209F3型熱重儀,德國耐馳公司;LC22010A型高效液相色譜儀,日本島津公司;Accupyc1340真密度分析儀,美國麥克公司。
1.2 目標化合物的合成
首先,以5-氨基四唑(5-AT)為原料,在氫氧化鈉水溶液中被高錳酸鉀氧化生成偶氮四唑鈉鹽五水合物(SZT·5H2O),經鎂粉還原及酸化得到5,5′-肼基雙四唑;其次,通過5,5′-肼基雙四唑與羥胺的酸堿中和反應,制備得到5,5′-肼基雙四唑二羥胺鹽。具體合成路線如下:
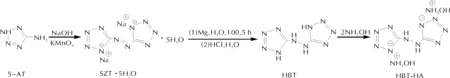
1.2.1 SZT·5H2O的合成
向裝有溫度計和機械攪拌的反應瓶中依次加入408.0g NaOH和510mL去離子水配制成2mol/L的水溶液,隨后加入25.5g的5-AT,溫度升至62℃時分多批加入47.6g KMnO4固體,使反應溫度不高于70℃時繼續反應0.5h,然后加入適量無水乙醇用于還原過量的KMnO4,再升溫至反應液沸騰,反應完成后趁熱過濾除去MnO2,濾餅用熱水淋洗,濾液減壓濃縮至原體積的1/3或1/2,冷卻2~3h后過濾,濾餅經水洗,乙醇淋洗,自然晾干得黃色固體35g,收率77.8%,純度大于99.5%(HPLC)。
13C NMR(DMSO-d6),δ: 172.06(四唑環上C)。
1.2.2 5,5′-肼基雙四唑(HBT)的合成
向裝有溫度計和機械攪拌的反應瓶中依次加入30.0g SZT·5H2O和500mL去離子水,然后分多批加入9.6g Mg粉,升溫至95~100℃反應5h,反應完成后,反應液溫度降至45~50℃時減壓過濾,濾液倒至質量分數25%鹽酸中快速攪拌,過濾、水洗、自然晾干得白色固體15.6g,收率92.9%,純度99.3%,分解溫度242.1℃(DSC法)。
IR(KBr),υ(cm-1):3433,3289,3209,3120,2997,1625,1528,1409,1376,1273,1071,1000,735,645;1H NMR(DMSO-d6),δ: 9.61(s,2H,四唑環上NH)[7, 10];13C NMR(DMSO-d6),δ:159.97(四唑環上C)。
元素分析(C2H4N10,%):計算值,C 14.28、H 2.38、N 83.33;實測值,C 13.99、H 2.29、N 83.07。
1.2.3 5,5′-肼基雙四唑二羥胺鹽的合成
向裝有溫度計和機械攪拌的反應瓶中依次加入0.168g(1mmoL)5,5′-肼基雙四唑和3mL去離子水,溫度降至10~15℃時加入0.33g(5mmoL)50%羥胺水溶液,加完后繼續反應1h,反應液倒入20mL無水乙醇中快速攪拌,析出白色固體,靜置,過濾,無水乙醇淋洗,得白色粉末狀固體0.22g,收率94.0%,分解溫度241.7℃(DSC法)。
IR(KBr),υ(cm-1):3295,1645,1625,1549,1410,1352,1272,1228,1131;1H NMR(DMSO-d6),δ:10.66(s,8H,2NH3OH+),8.92(s,2H,NH);13C NMR (DMSO-d6),δ:162.63;15N NMR(DMSO-d6),δ:-298.87,-284.75,-110.55,-4.70。
元素分析(C2H10N12O2,%):計算值,C 10.26,H 4.274、N 71.79;實測值,C 10.14、H 4.200、N 72.11。
1.3 性能測試
密度測試采用真密度分析儀,測試條件為:測試溫度25℃,樣品質量0.3~0.5g,載氣為氦氣,額定工作壓力15~20psi。
DSC測試采用Q-200型差示掃描量熱儀,測試條件為:氮氣流速50mL/min,升溫速率10℃/min,溫度區間為50~400℃,試樣質量0.5mg,試樣皿為鋁坩堝。
TG測試采用TG209F3型熱重儀,測試條件為:氮氣流速50mL/min,升溫速率10℃/min,溫度區間50~400℃,試樣質量約0.5mg,試樣皿為氧化鋁坩堝。
相容性測試采用Q-200型差示掃描量熱儀,測試條件為:流速50mL/min,升溫速率10℃/min,溫度范圍50~350℃,試樣質量HBT-HA約0.5mg,改性雙基推進劑試樣約0.5mg,試樣皿為鋁盤。
撞擊感度采用BAM落錘法測試,測試條件為:落錘質量10kg,藥量5mg。
2 結果與討論
2.1 還原反應工藝條件優化
2.1.1 Mg與SZT·5H2O摩爾比對收率的影響
保持還原溫度為95~100℃,反應時間5h,反應液冷卻至45~50℃,鹽酸質量分數為25%的條件下,考察了Mg與SZT·5H2O摩爾比對反應產物收率的影響,結果表明,當摩爾比分別為1∶1、2∶1、4∶1、6∶1、8∶1時,收率分別為73.1%、84.3%、92.4%、93.3%和93.6%。
當Mg與SZT·5H2O摩爾比為1∶1時,產物產率為73.1%,增加Mg加入量,摩爾比由1∶1增至4∶1,收率從73.1%增至92.4%;繼續提高Mg加入量,收率的增加趨于平緩。提高Mg與SZT·5H2O摩爾比為8∶1時,收率為93.6%。結合實驗結果和原子經濟,Mg與SZT·5H2O摩爾比為4∶1。
2.1.2 反應溫度的影響
保持Mg與SZT·5H2O摩爾比為4∶1,反應5h,反應液冷卻至45~50℃,鹽酸質量分數為25%,考察反應溫度對收率的影響,結果表明,當反應溫度分別為65~70℃、75~80℃、85~90℃、90~95℃、95~100℃時,收率分別為50.2%、73.8%、81.6%、88.3%和88.9%。
當反應溫度為65~70℃時,產物收率為50.2%,并且反應收率隨著反應溫度的升高明顯增加,反應濾液加入鹽酸溶液后攪拌時無固體產生,需放置過夜,且攪拌過程中產生氣泡,這是由于未反應的SZT·5H2O在酸性條件下易分解造成的。當反應溫度為90~95℃時,反應收率達到了88.3%,并且此時的濾液加酸攪拌時即可產生固體。繼續提高反應溫度,上升趨勢緩慢。當反應溫度為95~100℃時,反應收率達到了88.9%。綜合考慮,選擇反應溫度為95~100℃。
2.1.3 反應時間的影響
保持Mg與SZT·5H2O摩爾比為4∶1,反應溫度為95~100℃,反應液冷卻至45~50℃,鹽酸質量分數為25%,考察反應溫度對收率的影響,結果表明,當反應時間分別為1、3、5、7、9h時,收率分別為74.0%、82.6%、91.5%、91.1%和91.4%。
由此可知,反應對間對收率的影響較大,當反應時間為1h,收率為74.0%,隨著反應時間的延長,收率不斷提高。當反應時間為5h時,收率達到最大值;繼續延長反應時間,收率無明顯提高。因此,最佳反應時間為5h。
2.2 中和反應工藝條件優化
針對HBT-HA的工藝條件優化,選取水作為反應溶劑,主要考察物料比、反應溫度和反應時間對中和反應的影響。
2.2.1 物料比的影響
HBT用量為0.168g(1mmoL),控制反應溫度10~15℃,反應1h,研究了物料比n(HBT)∶n(NH2OH)對中和反應的影響,結果見表1。
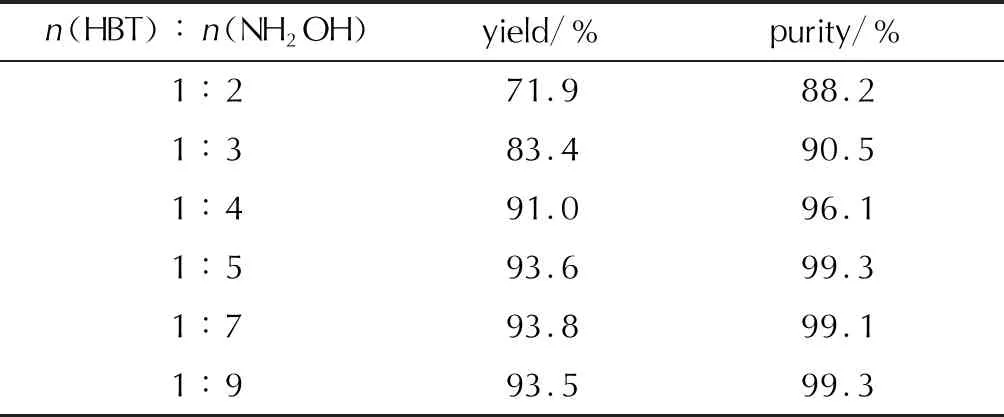
表1 物料比對中和反應的影響Table 1 The effect of the molar ratio of raw materials on the neutralization reaction
由表1可知,當n(HBT)∶n(NH2OH)為1∶2時,產物產率為71.9%,純度僅為88.2%。增加NH2OH的用量,產率和純度顯著升高。當n(HBT)∶n(NH2OH)為1∶4時,產物產率為93.6%,純度為99.3%,證明反應充分。繼續提高NH2OH的用量,n(HBT)∶n(NH2OH)為1∶7和1∶9時,產物的產率和純度變化不明顯。綜合考慮,羥胺的最佳加入量為HBT的5倍。
2.2.2 反應溫度的影響
當n(HBT)∶n(NH2OH)為1∶5,反應1h,研究了反應溫度對中和反應的影響,結果見表2。
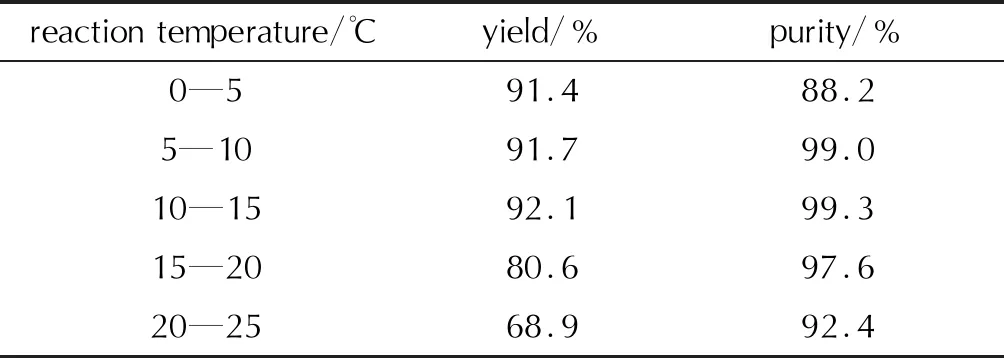
表2 反應溫度對中和反應的影響Table 2 The effect of reaction temperature on the neutralization reaction
由表2可知,反應溫度對目標產物收率的影響較為明顯,溫度從0~15℃,收率大于90%,且趨勢平穩。當溫度大于15℃,收率下降,將反應液倒入無水乙醇中,析出固體明顯變少,處理后固體表面發黃,不松散,經核磁檢測有偶氮化合物生成,分析原因可能生成的HBT-HA被氧化所致[7]。綜合考慮,在其他反應條件相同的情況下,選擇10~15℃反應。
2.2.3 反應時間的影響
當n(HBT)∶n(NH2OH)為1∶5,控制反應溫度在10~15℃,研究了反應時間對中和反應的影響,結果見表3。
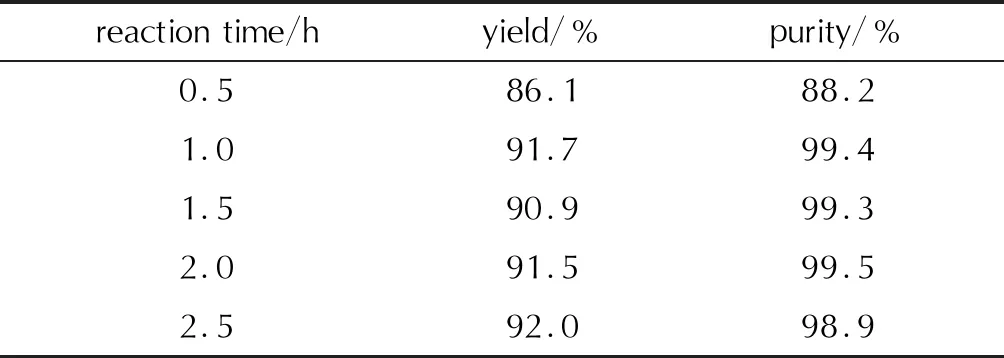
表3 中和反應時間對產物產率和純度的影響Table 3 The effect of reaction time on the neutralization reaction
由表3可知,當反應時間為0.5h,收率為86.1%,純度為88.2%。隨著反應反應時間的延長,反應更加充分,收率提高。當反應時間大于1h時,收率變化不大,穩定在90%以上。綜合以上數據,選取最佳反應時間1h。
2.3 HBT-HA 的性能
2.3.1 HBT-HA的熱性能分析
在升溫速率10℃/min的條件下,利用DSC和TG-DTG研究了HBT-HA的熱分解特性,結果如圖1所示。
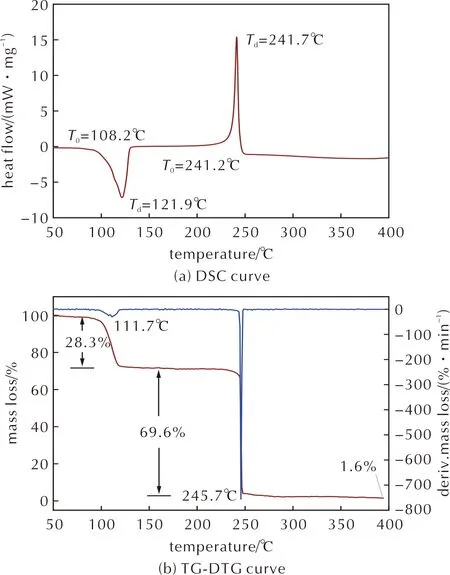
圖1 HBT-HA的DSC及TG-DTG曲線Fig.1 DSC and TG-DTG curves of HBT-HA
從圖1(a)可知,HBT-HA在121.9℃有一個明顯吸熱峰,而HBT-HA熱分解起始溫度為241.2℃,熱分解峰值溫度為241.7℃,高于文獻報道的多個雙四唑衍生物的熱分解溫度,這可歸于雙四唑分子的結構對稱性。HBT-HA的熱分解完成溫度為250.5℃。
由圖1(b)可知,HBT-HA存在兩個失重過程。第一個失重階段發生在50~130℃溫度區間,初始失重溫度為91.6℃,111.7℃時失重速率最快,該階段失重28.3%,結合失重量和DSC數據可以推測,該階段可能是2個羥胺陽離子吸熱分解導致。HBT-HA的第二個失重階段發生在229~300℃溫度區間,其中245.7℃時失重最快,300℃后曲線基本趨于平穩,該階段失重69.6%,最終殘渣質量分數為1.6%。查閱文獻得知[10], HBT有兩階失重,溫度在202.55℃開始失重,至218.93℃時,失重78.65%,至238.75℃時再失重18.02%,總失重96.67%,低于HBT-HA的總失重。可以看出即使羥胺鹽在第一階段已經分解,但會推遲HBT分解溫度,使其延遲分解。
根據HBT-HA的分子結構、DSC曲線和TG-DTG曲線,推測其可能的分解過程見圖2:第一個失重階段(Stage I)中,HBT-HA先后失去兩個羥胺陽離子,生成肼基雙四唑陰離子,對應的理論失重為29.0%,這與TG曲線中第一個階段的失重28.3%基本吻合;第二個失重階段(Stage II)中,推測為雙四唑環的裂解,產生了HCN和大量的N2,這與TG曲線中第二個階段較大比例失重相對應。
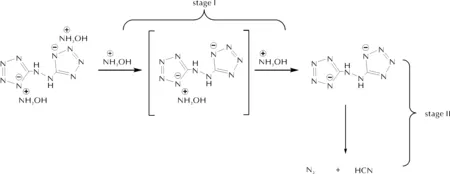
圖2 HBT-HA的分解過程Fig.2 The proposed thermal decomposition process of HBT-HA
2.3.2 HBT-HA的密度、感度及爆轟性能評估
通過Gaussian軟件以密度泛函理論B3LYP/6-31G(d,p)方法計算了生成焓,基于HBT-HA實測密度和生成焓,采用Explo 5 (V6.04)程序[11-12]預估了HBT-HA的爆速、爆壓和爆熱;并與兩種較為典型的四唑鹽5,5′-肼基雙四唑氨基胍鹽[7](AHBT)和偶氮四唑氨基胍鹽[13](AGZT)的綜合性能進行對比,結果見表4。
HBT-HA為白色粉狀固體,可溶于水、二甲亞砜。HBT-HA氮含量為71.8%,實測密度為1.519g/cm3,均略低于AHBT(79.7%,1.618g/cm3)和AGZT(80.2%,1.559g/cm3)。HBT-HA的撞擊感度大于60J,低于AHBT和AGZT,屬不敏感含能材料。HBT-HA的熱分解溫度為241.7℃,熱穩定性好于AHBT和AGZT。在爆轟性能方面,HBT-HA的生成焓、爆速、爆壓分別為1877.3kJ/mol、9118m/s和33.10GPa,均遠高于AHBT和AGZT。HBT-HA分子結構具有對稱性,熱穩定性較高、感度較低;HBT-HA氮含量較高,理論生成焓、爆速、爆壓也高于另外兩種典型四唑鹽。因此,HBT-HA是一種氮含量高、爆轟性能優異的四唑類富氮化合物。
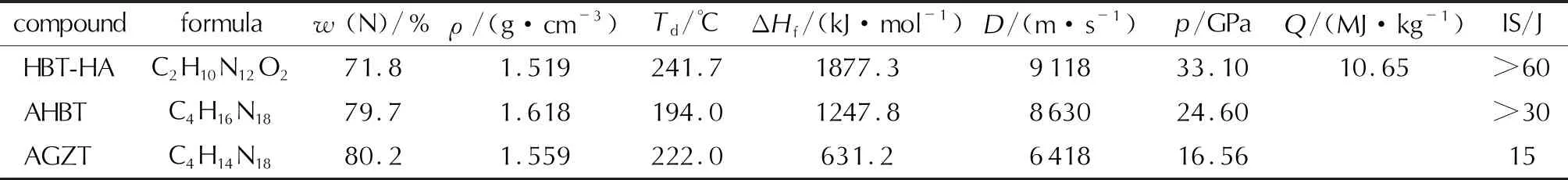
表4 HBT-HA, AGHB和AGZT的性能對比Table 4 Properties comparison of HBT-HA, AGHB and AGZT
2.3.3 HBT-HA的熱分解動力學
為深入理解HBT-HA的熱安全性,采用多升溫速率法計算其熱分解第二階段反應活化能[14],進一步計算獲得相應熱分解反應的活化焓、活化熵、活化吉布斯自由能以及熱爆炸臨界溫度。
(1)活化能
為獲得HBT-HA熱分解過程的反應活化能,在不同升溫速率下獲得了DSC曲線,然后運用Kissinger 法和Ozawa法[15-16],獲得HBT-HA 的熱分解動力學參數,結果列于表5。
Kissinger法計算公式為:
(1)
式中:β為升溫速率,℃/min;Tp為熱分解峰值溫度,℃;A為指前因子,min-1;R為氣體常數,為8.314J/(mol·K);E為活化能,kJ/mol。
得到擬合方程為:Y=32.93X+53.50,R2=0.9986。
Ozawa法計算公式為:
(2)
得到擬合方程為:Y=33.97X+67.99,R2=0.9987。
由表5可知,通過Kissinger方程和Ozawa方程獲得的活化能分別為273.81kJ/mol和268.55kJ/mol,基本相當,均值為271.18kJ/mol,并且兩種方法的線性相關系數R2分別為0.9986和0.9987,均接近于1,故采用這兩種算法對于所選化合物HBT-HA動力學參數的計算可信度較高。此外,HBT-HA的熱分解反應表觀活化能較高,表明該化合物的熱穩定性較好。

表5 HBT-HA 的熱分解動力學參數Table 5 Thermal decomposition kinetic parameters of HBT-HA
(2)活化焓、活化熵和活化吉布斯自由能
通過方程式(3)~(5),可分別計算出HBT-HA熱分解反應的活化焓ΔH、活化吉布斯自由能ΔG和活化熵ΔS分別為269.61kJ/mol,131.37kJ/mol和273.67J/(K·mol)。
(3)
Δh=E-RTp
(4)
ΔG=ΔH-TpΔS
(5)
(6)
式中:k為玻爾茲曼常量,J/K;h為普朗克常量,J·s;βi為第i種升溫速率,K/min;Tp, i為升溫速率βi下的熱分解峰值溫度,K;Tp0為β→0時的熱分解反應峰值溫度,K;m,n為擬合系數。
(3)熱爆炸臨界溫度
熱爆炸臨界溫度Tb是含能材料由熱分解轉為熱爆炸的關鍵溫度點,是反映和衡量火炸藥等危險品熱穩定性的一個重要參數,關系到火炸藥的加工、使用和貯存安全性,其值可通過式(7)計算:
(7)
式中:E0為β→0時的熱分解反應活化能,kJ/mol。由式(6)求得Tp0為505.15K,當E0取273.81kJ/mol時,由式(7)可得Tb為513.15K。
2.4 HBT-HA與雙基推進劑的相容性分析
為考察HBT-HA的應用性,將等質量的HBT-HA與常用改性雙基推進劑XKD(硝化棉+硝化甘油60%,RDX 30%,其余為催化劑+工藝添加劑)混合,并利用差示掃描量熱儀研究了HBT-HA與XKD的相容性,結果如圖3所示。
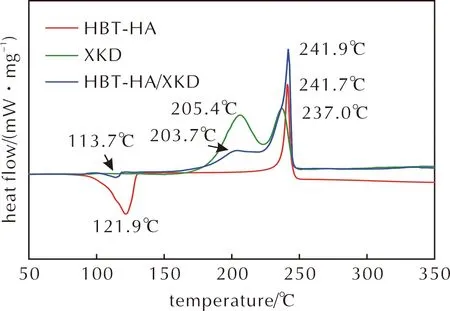
圖3 HBT-HA和XKD的DSC曲線Fig.3 DSC curves of HBT-HA and XKD
由圖3中的DSC曲線可知,雙基推進劑XKD呈現兩個放熱峰,其中205.4℃對應的是硝化棉和硝化甘油混合物的放熱峰,237.0℃對應的是RDX的放熱峰,且第一個放熱峰面積略大于第二個。與之相對比的是,HBT-HA與XKD的混合體系有一個吸熱峰和兩個放熱峰。HBT-HA與XKD混合物的吸熱峰溫度為115.0℃,較HBT-HA的吸熱峰溫度121.9℃相對提前,并且吸熱面積小于HBT-HA,可能原因是XKD中存在可以穩定HBT-HA的化合物。
HBT-HA與XKD混合體系的第一個放熱峰出現在203.7℃,較XKD的第一個放熱峰提前了1.7℃,第二個放熱峰出現在241.9℃,較XKD推后了4.9℃,HBT-HA推后了0.2℃。對比混合體系的DSC曲線和XKD的DSC曲線,發現第一個放熱峰面積變小,而第二個放熱峰面積變大,并且第二個放熱峰的分解時間縮短,是一個快速的固相分解過程。由此可以猜測,HBT-HA可以穩定XKD中的硝化棉和硝化甘油混合物中的部分化合物,使其推遲分解,也可以穩定XKD中的RDX,不僅可以推遲其分解溫度,還可以加速其分解過程。從相容性可以看出,HBT-HA在推進劑中具有較高的潛在應用價值。
3 結 論
(1)設計并合成新型富氮含能離子鹽HBT-HA,通過紅外光譜、核磁共振、元素分析等進行了結構鑒定。對HBT-HA的合成工藝進行了優化,較佳反應條件為:以水為反應溶劑,反應溫度為10~15℃,n(HBT)∶n(NH2OH)為1∶5時反應1h。
(2)HBT-HA的熱分解分為兩個階段:第一階段的熱分解溫度為121.9℃,第二階段熱分解峰值溫度為241.7℃,撞擊感度大于60J,生成焓、爆速、爆壓分別為1877.3kJ/mol、9118m/s和33.10GPa,是一種氮含量高、爆轟性能優異的四唑類富氮化合物。
(3)通過熱分析動力學計算,獲得HBT-HA熱分解反應第二階段的活化能(Ea)、活化焓(ΔH)、活化吉布斯自由能(ΔG)和活化熵(ΔS)分別為271.18kJ/mol,269.61kJ/mol,131.37kJ/mol和273.67J/(K·mol)。
(4)HBT-HA與XKD的相容性結果表明,HBT-HA可以提高XKD的熱穩定性,加速XKD中RDX的熱分解過程。

