作用于GABA受體的獸用殺寄生蟲藥物
鄭小嬌,劉根炎,巨修練
(武漢工程大學 化工與制藥學院,武漢 430205)
GABA (γ-aminobutyric acid)是哺乳動物中樞神經系統(central nervous system, CNS)內重要的抑制性神經遞質。GABA從突觸細胞釋放后作用于GABA受體(γ-aminobutyric acid receptor),激活離子通道打開使氯離子內流,從而對生物體的神經活動產生抑制作用。GABA受體是醫藥、獸藥、農藥的重要作用靶標,具有亞型多樣性及作用位點復雜性的特點[1-3]。在哺乳動物中,根據受體結構和功能區分及藥理特性,將GABA受體分為3種亞型:離子型通道GABAA受體、GABAC受體以及代謝型GABAB受體。GABAA受體屬于半胱氨酸環配體門控離子通道超家族,是一種五聚體跨膜糖蛋白,與其他神經遞質門控離子通道相似,GABA受體包含一個由5個跨膜亞基共同組裝的中央氯離子通道孔[4-5]。研究表明,在哺乳動物中,GABAA受體由19種亞基(α1-6,β1-3,γ1-3,δ1,ε1,Φ1,π1,ρ1-3)組合而成[6],每個亞基包含400~550個氨基酸殘基,由3個結構域組成:約220個氨基酸殘基組成的胞外N端配體結合區域(ligand-binding domain, LBD),這部分為長鏈的親水區,主要為折疊結構;4個跨膜疏水序列(TM1-TM4)構成的跨膜區域(transmembrane domains, TMDs),主要為螺旋結構,它們來回4次橫穿細胞膜,組成跨膜通道,其中TM2組成通道內壁;另外,還有處于細胞內基質的環,它是各亞基變異度最大的區域,目前對這部分序列的結構和功能研究較少[2]。
不同于哺乳動物,昆蟲GABA受體目前并無GABAA、GABAB、GABAC受體3種亞型之分,一般認為昆蟲GABA受體與哺乳動物的GABAA受體相似度較高[7]。對昆蟲GABA受體的研究遠不及哺乳動物GABAA受體,迄今為止,昆蟲離子型GABA受體僅通過克隆得到3種亞基:RDL (Resistance to dieldrin)、GDR (GABA and glycine-like receptor ofDrosophila melanogaster)和LCCH3 (Ligand-gated Chloride Channel Homologue 3)。其中,RDL亞基因對狄氏劑具有抗性而得名,研究表明,目前僅發現RDL亞基能形成功能性門控氯離子通道[8-10]。與哺乳動物GABAA受體相比,RDL氨基酸序列具有高度的相似性,RDL亞基的TM3和TM4之間的連接片段較長,但同樣具有跨膜疏水區,其結構與GABAA受體亞基相似。2004年Miller等首次報道了由5個β3亞基組成的人GABAA受體同源五聚體的三維晶體結構,對GABAA受體的研究具有劃時代的意義,隨后有關人的幾種GABAA受體也被相繼解析出來。但目前還沒有昆蟲GABA受體晶體結構被解析的報道[11-12]。
GABA受體調節劑(modulator)分為激動劑(agonist)和拮抗劑(antagonist),拮抗劑又分為競爭性拮抗劑(comparative agonist, CA)及非競爭性拮抗劑(nocomparative agonist, NCA)。目前作用于GABA受體作為殺寄生蟲的藥物主要分為4類:⑴ 多氯環烷烴,其中代表品種為林丹(lindane);⑵ 苯基吡唑類,其中代表品種為氟蟲腈(fipronil);⑶ 大環類酯,其中代表品種為伊維菌素(evermectin);⑷ 異噁唑啉類,其中代表品種為氟雷拉納(fluralaner)。現將這4類殺寄生蟲藥物分別予以介紹。
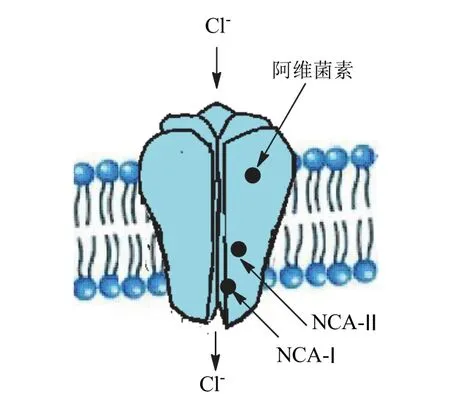
圖1 GABA受體及配體結合位點示意圖
1 多氯環烷烴
多氯環烷烴作為殺蟲劑具有較長的歷史。1825年Farady發現苯和氯氣在日光下反應可以得到一種固體產物六氯環己烷,由于分子結構為C6H6Cl6簡稱為六六六。1912年Lindene指出,在六六六混合物中存在4種立體異構體。直到1935年六六六的殺蟲活性才由Bender發現。隨后Dupire和Slade也各自發現了六六六的殺蟲活性。Slade還進一步指出,六六六的生物活性幾乎完全是由于γ-六六六異構體的存在所引起的。含γ-體99%以上的六六六就叫林丹(lindane),其具有觸殺和胃毒殺蟲作用,也有一定的熏蒸作用。在此基礎上,20世紀50-60年代先后開發上市的殺蟲劑有艾氏劑、狄氏劑、毒殺分、硫丹等多氯環烷烴類(圖2)。1982年Matsumura等通過同位素示蹤方法發現該類殺蟲劑作用于GABA受體的NCA作用位點,這是世界上首次報道該類殺蟲劑作用靶標為GABA受體[13-14]。該類殺蟲劑對土棲害蟲、植食性害蟲、衛生害蟲及一些動物寄生蟲均有效,20世紀60-70年代在我國得到廣泛應用,由于其在環境中不易降解及蓄積毒性,現已被禁止作為農藥及獸藥使用。該類殺蟲劑作用于GABA受體的NCA結合位點,該位點位于GABA受體離子通道跨膜段M2區域,為區別于其他NCA結合位點,稱為NCA-Ⅰ位點[15]。
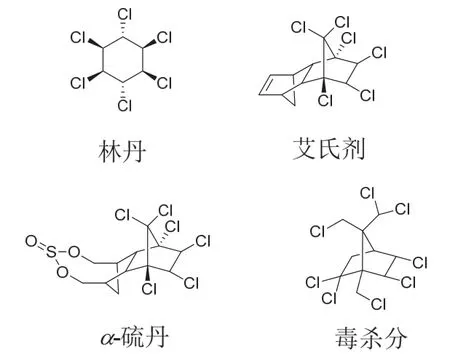
圖2 代表性多氯環烷烴分子結構
2 苯基吡唑類
苯基吡唑類殺蟲劑是20世紀80年代羅納-普朗克公司在開發除草劑的過程中開發出的一類新穎結構的殺蟲劑,代表品種有氟蟲腈(fipronil)、乙硫蟲腈(ethiprole)等。氟蟲腈是由羅納-普朗克農化公司于1987年研制開發,并于1993年開始商品化在全球范圍內推廣使用。它是一種高效、低毒的殺蟲劑,也是第1個上市的苯基吡唑類殺蟲劑,對哺乳動物和昆蟲具有較高的特異選擇性。通過同位素示蹤及電生理等方法確認該類殺蟲劑作用于GABA受體的NCA-Ⅰ位點,與多氯環烷烴類殺蟲劑作用位點一致,兩類殺蟲劑具有交互抗性[16]。其后,陸續有苯基吡唑類殺蟲劑被推向市場,如具有與銳勁特相類似的化學結構的乙蟲腈,吡唑環4位為乙基亞砜,是安萬特公司開發的殺蟲、殺螨劑,其生物活性與氟蟲腈相近,但生產成本低于氟蟲腈,安全性高于氟蟲腈。1996年Frontline (福來恩,fipronil)作為寵物用藥在美國上市,適用于寵物各階段的跳蚤蟲卵、幼蟲、成蟲,虱子以及蜱蟲,也可有效預防包括Lyme在內的多種疾病[17],目前作為殺寄生蟲藥物大量使用。
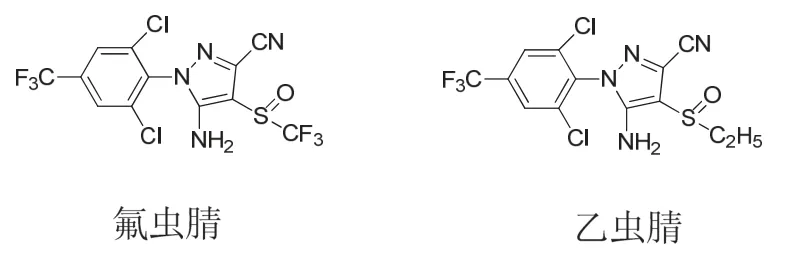
圖3 苯基吡唑類殺蟲劑氟蟲腈和乙蟲腈
3 大環內酯
阿維菌素從首次被發現至今已經有近半個世紀的歷史。1976年,科學家在日本靜岡縣意外發現了鏈霉菌(Streptomycesa vermitilisMA-4860),在此之后不久美國默克公司(Merck)則在Streptomycesa vermitilisMA-4860的發酵菌絲內發現了8種天然大環內酯類同系物[18-19]。該公司將此類化合物定名阿維菌素(avermectin),但其中活性最高的是阿維菌素B1a,又稱abamectin或簡稱AVM。默克公司在1981年向市場推出了商品化的阿維菌素。阿維菌素類化合物主要由以下結構組成:主體結構十六元內酯環,以及與環連接的二糖基、六氫苯并呋喃環系和螺縮酮系等[20-21]。自從阿維菌素問世后,鑒于其抗蟲譜廣、殺蟲活性高、對哺乳動物安全性高等優點,受到了全球藥物科研人員的追捧,該發明獲得2015年的諾貝爾生理學或醫學獎。迄今為止,人類基于天然阿維菌素母體結構改造得到了安全、高效的阿維菌素衍生物,其中不乏成功案例,諸如生物活性較高的有伊維菌素(ivermectin, IVM),目前作為醫藥及獸藥使用得到廣泛應用[22-23]。研究表明,阿維菌素作為GABA受體調節劑作用于該受體氯離子通道的亞基疏水段M1與M2或M3的交界區域,對GABA受體具有雙向調節作用,低濃度刺激氯離子內流,高濃度阻滯氯離子內流。阿維菌素作用位點與目前發現的殺蟲劑其他作用位點沒有交互抗性[24]。阿維菌素的衍生物仍在不斷開發中,甲胺基阿維菌素苯甲酸鹽在農業害蟲防治中得到了廣泛應用。
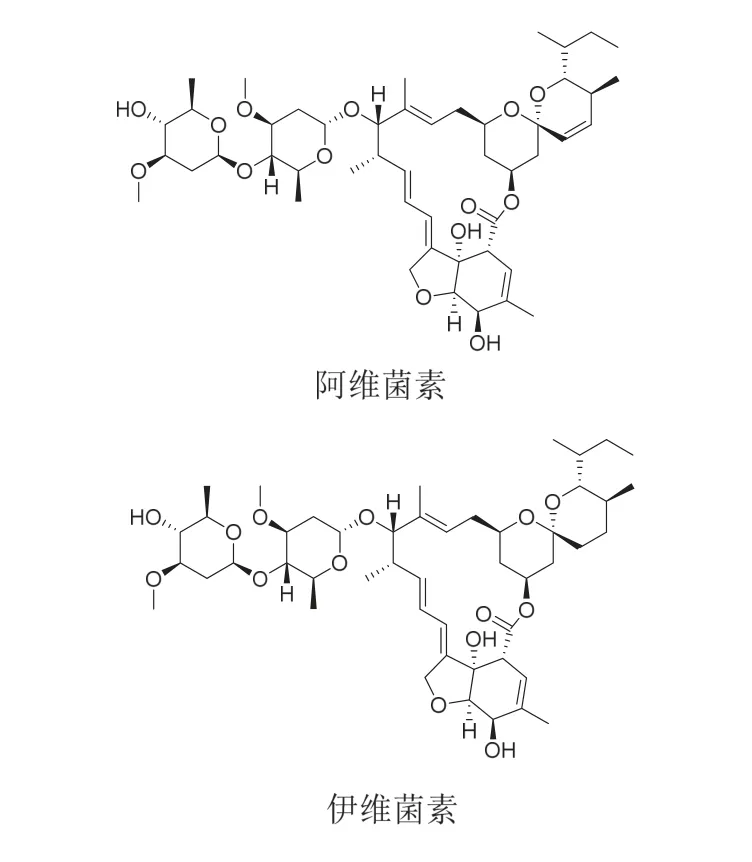
圖4 大環內酯類殺蟲劑阿維菌素和伊維菌素
4 異噁唑啉類
2004年,日本日產化學工業株式會社首次合成氟雷拉納,該化合物屬于異噁唑啉類,并于2005年獲得國際專利授權[25]。研究表明該類殺蟲劑作為GABA受體非競爭性拮抗劑作用于GABA受體的NCA-Ⅱ位點,NCA-Ⅱ位點可能位于GABA受體跨膜段亞基M1和M3的連接區域,因此該類殺蟲劑與多氯環烷烴類及苯基吡唑類殺蟲劑(作用于NCA-Ⅰ作用位點)沒有交互抗性。目前其作用機制和結合位點仍在研究中[26-27]。Ozoe等人發現化合物氟雷拉納不僅可作用于昆蟲GABA受體也作用于谷氨酸氯門控離子通道,但其對GABA受體的抑制作用比對谷氨酸氯離子通道的更強[28]。氟雷拉納是一種對寄生蟲比較高效的GABA受體NCAs,為全身性抗寄生蟲藥,驅殺犬體表的跳蚤和蜱的作用可持續12周,并表現出比氟蟲腈更高效的特點[29]。該劑于2014年1月首次在歐盟注冊,并于同年4月上市,目前商品化產品Bravecto已在歐洲、美洲市場投入使用。在氟雷拉納的結構基礎上,先后開發了阿福拉納、沙羅拉納、洛替拉納,并均已成功上市,用于寵物寄生蟲的防治[30-32]。目前,氟雷拉納已在超過85個國家注冊,銷售量超過1億片,在全球動物保健產品中銷量排名第一。該類化合物在農業上的應用正在研究中,具有較大的發展潛力。
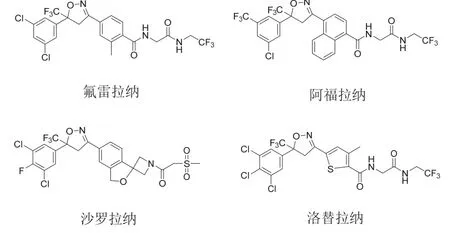
圖5 異噁唑啉類殺蟲劑氟雷拉納、阿福拉納、沙羅拉納、洛替拉納
5 展 望
目前發現作用于GABA受體的殺寄生蟲的藥劑有3個作用位點,分別為:NCA-Ⅰ、NCA-Ⅱ及阿維菌素作用位點。作用于NCA-Ⅰ位點的藥劑主要包括環戊二烯類、多氯環烷烴類、苯基吡唑類,作為獸藥代表品種有林丹、氟蟲腈等;作用于NCA-Ⅱ位點的主要品種有氟雷拉納、阿福拉納、沙羅拉納、洛替拉納。作用于阿維菌素作用位點的大環內酯類化合物代表品種有伊維菌素,仍在廣泛應用。另外,以溴蟲氟苯雙酰胺(broflanilide)為代表的結構新穎的間二酰胺類化合物與異噁唑啉類化合物均表現較好的殺蟲活性且作用于GABA受體同一位點NCA-Ⅱ[33-34],它們已在農業上推廣應用[35],2021年在我國上市。該類化合物也具有開發為殺寄生蟲藥物的潛力。GABA受體具有亞型多樣性及配體結合位點多樣性的特點,是研發殺蟲劑及其作用位點的良好選擇。

