磁性納米顆粒在DNA分離純化中的應用
李婧涵 董 玲
(復旦大學附屬中山醫院,上海 200032)
DNA是儲存、復制和傳遞遺傳信息的主要物質,隨著現代分子生物學技術不斷發展,DNA的檢測和定量分析可以作為許多臨床疾病診斷、臨床治療的評價及人類遺傳學等研究的基礎,而DNA的分離純化是分子生物學和臨床醫學中最為基本的操作步驟,也是下游分析如PCR、凝膠電泳和測序等生物學分析的先決條件。DNA的分離純化是指從細胞和細菌的裂解液、全血或其他含有DNA的雜質樣品中提取出達到一定純度的DNA的過程。DNA提取的質量如純度和完整性,會顯著影響后續分析的準確性和靈敏度。
目前,DNA的分離手段主要包括2大類:液相分離及固相分離。液相分離是最傳統的DNA分離方法,是基于有機溶劑的萃取,包括Chomczynski’s法、苯酚-氯仿提取法和十六烷基三甲基溴化銨(CTAB)提取法等多種方法。液相分離方法雖然有效且成本低,但存在著較大的局限性,如:所需樣品量大、分離時間長、步驟繁瑣、易受污染、回收率及純度較低等缺點,使其不適用于自動化和規模化的分離;使用的有機溶劑有毒性,會造成環境污染和操作者損傷;此外,液相分離中有機溶劑殘留可能對后續PCR等操作有抑制作用。為了提高提取DNA的純度與回收率,DNA分離方法在不斷更新,目前固相分離的方法受到更多研究者的青睞。固相分離的方法主要是指采用一些對DNA有吸附作用的固相材料顆粒,在一定條件下結合DNA,然后又在適當條件下脫附,實現DNA的分離。固相分離常使用吸附劑在離心旋轉柱下進行,二氧化硅基質、玻璃顆粒、硅藻土和陰離子交換樹脂等是常作為吸附劑的材料。與液相分離方法相比,固相分離方法減少了有機溶劑的使用,操作簡便,時間短,樣品不易污染與降解,提取的DNA濃度和純度都相對較高。1997年,Hawkins等提出了基于磁性材料快速分離核酸的方法,如今磁性材料迅速發展成為了主要的核酸固相分離工具。
1 磁性固相萃取(MSPE)
磁性固相萃取是應用功能化磁性納米材料從樣品中提取DNA等物質的方法。磁性納米材料是一種處于1~100 nm的磁性材料,不僅具有普通納米材料的小尺寸效應、表面效應、宏觀量子隧道效應和量子尺寸效應等性質,還具備特殊的磁性特征,包括超順磁性、高矯頑力以及磁化率。超順磁性指的是在外磁場作用下磁性納米顆粒的狀態,與順磁體在外磁場的反應類似,只是吸引力更大,因此稱為“超順磁性”,故磁性納米顆粒可以很容易在外部磁場的存在下被引導,從而實現與其他組分分離。磁性納米材料對DNA的分離主要原理是利用顆粒表面的功能基團(圖1),通過靜電作用、氫鍵和疏水作用等不同的結合手段,將DNA固定在磁性納米材料表面,使用磁性引導將DNA與材料的結合物從樣品中分離,再利用適當的條件進行解吸(圖2)。磁性固相萃取操作簡單,避免了繁瑣的離心步驟,也避免了毒性有機試劑的使用,還具有易實現自動化的優勢,可大規模從樣品中分離DNA。

圖1 磁性納米顆粒表面修飾的示意圖Fig.1 Schematic diagram of surface modification of magnetic nanoparticles
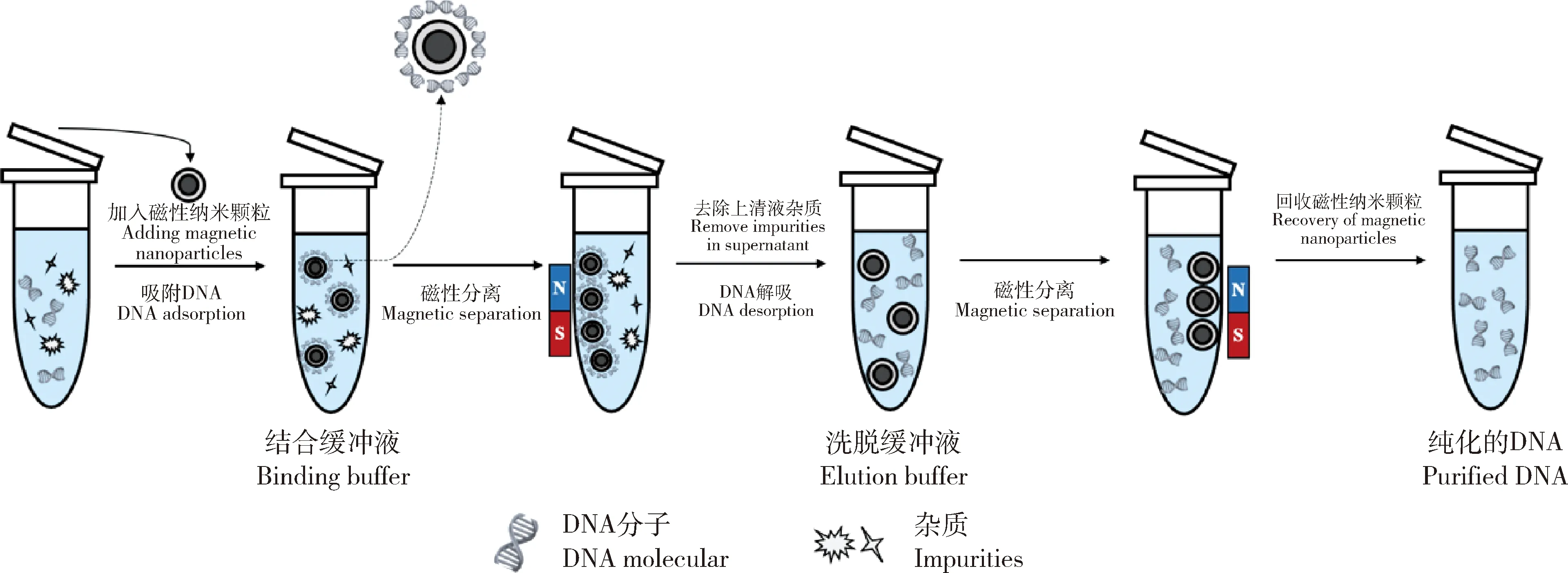
圖2 磁性納米顆粒吸附和洗脫DNA的示意圖Fig.2 Schematic diagram of DNA adsorption and elution by magnetic nanoparticles
磁性納米顆粒可以分為4類,分別為金屬氧化物如FeO、FeO及CoO等,純金屬如Fe、Co及Ni等,其它磁性化合物如鈷鐵氧體、錳鐵氧體及鎂鐵氧體等,磁性合金如鐵鉑合金及鈷鉑合金等。其中基于氧化鐵納米粒(IONP)的技術正在快速發展,因其制備過程較為容易,在納米尺度上具有超順磁性、在外磁場作用下分離快、分散性好、生物相容性好和安全性較好等特點,應用最為廣泛。
1.1 磁性Fe3O4納米顆粒
磁性FeO納米顆粒具有低毒性和比表面積較大等特點,可以搭載小分子物質、核酸、蛋白質或負載藥物;還具有優越的超順磁性,可以很容易地從混合物中分離出來;并且可以在表面改性附加上所需的功能基團,增強與物質的結合能力。因此在生物和醫學領域一直展現出獨特的優勢,應用最為廣泛。
但是磁性FeO納米顆粒由于其比表面積較大的特征,聚集傾向比較劇烈,分散性較差,穩定性較差;此外,FeO化學活性高,容易被氧化,結合DNA后的超順磁性有所減弱,會對磁性分離的高通量和自動化優勢有所影響。因此,多是在其表面進行功能化修飾,如負載二氧化硅及其衍生物和添加活性官能團等,可加大其分散程度,同時保障與外界接觸的組分不受氧化等影響。此外,表面功能化修飾還可通過靜電作用等結合核酸,用于快速分離。
對于磁性FeO納米顆粒的表面功能化修飾,按照修飾材料的種類可以分為3類:無機材料修飾、有機小分子修飾和高分子聚合物修飾。
1
.1
.1
磁性FeO納米顆粒的無機修飾1.1.1.1 SiO
在眾多可被用來修飾磁性FeO納米粒子的無機材料中,SiO的應用最為廣泛。主要是因為其具有以下優點:1)具有很好的生物相容性和惰性,防止磁性納米顆粒聚集,可以使磁性納米粒子在生物體系中穩定存在;2)制備SiO修飾的FeO納米粒子技術已經較為成熟,也相對簡單方便;3)易被進一步功能化,可與其他生物分子結合,方便引入其他活性基團。
早在2006年,Zhang等制備了1種由均勻分散在SiO中的磁性納米顆粒組成的新型介孔微球,并應用這些磁性粒子作為吸附劑從酵母細胞和玉米粒中分離基因組DNA,提取的DNA具有令人滿意的完整性、產率和純度,是較早期成功利用磁性納米顆粒提取DNA的試驗之一。SiO層對FeO納米粒子進行表面修飾可以提高其吸附質粒DNA的功能性和特異性,提取的DNA產量和純度均較高。包覆SiO的磁性納米粒子不但較裸露的FeO納米粒子具有更佳的DNA吸附能力,較商業化產品也不遜色。使用SiO包裹的磁性納米顆粒提取腸桿菌培養物的質粒DNA、提取乙型肝炎病毒和巴爾病毒的基因組DNA及從人全血中提取DNA,均較商業試劑盒提取速度快、產量高且自動化程度好,也可應用于下一步的分子生物學步驟。較多研究表明,顆粒的孔徑及吸附條件等均對DNA吸附能力具有影響。Sen等利用SiO包裹的磁性納米顆粒分別吸附鮭魚精子DNA和大腸桿菌RNA,最大吸附量高達10.6 mg/g DNA或7.7 mg/g RNA。而利用中孔SiO-磁性納米顆粒提取鮭魚精子DNA及從細菌裂解物中純化質粒DNA,提取效率均表明中孔材料具有較高的DNA結合能力。此外,增加鹽濃度或降低pH可以促進DNA在中孔SiO磁性納米粒子中的吸附,對RNA的吸附能力同樣是酸性條件大于堿性。故顆粒的孔徑及相關吸附條件均可成為提高材料提取DNA能力的研究方向。
1.1.1.2 SiO包覆后引入其他活性集團
SiO廣泛應用于包覆FeO制備磁性納米顆粒,不僅可以有效防止磁性納米顆粒聚集,同時也方便引入如氨基及血紅蛋白等其他活性基團。
相較SiO包覆的磁性納米顆粒,引入活性官能團后可提高DNA吸附效率。應用氨基功能化SiO涂層磁性納米粒子,可通過增強靜電相互作用產生選擇性DNA分離。與僅SiO涂層的納米顆粒相比,氨基官能化納米顆粒的吸附效率高4~5倍,與傳統的酚氯抽提方法相比也有很大的優勢。得到的質粒DNA保留了生物學活性,可應用于下游生物學分析。同樣是氨基功能化的SiO磁性納米粒子,其制備方法及吸附DNA的形態均會對提取DNA的能力造成影響。Sheng等改進了采用氨基硅烷來構建氨基改性的磁性介孔SiO納米粒子(MMSN @ EDPS)的方法,使其具有獨特的介孔結構和更大的比表面積,使DNA結合能力有著顯著的提高。Shan等通過在吸附前將細長的DNA縮合成緊密的小球,促進氨基修飾的SiO涂層磁性納米顆粒(ASMNPs)上的DNA負載。在不同環境條件下DNA-ASMNPs絡合形態不同,ASMNPs對縮合的DNA最大負載能力是伸長的卷曲DNA的4.4倍,達到385 mg/g。改變被吸附DNA的形態及改進材料制備的方法均可以提高材料吸附的效率,這為研究提供了新的方法和方向。多數研究表明,磁性納米顆粒對DNA的吸附作用較強,但解吸相對困難,對于提取效率及應用于后續生物學分析可能會有所影響。Bai等使用富含氨基的SiO包覆的磁性納米粒子吸附DNA后,使用脫脂奶粉封閉了磁性納米顆粒和DNA復合物, 可以直接將復合物添加到PCR體系中進行后續生物學分析, 而無需進行繁瑣且費時的洗脫和純化DNA的步驟,一定程度解決了DNA與材料解吸困難的問題。
除引入氨基修飾外,Chen等制得了血紅蛋白(Hb)修飾的磁性納米復合材料,從大腸桿菌培養物中分離質粒DNA,與使用商業試劑盒相比可獲得相當的產率和純度。
1
.1
.2
磁性FeO納米顆粒的有機基團修飾使用有機小分子修飾后,磁性納米粒子在水溶液中具有良好的分散性和穩定性,并且對細胞、DNA和蛋白質的吸附能力增強,毒性較小。
1.1.2.1 羧基
羧基是常用的有機小分子官能團,它易衍生化,并且羧基化的磁性納米顆粒在水溶液中分散穩定性較高。Sarkar等使用羧基包覆的磁性納米粒子簡單并高效的從哺乳動物細胞中分離mRNA,并成功從瓊脂糖凝膠中提取pDNA。Shan等使用羧基官能化的磁性納米顆粒(CMNPs)從粗大腸桿菌裂解物中純化質粒DNA并從尿液樣品中提取gDNA。與有機溶劑或商業試劑盒獲得的結果相比,該方法快速、簡單、具有成本優勢且對環境友好,適合自動化核酸提取。
1.1.2.2 水楊酸(SA)
SA是一種具有羧酸和酚類官能位的化學配體,通常用作螯合樹脂的修飾劑,并已被證明具有良好的吸附性能。SA包裹的磁性納米顆粒用于從哺乳動物細胞提取基因組DNA,整個提取分離過程可在30 min內完成。與傳統的離心過濾方法相比具有快速、簡便、可靠及環保等優點。
1.1.2.3 吖啶橙(ACO)
ACO具有強熒光和水溶性,是一種細胞滲透性染色劑,可通過嵌入或靜電引力與DNA和RNA相互作用。Liu等研究了質粒DNA和鮭魚精DNA在配體ACO包被的磁性納米顆粒上的吸附,并證實在溶液中加入0.5 mol/L的CaCl可進一步增強DNA的吸附量。
1.1.2.4 咪唑(IMI)
在中性pH條件下,IMI修飾的磁性納米顆粒(IMI-MNPs)的表面電荷可以為零。因此,通過改變pH很容易將表面電荷從正電荷轉變為負電荷,說明IMI-MNPs擁有電荷可逆性。低pH時,帶正電的IMI-MNPs可以通過靜電作用吸附DNA,而在pH較高時帶負電的IMI-MNPs由于靜電排斥而釋放DNA。Maeda等利用IMI-MNPs從單個細菌細胞中高效地回收了DNA。
1
.1
.3
磁性FeO納米顆粒的高分子聚合物修飾有機高分子材料表面含有大量的功能基團,具有良好的生物相容性,不僅能與磁性納米粒子表面進行有效的反應,還能有效防止聚合物團聚。
1.1.3.1 聚多巴胺(PDA)
多巴胺聚合條件溫和,PDA單體同時包含鄰苯二酚和胺官能團,在水性基質中顯示出良好的分散性,并具有出色的環境穩定性。PDA的親水性和生物相容性使其成為一種通用的表面改性方法。核-殼型結構的PDA@FeO可基于靜電相互作用與DNA結合,并通過pH調節PDA@FeO表面酚羥基和氨基的電荷轉換來捕獲和釋放DNA,提取率較離心柱法等傳統方法高。Wang等將PDA修飾在帶有羧基的FeO納米粒子表面,利用其在酸性條件下表面帶正電荷的特性,進行DNA的吸附和提取。在相同體積的結合溶液中制備一系列不同量的標準DNA溶液以測定PDA@FeO對DNA的吸附能力,在5~24 mg范圍內,PDA@FeO捕獲的DNA量與DNA原始量呈線性,超過該范圍,吸附量達到平臺期。實驗計算測得PDA@FeO對DNA的吸附能力為161 mg/g,捕獲量優于使用商業試劑盒和傳統苯酚-氯仿提取方法。該方法中未使用PCR抑制劑,也未使用任何有毒的有機溶劑。此外,結合及洗脫溶液的組成很簡單,整個吸附和解吸過程均在室溫下進行,無需高溫孵育,也不需要頻繁離心。
1.1.3.2 聚乙烯亞胺(PEI)
PEI是一種富含氨基的多價陽離子試劑,可與DNA的帶負電磷酸鹽骨干體和部分蛋白質形成強離子相互作用,以吸附DNA。用PEI在FeO納米粒子的表面進行涂層改性,可多次從細菌培養物中分離出高純度質粒DNA,也可與質粒DNA和基因組DNA相結合,且結合效率高于商用試劑盒,從生物樣品中分離出的DNA可直接用于PCR等下游應用。該技術不需要任何有機溶劑,也無需重復離心、真空過濾或色譜柱分離。
1.1.3.3 聚酰胺胺(PAMAM)
PAMAM涂層可以減少磁性納米顆粒團聚,并且可以定制外圍的末端基團來控制復合溶解度。PAMAM樹枝狀修飾的磁性納米粒子(PAMAM-MNPs)可吸附大量DNA,有效的DNA解吸率超過95%,添加二甲基亞砜(DMSO)可以大大改善DNA的回收率,該方法顯示出比市售磁性顆粒更高的DNA提取性能。硫醇功能化PAMAM修飾的磁性納米顆粒(G6 PAMAM-PE-MNPs),在優化條件可回收96%的λDNA。較高的氨基濃度可以提高其對DNA的吸附能力,然而G6 PAMAM-MNPs對DNA釋放率約為總DNA的80%,剩下20%的DNA分子通過靜電作用與固體表面的高密度氨基緊密結合,不容易從固體表面釋放出來。后續可針對DNA與材料的解吸條件進行更深入的研究。
1.1.3.4 殼聚糖(CTA)
CTA是從甲殼類動物殼中提取的幾丁質衍生物,易于獲得、價格低廉且具有生物相容性。因其含有豐富的胺基團,可以通過調整pH進行電荷調節,是一種有用的電荷轉換聚陽離子。CTA上胺基團的pK
約為6.4,即在pH低于6.4時呈陽離子狀態,并且很容易與陰離子核酸結合,形成復合物。低分子量CTA功能化二氧化硅顆粒已被證明可在與PCR兼容的中等高pH(約8.5)下有效洗脫DNA,與酚-氯仿提取方法相比,在操作簡便及選擇性好等方面具有突出的優勢。1.1.3.5 其他高分子聚合物
Percin等制備了新型材料——聚甲基丙烯酸羥乙酯磁性納米粒子,發現其對質粒DNA的總回收效率可以達到92%,且該磁性顆粒在不明顯降低質粒DNA吸附量的前提下可被循環使用6次。Gai等將聚苯胺(PANI)和聚吡咯(PPy)分別包覆在FeO納米粒子表面,證明使用該材料的DNA提取效率優于傳統苯酚-氯仿萃取的方法,且提取的DNA可用于后續生物學研究。Cotchim等使用亞甲藍(MB)、聚丙烯酸和改性氧化鐵磁性納米粒子(PAA/IOMNPs)的復合材料從樣品中吸附DNA,用外部磁鐵從溶液中分離吸附了DNA的MB-PAA/IOMNPs,并用乙酸從PAA/IOMNPs上洗脫MB-DNA,是一種新的提取、檢測和量化痕量級DNA的策略。
1.2 磁性Fe2O3納米顆粒
除FeO磁性納米顆粒之外,FeO磁性納米顆粒在DNA分離提取中也有著廣泛的應用。超順磁多孔FeO-SiO復合微球可提取HBV的DNA,利用該復合微球可初步建立一種穩定的磁性顆粒全血提取法,提取出純度高、產率高、重復性好且完整的全血HBV DNA樣本。γ-FeO@Chi@Pani磁性納米材料可應用于鮭魚精子DNA的吸附。Medina-Llamas等證明了磁性聚苯胺-磁鐵礦納米復合材料(PANI/γ-FeOMNC)是從水溶液中回收純雙鏈DNA的有效試劑,在水溶液中聯合作用10 min就達到了最大的DNA吸附量75.2 mg/g。通過改變溶液的pH值可以幾乎完全釋放由MNC捕獲的DNA。Medina-Llamas等還評估了MNC在多次回收過程后的可重復使用程度,結果表明,PANI/γ-FeOMNC是一種有前途的低成本可重復使用的材料,可實現快速、簡單和有效的DNA分離和提取。
1.3 其他磁性納米顆粒
Hu等通過靜電作用將PEI固定在FePO納米粒子表面制備了納米復合材料,其對DNA的吸附能力為61.88 mg/g。Lee等制造了生物素化的陽離子聚合物(聚吡咯/聚乙烯亞胺)的多功能磁性納米線(PEI/mPpy-NWs)用于從血液樣本中分離cfDNA。PEI/mPpy-NW對DNA的捕獲性能遠遠優于商業Qiagen試劑盒,故可將PEI/mPpy-NW用于處理肺癌血漿樣品獲得cfDNA。
表1 不同磁性納米顆粒對DNA提取效率的對比
Table 1 Comparison of DNA extraction efficiency of different magnetic nanoparticles
吸附材料Adsorbent material提取標本Extractedspecimens最大提取能力/(mg/g)Maximum extractioncapacity提取率/%ExtractionrateA260/A280時間/minTimeSiO2[16]人全血DNA96.4781.79±0.1240中孔SiO2[30]鮭魚精DNA122.2--1 300ASMNPs[35]縮合的DNA385-1.8020SiO2-Hb[37]大腸桿菌質粒DNA27.8668.31.8415MMSN@EDPS[34]小牛胸腺DNA210.2282.95-30Fe3O4吖啶橙[43]質粒DNA181.1--30鮭魚精DNA164.2PDA[47]小牛胸腺DNA161-1.8025PDA[46]人全血中基因組DNA116.790.21.82±0.0425PANI[56]黑曲霉DNA2.08-1.7940~60PPy[56]黑曲霉DNA2.60-1.75-γ-Fe2O3PANI[58]鮭魚精DNA75.294-20Chi@Pani[59]鮭魚精DNA49.5611.71-FePO4PEI[60]各種生物樣本61.88851.88~1.9015
2 磁性納米顆粒應用的發展與展望
綜上所述,磁性固相萃取作為一種新興的且迅速發展的DNA提取方法,其優勢主要在于:安全無毒、操作簡單并可重復使用;通過表面活性官能團與DNA特異性結合,使得提取的DNA純度高且濃度大,可以適合痕量DNA提取;并且能夠實現自動化和高通量操作。
基于磁性納米顆粒對核酸出色的吸附能力,其高通量及商業化的核酸提取程序有著可觀的發展前景。Li等研制了一種基于磁珠(MBs)的快速且高質量的通用核酸提取試劑盒,命名為MB-100,同時對其性能進行了探索。結果表明,它的提取效率遠高于其他2種商業化的試劑盒,隨后的PCR反應也有著更高的擴增效率。Chen等開發了一種全自動快速核酸提取器(NAE),可以使用MNPs同時處理16個樣品,多數樣品的提取過程可在30 min內完成;還優化了運動控制、機械結構和試驗配方以提高產量和凈化產品,并應用了肝癌樣本對產量及純化效果進行了驗證,表明了所開發的系統穩定可靠。
目前應用磁性納米顆粒提取核酸已經投入商業化的使用,常用的商用試劑盒有英國的PrimerDesign、荷蘭的Magtivio、美國的Omega、國內的博科、麥伯及百奧萊博等核酸快速提取試劑盒。試劑盒的核酸提取效率毋庸置疑,但價格昂貴,1 mL磁珠產品價格為1 000元左右不等。也有一體式的核酸提取機器如賽默飛的KingFisher全自動核酸提取儀和德國Chemagen全自動核酸提取儀等,但價格更為昂貴,對于需要批量多樣本提取核酸的操作可能會有比較高的經濟要求。
磁性納米顆粒的研究有幾十年的歷史,對于其特性、制備、類型和應用等多方面已有較為透徹的研究。通過綜合前人研究與對比,總結了多種不同活性修飾的磁性納米粒子對DNA分離提取的效率,如表1所示。綜合文獻的結論可知,磁性納米顆粒對DNA的分離提取效率取決于多種因素,而改進這些因素從而提高DNA提取效率,或在顆粒制作等過程中降低成本是磁性固相萃取進一步投入商業化發展的研究前景。
首先,磁性納米顆粒本身的性質如尺寸、孔徑大小及磁化強度等與分離提取的DNA質量息息相關。因此,構建結構完整、粒徑適宜均一且分散性好的磁性顆粒材料對DNA分離效率的提高極為重要。目前的文獻表明中孔徑的顆粒較大小孔徑有著更高的提取效率,改變顆粒其他性質如尺寸與磁化強度能否進一步提高DNA提取效率或降低制作成本可能是后續磁性納米顆粒的發展前景。
其次,磁性固相萃取的優勢很大一部分在于其可以以一種磁性納米粒子為核心,在此基礎上引入其他活性官能團,而活性官能團與DNA分子間的作用力強弱是影響DNA分離提取效率最重要的因素之一。根據表1對于不同活性官能團修飾的磁性納米顆粒對DNA提取效率的總結與對比可直觀的看到官能團修飾對于DNA提取效率的影響。所以嘗試引入新的活性官能團或改進引入官能團的方式方法,研發新型且高效的功能化磁性納米顆粒,是不斷優化磁性分離過程、提高分離效率和質量的重要手段。而在磁性納米顆粒發展的近20余年內,廣大研究者嘗試了很多種不同官能團的引入,也大致掌握了何種官能團對DNA提取的效率較高,故引入全新官能團以提高效率可能并不容易。但改進磁性納米顆粒的制作過程,可能會使其生產變得更高效或低成本,方便投入大批量生產從而進行商業化應用,這也是磁性固相萃取的發展前景之一。
此外,磁性納米材料的制備方法、所提取DNA的形態性質及結合緩沖液的pH或鹽濃度等實驗條件均對DNA吸附效率有影響。故在材料相同的情況下,改變實驗條件也可能成為提高DNA提取效率的方法。
與其他DNA分離方法相似,提取基因組DNA仍普遍受限于耗時的樣本裂解過程,限制了整體DNA提取的全過程通量及提取時效性。同時,從前人研究可看出,多數磁性納米顆粒對DNA的吸附作用較強,但解吸相對困難,所以DNA的提取效率會有所降低,應用于后續生物學分析的DNA量也會隨之減少。Bai等通過試驗證明,將磁性納米粒子與DNA的復合物直接作為PCR模板可以避免這個問題。但磁性顆粒對PCR擴增過程具有強抑制作用,雖然Bai等證明用脫脂奶粉等物質封閉,可減少磁性顆粒對PCR的抑制作用,但對于絕大多數下游生物學分析來說,洗脫過程不可避免。故在后續開發新型磁性納米顆粒的過程當中,除了關注其吸附DNA的能力,也要盡可能保證在適當條件下DNA能夠順利解吸,即洗脫緩沖液的性質也是探究如何提高磁性納米顆粒對DNA提取效率的切入點之一。
磁性納米顆粒除了在核酸提取中有著廣泛的應用,在很多其他生物醫學應用中也起到了重要的作用。比如磁性納米顆粒可以作為捕獲循環腫瘤細胞的工具,也可作為MRI的造影劑在醫學成像中使用;在疾病診斷中,可應用生物傳感器等進行病毒檢測及癌癥診斷;在疾病治療中,磁性納米顆粒可作為藥物載體,靶向釋放到作用部位,也可應用于腫瘤熱療及血液凈化等療法。基于磁性納米材料的獨特特性,其在SARS-CoV-2的預防和治療中也可有廣泛應用,也可在對抗COVID-19的斗爭中起到一定作用。
總而言之,磁性納米顆粒在生物醫學中的應用極為廣泛,有著很強的研究發展前景。
3 總 結
本研究通過多文獻綜合對比總結了以鐵氧化物為核心的磁性納米材料,總結了其結構與表面相關活性官能團的修飾對DNA提取效率的影響。
磁性固相萃取作為一種新興的且迅速發展的DNA提取方法,有著安全無毒、操作簡單、可重復使用、能夠實現自動化及高通量操作等多種優勢。目前磁性納米材料已經有著比較全面的研究。在后續研究中,可以通過改變磁性納米材料的尺寸、孔徑大小和磁化強度等性質,嘗試引入新的活性官能團,研發新型且高效的功能化磁性納米顆粒,或改變磁性納米材料的制備方法、所提取DNA的形態性質及溶液pH或鹽濃度等實驗條件,以提高DNA與材料的解吸率,不斷優化磁性分離過程并提高DNA分離效率和質量。基于磁性納米顆粒對核酸出色的吸附能力,發展高通量商業化的核酸提取程序,是磁性固相萃取可觀的發展前景。此外,磁性納米顆粒在核酸提取中有著廣泛的應用,表明該材料具有極強的研究發展前景。