糖尿病腎病患者血漿細(xì)胞游離DNA中羥甲基化修飾lncRNA的篩選及其ceRNA調(diào)控網(wǎng)絡(luò)構(gòu)建
儲(chǔ)金林,馬睿瑤,鐵璐,李琳琳
1新疆醫(yī)科大學(xué)藥學(xué)院,烏魯木齊 830011;2北京大學(xué)基礎(chǔ)醫(yī)學(xué)院藥理學(xué)系
糖尿病腎病(DKD)是終末期腎病的常見原因,是糖尿病的主要并發(fā)癥之一,嚴(yán)重影響糖尿病患者的整體生活質(zhì)量。細(xì)胞游離DNA(cfDNA)是由于不同組織細(xì)胞死亡而降解的DNA片段釋放到血漿中,攜帶了起源細(xì)胞的遺傳和表觀遺傳信息,檢測(cè)血漿cfDNA可視為一種“液體活檢”,有利于開展各種相關(guān)診斷,避免有創(chuàng)的組織活檢[1]。5-羥甲基胞嘧啶(5hmC)主要是5-甲基胞嘧啶通過TET酶氧化形成,是活性DNA去甲基化相對(duì)穩(wěn)定的中間體,被認(rèn)為是重要的表觀遺傳特征[2]。研究表明,血漿cfDNA的5hmC譜是癌癥及糖尿病等相關(guān)疾病早期檢測(cè)和進(jìn)展監(jiān)測(cè)的有力工具[3-5]。長(zhǎng)鏈非編碼RNA(lncRNA)是在轉(zhuǎn)錄和轉(zhuǎn)錄后水平上通過調(diào)控各種機(jī)制,從而影響基因表達(dá)的重要因子[6-7]。有研究表明,lncRNA基因表達(dá)也可能受到表觀DNA修飾的調(diào)控,如DNA甲基化和組蛋白修飾[8-9],而對(duì)編碼lncRNA的基因組區(qū)域中潛在5hmC變化的研究較少。2021年2月—2022年2月,我們采用5hmC-Seal測(cè)序方法探討DKD患者血漿cfDNA中編碼lncRNA的基因組區(qū)域的關(guān)鍵5hmC改變,再進(jìn)行l(wèi)ncRNA、miRNA和mRNA的調(diào)控網(wǎng)絡(luò)分析,篩選可能的作用分子,為DKD的后續(xù)機(jī)制研究及診療策略奠定基礎(chǔ)。
1 材料與方法
1.1 標(biāo)本來源 收集北京大學(xué)第三醫(yī)院收治的2型糖尿病(DM)患者14例,其中男9例、女5例,年齡31~62(47.9±6.9)歲;DKD患者17例,男9例、女8例,年齡32~77(51.1±16.7)歲。DM的診斷依據(jù)美國糖尿病協(xié)會(huì)(ADA)2020年發(fā)布的標(biāo)準(zhǔn)[10],DKD的診斷依據(jù)KDIGO 2020臨床實(shí)踐指南和2014年中國糖尿病學(xué)會(huì)糖尿病腎病防治共識(shí)[11]。本研究通過北京大學(xué)第三醫(yī)院倫理委員會(huì)審批,受試者均知情同意。
1.2 方法
1.2.1 DKD患者血漿cfDNA的提取 采集DKD患者外周靜脈血2 mL,4℃、1 350 g離心15 min分離血漿,取上清;4℃、13 500 g離心5 min去除白細(xì)胞,取上清。使用QIAamp循環(huán)核酸試劑盒(QIAGEN)提取血漿cfDNA。
1.2.2 DKD與DM患者血漿cfDNA中羥甲基化修飾差異表達(dá)基因的篩選 采用5hmC-Seal技術(shù)。通過Fragment Analyzer對(duì)每個(gè)文庫樣本的DNA條帶大小及分布情況進(jìn)行質(zhì)控,在使用qPCR的方法對(duì)文庫進(jìn)行準(zhǔn)確定量后,在NextSeq500測(cè)序平臺(tái)上進(jìn)行雙端38-bp高通量測(cè)序,測(cè)序試劑盒為Illumina公司的Nextseq500/550 High Output Kit v2(75 cycles),每個(gè)樣品的測(cè)序通量為1.5 Gb,測(cè)序條帶大小為38 bp,最后得到文庫中所有DNA片段的堿基序列。接著進(jìn)行測(cè)序數(shù)據(jù)前期處理:先用Trimmomatic軟件去除每個(gè)原始FASTQ數(shù)據(jù)一些低質(zhì)量、無用的數(shù)據(jù),來評(píng)估序列質(zhì)量,提高后續(xù)分析的效率。用Bowtie2軟件將原始reads數(shù)比對(duì)到人類hg19基因組上,并進(jìn)一步用SAMtools進(jìn)行篩選以保留與基因組的唯一非重復(fù)匹配,使用bedtools將對(duì)端讀取進(jìn)行擴(kuò)展并轉(zhuǎn)換為BedGraph格式,并將其歸一化為對(duì)齊讀取的總數(shù)量,然后使用UCSC基因組瀏覽器中的bedGraphToBigWig轉(zhuǎn)換為bigwig格式,以便在Integrated Genomics Viewer中進(jìn)行可視化。使用MACS識(shí)別潛在的5hmC富集區(qū)域,使用的參數(shù)為MACS14-p1e-3-f BAM-g hs。 使 用bedtools合 并 峰值,只保留出現(xiàn)在10個(gè)樣本以上且小于1 000 bp的峰值區(qū)域。X和Y染色體內(nèi)的5hmC富集區(qū)域被排除,并作為下游分析的輸入。用DEseq2包找出差異基因,篩選條件為|log2FC|>0.5且FDR<0.05(FC為差異表達(dá)倍數(shù),即DKD組與DM組差異表達(dá)倍數(shù)在1.5倍以上;FDR為校正后的P值)。
1.2.3 DKD患者血漿cfDNA中羥甲基化修飾lncRNA的篩選 采用加權(quán)基因共表達(dá)網(wǎng)絡(luò)(WGCNA)程序的R語言包來構(gòu)建差異羥甲基化基因的共表達(dá)網(wǎng)絡(luò)。以擬合指數(shù)R2>0.6使得基因之間的連接服從近似無尺度網(wǎng)絡(luò)分布,再繪制出模塊和性狀之間的相關(guān)性熱圖,以通過各個(gè)模塊與性狀之間的相關(guān)系數(shù)大小及P<0.05篩選出與DKD顯著相關(guān)的基因模塊,最后計(jì)算基因顯著性(GS)和模塊身份(MM),通過設(shè)置GS和MM的取值范圍對(duì)network-Screening函數(shù)計(jì)算得到的基因列表進(jìn)行篩選,從而識(shí)別和鑒定出關(guān)鍵樞紐基因,并從中篩選關(guān)鍵lncRNA進(jìn)行后續(xù)分析。
1.2.4 羥甲基化修飾lncRNA細(xì)胞定位lncRNA在細(xì)胞中具有廣泛的亞細(xì)胞分布,這決定了其功能調(diào)控的多樣性,只有定位在細(xì)胞質(zhì)中,才能形成ceRNA調(diào)控網(wǎng)絡(luò),從而為理解基因的作用機(jī)制提供研究方向。因此我們應(yīng)用 lncLocator(http://www. csbio. sjtu.edu. cn/bioinf/lncLocator/)對(duì) lncRNA 的亞細(xì)胞定位進(jìn)行預(yù)測(cè),尋找lncRNA所在的細(xì)胞位置。
1.2.5 靶向miRNA 的羥甲基化修飾lncRNA 篩選 Starbase 在線分析工具數(shù)據(jù)庫主要對(duì)高通量測(cè)序的CLIP-Seq 測(cè)序分析數(shù)據(jù)和降解組測(cè)序分析數(shù)據(jù)的整合來尋找miRNA 的靶標(biāo),可為探討miRNA的靶標(biāo)提供可視化過程,該數(shù)據(jù)庫包括大量miRNA-ncRNA、miRNA-mRNA、RBP-RNA 和RNA-RNA 的數(shù)據(jù)。因此,我們利用Starbase(http://starbase. sysu.edu.cn/)預(yù)測(cè)lncRNA的靶向miRNA。
1.2.6 羥甲基化修飾lncRNA 診斷價(jià)值及表達(dá)驗(yàn)證 對(duì)最終的關(guān)鍵lncRNA 進(jìn)行受試者工作特征曲線(ROC)分析,若曲線下面積(AUC)≥0.8,則認(rèn)為該基因具有較高的臨床診斷價(jià)值。取SPF 級(jí)雄性C57BL/6 小鼠 9 只,8 周齡,體質(zhì)量 20~22 g,購自北京華阜康生物科技股份有限公司,飼以蛋白含量為21%的標(biāo)準(zhǔn)飼料塊,不限制飲水飲食。適應(yīng)性飼養(yǎng)2 周后,將小鼠隨機(jī)分成 DM 組、DKD 組和對(duì)照組各3 只,DM 組和 DKD 組連續(xù) 5 d 腹腔注射 60 mg/kg STZ,對(duì)照組腹腔注射檸檬酸鈉緩沖液(pH 4.2~4.5)。96 h 后,斷尾取血,測(cè)定血糖濃度,以血糖>16.7 mmol/L為DM造模成功。繼續(xù)飼養(yǎng)16周,以空腹血糖>16.7 mmol/L,蛋白尿、尿素氮、血肌酐水平明顯升高,為DKD 造模成功。取小鼠腎組織,-80 ℃保存。使用TRIzol 試劑提取腎組織總RNA,按試劑盒說明書進(jìn)行RNA 逆轉(zhuǎn)錄,并進(jìn)行擴(kuò)增反應(yīng),目的基因的相對(duì)表達(dá)量用2-ΔΔCt法計(jì)算。
1.2.7 miRNA 靶基因的預(yù)測(cè)及功能富集 應(yīng)用miRDB(https:/www. mirdb. org/)和 TargetScan(https://www.targetscan.org/)2 個(gè)在線數(shù)據(jù)庫預(yù)測(cè)miRNA 的靶向 mRNA。此外,從 NCBI 的 GEO 數(shù)據(jù)庫(Gene Expression Omnibus,https://www. ncbi.nlm.nih.gov/geo/)中下載 mRNA 轉(zhuǎn)錄組測(cè)序(RNA-seq)數(shù)據(jù),數(shù)據(jù)編號(hào)為 GSE96804,使用相關(guān) R 包找到差異基因(|log2FC|>0.5 且FDR<0.05)。將3 個(gè)數(shù)據(jù)庫得到的靶基因取交集作為最后miRNA 靶基因集合。將靶向基因集提交Metascape(https://metascape.org/gp)網(wǎng)站,以P<0.05 為條件進(jìn)行基因本體(GO)分析。
1.2.8 競(jìng)爭(zhēng)內(nèi)源性RNA(ceRNA)調(diào)控網(wǎng)絡(luò)(即lncRNA-miRNA-mRNA 調(diào)控網(wǎng)絡(luò))的構(gòu)建 mRNA、lncRNA 和circRNA 任意類型的兩個(gè)RNA 分子間只要結(jié)合到相同的miRNA,就可能構(gòu)成ceRNA 對(duì),包括mRNA-mRNA、lncRNA-lncRNA、circRNA-circRNA。ceRNA 分析作為lncRNA 功能研究的一種方式,lncRNA-mRNA 共表達(dá)分析結(jié)果結(jié)合miRNA 靶基因數(shù)據(jù)集,基于篩選后競(jìng)爭(zhēng)性吸附結(jié)合miRNA 進(jìn)而調(diào)控靶mRNA表達(dá)的lncRNA-mRNA和circRNA-mRNA關(guān)系對(duì),對(duì)lncRNA 的功能進(jìn)行預(yù)測(cè)。我們使用Cytoscape(3.7.1版)繪制ceRNA網(wǎng)絡(luò),以確定ceRNA網(wǎng)絡(luò)中的lncRNA在疾病中是否有關(guān)鍵作用,調(diào)控關(guān)鍵蛋白。
1.2.9 統(tǒng)計(jì)學(xué)方法 使用SPSS17.0 軟件進(jìn)行數(shù)據(jù)統(tǒng)計(jì)與分析,三組間比較采用單因素方差分析,組間兩兩比較采用t檢驗(yàn)。P<0.05 為差異有統(tǒng)計(jì)學(xué)意義。使用Graph Prism 8.3.0 軟件作圖,使用R 語言版本4.1.0進(jìn)行數(shù)據(jù)分析并生成圖像。
2 結(jié)果
2.1 DKD 患者血漿cfDNA 中羥甲基化修飾差異表達(dá)基因的篩選結(jié)果 測(cè)序數(shù)據(jù)分析顯示,與DM患者比較,DKD 患者的5hmC 整體分布水平明顯降低。5hmC 主要在轉(zhuǎn)錄起始位點(diǎn)(TSS)和轉(zhuǎn)錄終止位點(diǎn)(TTS)內(nèi)富集,在側(cè)翼區(qū)域耗損(見OSID 碼圖1),說明5hmC 的累積與轉(zhuǎn)錄活性有關(guān)。以|log2FC|>0.5、FDR<0.05 為標(biāo)準(zhǔn),獲得 DKD 與 DM 的差異基因共1 644個(gè)。
2.2 DKD患者血漿cfDNA中羥甲基化修飾lncRNA的篩選結(jié)果 將獲得的差異基因用于樣本的聚類分析,表型熱圖分析結(jié)果見OSID 碼圖2A,無離群樣本。計(jì)算DKD 基因間的鄰接矩陣和拓?fù)渚仃嚕趧?dòng)態(tài)剪切樹法把輸入的差異基因分成3 個(gè)模塊,分別用3 種顏色矩形表示,相似度高的基因被聚類到同種顏色的模塊中,結(jié)果見OSID 碼圖2B。為了得到各個(gè)模塊與臨床表型之間的關(guān)系,我們對(duì)共表達(dá)模塊與臨床表型進(jìn)行關(guān)聯(lián)性分析,以相關(guān)性熱圖表示,結(jié)果見OSID 碼圖2C。結(jié)果顯示與DKD 表型相關(guān)性最強(qiáng)的模塊是藍(lán)綠色模塊(r=0.73,P<0.001),總體上與DKD 表型呈正相關(guān)。進(jìn)一步將藍(lán)綠色模塊作為關(guān)鍵模塊進(jìn)行GS 和MM 分析,藍(lán)綠色模塊的GS 與 MM 的相關(guān)系數(shù)r=0.82,P<0.001,結(jié)果見OSID 碼圖 2D,最后通過對(duì) GS 和 MM 設(shè)定條件,以GS>0.7,MM>0.9 的標(biāo)準(zhǔn)來篩選藍(lán)綠色模塊中與DKD 相關(guān)性高的關(guān)鍵樞紐基因。由于本研究主要分析和篩選關(guān)鍵羥甲基化修飾lncRNA,故最終獲得15個(gè)lncRNA,見表1。
2.3 羥甲基化修飾lncRNA的亞細(xì)胞定位 為了分析這些差異lncRNA 是否參與ceRNA 競(jìng)爭(zhēng)機(jī)制,利用lnclocater 網(wǎng)站對(duì)其亞細(xì)胞定位進(jìn)行分析,結(jié)果顯示,這15 個(gè)關(guān)鍵lncRNA 均定位于細(xì)胞質(zhì),大部分lncRNA 預(yù)測(cè)分?jǐn)?shù)都大于0.8,結(jié)果見表1,說明對(duì)亞細(xì)胞定位的預(yù)測(cè)結(jié)果的準(zhǔn)確性很高。
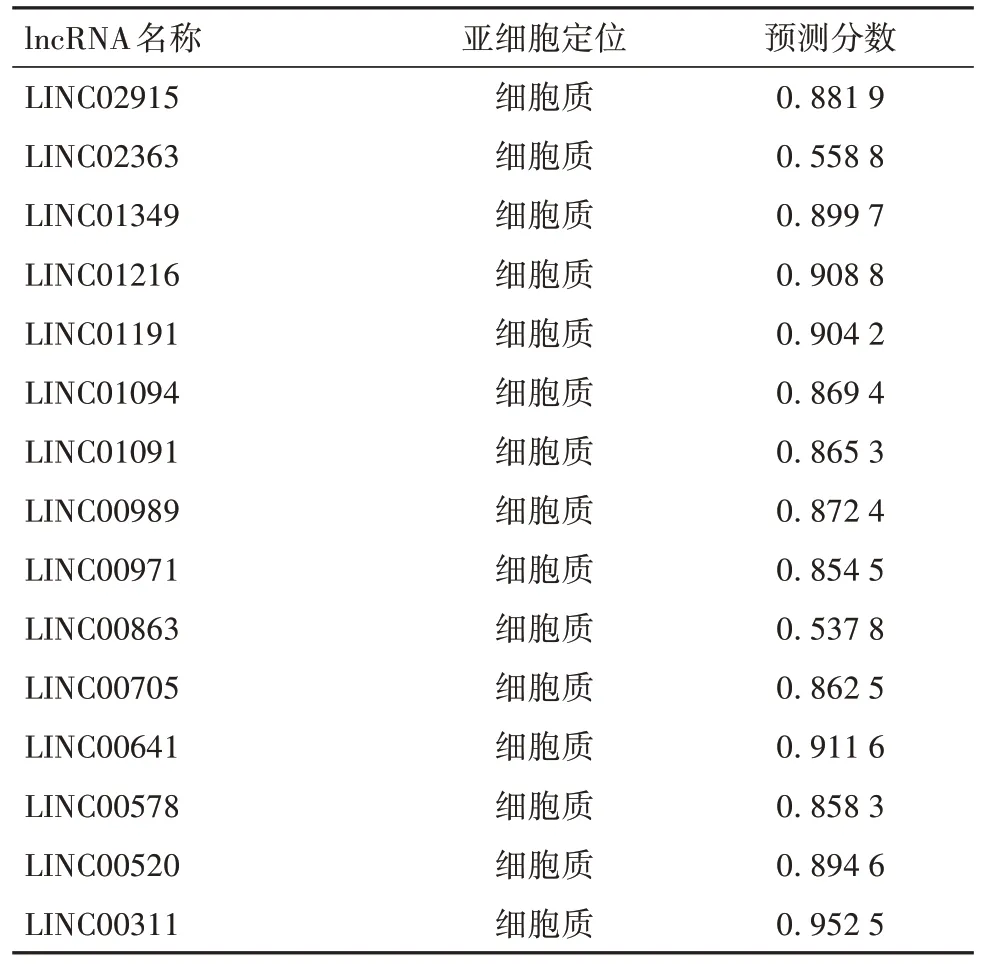
表1 羥甲基化修飾lncRNA的亞細(xì)胞定位
2.4 lncRNA 靶向miRNA 的預(yù)測(cè)結(jié)果 使用Starbase分析工具預(yù)測(cè)lncRNA的靶基因miRNA,發(fā)現(xiàn)只有2 個(gè)lncRNA 在數(shù)據(jù)庫中有預(yù)測(cè)結(jié)果,分別是LINC00641和LINC00863。其羥甲基化水平見OSID碼圖 3 所示,與 DM 患者相比,DKD 患者的 2 個(gè)關(guān)鍵lncRNA 羥甲基化水平降低(P均<0.05)。接著以bioComplex>1 為篩選條件,LINC00641 的靶基因有12 個(gè),分別為 hsa-miR-320b、hsa-miR-194-5p、hsamiR-320d、hsa-miR-539-5p、hsa-miR-320c、hsa-miR-153-3p、hsa-miR-378b、hsa-miR-425-5p、hsa-miR-378d、hsa-miR-378a-3p、hsa-miR-378h、hsa-miR-206。LINC00863 的靶基因?yàn)閔sa-miR-218-5p。最終確定的2個(gè)關(guān)鍵lncRNA預(yù)測(cè)的靶基因共有13個(gè)。
2.5 羥甲基化修飾lncRNA 診斷價(jià)值及表達(dá)驗(yàn)證結(jié)果 對(duì)篩選得到的2 個(gè)關(guān)鍵lncRNA 進(jìn)行ROC曲線分析,結(jié)果顯示LINC00641 和LINC00863 在本數(shù)據(jù)集中診斷DKD 準(zhǔn)確性均滿足AUC≥0.8,具有較好的診斷價(jià)值,見OSID 碼圖4。與對(duì)照組和DM組 相 比 ,DKD 組 腎 組 織 LINC00863、LINC00641 mRNA 表達(dá)水平降低(P均<0.05),見表2。
表2 DKD小鼠腎組織中相關(guān)lncRNA的表達(dá)水平()

表2 DKD小鼠腎組織中相關(guān)lncRNA的表達(dá)水平()
注:與對(duì)照組相比,*P<0.05;與DM組相比,#P<0.05。
組別對(duì)照組DM組DKD組LINC00641 1.01±0.16 0.80±0.08 0.57±0.04**#n 3 3 3 LINC00863 1.00±0.16 0.92±0.14 0.66±0.06*#
2.6 miRNA 靶基因的篩選及功能富集結(jié)果 對(duì)DKD 腎組織轉(zhuǎn)錄組數(shù)據(jù)進(jìn)行差異分析(|log2FC|>0.5,F(xiàn)DR<0.05),上調(diào)基因 1 259 個(gè),下調(diào)基因1 386 個(gè),見 DSID 碼圖 5A。使用數(shù)據(jù)庫 miRDB 和TargetScan 分別預(yù)測(cè)上述13 個(gè)miRNA 的靶向mRNA,然后分別與DKD 轉(zhuǎn)錄組差異基因取交集、去重后,最終得到可在外部數(shù)據(jù)集中驗(yàn)證出的246個(gè)差異靶基因。對(duì)這246 個(gè)基因進(jìn)行GO 富集分析,主要與泌尿生殖系統(tǒng)發(fā)育、腎臟發(fā)育、腎系統(tǒng)發(fā)育、腎上皮細(xì)胞及后腎的發(fā)育等生物學(xué)途徑相關(guān),見 DSID 碼圖 5B。
2.7 ceRNA 調(diào)控網(wǎng)絡(luò)構(gòu)建結(jié)果 將所得lncRNA、miRNA 與 mRNA 在 Cytoscape3.8.0 中繪制出 ceRNA網(wǎng)絡(luò),共246條通路,261個(gè)節(jié)點(diǎn),259條邊。見OSID碼圖6。
3 討論
DKD 是一種由于DM 患者長(zhǎng)期處于高血糖狀態(tài)引起的慢性腎臟病,其發(fā)病機(jī)制復(fù)雜。研究顯示,lncRNA 在多種慢性疾病的進(jìn)展中起關(guān)鍵作用。動(dòng)物實(shí)驗(yàn)顯示,使用TGF-β1處理小鼠系膜細(xì)胞后,通過lncRNA 啟動(dòng)子和原癌基因Ets-1 的組蛋白乙酰化,miR-192 與其宿主 lncRNA CJ241444 共同調(diào)節(jié),導(dǎo)致Smads 的富集和lncRNA 以及miR-192 的上調(diào)[12]。KATO 等[13]研究顯示,具有 DKD 相關(guān)功能的關(guān)鍵miRNA(miR-216a和miR-217)由TGF-β1及其宿主lncRNA RP23-298H6.1-001 在系膜細(xì)胞中被誘導(dǎo)。其后續(xù)研究顯示,lnc-megacluster(lnc-MGC)是miR-379 簇中近 40 個(gè) miRNA 的 lncRNA 宿主,可在早期DKD 小鼠中促進(jìn)系膜細(xì)胞的細(xì)胞外基質(zhì)積累和肥大[14]。在 1 型和 2 型 DM 小鼠的腎小球以及暴露于高糖培養(yǎng)的小鼠系膜細(xì)胞中,lnc-MGC 及其幾種駐留miRNA 表達(dá)增加,主要是TGF-β1通過涉及內(nèi)質(zhì)網(wǎng)應(yīng)激相關(guān)轉(zhuǎn)錄因子CHOP(C/EBP 同源蛋白)的機(jī)制。因此,lnc-MGC 可以增加DKD 中的內(nèi)質(zhì)網(wǎng)應(yīng)激,這反過來可能導(dǎo)致lnc-MGC 的持續(xù)表達(dá),繼續(xù)循環(huán)并可能有助于代謝記憶。值得注意的是,在暴露于高葡萄糖和TGF-β1下,人類系膜細(xì)胞中的lnc-MGC 直系同源物也會(huì)上調(diào)。這是個(gè)重要發(fā)現(xiàn),因?yàn)榕cmiRNA 不同,lncRNA 通常在物種間不太保守,這提示該lncRNA 簇可能與人類DKD 相關(guān)。此外,有研究報(bào)道,血漿cfDNA 攜帶了起源細(xì)胞的遺傳和表觀遺傳信息[1]。所以,本研究基于人血漿來源cfDNA 的羥甲基化修飾lncRNA 在DKD 調(diào)控網(wǎng)絡(luò)中進(jìn)行初步探索。
本研究通過對(duì)DKD及DM 患者血漿cfDNA 進(jìn)行5hmC 全基因組測(cè)序,結(jié)果顯示整體5hmC 信號(hào)主要在 TSS 區(qū)域富集,RNA 的轉(zhuǎn)錄始于 TSS,并且 DM 與DKD 患者之間存在顯著差異,表明這些區(qū)域在通過5hmC調(diào)節(jié)疾病基因(如lncRNA基因)表達(dá)中發(fā)揮關(guān)鍵作用。使用WGCNA 算法得到與DKD 相關(guān)編碼lncRNA 的關(guān)鍵5hmC 標(biāo)志物,用這種計(jì)算方法的優(yōu)勢(shì)是:以生物網(wǎng)絡(luò)構(gòu)建為基礎(chǔ),能夠更加精準(zhǔn)的展現(xiàn)生物學(xué)特性;可幾乎覆蓋到人類的所有編碼基因;與已發(fā)表的研究偏倚性較小。該結(jié)果為后續(xù)疾病的深入研究提供了更廣泛的理論基礎(chǔ)。
此外,本研究通過亞細(xì)胞定位確定了15 個(gè)lncRNA 在細(xì)胞質(zhì)中的表達(dá),表明上述lncRNA 可通過ceRNA 機(jī)制調(diào)控基因表達(dá)參與DKD 的發(fā)病。Starbase 預(yù)測(cè)結(jié)果顯示,相關(guān)lncRNA 可通過調(diào)控miRNA 從而影響DKD 中的基因表達(dá),但我們發(fā)現(xiàn)只有2 個(gè)lncRNA 在Starbase 數(shù)據(jù)庫中有預(yù)測(cè)結(jié)果,分別為 LINC00863 和 LINC00641,同時(shí)發(fā)現(xiàn)這 2 個(gè)lncRNA 的羥基化水平能很好的區(qū)分DKD 和DM。另外,在DKD小鼠腎臟組織中對(duì)這2個(gè)lncRNA的表達(dá)水平也得到了與預(yù)測(cè)一致的實(shí)驗(yàn)驗(yàn)證結(jié)果。因此,我們認(rèn)為L(zhǎng)INC00863 和LINC00641 很可能成為DKD 診斷的潛在生物標(biāo)志物和治療靶點(diǎn)。我們進(jìn)一步對(duì)已在小鼠腎組織中得到有效驗(yàn)證的lncRNA,篩選得到下游調(diào)控miRNA,最后基于數(shù)據(jù)庫預(yù)測(cè)上述miRNA 的靶向mRNA,為了得到較為準(zhǔn)確的lncRNA-miRNA-mRNA 調(diào)控網(wǎng)絡(luò)圖,我們篩選與外部DKD 轉(zhuǎn)錄組數(shù)據(jù)集差異表達(dá)的靶向mRNA,得到具有一定可信度的ceRNA 調(diào)控網(wǎng)絡(luò)圖。但事實(shí)上ceRNA 目前還處于一個(gè)起步階段,具體的研究案例比較少,本研究只是可視化構(gòu)建了一個(gè)基本的網(wǎng)絡(luò),具體的調(diào)控方式還有待繼續(xù)探究。另外,對(duì)于最終篩選得到的關(guān)鍵lncRNA文獻(xiàn)報(bào)道較少,有研究表明LINC00641 過表達(dá)會(huì)抑制乳腺癌細(xì)胞增殖、遷移和侵襲,可通過海綿化miR-194-5p 抑制乳腺癌細(xì)胞增殖、遷移和侵襲[15]。
最后,基于Metascape網(wǎng)站對(duì)我們篩選出的基因進(jìn)行GO 功能富集分析,結(jié)果顯示,主要參與泌尿生殖系統(tǒng)發(fā)育和腎臟發(fā)育通路,說明持續(xù)高血糖的環(huán)境對(duì)于腎臟功能及結(jié)構(gòu)會(huì)存在一定的不利影響,與DKD的發(fā)病機(jī)制息息相關(guān)。
綜上所述,本研究基于臨床樣本數(shù)據(jù),通過對(duì)DKD 及 DM 患者的血漿 cfDNA 進(jìn)行 5hmC-Seal測(cè)序,發(fā)現(xiàn)了與DKD 相關(guān)編碼lncRNA 的關(guān)鍵5hmC 標(biāo)志物,構(gòu)建了完整的ceRNA 調(diào)控網(wǎng)絡(luò),為DKD 分子機(jī)制的深入研究提供了嚴(yán)謹(jǐn)?shù)臄?shù)據(jù)支持。

