只減脂不減肉?針對肥胖癥,助力研發下一代胰淀素及降鈣素受體的雙激動劑藥物
有人說,三分運動七分吃。日前,社交媒體上分享了“米飯的花樣吃法”,其中提到“七色糙米”的搭配:即黑米、紅米、玉米磣、燕麥仁、糙米、青稞、小麥仁。這些粗糧除了健康之外,飽腹感也更強。
如果你嘗試過減肥,應該也聽說過飯前喝水增加飽腹感,以避免攝入更多能量的做法。那么,人體的飽腹感又是從何而來呢?
這就要從胰淀素和它的受體蛋白的發現說起。1986年,科學家發現了胰淀素的存在,借此人們發現當我們進食時,胰島便開始分泌胰島素和胰淀素。前者可幫助迅速控制血糖,而胰淀素則與腦部分布的胰淀素受體結合,產生飽足感信號。收到信號后,我們就會停止進食,借此可避免過度飲食造成的代謝性疾病。
利用這一人體自身能量平衡的天然機制,2005年,胰淀素的衍生多肽——普蘭林肽作為糖尿病患者的血糖控制藥物順利上市并沿用至今。后續研究更是揭示了胰淀素信號通路具備開發減重療法的巨大潛力。由此,胰淀素及其受體的研究,吸引了多家藥物公司,他們希望開發出減重和肥胖癥治療領域的新療法。
如何實現只減脂肪、不減肌肉的優異減重效果?
1998年~1999年,胰淀素受體的獨特組成得到首次闡明,它本身是由一個降鈣素受體和一種受體活性調節蛋白結合而形成的異源二聚體。降鈣素受體本身并不會影響人體代謝,當被降鈣素多肽激活,則會產生調節血液中鈣的濃度的生理信號,促使血鈣向骨骼沉積。
但是,一旦它和受體活性蛋白相結合,便不再響應降鈣素多肽,而是去響應胰淀素多肽,進而形成相應的胰淀素受體。最新研究表明,如果人工改造出一種多肽,讓它同時激活降鈣素受體和胰淀素受體,就能更好地刺激基礎代謝,增加能量消耗,實現只減脂肪、不減肌肉的優異減重效果。
但是,由于這兩種受體并沒有蛋白結構信息,因此相關藥物研發只能集中于對天然多肽進行突變。然而,降鈣素多肽和胰淀素多肽的天然序列不同,甚至連長度都不一樣。如果想人工制造一種混合型的多肽,并讓它同時能刺激兩個受體,那么必須面對的問題是:到底以哪種天然多肽作為基礎模板?
在此前研究中人們發現,大馬哈魚降鈣素和人體降鈣素的差異在于:大馬哈魚降鈣素能同時激活人體內的降鈣素受體和胰淀素受體。所以,最早十多年的研究均以大馬哈魚的降鈣素為模板進行突變改造,其具備32個氨基酸長度。這些研究在藥理和動物模型均取得了有效成果,并進入臨床實驗階段。
但是,當進行人體實驗時,實際效果卻并不理想。最近幾年,有藥物公司嘗試從胰淀素多肽模板出發。其中,國際生物制藥公司諾和諾德研發的卡格列肽,取得了令人驚喜的臨床實驗結果。但在實際藥物研發中,還面臨著一個無法回避的困難。當建立藥理學分析實驗時,由于胰淀素受體組成的特殊性,降鈣素受體會同時存在于體系中,并且無法排除降鈣素受體所產生的信號,這使得相應藥物表征十分困難。這種情況下,如果掌握可視化的蛋白結構信息,則對藥物研發具有重大意義。但是,在結構生物學方面,這兩種受體也長期存在結構難以表征的問題。
兩種受體其本身屬于G蛋白偶聯受體,是藥物研發領域的一類重要靶點,現存上市藥物中的30%均作用于G蛋白偶聯受體。但是,G蛋白偶聯受體的結構學研究,常年處于艱難狀態。根本原因在于,G蛋白偶聯受體本身的蛋白分子量特別小,卻又特別動態化。這讓傳統蛋白結晶學很難實現有效的晶體生長,除非對受體進行基因改造,并引入大量熱力學穩定修飾,而這種人工修飾則會讓天然結構失真。
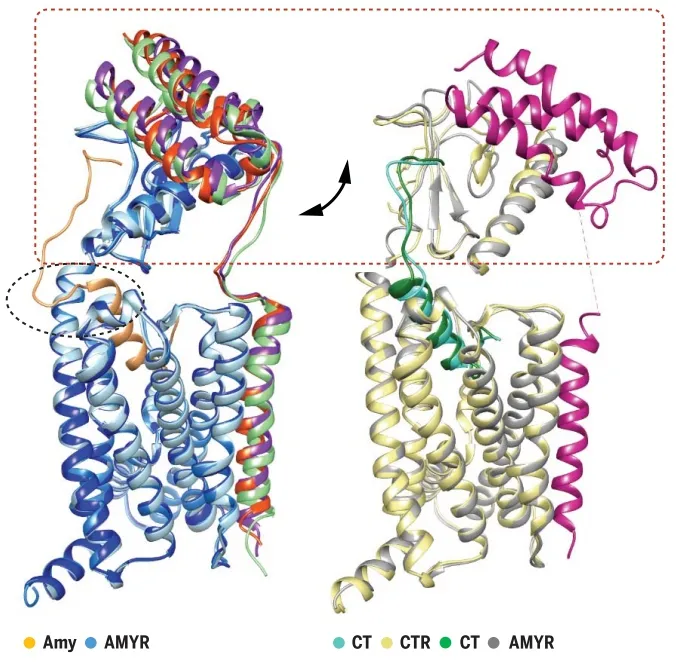
直到2017年,這一困境才得到解決。憑借冷凍透射電鏡技術的飛速發展,澳大利亞莫納什大學藥物科學研究所博士生曹劍駿,其所在的Wootten/Sexton課題組首次實現冷凍透射電鏡解析G蛋白偶聯受體結構。得益于這一技術突破,曹劍駿讀博期間的研究課題由此開展。由于傳統藥理學工具無法完全區分降鈣素受體和胰淀素受體的信號,而新興的冷凍電鏡技術恰好能完整表征兩類受體的結構特征,借此即可彌補這一信息缺口。
同時他表示,構成胰淀素受體的受體活性調節蛋白家族總共有三個亞型,并分別和降鈣素受體結合,從而形成三種亞型的胰淀素受體。對于不同多肽的響應,這三種胰淀素受體存在一定差異,而這種差異很難通過傳統的藥理學實驗來解釋。
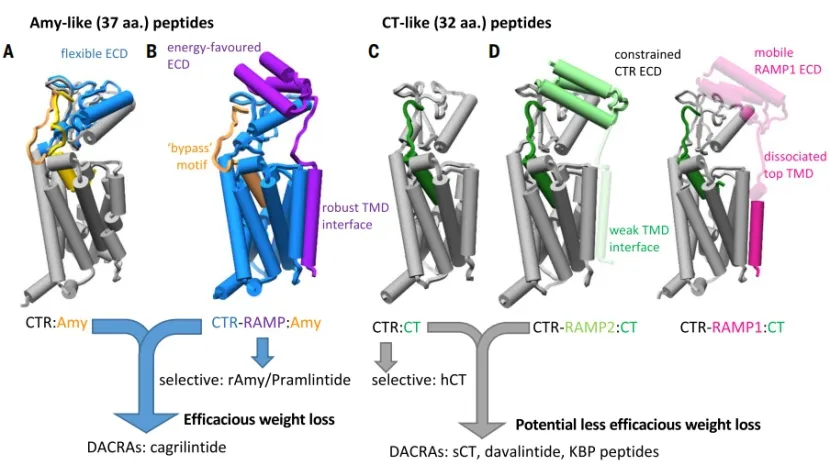
曹劍駿最近發表的一作論文《胰淀素受體表型的結構基礎》,其中的結構數據特別豐富,論文中總計有十個結構:分別羅列了四種受體(降鈣素受體和三種亞型的胰淀素受體)與三種天然多肽(人降鈣素,大馬哈魚降鈣素,鼠胰淀素)相互結合的模式。
通過分析這種不同交叉組合的結合模式,大量結構學信息得以被呈現,借此可以解釋這兩種多肽分別和相對應的受體、以及非對應的受體結合時的不同機制。
他表示,“這是人們第一次直觀地認識到這種不同,而這種認識是之前通過其他手段沒有辦法實現的。審稿人覺得我們的研究非常系統,可給將來的藥物研發提供非常詳細的信息。”
往返于東京-墨爾本的結構解析
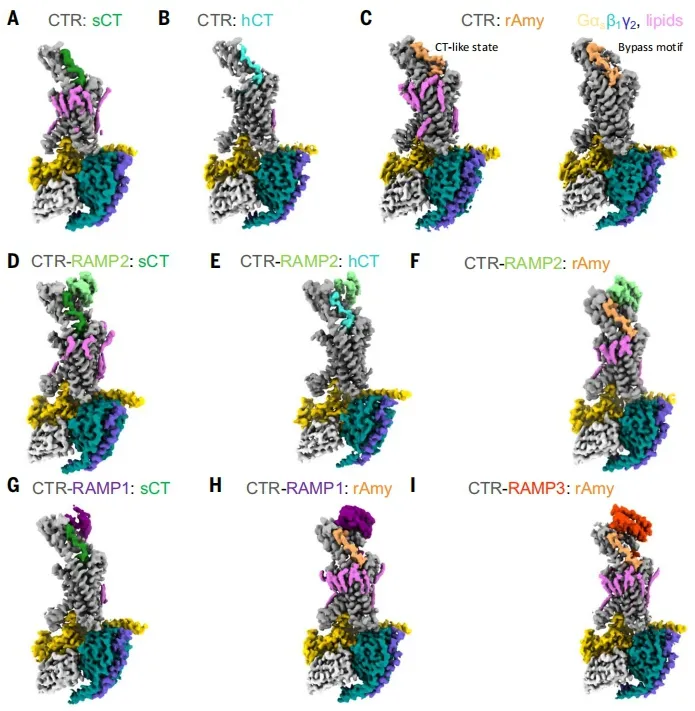
盡管在2017年,該課題組第一次突破性實現了冷凍電鏡技術對G蛋白偶聯受體的結構解析。但是由于胰淀素受體特殊的異源二聚體組成,造成蛋白表達和純化過程更為困難和復雜。這一問題在2018年,由該團隊的Yi-Lynn Liang博士在胰淀素受體的同源類似蛋白,CGRP受體的研究中得到解決和完善。2018年,曹劍駿適逢加入該課題組,開始博士學習和研究。
在他入學后,上述課題正式立項。隨后爆發的全球新冠疫情,給科研實操帶來了困難。在課題前期,組里的電鏡設備尚未優化完畢。于是,他們將樣品寄到東京,由長期合作方東京大學醫學研究生院拉多斯汀·達涅夫教授進行冷凍電鏡成像,再將數據返回墨爾本進行結構學解析比對,最終對結構學特征和藥理學聯系進行闡述。通過這樣國際長距離往返作業,研究主體的六個結構得以解析完畢。
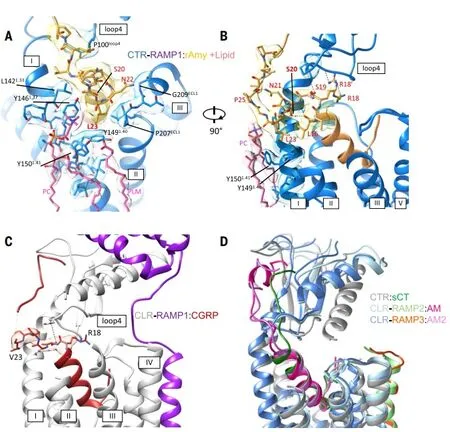
曹劍駿說:“結構解析得到了莫納什大學超算中心的支持。尋找過程中我們發現,必須將更多結構信息納入到體系中,從而讓體系更完整周延。而在課題進展后期,位于墨爾本的Bio21的ARC膜蛋白冷凍電鏡中心已然完備。那時,設備條件已經比較完善,我們就地進行了四個結構的補充拍攝,最后實現了十個結構的完全解析。”
實現專一針對脂肪組織的減重作用
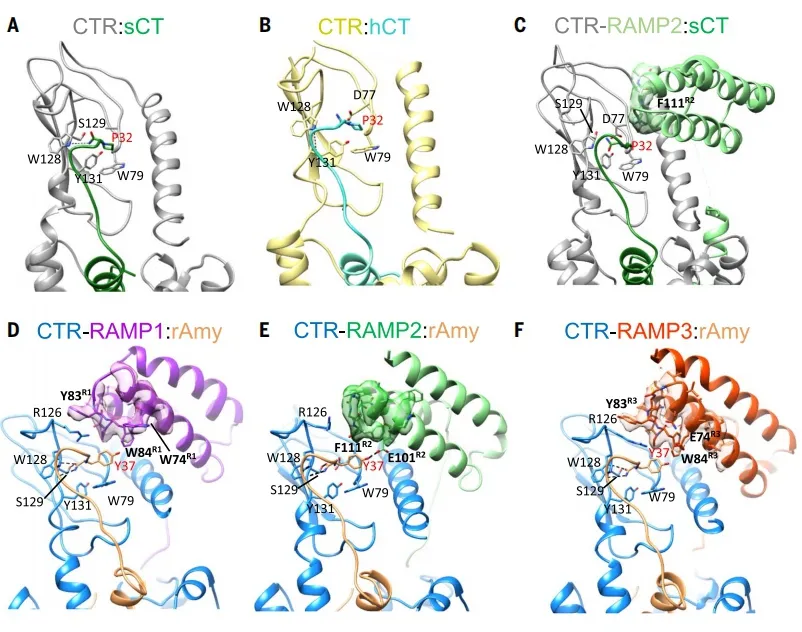
相關的臨床應用場景,已經近在眼前。雖然藥物公司并沒有結構學信息,但他們也在基于多肽序列進行相關探索。2020年,諾和諾德公司開發的卡格列肽就是基于胰淀素多肽的37個氨基酸序列模板得以實現的。
基于臨床一期和臨床二期的研究,相關團隊已經在《柳葉刀》發了兩篇論文,這些研究證明了基于胰淀素多肽的衍生人工多肽可以同時激活降鈣素受體和胰淀素受體,從而實現肥胖癥患者的有效減重。另外,這種減重作用專一針對脂肪組織的,因此不會減少肌肉重量。
曹劍駿估計,上述多肽應該已經在臨床三期的人體實驗當中,而這僅僅是藥物公司在未得到結構學信息的前提下,做出的一些初步嘗試。他所在課題組及其主持的ARC膜蛋白冷凍電鏡中心與十余家藥物研發企業達成長期合作。
他說:“基于我們的結構和藥企之前的探索,最終所生成的結果讓他們非常振奮。我們現在發表的論文,雖然僅是內源的天然多肽,但也提供了大量結構信息供藥企參考。如果可以基于結構進一步優化,很快就能進入臨床實驗階段。”
同時,如果這些藥物研發公司缺乏結構學信息,則不知該如何優化多肽序列,無法實現更好的治療效果,也就無法繼續說服潛在投資者。而有了曹劍駿所在課題組的結構學信息,這些公司便得到了進一步優化的方向。預計將來會有更多基于胰淀素受體模板的人工多肽出現,這些人工多肽能同時激活兩種受體信號并實現減重功能。預計類似藥物將會不斷進入臨床實驗,直到最后被獲批使用。
在中山大學擔任一年實驗室助理后,來到澳洲讀博
據介紹,曹劍駿的兩位主要導師,分別是莫納什大學藥物科學研究所丹尼斯·伍滕教授和帕特里克·塞克斯頓教授所主持的實驗室,長年致力于并且對G蛋白偶聯受體的研究。
在該實驗室學習期間,馬修·貝魯索夫博士十分精通蛋白結晶學和冷凍電鏡技術,曾教過曹劍駿使用冷凍透射電鏡解析蛋白結構。連依琳博士則直接傳授他相關蛋白表達和純化方法,2017年,隨著當時課題組的成果公布,她也成為當時世界首個G蛋白冷凍電鏡結構的解析者。

曹劍駿
曹劍駿說:“連依琳博士是我的一個很重要的技術導師,在疫情前給了我很多幫助。后來,她轉職去了工業界,但也將相應方法技術全部傳授給我。2019年底,新冠疫情爆發,各國邊境突發管制。我當時身處中國,Patrick和Denise得到消息第一時間資助我緊急在泰國隔離14天,最后成功入境澳洲,接續完成了這個項目,要不我可能就要去面對退學之類的情況。而在疫情初期的長期居家封城過程中,Matt和我每天進行線上會議,遠程手把手教我處理和解析數據。如果沒有這四位分別在各自領域的專家的培養,我一個人是完全無法完成這樣的研究工作的。我經常戲稱我擁有一個導師‘夢之隊’。”
據介紹,曹劍駿是安徽省馬鞍山市人,出生于1991年。本科在中山大學化學專業學習,之后加入中山大學化學學院毛宗萬教授的實驗室,碩導分別是毛宗萬教授、中國科院院士暨中山大學化學與化學工程學院教授計亮年、和該院副教授譚彩萍。碩士階段,曹劍駿主要從事過渡金屬配合物在抗腫瘤治療方向的研究。畢業后,在毛宗萬實驗室擔任為期一年的實驗室助理,碩士期間累計發表11篇論文,這也使曹劍駿的研究興趣從化學延伸到生物醫學方向。

