基于網(wǎng)絡藥理學和分子對接探尋人參治療特發(fā)性肺間質(zhì)纖維化的關鍵靶標及作用機制
呂鵬,劉曉明,李芮※
(1.山東中醫(yī)藥大學,山東 濟南 250014;2.山東中醫(yī)藥大學附屬醫(yī)院,山東 濟南 250014)
肺間質(zhì)纖維化(idiopathic pulmonary fibrosis,IPF)是各種原因引起的急慢性間質(zhì)性肺病(interstitial lung disease,ILD)的最終結(jié)局,其病因多樣,預后較差,發(fā)病機制復雜,目前認為IPF的發(fā)生與先天和獲得性免疫反應的激活、炎癥、上皮/內(nèi)皮損傷、上皮間充質(zhì)改變以及細胞凋亡有關[1-3]。西醫(yī)主要采用激素制劑、吡非尼酮和尼達尼布等藥物進行治療,這些治療方案僅能緩解IPF的癥狀或延緩病情進展,尚不能滿足IPF患者的醫(yī)療需求[4],因此,在中醫(yī)藥寶庫中探索治療IPF的新藥具有重要意義。當前,已有中醫(yī)藥研究者對療效明確的單藥和復方進行數(shù)據(jù)挖掘,發(fā)現(xiàn)補氣藥的累計頻次最高,居各類藥物之首[5],人參便是其中的重要代表,同時,國外多項研究也已經(jīng)證實,多種人參皂苷具有抗纖維化的潛力,但機制尚不明確。所以,本研究通過運用網(wǎng)絡藥理學和分子對接技術對人參治療IPF的關鍵靶標和潛在作用機制進行初步探索與驗證,以期為后續(xù)研究提供可靠的科學依據(jù)。
1 資料與方法
1.1 研究路線與方法
研究路線與方法,見圖1。

圖1 研究路線與方法圖Fig.1 Diagram of the research path and technique
1.2 人參中活性成分的篩選與ADME參數(shù)的確定
在中藥系統(tǒng)藥理學數(shù)據(jù)庫與分析平臺(TCMSP)中,對“renshen”進行檢索,搜索得到人參的全部成分及其吸收、分布、代謝、排泄(ADME)信息。以藥物口服生物利用度(oral bioavail,OB)與類藥性(drug likeness,DL)作為本研究衡量化合物藥效的主要依據(jù),篩選條件參照TCMSP數(shù)據(jù)庫“parameter information”中的建議,確定為OB≥30%,DL≥0.18,將篩選出的有效成分作為人參的活性成分進行后續(xù)研究。
1.3 構(gòu)建人參已知的活性成分 靶標數(shù)據(jù)庫
在TCMSP中搜索得到人參活性成分的對應靶標,對其中經(jīng)DrugBank平臺驗證的靶標信息進行保留。此外,《中華人民共和國藥典》2020版(一部)規(guī)定人參皂苷Rg1(C42H72O14)、人參皂苷Re(C48H82O18)和人參皂苷Rb1(C54H92O23)的含量是藥材質(zhì)量評價的重要指標[6],故本研究將對這一重要化合物的靶標信息加以補充,最終,將以上篩選出的所有化合物 靶標信息去重整合到構(gòu)建好的人參活性成分 靶標數(shù)據(jù)庫中。
1.4 人參皂苷潛在藥靶篩選與分子對接驗證
在PubChem數(shù)據(jù)庫中下載人參皂苷(Ginsenoside Re、Ginsenoside Rg1及Ginsenoside Rb1)的2D-sdf模型文件,將文件導入Swiss target prediction平臺,并對其潛在靶標進行預測,將probability≥0.06的靶標作為候選進行分子對接。在RCSBPDB數(shù)據(jù)庫中下載候選靶標的PDB蛋白晶體模型文件,選擇PDB文件的基本原則參考Yang等人的研究[7]。利用AutoDock vina重新進行原位點對接,通過計算均方根差(root mean square Dis-placement,RMSD)值以比較對接前后復合物的構(gòu)象差異,若RMSD<[8],則證明對接方法可靠并保留相應靶蛋白以進行后續(xù)操作,將保留下來并去除原配體結(jié)構(gòu)的靶標重新導入AutoDock vina中,經(jīng)過分子加氫、除水等操作后,采用上述對接方法進行對接,研究假定結(jié)果中若蛋白與配體間的Affinity<0 kJ/mol[8],則說明人參皂苷能較好地與該蛋白進行自發(fā)結(jié)合,并將其視作人參皂苷的潛在有效靶標,利用PyMOL軟件進行可視化分析。
1.5 構(gòu)建已知的IPF疾病靶標數(shù)據(jù)庫
在NCBI Gene Database、GeneCards、Disgenet、OMIM和DrugBank數(shù)據(jù)庫中輸入“idiopathic pulmonary fibrosis”或“IPF”進行已知疾病基因的獲取,篩選出物種為智人(Homo Sapiens)的靶標,并將其去重添加至“IPF-靶標數(shù)據(jù)庫”。
1.6 靶標互作網(wǎng)絡與關鍵靶標的篩選
查詢Uniprot數(shù)據(jù)庫,將基因名稱轉(zhuǎn)換為Gene Symbol,將藥靶和疾病靶標取交集以篩選出共同靶標,即人參中參與治療IPF的靶標,在String數(shù)據(jù)庫中進行PPI網(wǎng)絡分析。本研究采用“Medium Confidence(0.400)”的條件對節(jié)點數(shù)據(jù)進行過濾,將處理后的數(shù)據(jù)導入Cytoscape3.8.1進行網(wǎng)絡可視化展示,并對生成的網(wǎng)絡圖進行拓撲分析,按照degree值(與該節(jié)點相關聯(lián)的邊的條數(shù))的高低順序選擇前10個基因作為人參治療IPF的關鍵靶標。
1.7 GO、KEGG富集分析與構(gòu)建生物調(diào)控網(wǎng)絡
采用metascape數(shù)據(jù)庫對人參 IPF共同靶標進行基因本體論(Gene Ontology,GO)富集分析和京都基因和基因組數(shù)據(jù)庫(Kyoto Encyclopedia of Genes and Genomes,KEGG)富集分析,根據(jù)以上活性成分及其靶標、通路的對應關系,使用Cytoscape3.8.1構(gòu)建活性成分 靶標 通路 疾病生物層次網(wǎng)絡,對網(wǎng)絡中重要節(jié)點的生物效應進行分析。
1.8 分子對接分析
基于1.7所作的生物網(wǎng)絡圖結(jié)果,對本研究中的關鍵靶標與除外人參皂苷的人參活性成分進行分子對接,方法同1.4。
2 結(jié)果
2.1 活性成分篩選結(jié)果
通過TCMSP數(shù)據(jù)庫共篩選出包括人參皂苷、山柰酚、-谷甾醇和花生四烯酸等在內(nèi)的22種活性成分,篩選結(jié)果詳見表1。

表1 人參中活性成分ADME信息Table1 ADME information of active components in ginseng
2.2 人參皂苷潛在藥靶與分子對接預測結(jié)果
經(jīng)預測得到人參皂苷Rg1、Rb1、Re的潛在靶標有16個,見表2。對接后得到Affinity<0 kJ/mol的潛在有效靶標有3個,分別是IL2、LGALS8和LGALS3,見圖2。

圖2 潛在有效靶標對接示意圖Fig.2 Diagram of potential effective targets docking

表2 人參皂苷Rg1、Rb1、Re潛在靶標預測Table 2 Prediction of potential targets of ginsenosides Rg 1、Rb1 and Re
2.3 人參化合物靶標與疾病靶標篩選結(jié)果
此次研究共發(fā)現(xiàn)人參相關靶標87個,IPF相關靶標1 641個,結(jié)果見表3。圖3表示化合物靶標與疾病靶標交集結(jié)果,得到TNF、IL1B、PPARG、PTGS2和UN等25個共同靶標。

表3 人參化合物靶標與IPF疾病靶標篩選結(jié)果Table 3 Screening results of ginseng compound targets and IPF disease targets

圖3 人參化合物靶標-肺間質(zhì)纖維化基因交集圖Fig.3 Venn plot of compositional targets and IPF-related targets in ginseng
2.4 PPI互作網(wǎng)絡
將25個共同靶標導入STRING數(shù)據(jù)庫,得到構(gòu)建好的靶標互作網(wǎng)絡,見圖4。圖中黃色節(jié)點代表節(jié)點度排名前10的關鍵靶標,即TNF、IL1B、PPARG、PTGS2、JUN、IFNG、VCAM1、IL2、HMOX1和NOS2,綠色表示其他靶標。整個網(wǎng)絡中共存在115條邊,其中邊的粗細反映了置信度的高低。該網(wǎng)絡的主要參數(shù)見表4,其中節(jié)點間的平均距離為1.753,意味著靶標在網(wǎng)絡中可以迅速地傳遞信息,平均相鄰節(jié)點數(shù)目為9.2,說明每個靶標平均與9.2個其他靶標密切聯(lián)系,網(wǎng)絡的整體密度為0.757,意味著任意兩個靶標互作的發(fā)生概率為75.7%,這些都能在一定程度上反映人參中的活性成分能夠通過多靶點、多通路的網(wǎng)絡調(diào)控作用[9],改變IPF的疾病狀態(tài)。
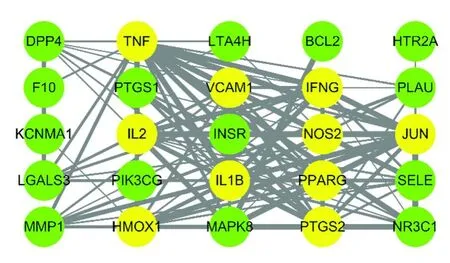
圖4 人參靶標 蛋白互作網(wǎng)絡Fig.4 Ginseng targets-protein interaction network

表4 人參靶標 蛋白互作主要參數(shù)Table 4 Main parameters of ginseng targets-protein interaction
2.5 GO與KEGG通路富集分析結(jié)果
對25個共同靶標進行GO分析共識別得到649條結(jié)果,其中發(fā)現(xiàn)615條生物過程(Biological Process,BP)信息,包括小分子代謝過程正調(diào)控、細胞遷移正調(diào)控、細胞粘附調(diào)控、凋亡信號通路、缺氧反應、蛋白磷酸化的正調(diào)控以及白細胞與細胞粘附的調(diào)節(jié)等功能;22條分子功能(molecular function,MF)信息,包括受體配體活性、信號受體激活劑活性、信號受體調(diào)節(jié)劑活性、血紅素結(jié)合、四吡啶結(jié)合、氧化還原酶活性和細胞因子受體結(jié)合等;12條細胞組分(cellular component,CC)信息,包括小窩、膜筏、膜微域、質(zhì)膜筏、質(zhì)膜外側(cè)和膜側(cè)面等,按照lg(p value)由小到大的順序,GOBP、GOMF以及GOCC的前10條富集結(jié)果見圖5。KEGG通路富集分析共識別到25個基因,得到55條結(jié)果,包括流體切應力與動脈粥樣硬化、IL-17信號通路、糖尿病并發(fā)癥中AGE-RAGE信號通路、TNF信號通路、癌癥中的通路、NF-kappaB信號通路、Th17細胞分化等,按照lg(p value)值由小到大排序,前20條通路結(jié)果見圖6,各通路包含的靶基因見表5。
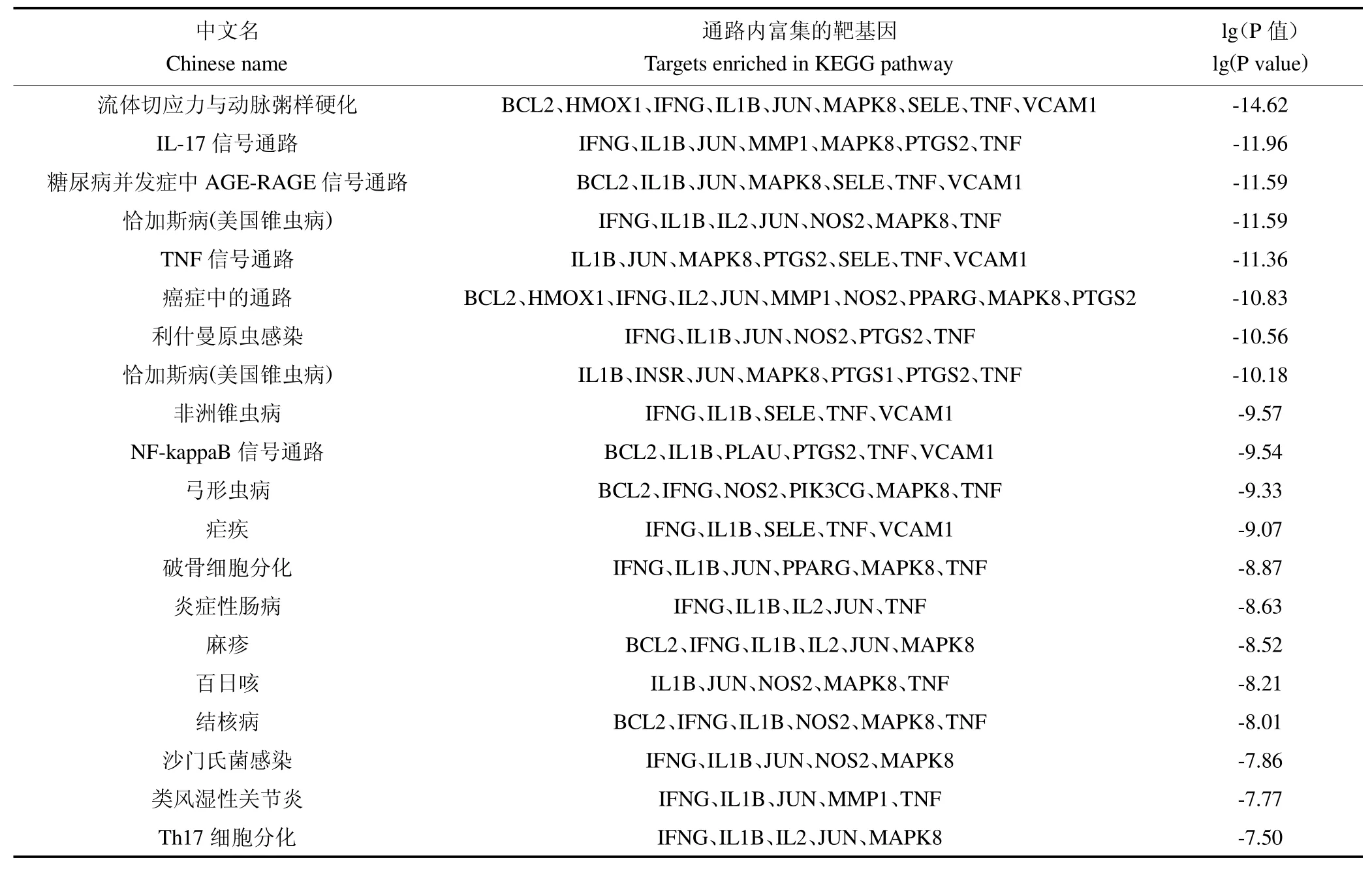
表5 人參影響KEGG信號通路(Top20)中包含的靶基因Table 5 Ginseng affects the targets contained in KEGG signal pathway(Top20)
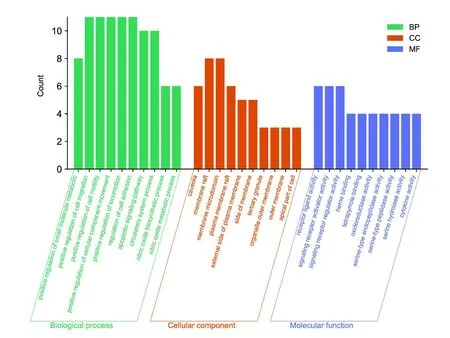
圖5 GO功能富集分析圖Fig.5 The GO function enrichment analysis diagram

圖6 KEGG通路富集分析氣泡圖(Top20)Fig.6 The KEGG pathway enrichment analysis diagram(Top20)
2.6 生物網(wǎng)絡構(gòu)建結(jié)果
構(gòu)建關于10個關鍵靶標、其關聯(lián)的活性成分及信號通路的生物網(wǎng)絡,見圖7,其中10個關鍵靶標與5個活性成分、20條信號通路關聯(lián)。網(wǎng)絡分析顯示,山柰酚、-谷甾醇、人參皂苷Rb1、人參皂苷Rh2與豆甾醇等活性成分能作用于網(wǎng)絡中的多個靶標,而TNF、IL1B、PPARG、PTGS2、JUN、IFNG、VCAM1、IL2、HMOX1和NOS2等靶標也能與多個成分、多條通路發(fā)生作用,再次證明人參能夠發(fā)揮多成分、多靶標、多通路的協(xié)同作用對IPF進行全面系統(tǒng)的治療。

圖7 人參10個關鍵靶標的活性成分 靶標 通路網(wǎng)絡圖Fig.7 Active component-10 key targets-pathway network diagram
2.7 分子對接驗證
將前10位的關鍵靶標IL1B(PDBID:1T4Q)、TNF(PDB ID:5WJJ)、IFNG(PDB ID:4BZB)、JUN(PDB ID:4EBV)、NOS2(PDB ID:4NOS)、PTGS2(PDB ID:5IKQ)、VCAM1(PDB ID:IVCA)、IL2(PDB ID:1M48)、PPARG(PDB ID:6FZF)和HMOX1(PDB ID:3HOK)與Stigmasterol、Kaempferol及beta-sitosterol進行對接,對接的最佳結(jié)合力見圖8。Best affinity越小,二者能更好地自主結(jié)合,由圖8可知,Kaempferol(山柰酚)與各個靶標的結(jié)合能大部分都小于-29.2 kJ/mol,而當Affinity<-29.2 kJ/mol時,說明配體與受體強烈結(jié)合[10],在本研究中可以被視為最有可能在人參治療IPF中發(fā)揮重要作用的活性成分。

圖8 人參活性成分與關鍵靶點分子對接最佳結(jié)合力熱圖Fig.8 Heatmap of the best binding between the active components of ginseng and key targets
3 討論
IPF屬于中醫(yī)的“肺萎”、“咳嗽”和“喘證”的范疇,病位在肺,久則及腎,其發(fā)病機理與虛、瘀、痰、毒相關[11],古今常見的治法有活血化瘀、益氣養(yǎng)陰、清熱化痰等等[12-14]。人參作為重要的補氣藥,早在《神農(nóng)本草經(jīng)》中就被視作“上品”,可以“補五臟,安精神,定魂魄,止驚悸,除邪氣,明目開心,益智,久服輕身延年”[15]。現(xiàn)代藥理研究也認為,人參具有抗腫瘤、抗衰老、抗疲勞、調(diào)節(jié)免疫力以及抗菌等作用[16]。
近年來,人參的抗纖維化作用也受到了廣泛的重視與研究,本研究富集到的人參皂苷、-谷甾醇、山柰酚和豆甾醇等成分在實驗研究中被證實具有較好地抗纖維化活性[17-19],如-谷甾醇可以通過TGF-/smad依賴的信號通路抑制上皮間充質(zhì)轉(zhuǎn)化,并減少細胞外基質(zhì)的沉積[20];山柰酚可以通過調(diào)節(jié)自噬來減輕二氧化硅誘導的肺間質(zhì)纖維化[21]等等。當然一些成分也同時存在于其他天然藥物中,當與其他藥物根據(jù)藥物性味、七情理論配伍時,這些有效成分可能更好地表達,在協(xié)同減毒的基礎上發(fā)揮更好的治療效應[22],所以,篩選不同配比的人參藥對研發(fā)抗纖維化藥物頗具潛力。
本研究富集到的通路多數(shù)與環(huán)境信息處理、免疫等相關,見圖9。其中,受影響最大的通路是流體切應力與動脈粥樣硬化,該通路在血管生物學中起著核心作用。這一通路中控制血管內(nèi)皮細胞(EC)基因表達的關鍵轉(zhuǎn)錄因子分別是KLF2、Nrf2、AP-1和NF-kappaB[23,24],圍繞這些內(nèi)皮轉(zhuǎn)錄因子進行的抗纖維化探索也是近幾年的熱點方向。其中關于激活Nrf2的研究較多,與纖維化中氧化應激這一病理機制有關。目前已批準治療IPF的藥物吡非尼酮就可以通過抑制Bach1和激活Nrf2,恢復Nrf2/Bach1平衡來發(fā)揮抗纖維化作用[25],并且人參中的活性成分也被證實可以通過上調(diào)Nrf2核轉(zhuǎn)位來發(fā)揮抗肝纖維化作用[26,27]。但是,人參作為具有潛力的多器官組織抗纖維化藥物,其有效成分通過調(diào)控Nrf2來抗肺間質(zhì)纖維化的機制研究尚屬空白,因此,填補這一空白具有重要意義。此外,IL-17信號通路是另一條重要的作用通路,它不僅在保護宿主抵抗細胞外病原體方面具有重要作用,還促進了自身免疫性疾病中的炎癥病理[28]。本研究將富集到的關鍵靶標投射到IL-17通路中,可以發(fā)現(xiàn),人參中的活性成分調(diào)控了這一通路中的13個靶點,其中的IL-17A經(jīng)過實驗證實可以促進肺間質(zhì)纖維化的發(fā)生,而敲除它的受體則可以改善由博萊霉素誘導的肺間質(zhì)纖維化中的急性炎癥反應,抑制肺間質(zhì)纖維化的發(fā)生[29],并且,有效誘導自噬,促進膠原的自噬降解和自噬相關的細胞死亡[30]。因此,IL-17A也是人參治療肺間質(zhì)纖維化的潛在治療靶點。

圖9 KEGG通路分類圖Fig.9 KEGG path classification diagram
結(jié)合本研究的結(jié)果可以推測,人參中的人參皂苷、山柰酚可能通過Nrf2或IL-17A所在的信號通路介導氧化還原或者細胞自噬過程來發(fā)揮抗肺間質(zhì)纖維化的作用,這一機制有待在未來的實驗研究中進一步驗證。

