2型糖尿病患者瞼板腺功能障礙與血脂的相關性研究
劉 佳,高亞強
0 引言
瞼板腺功能障礙(meibomian gland dysfunction,MGD)是一種慢性、彌漫性瞼板腺病變,可引起淚膜穩定性下降、眼表炎性反應、眼部不適等一系列癥狀[1],瞼板腺終末導管的阻塞和瞼板腺分泌的瞼酯異常是發病過程的中心環節[2]。研究表明相比正常人群,MGD患者分泌的瞼酯中蠟酯和固醇酯成分增加,提高了瞼酯的熔點和黏度[3]。這種成分的改變導致腺管阻塞并影響了淚膜的穩定性[4]。已有部分研究探索MGD患者分泌瞼酯成分的改變可能與多種類型的血脂異常相關[5-7],其中膽固醇的高水平已被公認為MGD患病的危險因素[2]。2型糖尿病(type 2 diabetes mellitus, T2DM)患者易合并血脂異常、脂肪肝、高尿酸血癥等多種代謝異常[8],同時糖尿病患者亦是眼表疾病的高發人群[9],但關于血脂異常是否會增加T2DM患者MGD發生的風險,目前尚未見到相關研究。本研究通過分析伴有MGD的T2DM患者的各項血脂指標,探索T2DM患者MGD與脂質代謝水平之間的相關性,旨在為臨床預防與治療提供依據。
1 對象和方法
1.1對象本研究為回顧性病例對照研究。收集2020-07/2021-10入住于我院內分泌科已由專科醫師確診為T2DM患者184例。完成眼表檢查后MGD患者94例為MGD組;不合并MGD的T2DM患者90例為對照組。納入標準:根據2017年我國瞼板腺功能障礙診斷與治療專家共識[2]:(1)瞼板腺和瞼緣開口異常;(2)瞼酯分泌異常;(3)具有眼部相關癥狀;(4)瞼板腺缺失;(5)脂質層厚度異常。(1)或(2)項合并(3)即診斷為MGD,(4)和(5)為加強診斷指標。排除標準:(1)曾應用過他汀類、血脂康、阿托品、新斯的明、激素、人工淚液等其他影響血脂水平和眼表功能藥物的患者。(2)近6mo存在需要局部藥物治療的眼病或眼外傷、眼部手術的患者。(3)存在影響瞼板腺功能的全身性疾病,如甲狀腺功能亢進、Steven-Johnson綜合征、干燥綜合征、皮膚病(類天皰瘡、紅斑狼瘡、痤瘡、酒糟鼻)、圍絕經期綜合征、抑郁癥、焦慮癥等。本研究通過河北港口集團有限公司港口醫院倫理委員會審查,遵循《赫爾辛基宣言》,所有受試者均自愿參加研究,并簽署知情同意書。
1.2方法所有瞼板腺檢查項目由同一經驗豐富技師操作:(1)裂隙燈下觀察瞼板腺開口及瞼緣形態改變。瞼板腺口的變化:瞼緣腺口酯帽、隆起、酯栓、先天性缺乏、狹窄、閉塞、移位。瞼緣形態的變化:瞼緣充血和毛細血管擴張、過度角化、形態不規整、肥厚及新生血管。(2)裂隙燈下擠壓瞼板腺使瞼酯排出,觀察瞼酯的性狀和中央5條腺體分泌。瞼板腺分泌物性狀:0分:清亮、透明液體;1分:混濁的液體;2分:混濁顆粒狀的半固體;3分:濃稠如牙膏狀態。上下瞼分別評分記錄,1分及以上為異常。評價中央5條腺體的分泌物排出評分:0分,5條腺體均有分泌;1分,3~4條腺體分泌物排出;2分,1~2條腺體分泌物排出;3分,無瞼板腺腺體分泌物排出。上下瞼分別評分記錄,3分及以上為異常。(3)應用Keratograph 5M眼表綜合分析儀紅外線瞼板腺照相及脂質層厚度檢查。瞼板腺缺失面積評估:通過紅外攝像系統分別對上下瞼結膜進行拍攝,拍攝的照片自動經過Meibo-Scan增強對比模式處理,瞼板腺表現為白色紋路,其余部分為灰色背景。上下瞼任一缺失面積達到1/3為異常。脂質層厚度評估:脂質層模糊,顏色灰暗,無色彩為脂質層厚度異常。(4)所有受試者空腹10h以上,于次日清晨抽取肘靜脈血,測定空腹血糖(fasting levels of serum glucose, FBG)、糖化血紅蛋白(glycosylated hemoglobin A1c, HbA1c)、總膽固醇(total cholesterol, TC)、甘油三酯(triglyceride, TG)、低密度脂蛋白膽固醇(low-density lipoprotein cholesterol, LDL-C)、高密度脂蛋白膽固醇(high-density lipoprotein cholesterol, HDL-C),所有生化指標檢查均由同一實驗室進行化驗檢測。(5)由1名經過培訓的醫生負責記錄一般人口學資料、癥狀、BMI、糖尿病病程等。
血脂異常標準參照《中國成人血脂異常防治指南(2016年修訂版)》的診斷標準[10],TC≥6.22mmol/L為高TC血癥、TG≥2.26mmol/L為高TG血癥、LDL-C≥4.14mmol/L為高LDL-C血癥、HDL-C<1.04mmol/L為低HDL-C血癥,有以上情況之一者即為血脂異常。肥胖標準參照《中國2型糖尿病合并肥胖綜合管理專家共識》[11],體質量指數(BMI)=體質量(kg)/身高2(m2),BMI<28kg/m2為正常或超重,BMI≥28kg/m2為肥胖。HbA1C控制標準參照《中國2型糖尿病防治指南(2020年版)》[12]:HbA1c<7%為血糖控制正常,HbA1c≥7%為血糖控制不良。
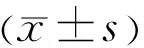
2 結果
2.1兩組患者一般資料比較本研究中MGD患者94例為MGD組:其中男50例,女44例,年齡42~79歲;不合并MGD的T2DM患者90例為對照組:其中男50例,女40例,年齡43~81歲。兩組患者一般資料比較差異均無統計學意義(P>0.05,表1)。

表1 兩組患者一般資料比較
2.2兩組患者血生化指標比較兩組患者空腹血糖比較,差異無統計學意義(P>0.05);MGD組患者HbA1c、TC、TG、LDL-C均值均明顯高于對照組,差異均有統計學意義(P<0.001);MGD組患者HDL-C均值略高于對照組,但差異無統計學意義(P>0.05),見表2。
表2 兩組患者血生化指標比較
2.3兩組患者血糖控制不良和肥胖及血脂異常情況比較MGD組患者血糖控制不良率、高TC血癥、高TG血癥、高LDL-C血癥、血脂異常情況均高于對照組,差異均有統計學意義(P<0.05)。兩組患者肥胖和低HDL-C血癥患病率比較差異均無統計學意義(P>0.05),見表3。
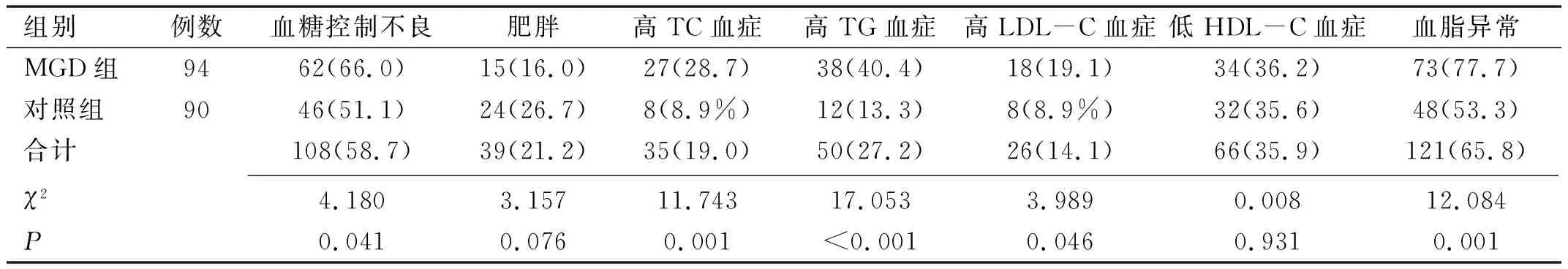
表3 兩組患者血糖控制不良和肥胖及血脂異常情況比較 例(%)
2.4影響T2DM合并MGD發生因素的Logistic回歸分析采用多因素Logistic回歸分析T2DM合并MGD的相關危險因素,以是否患有MGD(否=0,是=1)為因變量,將表3中P<0.1的自變量均以直接法納入方程。多因素Logistic回歸結果顯示高TC血癥(OR=5.846,95%CI:1.867~18.306,P<0.001)、高TG血癥(OR=5.822,95%CI:2.654~12.774,P=0.002)是T2DM合并MGD發生的危險因素,見表4。

表4 影響T2DM合并MGD發生因素的Logistic回歸分析
3 討論
MGD是一種慢性、彌漫性瞼板腺病變,臨床上可引起眼表慢性炎癥反應和淚膜異常,從而導致眼干、眼癢、燒灼感、異物感、分泌物增多、視力波動性模糊等一系列不適癥狀,是干眼的主要病因[1]。MGD的病因目前尚未完全明確,目前已知發病的中心環節為瞼板腺終末導管的阻塞和/或瞼酯分泌異常[2]。瞼板腺分泌的正常瞼酯是清亮透明的,呈蛋清狀,在眼瞼溫度下保持液態,隨瞬目動作被眼輪匝肌和Riolan肌收縮壓迫瞼板腺而排出,并隨著開瞼拉伸變為膜狀,從而形成淚膜的脂質層[13]。但在MGD患者,分泌物性狀變為黃色、混濁黏稠甚至呈牙膏樣,無法形成穩定的淚膜,從而導致淚液蒸發加快。同時瞼緣微生物釋放的脂肪酶分解脂質,其分解產物介導眼表炎癥反應,產生一系列不適癥狀[14]。研究表明[13],MGD患者分泌的瞼酯性狀和顏色的改變與瞼酯的成分變化密切相關,瞼酯的熔點、流動性及淚膜脂質的完整性是由其所含脂質的類型和脂肪酸的不飽和性、支鏈程度決定的。Joffre等[3]應用質譜法和氣相色譜法發現在MGD患者的瞼酯中,蠟酯、膽固醇酯、甘油三酯等支鏈脂肪酸成分明顯增加,引起瞼酯的熔點和黏度升高,進而導致了腺管的堵塞。Shine等[15]發現膽固醇酯在MGD患者的瞼酯中持續存在,而正常人群并非如此。上述研究均表明瞼酯中膽固醇酯成分的升高可能是MGD患者發生腺管堵塞和瞼酯質量改變的重要因素。部分臨床研究基于此進一步探索機體脂質代謝異常是否會增加MGD患病的風險,Bu等[16]通過敲除Apo-E基因制作高膽固醇血癥的小鼠,與野生型小鼠對照觀察到高膽固醇血癥導致小鼠的瞼板腺阻塞、角化過度、萎縮,腺泡細胞增生分化異常及炎性浸潤增加,導致了MGD和眼表的改變。一項為期10a針對39336例干眼患者的病例對照研究顯示,高TG血癥、高TC血癥、高LDL-C血癥及低HDL-C均為干眼發病的獨立危險因素[17]。Braich等[6]和Dhawan等[18]的研究結果也表明MGD與多種血脂異常相關,MGD患者較對照組TC、TG、LDL-C均出現不同程度的升高。
由于胰島素分泌不足、胰島素抵抗等代謝因素,糖尿病患者的血脂異常發生率要遠高于非糖尿病患者[19]。盡管在本研究選擇研究對象時,已排除發現血脂異常并治療的T2DM患者,參與研究的受試者任一項血脂異常的患病率依然高達65.8%。同時,糖尿病患者的慢性高血糖狀態、低胰島素水平、微血管病變以及繼發的炎癥和免疫反應從多個方面增加MGD的患病風險[9],本研究發現MGD組患者的HbA1c較對照組水平升高,血糖控制不良的比率增高,與Fan等[20]的研究結果相一致。但關于T2DM患者的血脂異常是否會進一步增加T2DM患者MGD發生的風險,目前尚未見到相關研究,由于T2DM患者的眼表疾病存在其特殊性及難治性[21],積極探索T2DM患者并發MGD與血脂異常的關系有重要意義。
本研究選擇T2DM伴發MGD患者為研究對象,與對照組血脂各個成分相比,發現TC、TG、LDL-C均出現明顯升高,差異具有統計學意義,且回歸分析表明高TC血癥、高TG血癥是2型糖尿病合并MGD發生的危險因素,與Braich等[6]、Pinna等[5]在不伴有T2DM的MGD患者與血脂代謝異常中的研究結果相類似,說明血液中的TG、TC升高確實增加了MGD的患病風險,但血脂異常對瞼板腺功能影響的病理基礎研究尚需進一步探尋。Braich等[6]的回歸分析發現高LDL-C血癥也是導致MGD的危險因素,但本研究未能在T2DM患者中得到類似的陽性結果,這可能與T2DM患者的糖代謝異常影響LDL-C的合成與分解有關。同時,Braich等[6]和Pinna等[5]均發現,對血管具有保護作用的HDL-C,在MGD組患者中也同樣高于對照組,且差異具有統計學意義,相關分析發現高HDL-C血癥同樣是MGD發病的危險因素[5-6]。關于HDL-C在MGD發病中起到的作用尚未明確,動物模型中HDL-C[22]能促進皮脂腺上皮分化,加速TG、TC的積累和分泌,瞼板腺是一種特化的皮脂腺,是否會同樣受到HDL-C的影響還需進一步探索研究。本研究中兩組患者比較HDL-C差異無統計學意義,這可能與T2DM患者的胰島素抵抗引起脂蛋白酶活性降低,導致HDL-C顆粒合成和成熟的減少有關[23]。
近年來,我國人群的平均血脂水平迅速上升,血脂異常患病率明顯增加[10]。大量國內外流行病學前瞻性研究表明,血脂異常是動脈粥樣硬化性心血管疾病(atherosclerotic cardiovascular disease,ASCVD)發病及死亡的重要危險因素[24],是預防心血管卒中的重要指標。既往研究充分證實,T2DM患者如合并血脂異常將進一步增加大血管病變和微血管并發癥的風險[19]。但由于血脂異常無明顯臨床癥狀,往往通過體檢或發生心血管事件后才發現,早期發現血脂異常并進行良好的血脂管理對T2DM患者具有重要意義。本研究發現伴有MGD的T2DM患者較對照組更易并發TG、TC、LDL-C的升高,臨床上眼科醫生或可通過觀察瞼板腺的改變早期發現患者血脂代謝異常的證據,從而盡早對T2DM患者的血脂異常做到早期發現及控制。除此之外,根據本研究結果進一步推測,血脂異常可能在T2DM患者的MGD發生發展中起到重要作用,調脂藥物的應用可能為MGD的一種治療方法。丁小珍等[25]研究發現ω-3的補充可以有效降低TC、TG、LDL-C,同時顯著降低了MGD的評級。他汀類藥物對MGD是否具有治療作用尚需進一步研究探索。
綜上所述,本研究發現T2DM合并MGD患者的TG、TC、LDL-C均高于不合并MGD的T2DM患者,高TC血癥、高TG血癥為MGD發生的危險因素。本研究受限于樣本量,觀察指標有限,且為病例對照研究不能得出因果聯系,關于T2DM患者合并MGD的更多影響因素有待進一步大樣本前瞻性研究中證實和補充。

