鐵死亡在多形性膠質母細胞瘤治療中的研究進展
斯 寶, 張剛利, 胡昌辰
(山西醫科大學第五臨床醫學院 神經外科, 山西 太原, 030000)
細胞死亡是存在于所有生物體中的一個共有過程,根據2018年細胞死亡命名委員會的最新建議,目前有2種類型的細胞死亡: 意外細胞死亡(ACD)和調控細胞死亡(RCD)[1]。ACD是由化學、物理或機體嚴重應激等引起的不受控制且不可避免的細胞死亡過程,與之對應的RCD則可以通過物理、化學等干預來調控。RCD又分為凋亡型和非凋亡型(鐵死亡、壞死性凋亡、細胞焦亡和堿死亡等),這2種類型具有不同的分子特征,因此對于疾病的影響也存在很大差異[2]。細胞鐵死亡是一種區別于細胞凋亡、細胞壞死和細胞自噬的新型鐵依賴性細胞程序性死亡方式。從形態學角度看,細胞鐵死亡具有典型的壞死樣改變特征,如細胞水腫、質膜破裂。從生物化學角度看,鐵死亡具有產生致命程度的鐵依賴性脂質過氧化的特點[3]。然而,細胞凋亡的經典生化特征,如染色質碎裂、含半胱氨酸的天冬氨酸蛋白水解酶激活和線粒體細胞色素C的釋放,在鐵死亡中則很少存在。雖然鐵死亡最初被定義為一種與自噬無關的細胞死亡,但越來越多證據[4]表明,自噬特別是選擇性自噬在促進細胞鐵死亡過程中發揮著重要作用。研究[5]表明,細胞鐵死亡在多形性膠質母細胞瘤(GBM)治療中發揮著重要作用。
1 GBM
GBM屬于Ⅳ級膠質瘤,占所有顱內腫瘤的12%~15%, 其在膠質瘤中惡性程度最高,預后最差,5年生存率僅為 5%[6]。目前, GBM最有效的治療方法是最大程度切除腫瘤并盡可能保留腦功能,術后輔助放療和采用替莫唑胺 (TMZ) 化療[7]。過去幾年GBM手術和放化療方案取得了一定程度進展,但患者平均生存期仍僅為 15 個月左右[8]。導致預后不良的原因包括以下幾點: 首先, GBM往往邊界不清且與正常腦組織難以完全分離,較少有進行二次手術的機會[9]; 其次,血腦屏障 (BBB) 的存在和腫瘤細胞的快速增殖常導致腫瘤血管化不足,這使化療藥物難以到達目標位置發揮療效[10]; 最后, GBM存在廣泛的腫瘤異質性,這可能導致一系列多變的生物學反應。GBM瘤內分子異質性是臨床對抗復發、侵襲所面臨的主要難題。GBM瘤內分子異質性具有兩面性: 一方面其可作為預后標記物指導GBM個體化治療; 另一方面其又是導致分子靶向治療失敗的因素。研究[11]表明,GBM的遺傳改變主要涉及3大信號通路: 磷脂酰肌醇3激酶(PI3K)相關信號通路、P53相關信號通路 和RB相關信號通路。因此,單一療法方案通常會導致腫瘤變異和腫瘤耐受性增大,進而引起腫瘤復發和產生復雜的腫瘤異質性,而靶向通路治療能夠針對性地作用于一類高表達特定蛋白的細胞亞群,且不影響其他正常細胞。
此外,膠質瘤干細胞是一個不斷增殖的膠質細胞瘤細胞亞群,具有高致瘤能力、無限自我更新和多向分化潛能,在初始治療期間對抗癌藥物的敏感性常表現出廣泛的腫瘤間異質性[12]。同時,膠質瘤干細胞對放療和化療具有強耐受性是膠質瘤復發的重要因素[10]。
2 鐵死亡通路的一般機制
2.1 氨基酸代謝和鐵死亡
研究[13]發現,半胱氨酸/谷胱甘肽耗竭途徑可導致脂質過氧化,進而發生細胞鐵死亡。胱氨酸/谷氨酸反向轉運系統(system Xc-)由溶質載體家族7成員11(SLC7A11)重組蛋白和溶質載體家族3成員2(SLC3A2)重組蛋白載體組成,可以參與包括生產還原型谷胱甘肽在內的一系列代謝反應。L-胱氨酸通過谷氨酸的system Xc-進入細胞。首先,L-半胱氨酸在γ-谷氨酰半胱氨酸合成酶的作用下轉化為γ-谷氨酰半胱氨酸,然后在谷胱甘肽合成酶和甘氨酸的作用下進一步轉化為谷胱甘肽[14]。谷胱甘肽作為活性氧自由基(ROS)的一種清除劑,可被氧化成谷胱甘肽二硫化物(GSSG), 維持細胞氧化還原平衡。
谷胱甘肽過氧化物酶4(Gpx4)具有清除脂質過氧化物的功能,失活的Gpx4可打破氧化平衡,導致脂質過氧化物破壞膜結構,激發鐵死亡[15], 因此其是唯一一種通過消耗還原型谷胱甘肽將膜脂過氧化氫(LOOH)還原為無毒脂醇(LOH)的酶。由于Gpx4主要利用抗氧化劑谷胱甘肽來降低脂質過氧化氫,因此Gpx4的活性在很大程度上依賴于細胞內的谷胱甘肽水平。抑制Gpx4活性可導致過度的脂質過氧化,繼而發生細胞鐵死亡,例如RSL3 Gpx4抑制劑能通過降低 Gpx4 的表達誘導細胞發生鐵死亡。盡管Gpx4在鐵死亡中起著至關重要作用,但某些癌細胞對Gpx4抑制劑引起的鐵死亡具有抗性,這表明鐵死亡可能還受其他因素調節[16]。
2.2 脂質代謝和鐵死亡
多不飽和脂肪酸(PUFAs)是鐵死亡的關鍵成分。PUFAs要導致鐵死亡首先必須先轉變為磷脂酰乙醇胺(PE)多不飽和脂肪酸[17]。PE-PUFAs是由乙酰輔酶A合成酶長鏈脂肪成員4(ACSL4)在溶血磷膽堿酰基轉移酶3的作用下形成的。在15-脂氧合酶(LOX)和亞鐵離子(Fe2+)的作用下, PE-PUFAs可發生脂質過氧化,進而導致細胞鐵死亡。
2.3 鐵離子代謝和鐵死亡
鐵在細胞代謝中主要以2種形式存在: Fe2+和三價鐵離子(Fe3+)。血液中的Fe3+附著在轉鐵蛋白受體(TFR)-1上,通過胞吞作用進入細胞內。進入細胞內的Fe3+被前列腺6次跨膜蛋白3 (STEAP3)還原為Fe2+, 然后通過內膜的二價金屬轉運體1(DMT1)進入細胞質。亞鐵通過鐵死亡的負性調控因子鐵蛋白離開細胞[18]。在過氧化氫(H2O2)的作用下, Fe2+可發生芬頓反應[19](雙氧水和過渡金屬如Fe2+之間的反應是羥基的主要來源)產生ROS。研究[20]表明,低而可控的ROS水平對正常的細胞和機體功能至關重要,中等水平的ROS水平有利于腫瘤發展,但高水平的ROS會導致細胞損傷和死亡。
2.4 FES1-NADPH通路和鐵死亡
研究[21]表明,在Gpx4基因敲除的細胞中發現,鐵死亡抑制蛋白1(FSP1)具有和Gpx4相似的作用, FSP1也稱為線粒體相關凋亡誘導因子2(AIFM2)或p53反應基因(PRG3)。
FSP1是一種NADPH依賴的輔酶Q10(CoQ10)氧化還原酶,其作用是將細胞壁中的泛醌Q10轉化為泛酚Q10。泛酚作為ROS清除劑可以防止發生鐵死亡特征的脂質過氧化。研究[22]發現, FSP1可以通過非依賴性輔酶Q10途徑阻斷藥物誘導的鐵死亡,因此FSP1抑制鐵死亡的確切機制還需要進一步研究。研究[23]發現,在多種癌癥中, FSP1水平與較低的總生存率和無病間隔時間顯著相關,并可作為預后標志物。臨床治療中發現和了解這些代償途徑十分重要,因為通過增加Gpx4來促進癌細胞發生鐵死亡可能會因為這些代償機制的激活而無法達到預期效果。
上述途徑的任何改變都會阻礙或促進鐵死亡。例如,細胞內Fe2+的增加和谷胱甘肽生成的減少可導致ROS增加和脂質過氧化; 抑制Gpx4會阻礙過氧化脂質向脂醇轉化,而過氧化脂質的增加會破壞細胞器和細胞膜的結構導致膜通透性喪失,最后發生細胞鐵死亡。
3 細胞鐵死亡在癌癥中的治療潛力
近年來,研究人員發現,鐵死亡存在于乳腺癌、腎細胞癌、肺癌、胰腺癌、彌漫性大B細胞淋巴瘤、頭頸部鱗狀細胞癌和肝細胞癌等多種癌癥中,聯合應用鐵死亡激活劑與抗腫瘤藥物或者誘導腫瘤細胞發生鐵死亡均有利于對腫瘤的干預、抑制和清除[24-26]。已有實驗[27]證明,在Ptgs2基因高表達的BJeLR細胞來源的異種移植小鼠模型中,鐵死亡陽性調控因子RSL3可抑制腫瘤生長,而Ptgs2是RSL在腫瘤細胞中導致鐵死亡的特異性標志物。Gpx4是RSL3的主要靶點,可特異性地誘導含有HRAS的BJ源性成纖維細胞發生鐵死亡,敲除Gpx4基因可誘導腎癌鐵死亡[27]。此外,鐵死亡誘導劑還可與順鉑、替莫唑胺、阿糖胞苷和阿霉素等藥物聯合應用于不同類型癌癥的抗癌治療。研究[28]表明,細胞密度也可以影響其對鐵死亡的敏感性,鐵死亡誘導劑可促進線粒體活性氧自由基(MitoROS)的產生,導致線粒體通透性轉換孔(MPTP)開放,進而導致線粒體消失和ATP耗盡[29],見圖1。因此,研究人員推測MitoROS在破壞線粒體穩態和鐵死亡的過程中起到了正反饋作用。
新的技術已經開始應用于鐵死亡在癌癥治療中的研究。例如,因鐵死亡能以波狀方式在細胞群中擴散,已有一些研究小組開始嘗試使用納米粒子以精確誘導腫瘤組織中癌細胞的鐵死亡。有研究[30]通過 Fe3+/Gd3+與多酚的螯合反應,將兩親性高分子骨架(P-SS-D)、肉桂醛前體藥物(CA-OH)和Fe3+/釓離子(Gd3+)結合,設計了一種熱塑性納米晶,當納米顆粒被投放到高谷胱甘肽水平的腫瘤微環境中時,其可被 P-SS-D 的多硫化物主鏈解聚,激活的CA消耗谷胱甘肽使內源性H2O2產生羥自由基(·OH), 同時抑制Gpx4的活性。二硫化物、CA和 Fe3+對谷胱甘肽的消耗可使 Gpx4減少并產生羥基,加速脂質過氧化物的積累,從而促進鐵死亡的發生。
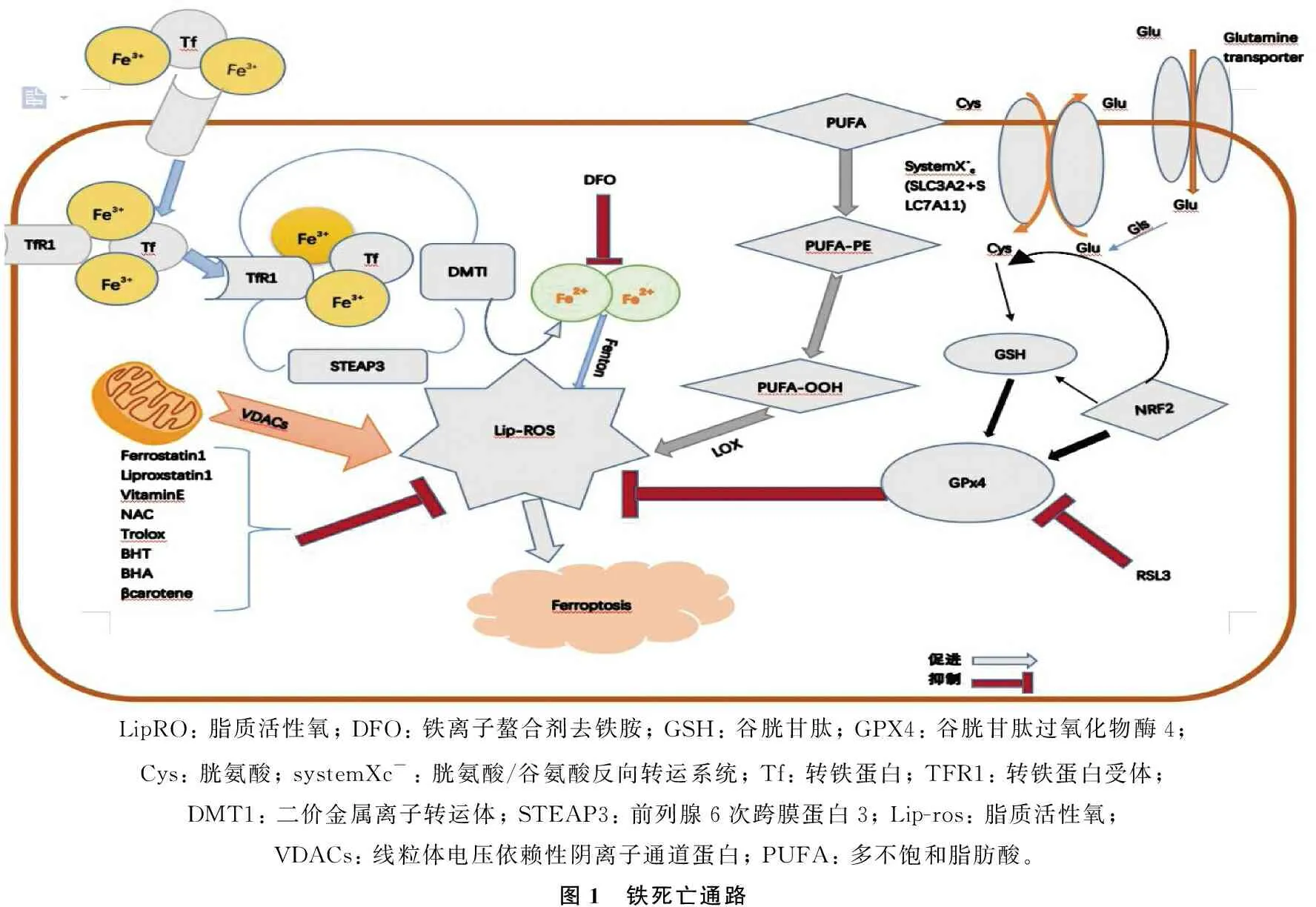
LipRO: 脂質活性氧; DFO: 鐵離子螯合劑去鐵胺; GSH: 谷胱甘肽; GPX4: 谷胱甘肽過氧化物酶4; Cys: 胱氨酸; systemXc-: 胱氨酸/谷氨酸反向轉運系統; Tf: 轉鐵蛋白; TFR1: 轉鐵蛋白受體; DMT1: 二價金屬離子轉運體; STEAP3: 前列腺6次跨膜蛋白3; Lip-ros: 脂質活性氧; VDACs: 線粒體電壓依賴性陰離子通道蛋白; PUFA: 多不飽和脂肪酸。圖1 鐵死亡通路
4 GBM與細胞鐵死亡的關系
近年來越來越多的研究[31]已經開始探索鐵在神經系統中的作用機制。研究在腦毛細血管的表面發現了轉鐵蛋白受體。轉鐵蛋白(Tf)已被證明通過受體介導的胞吞作用進入大腦內皮細胞,隨后進入大腦。Tf代謝失調會導致大腦中的不穩定鐵增加,而不穩定鐵的增加會導致脂質過氧化。事實上,這主要取決于芬頓反應和脂氧合酶LOX。對于這個反應,循環中必須要求有足夠的不穩定鐵。鐵死亡導致的不穩定鐵含量增加正好符合這一條件。研究結果顯示,抗氧化劑如鐵螯合劑、去鐵胺等,可以終止此反應,減少細胞內的鐵含量,抑制鐵依賴的脂質ROS的產生。
研究[32]表明,轉鐵蛋白在GBM中的表達程度遠高于其他級別膠質瘤,并且衡量氧化應激水平的8-羥化脫氧鳥苷(8-OHdG)也處于首位,說明腫瘤細胞惡性程度與細胞鐵死亡的發生具有正相關。Tf是血漿中發現的一種80 kDa的糖蛋白,是細胞增殖中必不可少的生長因子,能夠結合鐵,因此Tf可作為鐵通過血液進入腦細胞的載體。但是并非所有大腦區域都存在Tf, 其主要存在于少突膠質細胞、腦脊液和腦毛細血管內皮細胞中。
大腦和神經膠質母細胞瘤中鐵代謝的調節是通過一組特定的蛋白質來完成的,這些蛋白質可以調節腫瘤細胞中鐵的濃度。研究[33]表明, BBB是血液和大腦之間的獨特結構,嚴密調節離子和分子進出大腦的運輸。構成BBB的內皮細胞主要通過 Tf/TFR1 途徑吸收并介導 Fe2+從血管轉運至大腦[34]。腦細胞吸收鐵有2種基本方式: 第1種是 Tf/TFR1 途徑,大多數細胞外鐵以Fe3+形式存在,與血漿中的循環 Tf 結合,然后與細胞表面的 TFR1 結合并通過胞吞作用進入細胞; 第2種是非 Tf 結合的鐵途徑,Fe3+通過十二指腸細胞色素b和朊病毒蛋白被還原為Fe2+,其再由ZIP家族成員 (ZIP8/14) 或二價金屬轉運蛋白1(DMT1) 運輸,見圖1。每個同工型DMT1都遵循不同的途徑并具有不同的位置。特別是在不同的腦細胞中,鐵外流由鐵轉運蛋白(FPN1)/銅藍蛋白和FPN1/膜鐵轉運輔助蛋白(Hp)通路介導。
相對于正常腦組織,GBM對鐵的需求顯著增加。GBM不僅增加了TFR1的表達以吸收更多的鐵,而且還增加了不受鐵水平調節的 TFR2[32],可能破壞正常的鐵代謝平衡,使癌細胞吸收更多的鐵。此外,TFR和鐵蛋白輕鏈(FTL)表達增加可導致鐵攝入量增大,因此神經膠質瘤干細胞的鐵攝入量比非干細胞腫瘤高2倍。單細胞磁泳法分析膠質瘤干細胞和非干細胞腫瘤細胞的鐵吸收效率和鐵含量的實驗[5]表明,前者具有更出色的鐵吸收和鐵儲存能力。膠質瘤惡性程度還與一系列促進鐵吸收的調節因子的表達增加有關,包括 DMT1、STEAP3、多聚結合蛋白 (PCBP) 2和可改變鐵儲存能力的FTH、FTL等。STEAP3可通過激活STAT3-FoxM1軸促進TFR1的表達并增加細胞鐵含量,從而在GBM中誘導上皮間質轉化 (EMT), 這是GBM侵襲和轉移的有效機制[35], 見圖1。STAT3的激活還可抑制ACSL4表達并保護細胞避免發生鐵死亡。最近報道[36]顯示,缺氧誘導的FTL可調節EMT并可作為預后標志物。研究表明,GBM細胞分裂的活躍程度受其對鐵需求量的影響,這些發現與GBM具有極高的惡性度和病死率相符。
目前,治療GBM的一線藥物是TMZ,TMZ在DNA復制過程中形成不匹配的致死堿基對,導致DNA單鏈和雙鏈斷裂,最終導致細胞凋亡[37]。然而,TMZ的臨床表現并不令人滿意,除了已知的O6-甲基鳥嘌呤-DNA-甲基轉移酶(MGMT)和錯配修復系統機制,TMZ還能激活核因子Nrf2和轉錄因子4 (ATF4),增加對鐵死亡的抵抗[38]。這些機制有助于維持細胞內穩態和增加GBM的化療耐藥性。TMZ被證明選擇性地誘導了神經膠質瘤干細胞的鐵死亡,而不是凋亡或壞死。嗜鐵誘導藥物也可增加TMZ敏感性。以上研究[39]表明,GBM細胞對鐵有很強的依賴性,鐵死亡不僅參與TMZ的耐藥過程,而且還參與GBM的致敏過程。
在此基礎上,研究人員開始應用鐵螯合劑治療GBM, 以期延長GBM患者生存期。應用螯合劑可以阻止細胞周期,通常是阻止G0/G1期,導致細胞發生凋亡。臨床研究[40]表明,鐵螯合劑是潛在的新的抗腫瘤藥物。神經母細胞瘤細胞和神經母細胞瘤兒童的早期研究[41]表明,鐵離子螯合劑去鐵胺(DFO)具有抗增殖和抗腫瘤作用。然而也有報道表明,其具有很強的毒副作用,去鐵酮已被證明具有抗增殖和細胞毒性作用。但是在人類神經母細胞瘤的嚙齒動物異種移植模型中,其未能延緩腫瘤的生長[42]。因此鐵螯尚不足以作為一種治療GBM的手段,其問題主要在于缺氧誘導因子-1(HIF-1)通路的非特異性作用和潛在的激活可能[43]。因此,通過藥物載體系統進行靶向運輸或者合成新的具有特異性定向能力的鐵螯合劑是有必要的。鐵螯合劑作為一種新的GBM治療藥物,可減少腫瘤細胞內鐵含量,導致鐵蛋白表達水平降低,TFR1表達增加從而延長GBM患者的生存期[44]。鐵和GBM存在復雜的關系,鐵可能通過激活ROS的產生或HIF-1的信號通路不同程度地影響GBM的治療。最近的一項研究[45]表明,抑制核因子KB(NF-KB)信號不僅可導致鐵蛋白重鏈表達不足還可以導致細胞活性鐵和ROS的產生增加,進而導致細胞死亡。因此,在這種情況下DFO可阻止ROS的產生,使其不能誘導細胞死亡。
此外,鐵螯合劑水楊醛異煙酰腙可顯著降低GBM細胞對電離輻射的敏感性,這種輻射防護作用可能是由硅依賴的溶酶體經輻射誘導后穩定性增加導致[46-47]。輻射前或輻射期間使用高分子量DFO(僅定位于溶酶體內)可防止發生細胞死亡[48]。此外,Tf可增強鐵螯合劑對GBM細胞的放療敏感性[49], 但是抑制β2-微球蛋白/血色素沉著癥(HFE)復合體可誘導鐵超載和隨后的ROS產生以及減少DNA修復酶增加前列腺癌細胞對放療的敏感性[50]。這些觀察結果顯示,發生于不同細胞內鐵的還原作用可能對腫瘤細胞的輻射清除有不同的影響,因此使用鐵螯合劑作為抗腫瘤藥物可能并不總是適用。
鐵螯合劑對細胞內鐵的還原作用可抑制PHD的活性,從而激活HIF-1途徑,增強GBM的侵襲性。DFO導致游離鐵缺乏,其除了可誘導HIF-1的激活,還可以促進尿激酶型纖溶酶原激活物(UPAR)和基質金屬肽酶2(MMP2)的表達,從而降解GBM細胞外基質而增強GBM侵襲性[44]。DFO的細胞毒性作用可能是由于其可使血管生成因子表達增加導致[51]。
5 小 結
綜上所述,應用鐵螯合劑治療GBM必須保持謹慎,參與鐵代謝的酶的調節是否因GBM治療(包括放射治療和TMZ治療)而發生變化的問題有待于解決,這些變化對延長GBM患者生存期是否有效仍有待確定。因此,應用鐵螯合劑來治療GBM就必須探索出合適的治療方案,以確保達到預期的治療效果。
研究[52]發現,鐵死亡在T細胞介導的抗腫瘤免疫中可影響免疫治療的效果,因為免疫治療除了可誘發腫瘤性鐵死亡外,T細胞本身也可能發生鐵死亡,從而減弱其免疫反應。缺乏Gpx4的T細胞可迅速積累膜脂質過氧化物,同時發生鐵死亡,因此通過Gpx4抑制劑在癌細胞中治療性誘導鐵死亡可能會對T細胞產生不必要的靶向效應,并產生毒副作用。因此,未來對GBM中結合免疫治療的鐵死亡調節方式仍需進一步探索,以期為治療GBM提供新的思路和方法,從而進一步延長GBM患者的生存期。

