電子自旋密度可視化在環境化學涉自由基反應教學中的應用
洪冉,徐繪,張慶云,陳張浩,呂占傲,張宗瑞,宋珍霞,楊曉凡,唐海 ,徐大勇 ,谷成 ,3,*
1安徽工程大學化學與環境工程學院,安徽 蕪湖 241000
2南京大學環境學院,南京 210023
3南京大學污染控制與資源化研究國家重點實驗室,南京 210023
1 引言
環境化學是基于四大化學的專業課程,是基礎化學知識的應用,也是延伸和拓展。因此要求授課教師具有扎實的化學基礎,能融會貫通課程要點和難點,降低“學習能壘”,激發學習興趣。自由基反應是環境化學中的重要內容,包括光照條件下的大氣圈層和水圈層中發生的自由基反應(均相或非均相)以及高級氧化技術中所涉及的自由基過程,這些反應中包括了羥基自由基、硫酸根自由基、鹵素自由基以及有機自由基等自由基物種,比較這些物種的異同是重要的學習內容。一方面有利于理解地球生態系統中最重要的能量來源——太陽輻射對環境圈層產生影響;一方面有利于建立對污染物環境歸趨(遷移轉化)的科學認識。
“自由基”部分往往也是教學難點,主要有如下幾個原因。首先,環境化學課程往往開設在中高年級,距“有機無機分析物理化學”等基礎化學課程的學習已比較“遙遠”,在高強度學習氛圍下,學生的基礎化學概念已不夠清晰。以本授課班級為例(111人),只有不到30%的同學能夠在教師提問后迅速的回答出水分子(環境化學中最重要的環境介質分子)的氧原子雜化類型,對后續水分子間相互作用——氫鍵以及氫鍵籠的學習不利;只有15人回答出氧氣分子的基態是三線態但無法給出解釋;部分同學無法建立激發能和紫外吸收光譜的相關性;部分同學對“孤對電子”和“未成對電子”混淆不清。其次,環境化學教材中對自由基反應過程的描述通常使用的是Lewis結構式,使用居中黑點(如“·”)來表示未成對電子(式1),這種較為抽象的表達造成了一定程度理解上的困難,也缺乏和分子軌道等現代化學理論的結合。

計算化學的各種理論方法和實踐手段日趨完備,特別是密度泛函概念的提出和應用直接促進了分子性質的理論計算方法的大爆發。通過對計算得到的波函數進行處理,能得到譬如“電子密度”(波函數的模方)、偶極矩、靜電勢以及自旋密度等分子性質,這些性質是實驗數據的重要支持和有力解釋,可用于驗證或預測。電子自旋分為alpha和beta兩種,一般作圖為向上和向下的箭頭(↑↓),通常情況下基態分子的alpha和beta自旋的電子數是相等的,且兩兩耦合(閉殼層)。自由基是具有未成對電子的物理實體(教學時僅考慮單自由基),因此必然存在具有alpha或beta自旋態的單個電子。為了定量討論分子結構中自旋電子分布的特性,楊偉濤等人[1]將電子自旋密度定義為Q(r)= ρα(r)- ρβ(r)。通過該方程,量化計算可以定量考查電子自旋密度等值面的空間分布以及自由基反應前后電子自旋密度的變化或遷移情況,通過圖形化方法對這些自由基的反應進行直觀描述,應用到環境化學的課程教學中,顯得生動有趣,利于理解學習。
本研究通過比較三種常見自由基分子(羥基自由基、氯自由基、甲基自由基)及其共軛閉殼層分子的自旋密度,得到單電子分布情況,通過圖形化,建立了電子結構的三維圖像,將自由基分子特有的未成對電子的空間分布進行了直觀展示,取得了良好的教學效果。自由基反應并非環境化學所特有,高分子化學、有(無)機化學、合成化學等各門課程都廣泛涉及該類反應,因此本教學方法具有推廣價值。
2 授課對象、課程概況與圖形化方法
2.1 授課對象與課程概況
環境科學與工程專業本科三年級學生已修的前置課程包括“有機無機分析物化”等化學課程,未修“結構化學”和“計算化學”,總人數111人。環境化學課程總計32學時,時間緊任務重。需要以教材為基礎,由授課教師小組將主要授課內容凝練為八個方向,平均每方向使用4個課時進行教學,根據具體內容進行彈性調整,但最多不超過6課時/方向。八個方向分別是:1) 天然水體與土壤概述;2) 溶解沉淀與氧化還原;3) 大氣擴散模型與氣相反應;4) 均相與非均相光化學反應:光子、分子與界面的相互作用;5) 污染物形態與生態系統;6) 環境污染物反應機理;7) 新型污染物起源與控制;8) 環境化學與人體健康。這種做法兼顧了具體的學情和教情,在學時極度緊張的條件下,盡可能多地進行知識傳遞。電子自旋密度可視化的教學方法主要在第6個方向中使用。
2.2 計算與圖形化方法
基態分子和自由基分子使用高斯16計算[2],波函數分析和可視化分別使用Multiwfn[3]和ChimeraX進行。鑒于教學便利性和低計算成本的要求,在M06-2X-GD3/Def2-TZVPP水平下對羥基自由、氯自由基、甲基自由基以及它們的共軛閉殼層分子進行結構優化,對羥基自由基和苯環的提氫反應進行過渡態計算。本研究主要以環境化學中最常見的羥基自由基為例,考查其電子自旋密度在提氫反應中的變化。結合分子軌道理論的軌道分析方法,剖析環境自由基過程的本質,以提高此類教學的直觀性、趣味性和深刻性。
3 實施與效果
3.1 分子軌道理論與羥基自由基教學的結合
分子軌道(MO,molecular orbital)是原子軌道的線性組合,組合過程中遵守軌道數守恒原則,即組合前后軌道數不變。作為一種雙原子分子,MO理論是分析羥基自由基(·OH)電子結構的理想工具。明確氧和氫的原子軌道是運用MO理論分析·OH自由基電子結構的前提。氫原子是最簡單的單電子原子,基態狀況下核外電子位于s殼層,寫作1s1;氧原子核外總計8個電子,結構為1s22s22p4。p殼層具有3個軌道,記作pz、px、py,其中一個被一對自旋耦合電子占據,另外兩個分別被2個自旋平行電子占據(洪特規則)。由于氫原子的s殼層和氧的p殼層能量接近,所以優先組成分子軌道,詳細情況見圖1。·OH自由基分子軌道中的非鍵軌道由氧原子p軌道的兩個分軌道組成(圖1),顯然·OH自由基具有典型的未成對電子結構。
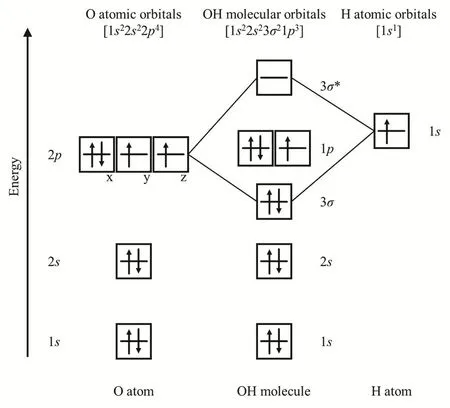
圖1 氧(氫)原子軌道和羥基自由基分子軌道
為了對比氫的s軌道和氧的p軌道能量,使用量化計算得到軌道能量。計算結果表明氫的s軌道能量為?0.3750 a.u.,氧的p軌道能量為?0.5470 a.u.,與其他軌道相比,兩者能量更為接近,滿足軌道組合的前提要求。為了幫助學生理解·OH自由基的多重度,可以適當介紹σ態的單線態氧(1Σg+,電子均自旋耦合,但其中兩個電子分布在兩個獨立π軌道上,實為雙自由基分子)作為反例,加深學生認識,但不必深入展開(為結構化學或量子化學的內容)。MO理論可以對·OH自由基的電子結構進行非常詳盡的解釋,但對于多原子分子,手動推導分子軌道比較困難。為了直觀體現半充滿的軌道的反應活性,我們對自由基分子的自旋密度進行了可視化處理,以一個過渡態反應為例進行了深入探討,見3.2小節。
3.2 自旋密度可視化在苯環-羥基自由基反應過渡態教學中的應用
苯分子是環境化學里較為常見的有機分子之一,常用作氣相有機污染物的遷移轉化的模式分子,且苯分子具有極高的對稱性(D6h),便于對其進行量化計算的研究。因此,以·OH自由基和苯的提氫反應為例,考查自旋密度在反應過程中的變化情況,并將之圖形化。首先為學生推演氣相提氫反應的過程:·OH分子和苯分子逐漸靠近(由靜電力主導)→苯環上某個H原子受到·OH作用(波函數發生相互作用)→·OH奪取苯環一個H原子形成水和苯自由基。
由MO理論分析可知(圖1 hydroxyl radical molecular orbitals),·OH在氧原子上有一個未成對電子,具有很高的活性。由自旋密度的可視化可見,·OH的單電子主要分布在O原子上(圖2a);提氫反應過渡態是C―H鍵斷裂和H―O鍵形成的中間態,由圖2b可見TS結構中的電子自旋密度同時存在于·OH和苯分子上,表明正處于舊鍵斷裂和新鍵形成的過程中;產物的自旋密度等值面表明水分子是一個閉殼層分子,而新形成的苯自由基成為新的高活性反應對象。此時可對后續可能發生的·OH加成反應做進一步討論。
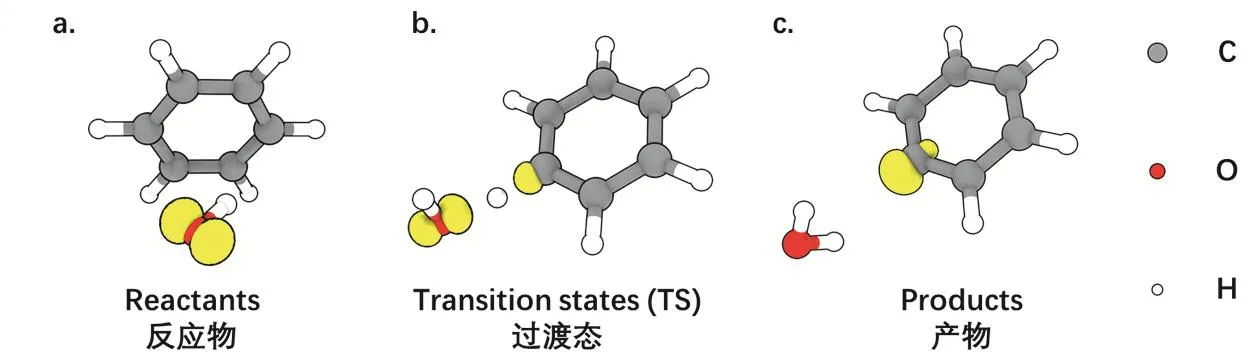
圖2 羥基自由基-苯分子提氫反應中的自旋密度變化
對反應物-過渡態-產物的能量進行比較可以從能量的角度更深入的理解反應。如圖3所示,提氫反應能壘較低(實際應當使用自由能壘,電子能壘用于教學足以定性正確),反應速率較大,易于發生反應,符合·OH反應特性。但此內容和自旋密度無關,不在本文討論。
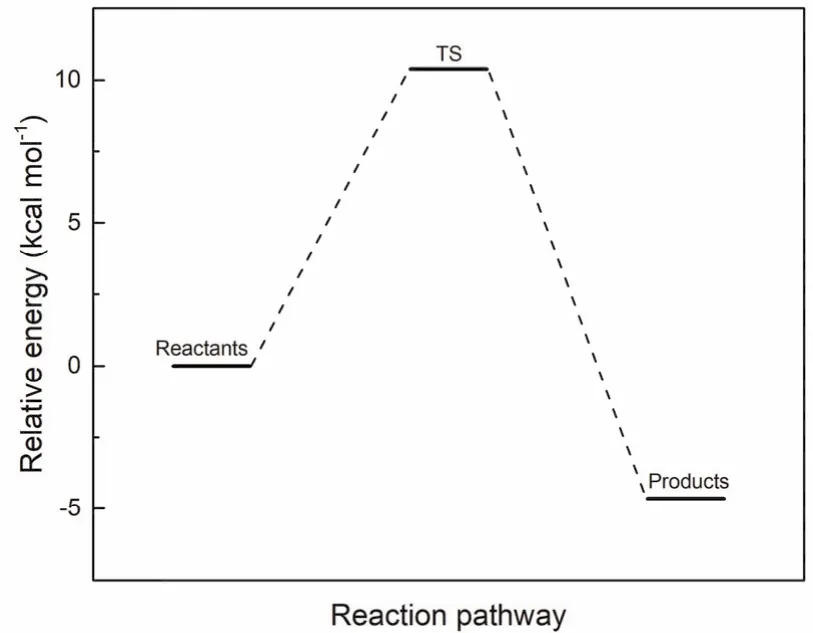
圖3 密度泛函計算得到的提氫反應能壘圖
3.3 自旋密度可視化方法的普適性及其與靜電勢耦合使用
自旋密度可視化方法適用范圍很廣,所有牽涉未成對電子的反應過程都能使用這種方法進行可視化的直觀研究。例如,環境化學關注的其他類型自由基:鹵素自由基、簡單的有機自由基等活性物種都可以用自旋密度進行研究。為了比較開閉殼層分子的自旋密度差異,這里將這些自由基對應的閉殼層的共軛物種一并列出(表1),方便學習比對。

表1 環境化學中常見自由基與共軛物種分子結構
由圖4可見,在本文的幾個例子中電子自旋密度等值面代表著自由基分子單電子分布情況,與分子軌道方法得到的結論一致,即所有閉殼層分子的自旋密度均為零。例如,羥基自由基的單電子(自旋密度等值面)主要集中在氧原子上,分子軌道理論也指出該單電子位于氧原子的P殼層的pi軌道上(圖1);氯原子(氯自由基)的3P殼層上具有一個單電子,在圖4中也得到了很好的體現,存在一個典型的pi軌道節面,閉殼層的氯離子的自旋密度為零;甲基自由基及其對應的甲烷分子不僅有自旋布居差異,其結構也發生了顯著變化,失去一個H原子后本來是四面體結構的甲烷分子變成了平面結構,這種現象是一個非常好的原子雜化案例,適合在學習價鍵理論時使用,此處不展開。甲基自由基中,C原子2P層有2個電子,因此存在2個半空1個全空軌道,接受3個H原子的電子后(回避雜化理論),必然會形成一個新的半空軌道,對應著C原子上自旋密度分布(圖4甲基自由基)。
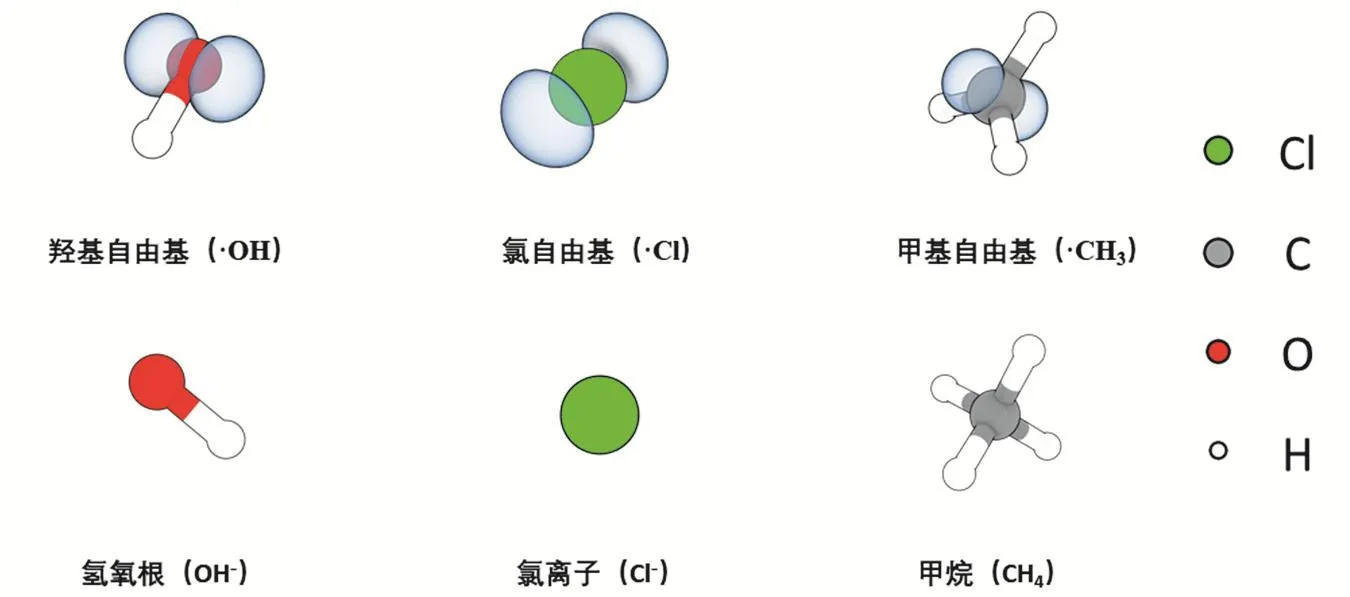
圖4 自旋密度在三種自由基分子中的分布情況
由上可見,自旋密度與“活性單電子”或“半空軌道”存在良好的對應關系,對于教科書中各種電子弱相關體系而言,是很好的反應活性位點的指示參數,值得推廣使用到其他化學課程中,例如卡賓自由基不同自旋態分辨、鹵化氫烯烴光照加成反應過程研究等。
為了更深入地理解分子反應特性,對范德華表面(電子密度為0.001 a.u.的等值面[4])的靜電勢(Electrostatic potential,ESP)進行研究,并與自旋密度建立關系。靜電勢體現了分子表面的電性特點,對反應朝向、反應位點發揮著一定程度的影響,是最容易被學生接受的分子性質之一。通過ESP的學習可以直觀理解“同性相斥,異性相吸”的分子間作用規律,將ESP和電子密度建立相關性是科學研究中的常見方法,但在教學中并不常見。
氫氧根帶一個負電荷,具有較強的彌散特征,表現為整個范德華表面電勢為負(圖5氫氧根),其最大最小值均為負值。失去一個電子形成羥基自由基后,分子表面電荷顯著增加,極大值有1處(59.59 kcal·mol?1),最小值有2處(?26.92 kcal·mol?1) (圖5羥基自由基)。其極小值點和電子自旋密度分布恰好對應了,由圖4可知,羥基自由基的氧原子上存在兩個相對獨立的自旋密度區域,結構特征與ESP很接近,ESP不僅僅受自旋電子分布影響,也受到H原子正電荷影響,整體表現出朝氧原子方向的軸端偏移的現象;氯離子的電勢表現出顯著的各向同性,沒有結構特征(圖5氯離子),氯自由基的電子自旋密度的分布受其pi軌道影響,形成了很明顯的結構特征(圖4氯自由基),其ESP形成了“兩極高赤道低”的特征,恰好與自旋密度分布特點是互補的,這是因為極高的對稱性和另外兩個全滿pi軌道共同導致。甲基自由基的自旋密度和ESP保持了很好的一致性,其ESP最小值點與自旋密度分布吻合。通過ESP和自旋密度的分析可知,這兩者既在空間分布上保持一定的關聯,也在對稱性等其他因素的作用下存在互補關系。分子反應一般是以“擴散-靜電作用-波函數作用”這樣的空間順序進行,ESP在靜電作用和分子朝向部分發揮重要作用,自旋密度在波函數作用發揮重要作用,幫助學生建立兩者之間的關系,能極大加深他們對化學反應過程的理解,以及對污染物遷移轉化的理解。
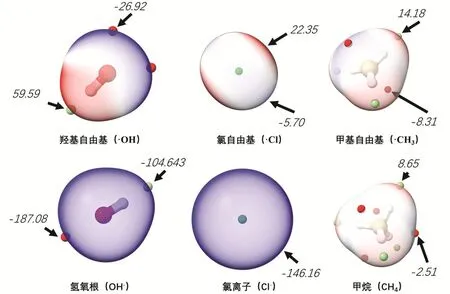
圖5 三種自由基及其共軛閉殼層分子的靜電勢
4 結語
通過與分子軌道等現代化學理論的結合,賦予了環境自由基反應更豐富的內涵并增加了更多可供研究的“手柄”,能從各個方面對反應過程進行解讀、研究乃至操縱。有利于擺脫“乏味的點線式”和“枯燥的講解”,有利于提高“抬頭率”,激發學生的主動學習熱情。本研究的主要結論如下:
1) 通過圖形化量化計算,將化學反應過程中的重要物種運用三維圖形展示,有利于知識的傳遞與接受。
2) 電子自旋密度能夠很好地體現自由基分子上的未成對電子分布情況,其分布結構對自由基分子的靜電勢分布存有一定影響。同時對兩者進行考查能更全面地研究自由基分子的電子結構與反應特點,從而能夠更加深入地對環境過程或環境工程中的自由基反應進行解釋。
3) 在環境化學等“應用化學”專業課程的教學過程中,根據具體的學情,有目的性地回顧基礎化學知識點,主動跳出專業舒適圈,能更好地激發學生的探索欲和挑戰心。
致謝:感謝安徽工程大學化學與環境工程學院計算化學中心提供的硬件支持。

