ICU機械通氣患者感染鮑曼不動桿菌臨床特征及預后分析
陳晨 楊德湘 吳昊 方平
鮑曼不動桿菌(Acinetobacter baumannii,AB)是一種需氧、非發酵的革蘭陰性菌,在自然界中廣泛存在,是醫院感染中常見的不動桿菌屬,也是醫院重癥監護室(Intensive care unit,ICU)感染的主要致病菌之一[1-2]。因抗生素的廣泛應用,AB的耐藥性不斷增加,多重耐藥AB的出現,為臨床治療帶來了極大困難[3]。因此,了解AB感染后的臨床特征,并分析影響其預后的相關因素以制定相應的防治策略,對于控制ICU感染率,改善患者預后有重要意義。本研究選擇2018年1月~2019年12月期間本院ICU有創呼吸機機械通氣的136例患者,統計AB感染情況,分析其臨床特征及預后影響因素,以期為臨床治療提供參考。
資料與方法
一、一般資料
收集2018年1月~2019年12月期間在本院ICU有創呼吸機機械通氣治療患者136例。納入標準:①ICU機械通氣時間>48h;②年齡≥18歲;③至少進行2次病原菌培養及藥敏實驗。排除標準:①入ICU前行機械通氣治療48 h內診斷為肺炎者;②下呼吸道檢出多種致病菌者。
二、 研究方法
1 細菌培養 采取患者下呼吸道深部無菌痰液或肺泡灌洗液標本,使用MicroScan WalkAway plus 96/40全自動微生物鑒定與藥敏分析系統,質控菌株由衛健委臨床檢驗中心提供,藥敏試驗結果參照美國國家臨床試驗室標準化委員會(NCCLS)推薦的標準,同一患者相同部位同一菌株則計數首次分離菌株,參照《中國鮑曼不動桿菌感染診治與防控專家共識解讀》[4],至少2次痰液或肺泡灌洗液標本分離出AB確定為感染,納入感染組,否則為未感染組。
2 資料收集 根據醫院病案信息收集患者的相關資料,包括:性別、年齡、住院時間、是否合并呼吸機相關性肺炎(Ventilator associated pneumonia,VAP)、是否合并感染性休克、是否合并基礎疾病、機械通氣時間、急性生理學與慢性健康狀況評分系統Ⅱ(Acute physiology and chronic health evaluationⅡ,APACHEⅡ)評分、入院前90 d內是否使用抗生素、是否多重耐藥、連用抗生素時間、撤機結果及實驗室檢查指標,包括白細胞計數(White blood cell,WBC)、C-反應蛋白(C-reactive protein,CRP)、降鈣素原(Procalcitonin,PCT)。
3 預后判斷及分組 根據患者住院28 d的預后結局分為生存組與死亡組[5]。
三、 統計學方法
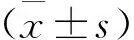
結 果
一、 AB感染情況及臨床特征分析
136例患者中69例發生AB感染,感染率為50.74%。感染組性別、年齡≥60歲、合并感染性休克、合并基礎疾病、APACHEⅡ評分≥15分、入院前90 d內使用抗生素、多重耐藥、深靜脈置管占比與未感染組比較,差異無統計學意義(P>0.05);感染組住院時間≥30 d、連用抗生素時間≥7 d、發生VAP、機械通氣時間≥5 d、撤機失敗占比高于未感染組,差異有統計學意義(P<0.05)(見表1)。
表1 AB感染患者與未感染患者臨床特征對比
二、影響ICU機械通氣AB感染患者預后的相關因素分析
69例AB感染患者中住院28 d內死亡46例,存活23例。死亡組性別、年齡≥60歲、住院時間≥30 d、發生VAP、合并基礎疾病、機械通氣時間≥5 d、入院前90 d內使用抗生素、連用抗生素時間≥7 d占比和實驗室指標中WBC異常、PCT升高占比比較,差異無統計學意義(P>0.05);死亡組合并感染性休克、多重耐藥、CRP升高、APACHEⅡ評分≥15分、撤機失敗、深靜脈置管占比高于生存組,差異有統計學意義(P<0.05)(見表2)。

表2 影響ICU機械通氣AB感染患者預后的相關因素分析
三、Logistic回歸分析影響ICU機械通氣AB感染患者死亡的危險因素
將相關因素分析中有統計學差異的包括:合并感染性休克、多重耐藥、CRP、APACHEⅡ評分、撤機結果、深靜脈置管作為自變量(X),入院后28 d內死亡為因變量(Y),發生入院28 d內死亡記為1,否則記為0進行賦值,納入多因素Logistic回歸分析,結果顯示多重耐藥、合并感染性休克、APACHEⅡ評分≥15分、深靜脈置管是導致死亡的獨立危險因素(P<0.05)(見表3、4)。

表3 變量賦值結果
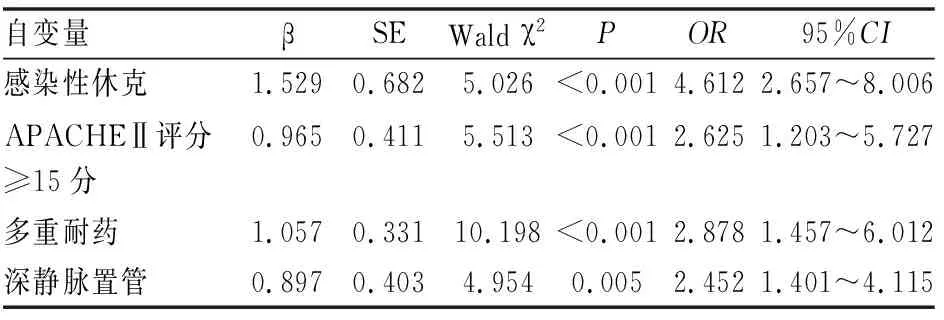
表4 Logistic回歸分析影響ICU機械通氣AB感染患者死亡的危險因素
討 論
2016年中國CHINFT細菌耐藥性監測報告顯示不動桿菌屬占30家醫療機構所有標本的10.76%,其中AB占呼吸道標本分離菌的首位[6]。AB具有能快速定植,存活時間久的特點,是醫院ICU獲得性肺炎的主要致病菌之一[7]。目前認為AB作為條件致病菌,其毒力低于肺炎克雷伯菌及大腸桿菌等其他條件致病菌,因此盲目地對分離出AB的患者進行抗感染治療,會導致抗生素的不合理應用及醫療資源的浪費[8]。故了解ICU機械通氣患者AB感染的臨床特征及預后影響因素意義重大。
本研究中統計136例ICU機械通氣患者AB感染率為50.74%,說明本院ICU機械通氣患者AB感染率較高,應引起重視。此外對136例患者中AB感染組與未感染組的臨床特征進行分析,發現感染組住院時間≥30 d、發生VAP、機械通氣時間≥5 d、連用抗生素時間≥7 d、撤機失敗占比高于未感染組,說明AB感染能加重患者病情,增加合并VAP及撤機失敗風險,延長患者的治療時間,增加了醫患雙方負擔。因AB對生存條件需求低,在醫院環境中易于定植,且ICU機械通氣患者多病情嚴重,機械通氣時間長,是AB的易感人群,極易引發VAP[8-9]。此外因多重耐藥AB的出現,導致抗生素藥物治療方案選擇有限,易出現撤機困難、住院時間延長等情況[10]。國外研究發現[11-12],AB是導致ICU患者VAP的常見耐藥革蘭陰性菌,且是延長患者住院時間、增加病死率的重要原因。
本研究中對AB感染患者的預后影響因素進行分析,發現死亡組合并感染性休克、多重耐藥、CRP升高、APACHEⅡ評分≥15分、撤機失敗、深靜脈置管占比高于生存組,經Logistic回歸分析結果顯示多重耐藥、合并感染性休克、APACHEⅡ評分≥15分、深靜脈置管,是導致死亡的危險因素。多重耐藥AB除對多粘菌素類和替加環素類藥物敏感外,對其他類抗菌藥物幾乎都耐藥,因此ICU機械通氣患者一旦出現多重耐藥則治療難度大,死亡風險高[8]。Salehi等[13]研究表明,多重耐藥AB引起的VAP較廣譜產β內酰胺酶肺炎克雷伯菌引起的VAP治療難度更大,其病死率更高。感染性休克多是由革蘭陰性菌感染引起的嚴重感染,具有急性發作、進展迅速的特點,可引起多個器官功能衰竭,大大增加了患者的死亡風險[14]。謝和賓等[15]研究顯示,休克是導致AB感染患者死亡的重要原因。APACHEⅡ評分是廣泛用于多種危重患者預后評估的評分系統,能較全面反映危重患者的預后情況。研究顯示[16],APACHEⅡ評分以15分為分界值,≥15分患者病情嚴重、預后差、病死率高。深靜脈置管雖然是各種危急重癥患者長期進行監測用藥、抽血、化驗等情況時的有效手段,但作為有創性的侵入性操作,可破壞機體的防御功能,增加ICU患者感染AB風險,預后較差[17]。因此對于ICU機械通氣AB感染患者,存在多重耐藥、合并感染性休克、APACHEⅡ評分≥15分、深靜脈置管等情況時應加強病情監測,及時進行應對搶救處理,以降低患者死亡率,改善預后。
綜上所述,ICU機械通氣患者的AB感染率較高,且AB感染后合并VAP、撤機失敗風險增加,治療難度增大。多重耐藥、合并感染性休克、APACHEⅡ評分≥15分、深靜脈置管是AB感染患者預后不良的危險因素。對于ICU機械通氣患者應識別上述危險因素,加強針對性干預以改善預后。

