4-硝基-1-萘基-β-D-半乳糖苷的合成研究
黨濟政 易 莉
1.重慶醫科大學附屬大學城醫院藥學部,重慶 401331;2.重慶市萬州中心血站檢驗科,重慶 404000
糖作為三大營養物質之一在人體中承擔著非常重要的角色,而很多糖苷類化合物具有特殊的生物活性,如抗菌性、抗病毒和抗腫瘤活性[1]。β-半乳糖苷酶是指一類水解含半乳糖苷鍵物質的酶類,現今該酶在生物技術領域如基因工程、酶工程、蛋白質工程等方面也都發揮著重要作用,并開始廣泛應用于醫藥等領域。β-半乳糖苷類化合物是β-半乳糖苷酶水解的底物,通過該酶-底物水解反應過程可測定酶活性,并可將其廣泛用于篩選酶抑制劑類藥物、測定血清酶及免疫分析標記酶、監測特殊毒害性酶抑制劑等[2]。
4-硝基萘酚、4-硝基苯酚等化合物因在410 nm左右有較強的紫外吸收經常被選擇作為顯色團。本文初步選擇4-硝基-1-萘基-β-D-半乳糖苷作為β-半乳糖苷酶的顯色底物,該底物用于β-半乳糖苷酶活性測定等有著廣泛的應用前景,因而4-硝基-1-萘基-β-D-半乳糖苷的合成也具有重要的意義[3]。
糖苷類化合物中含有較多羥基和縮醛結構,一般合成過程都較為復雜,且產物中存在α 與β 異構體,而如何高效地得到單一構型的產物一直是糖苷合成中的重點,現常用的糖苷合成方法如磷酸酯糖供體法、三氯乙酰亞胺酯法等操作過程較復雜,對實驗設備要求高且得到的產物選擇性不高。本文路線設計先將所有羥基酰化保護即以D-半乳糖為起始原料與乙酸鈉反應,通過高溫回流乙酰化得到高度選擇性β-D-半乳糖五乙酸酯。β-D-半乳糖五乙酸酯經過溴化氫溴代、4-硝基-1-萘酚取代、甲醇鈉去乙酰化最后重結晶得到目標化合物4-硝基-1-萘基-β-D-半乳糖苷,合成路線見圖1,與常用的方法相比,本研究的合成方法反應條件溫和,操作簡便可行且產物選擇性高,是具有應用價值潛力的合成方法路線。因此該研究為β-半乳糖苷酶-底物水解反應測定酶活性及之后的應用奠定了重要基礎。
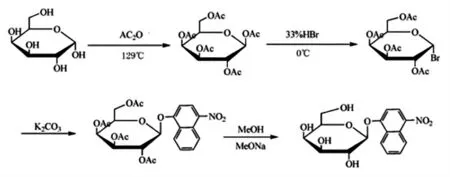
圖1 4-硝基-1-萘基-β-D-半乳糖苷的合成路線
1 儀器與試劑
1.1 儀器
BS210S 型電子天平(德國賽多利斯公司);恒奧德HWC-RDY-1B 熔點儀(北京恒奧德儀器儀表有限公司);Bruker-AV-500 型核磁共振儀(瑞士Bruker 公司);MicrOTOF QII 高分辨質譜(德國Bruker 公司);旋轉蒸發器RE-52(上海青浦瀘西儀器廠);85-2型恒溫磁力攪拌器(上海司樂儀器廠);電熱恒溫水浴鍋(鄭州長城科工貿有限公司);SHZ-D(Ⅲ)循環水真空泵(河南鞏義市英峪予華儀器廠);超純水生成儀(美國Elix MILLIPOER)。
1.2 試劑
4-硝基-1-萘酚(Alfa Aesar,純度≥98%,批號:10218521);D-半乳糖、N-溴代琥珀酰亞胺(上海晶純實業有限公司,純度≥98%);液溴、磷(國藥集團化學試劑,化學純);無水乙酸鈉、乙酸酐、乙醇、二氯甲烷、碳酸氫鈉、無水硫酸鈉、無水碳酸鉀、甲醇鈉(重慶川東化工基團有限公司,分析純);溴化氫溶液、乙醚、石油醚、丙酮、甲醇(成都市科龍化工試劑廠,分析純)。
2 方法與結果
2.1 β-D-半乳糖五乙酸酯的合成
將5.0 g(27.8 mmol)D-半乳糖,4.6 g(55.6 mmol)無水乙酸鈉放入100 ml 單口燒瓶。室溫下加24 ml乙酸酐并攪拌溶解,加熱至130℃回流3 h。另取一燒瓶加入200 ml 蒸餾水冷卻至10℃后將反應液緩慢倒入,冰浴下攪拌2 h,靜置待反應液分層后分離上下層,棄去上清液,下層褐色液體加100 ml 水攪拌1 h,褐色固體逐漸析出。減壓抽濾,并用少量水洗,用乙醇重結晶,得白色固體7.8 g。經測定熔點145℃,為產物β-D-半乳糖五乙酸酯[4]。
2.2 溴代半乳糖四乙酸酯的合成
取“2.1”項下所得的β-D-半乳糖五乙酸酯2 g(5.1 mmol)溶于7 ml 乙酸置于100 ml 單口燒瓶中并攪拌溶解,冰浴條件下待燒瓶內溫約10℃時將33%溴化氫的乙酸溶液2 ml 緩慢滴加,反應2 h。向燒瓶內加入二氯甲烷50 ml,用飽和碳酸氫鈉溶液洗至中性,在用水洗2 次,有機層無水硫酸鈉干燥1 h 后抽濾,濾液減壓蒸餾得到褐色固體,該產物用乙醚-石油醚(1∶2)重結晶,得白色固體1.2 g。熔點80℃,為產物溴代半乳糖四乙酸酯[5-6]。
2.3 4-硝基-1-萘基-β-D-半乳糖四乙酸酯的合成
取“2.2”項下所得的溴代半乳糖四乙酸酯0.23 g(0.56 mmol)加入50 ml 單口燒瓶中,之后依次加入4-硝基-1-萘酚0.11 g(0.58 mmol)無水碳酸鉀0.08 g,丙酮5 ml,攪拌下58℃回流5 h,反應完后冷卻至室溫,減壓蒸餾,剩余殘渣用二氯甲烷溶解,少量飽和碳酸氫鈉溶液洗有機相,有機層無水硫酸鈉干燥1 h 后抽濾,濾液減壓蒸餾,得褐色油狀物0.17 g,為產物4-硝基-1-萘基-β-D-半乳糖四乙酸酯[7-8]。
2.4 4-硝基-1-萘基-β-D-半乳糖苷的合成
取“2.3”項下所得的4-硝基-1-萘基-β-D-半乳糖四乙酸酯0.56 g(1.08 mmol)溶于3 ml 甲醇,加入催化量(200 μl)的1 mol/L 的甲醇鈉的甲醇溶液,室溫攪拌30 min,靜置反應液于0~5℃約8 h,固體析出,抽濾得到濾餅用甲醇/水(3:1)重結晶,得黃色固體0.19 g,為終產物4-硝基-1-萘基-β-D-半乳糖苷[9-10]。
2.5 結構表征
采用核磁共振(1H-NMR、13C-NMR)和高分辨質譜(ESI-HRMS)對終產物4-硝基-1-萘基-β-D-半乳糖苷進行結構表征。
核磁共振1H-NMR(Brucker Avance 500 MHz)數據見下圖2、表1。

圖2 4-硝基-1-萘基-β-D-半乳糖苷核磁共振(1H-NMR)結構表征

表1 4-硝基-1-萘基-β-D-半乳糖苷核磁共振(1H-NMR)解析數據
根據C1 位置氫和C2 位置氫的耦合常數判斷絕對構型是糖苷構型確認的常用方法[11]。β 構型的半乳糖苷其C1 位氫和C2 位氫之間的角接近180°,J1,2耦合常數較大,常在7~8。而α 構型其二面角接近60°,J12 耦合常數常在2~4。本研究合成的半乳糖苷核磁共振(1H-NMR)C1 位氫(e)和C2 位氫(d)之間的J1,2 為7.5,說明該化合物為β 構型。
核磁共振13C-NMR(DMSO,BruckerAvance500MHz)數據見下圖3、表2。

圖3 4-硝基-1-萘基-β-D-半乳糖苷核磁共振(13C-NMR)結構表征

表2 4-硝基-1-萘基-β-D-半乳糖苷(13C-NMR)解析數據
高分辨質譜結果顯示,4-硝基-1-萘基-β-D-半乳糖苷計算質荷比[M+Na]+為374.0846,實測結果為374.0848。測定結果支持該終產物即為化合物4-硝基-1-萘基-β-D-半乳糖苷。
2.6 反應條件的優化與關鍵試劑的選擇
因為糖苷產物存在α 與β 兩個異構體,而乙酰化反應條件較難控制,溴代反應產物不穩定。為了得到單一的β 構型終產物,故對乙酰化和溴代的反應條件進行了優化。
2.6.1 乙酰化反應條件的選擇 D-半乳糖的乙酰化會因反應溫度影響而產生不同構型的異構體,α-D-半乳糖五乙酸酯熔點90~95℃與β-D-半乳糖五乙酸酯熔點140~145℃差異較大。而原料D-半乳糖的熔點為165~168℃,兩種異構體產物熔點均低于原料D-半乳糖。若反應生成了α 異構體,則產物會在90℃左右開始熔融,若反應全生成了β 構型異構體則產物會在140℃開始熔融。故原料是否反應完全即產物中是否存在原料不影響是否生成α 異構體的判斷。據此以產物熔點測定觀察其熔融時的溫度以確定其中是否存在α 異構體。現固定D-半乳糖和乙酸鈉的投料比,以不同的反應溫度和時間為影響因素,以D-半乳糖的消耗和是否產生α 構型產物為監測指標,用薄層色譜法(thin layer chromatography,TLC),以展開劑丙酮/石油醚(3∶10)監控反應中原料D-半乳糖是否反應完全,以熔點儀測定產物初始熔融溫度判斷是否產生了α 異構體。對乙酰化反應條件進行優化(表3)。

表3 酰化反應結果
在溫度低于100℃時不論是延長反應時間還是增加反應溫度,原料D-半乳糖均無法完全反應且產物中始終存在α 構型產物,當溫度為100℃時,反應1 h仍存在原料,將反應時間延長至3 h 后監控反應原料消失反應完全,但后處理之后用產物測定熔點后發現存在α 構型異構體。后將反應溫度增加至130℃回流后反應1 hTLC 監控仍然存在原料,延長反應時間至3 hTLC 監控反應完全,再將后處理得到的產物測定熔點發現其在141℃才開始熔融,說明沒有產生α 異構體。綜合考慮后,將反應條件設定為回流溫度130℃,反應時間為3 h,即為上文“2.1”項中的反應條件。
2.6.2 溴代試劑的選擇 在乙酰鹵代糖中鹵原子具有良好的離去性,使糖基有足夠活性可與醇羥基或酚羥基發生取代反應。也因此鹵代糖的穩定性較低。而在氟與氯溴相比,以氟代糖的離去性最低,穩定性最好。在和4-硝基-1-萘酚的取代反應中,因與酚羥基發生反應故應選擇活性較高的鹵代糖,本文選擇了活性與穩定性均較好的溴代糖基作為中間體。選擇較常用的三種溴代方法對β-D-半乳糖五乙酸酯進行溴代反應實驗,反應條件參數見表4,實驗具體操作參考文獻[8,12-14],根據實驗可操作性、經濟性和收率綜合考慮選擇了最適合的溴代方法,收率=B/A×100%。

表4 不同溴代法反應條件參數及收率
三種溴代方法中,液溴-磷溴化收率最高,但液溴有較強的毒性與腐蝕性會揮發出有強烈刺激性的煙霧,刺激眼睛和呼吸道的黏膜,對實驗保護要求很高,且該方法產生雜質較多,分離難度大。N-溴代琥珀酰亞胺溴代收率較低,且原料N-溴代琥珀酰亞胺價格較高。溴化氫的乙酸溶液作溴代法反應條件溫和且收率較高。綜合考慮成本與實驗可操作性選擇溴化氫的乙酸溶液作為溴代試劑。
3 討論
本研究以D-半乳糖為原料,與乙酸鈉反應,酯化后得到β-D-半乳糖五乙酸酯。β-D-半乳糖五乙酸酯經過溴化氫溴代、4-硝基-1-萘酚取代、最終水解除去乙酰基,再重結晶得到目標化合物4-硝基-1-萘基-β-D-半乳糖苷。經核磁共振(1H-NMR、13C-NMR)和高分辨質譜(ESI-HRMS)確定了最終產物的結構。為了得到單一β 構型的產物,對關鍵節點乙酰化反應條件進行了優化。從實驗結果可推斷出反應溫度是產生不同構型產物的最關鍵因素,并根據原料與兩個不同構型產物的熔點差異定性監控是否產生α 異構體,與現今常用的高效液相色譜監控異構體方法相比更加簡單易行。考慮到溴代糖的穩定性較低,在對最常用的三種方法進行篩選時除考慮原材料成本、收率和產生的雜質之外,還需要考慮到后處理過程對產物的影響。而用溴化氫乙酸溶液進行溴代反應不僅成本低條件溫和,而且后處理簡單便捷,更加適合糖類化合物的溴代。
酶聯免疫吸附測定是利用抗原抗體特異性結合進行免疫反應的定性和定量檢測方法,是目前最常用、最經典的免疫學測定方法。而堿性磷酸酶和β-半乳糖苷酶是酶聯免疫吸附測定中最常用的酶。本文中合成的4-硝基-1-萘基-β-D-半乳糖苷是β-半乳糖苷酶的底物。在該底物的應用研究中,當PH 在5.5~7.6 時4-硝基-1-萘酚在450 nm 的吸收是對硝基苯酚的2.1 倍,是鄰硝基苯酚的9.6 倍[15]。而作為顯色底物4-硝基-1-萘基-β-D-半乳糖苷在弱酸性或者中性條件下對應的水解酶活性高于現酶聯免疫吸附測定常用的顯色底物[16-17]。這使得本研究合成的顯色底物4-硝基-1-萘基-β-D-半乳糖苷有著較廣闊的應用前景和推廣價值。
綜上所述,本研究成功合成了β-半乳糖苷酶的顯色底物4-硝基-1-萘基-β-D-半乳糖苷。反應條件溫和,操作簡單,原料廉價易得。為β-半乳糖苷酶-底物水解反應測定酶活性及之后的應用奠定了重要基礎。

