基于項目學習的“探秘乙醇”單元復習課
周玲玲

摘要:“探秘乙醇”單元復習課,運用項目學習的方式進行“認識化學變化”單元復習,學生通過認識乙醇的用途、探究乙醇的組成、感悟乙醇的來源等三個任務驅動提升了興趣和核心素養,建立了知識和思維模型,實現了個性發展。
關鍵詞:認識化學變化;項目學習;核心素養;思維模型;個性發展
文章編號:1008-0546(2022)03x-0067-03??? 中圖分類號:G632.41??? 文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2022.03x.016
一、項目主題的確立
“認識化學變化”是滬教版初中化學第四章的內容,該章節以質量守恒定律為主線,包含了燃燒與滅火、爆炸、質量守恒定律的實質與應用、化學方程式的書寫等瑣碎知識點,學生學習完新課后,知識在大腦中處于碎片化的狀態。“探秘乙醇”圍繞乙醇的用途、組成、來源等對第四章內容進行復習,既能幫助學生梳理知識、又能加深學生對化學變化和質量守恒定律定義的理解、提升運用能力,同時培養學生多角度分析問題、解決問題、遷移應用的能力和意識。
新課標指出,復習不是將知識進行簡單的羅列,而是通過真實情境對學生的知識和能力進行診斷、查缺補漏、重新整合,提升學生知識運用能力、思維能力,培養學生的化學核心素養[1]。著名教育家蘇霍姆林斯基曾說過:“如果教師不想方設法使學生進人情緒高昂和智力振奮的內心狀態,就急于傳授知識,那么,這種知識只能使人產生冷漠的態度,而不動情的腦力勞動就會帶來疲倦”[2]。項目式學習能使學生處于高昂的學習狀態中,引導學生在真實情境中分解任務、在實驗探究、小組活動中完成任務,在任務中學習、在學習中反思、在反思中提升[3,4]。利用項目式學習的方式來復習第四章內容,在鞏基、強技、提升能力的基礎上,感受微粒觀、變化觀、守恒觀等化學觀念。
二、項目任務及教學流程
項目式學習是一種以學習者為中心,真實情境為前提、挑戰性任務為驅動、科學探究為路徑的學習方式,在團隊合作中,活化知識,解決問題,建構模型,提升素養。具體流程見圖1:
三、項目實施過程
任務1認識酒精的用途
導人:現在正值新冠肺炎時期,大家防毒消毒意識也逐步增強,酒精溶液是大家首選的消毒用品。酒精(又叫乙醇)還有哪些用途呢?
學生:課前查閱資料,做成PPT,課堂分享。學生總結出酒精溶液的用途有:消毒用品(乙醇濃度不同,消毒效果不同,適用的范圍不同)、飲料制品、有機溶劑(生物學中的用途:葉綠體中的色素能溶在有機溶劑無水乙醇中)、燃料。
教師:保存、使用酒精消毒時,有哪些注意事項呢?
學生:根據已有的知識儲備,總結出酒精密封、低溫保存,遠離火種,消毒時不能噴灑。
教師:利用自制裝置演示酒精爆炸實驗。
學生:觀察現象,回顧燃燒的條件,分析爆炸的原因,為正確使用酒精提供理論指導。
教師:由于酒精使用不當,造成火災,應如何滅火?
學生:回顧滅火的原理,小組總結滅火的方法,同時體會滅火方式要根據環境選擇。
設計意圖:項目式學習背景下的單元復習不同于傳統的復習方式,是引導學生利用所學知識處理項目中的子任務,在任務驅動中加強跨學科和深度學習能力,使問題解決思路、核心知識、認識發展三線融合。本環節從生活出發、引出生物、化學、科學等學科知識、再回歸到生活實踐,學生在查閱資料、做PPT的過程中,對燃燒、爆炸、滅火的知識進行串聯和并聯,使學生在學習過程中將知識進行有機融合,得到持續發展。
任務2探究酒精的組成
教師:如何確定酒精(乙醇)的組成呢?
學生:根據學習經驗,小組討論總結出通過檢測燃燒產物、根據元素守恒即可確定酒精的元素組成。同時選擇干冷的燒杯和澄清石灰水分別檢測產物中有水和二氧化碳,確定酒精中一定有氫元素和碳元素,但是是否有氧元素有待繼續探究。
教師:如何用定量方法測定乙醇中是否含有氧元素呢?
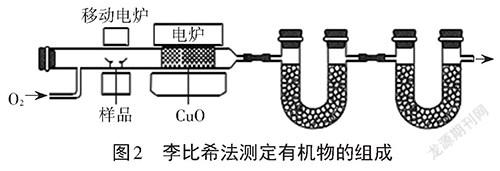
學生:能夠講出利用李比希法測定乙醇中是否含有氧元素的思路(見圖2)。
資料:氯化鈣具有強烈的吸水性,但不吸收二氧化碳;堿石灰可以吸收水,也可以吸收二氧化碳。
教師:兩支U形管中分別放什么物質?
學生:小組討論,在稱量水的質量時,為了防止二氧化碳的干擾,第一支U形管中放置氯化鈣,第二支U形管中放置堿石灰。
教師:4.6g的乙醇完全燃燒的產物依次通入氯化鈣和堿石灰中,盛有氯化鈣的U形管增重5.4g,盛有堿石灰的U形管增重8.8g,請通過計算確定乙醇的組成中是否含有氧元素。
學生:根據元素守恒進行計算,得出乙醇中含有氧元素。小組間的同學對于板演同學的思路和書寫格式進行評價。
教師:Mr(乙醇)=46,你能求出乙醇的化學式嗎?
學生:根據碳、氫、氧元素的質量求出碳、氫、氧原子的個數比,確定乙醇的化學式。
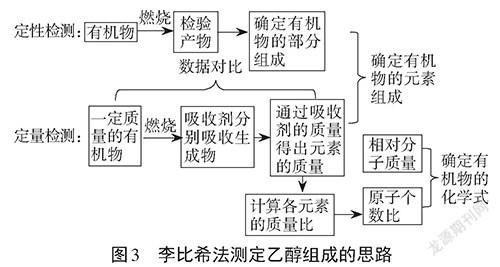
師生:小結測定物質組成的思維模型(見圖3)。
教師:測定乙醇的組成利用了乙醇燃燒這一化學變化,請用化學方程式表示這一過程?
學生:書寫乙醇燃燒的化學方程式。
設計意圖:本環節利用乙醇的組成這一任務引發學生思考,小組討論、理論分析、定性檢測、定量計算、得出乙醇的組成和化學式。整個過程符合學生的認知規律,利用物質變化過程,得到物質的宏觀組成,體驗了探究過程,感受了質量守恒定律的應用,建立了測定物質組成的思維模型。此過程使學生認識到科學探究的過程不是一蹴而就的,也不是隨意而行的,學習也要嚴謹、厚積薄發。
任務3感悟乙醇的來源
教師:乙醇的來源有哪些呢?
學生:脫口而出糧食釀酒。
教師:播放米酒釀制的視頻,講解糯米中含有淀粉,在酒曲酶的作用下水解生成葡萄糖,葡萄糖通過進一步變化生成乙醇。引導學生利用化學方程式表示這一過程。
學生:觀看視頻,得出釀酒的原材料和過程,同時觀察到有氣泡冒出。利用化學方程式表示淀粉轉化為乙醇的過程時,發現化學方程式配不平,小組討論,米酒釀制過程中產生的氣泡不是空氣,而是生成物;根據元素守恒,初步猜測氣泡的成分是二氧化碳或氧氣。
學生:小組自選儀器和試劑證明產生的氣體是二氧化碳,然后將化學方程式補充完整。
教師:變化是守恒的,變化是永恒的。同時,詳細講述工業制乙醇的方法,煤可以制取大量的乙醇,為緩解能源危機和溫室效應,研究發現二氧化碳和氫氣反應也能制取乙醇。
資料:展示二氧化碳、氫氣、水、乙醇的微觀構成。
學生:用小磁扣在白板上表示出二氧化碳和氫氣制取乙醇的過程。從微觀層面解釋質量守恒定律和化學變化的過程是分子分解成原子,原子重新結合生成新的分子。
教師:欲得到4.6t高附加值的液體燃料一乙醇,能減排多少二氧化碳?
學生:根據化學方程式計算,得出二氧化碳的質量。
設計意圖:本環節進行了兩次探究過程,第一次在用化學用語表示乙醇的變化過程時,利用質量守恒定律探究了氣體的成分,加深了學生證據推理的意識,加深了學生對元素觀和守恒觀的理解。第二次從微觀層面探究了CO制乙醇的過程,同時利用定量思想進行了計算,增強學生環保意識的同時,提升了學生思維。兩次探究過程幫助學生建立了學科觀念,將化學知識從課本應用到生產生活中。
四、項目教學反思
1.項目真實助提興趣
“教育即生活”“為社會生活做準備的唯一方式就是投身于社會生活中”,這是杜威的教育理論。《義務教育化學課程標準(2011版)》和《普通高中化學課程標準(2017版)》也從不同角度闡述了真實情境的重要性。源于真實情境的項目式教學可以激發學生學習動機,化被動為主動,實現教師從講授者和指導者向學習活動的資源提供者、參與者、促進者的轉變。本節課從新冠肺炎的消毒用品乙醇這一社會熱點出發,符合學生的認知思想規律,學生在這一背景下愿意主動去探索乙醇的用途、組成和來源,如主動查閱資料、制作PPT、積極的進行實驗探究等;教師在整個課堂中將主動權交給學生,給學生提供必要的資料和方向引領,有助于學生體驗成功的快樂。
2.任務驅動助構模型
新授課傾向于雙基知識的傳授,學生大腦中的章節知識處于碎片化狀態。單元復習非常有利于學生對化學知識進行意義建構,形成自己的知識樹。因此在單元教學時,教師應有意識地從課時向課程轉變,而項目式教學是實現這一目的的最優選擇之一。項目式教學是將一個主題分解成幾個任務,學生在完成任務的過程中,決策整合、對知識的掌握從點延伸到面,思考問題的方式從一維進階到多維。本節課以新冠疫情為背景,乙醇為主線展開,進行了識用途、探組成、悟來源等三個任務的探究,從定性定量、宏微結合、宏觀表征等方面重新認識了化學變化,從物質變化和能量變化角度感受化學變化的奧妙,為后續學習新的化學變化建立思維模型。
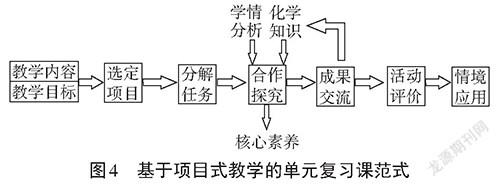
通過任務驅動,幫助學生建立知識和思維模型,有助于學生在解決實際問題時,快速提取知識,為認識事物提供了清晰的思路。建立某一主題的教學模型能夠為其它教師教學工作提供一種教學思路,本節課以“識用途、探組成、悟來源”三個任務為驅動,有效構建了基于項目式教學的單元復習課的范式(如圖4)。
3.小組合作助升素養
新課改背景下的化學教學不僅僅注重知識的獲得,更加強調化學核心素養的發展、知識的學科價值,立德樹人,小組合作是實現這一目標的有效途徑之一。本節課每一環節均設置了同伴互助,如認識乙醇用途、從定性和定量的角度探究乙醇的組成和化學式、米酒釀制過程中氣泡的探究、微觀角度探究二氧化碳制取乙醇的過程等,三任務驅動、四小組合作的難度呈螺旋式上升,學生在不同的任務和活動中體驗了核心素養的不同角度。小組內學生的水平參差不齊,形成差異,學生在差異中交流、在差異中互助、在差異中成長,因此小組內的差異是提升學生核心素養的高階催化劑。
參考文獻
[1]戴素柳.初中化學單元復習教學設計的策略探討——以“化學方程式”單元復習教學設計為例[J].化學教與學,2017(08):48-50,30.
[2] 趙春福.初中化學教學導入環節的設計[J].課程教育研究,2015(02):179.
[3]曹葵,王巧玲.基于提升學生核心素養的項目式學習——以淀粉的改性研究為例[J].化學教與學,2021 (05):43- 45,64.
[4]沈澗宇.基于項目式學習的離子反應教學設計[J].中學化學教學參考,2021(02):52-54.
3148500589275

