地塞米松誘導的人小梁網基因表達譜變化及生物信息學分析
彭 毅,周文君,鄧 軍
0引言
糖皮質激素(glucocorticoid,GC)因其具有有效的抗炎和抗免疫作用而被廣泛應用于各種全身性及眼部疾病,但長期大量使用糖皮質激素可對全身及眼部產生多種副作用。人眼是GC重要的靶器官,局部和全身使用GC都有使眼內壓增高的風險,誘發激素性青光眼(glucocorticoid-induced glaucoma, GIG)[1]。GC通過與糖皮質激素受體(glucocorticoid receptor,GR)結合而發揮其藥物學作用。研究顯示,在原位和體外培養的小梁細胞內均有GR的表達,長期使用GC可導致小梁網超微結構重塑和小梁網功能異常,進而引起房水流出阻力增加,最終導致眼內壓的升高[2-3]。但GC誘發小梁網結構和功能改變的這一生物過程中所涉及的具體致病分子和通路仍不清楚。
隨著高通量基因芯片和測序技術的發展,基于基因表達譜數據的生物信息學分析能高效挖掘、篩選與疾病發生發展相關的重要基因和通路。本研究基于公共基因芯片數據庫(Gene Expression Omnibus,GEO)中的基因表達數據,利用生物信息學方法分析地塞米松誘導的人小梁網基因表達譜變化,篩選其差異表達的基因,找到關鍵致病基因及通路,為GIG的分子機制研究提供新的思路。
1材料和方法
1.1材料數據收集和處理:從美國國立生物技術信息中心(NCBI)平臺下的基因表達綜合數據庫GEO (http://www.ncbi.nlm.gov/geo/)獲取基因表達數據集GSE37474。芯片信息:Affymetrix Human Genome U133 Plus 2.0 Array,平臺是GPL570。該數據集包含5個實驗樣本和5個對照樣本(5對配對供體眼),所有樣本均來自當地眼庫。實驗樣本處理:供體眼的眼前段組織在含有地塞米松的培養液培養10d。對照樣本處理:供體眼的眼前段組織在不含地塞米松的培養液培養10d。10d后小梁網組織被切除下來用于提取RNA。
1.2方法
1.2.1差異表達基因篩選GEO2R (https://www.ncbi.nlm.nih.gov/geo/geo2r/)是一個基于R語言的Web數據分析工具,可對GEO數據集中兩組或多組樣本進行差異表達基因分析。我們利用GEO2R對所選的芯片進行差異表達基因篩選及數據下載,并將探針名稱轉化為標準基因名稱。篩選標準為P<0.05和|log2FC|>1[差異表達倍數(fold change,FC)]。
1.2.2GO功能注釋和KEGG信號通路富集分析將篩選出來的差異表達基因導入DAVID 6.8數據庫(https://david.ncifcrf.gov/),依據GO(Gene Ontology)數據庫,以人源基因為背景,對差異表達基因進行生物學功能注釋。并利用KEGG(Kyoto Encyclopedia of Genes and Genomes)通路數據庫進行信號通路的富集,尋找差異表達基因所富集的信號通路。
1.2.3蛋白相互作用網絡構建及關鍵樞紐基因的篩選通過STRING 10.5數據庫(http://string-db.org/),以互作評分combination score>0.4為條件構建差異表達基因蛋白質相互作用網絡(protein-protein interaction,PPI),然后將數據導入Cytoscape軟件,利用Cytoscape軟件中的CytoHubba插件進行拓撲學分析,計算邊緣滲透組件(edge percolated component,EPC) ,度值(Degree) 和最大鄰域組件(maximum neighborhood component,MNC)以篩選出PPI網絡中的重要節點,并根據節點度大小進行排序。最后,對EPC、Degree 和MNC分別篩選出的前10個重要節點取交集得出本研究的關鍵樞紐基因。
1.2.4關鍵樞紐基因RT-PCR驗證人小梁網細胞購于上海拜力生物公司,小梁網細胞分為兩組:實驗組用含100 nmol/L地塞米松的DMEM培養基培養10d,對照組用不含地塞米松的DMEM培養液培養10d。用Trizol提取細胞RNA,Nanodrop測RNA濃度,使用Prime Script RT試劑盒合成cDNA,用SYBR Green Master Mix試劑盒對篩選出來的關鍵樞紐基因的表達量進行RT-PCR檢測驗證。使用ΔΔCt方法計算mRNA的相對表達量。
2結果
2.1地塞米松處理的小梁網組織和正常小梁網組織之間的差異表達基因本研究選擇的基因表達譜芯片GSE37474包括5對配對樣本,地塞米松處理的小梁網組織的5個樣本為實驗組,無地塞米松處理的小梁網組織的5個樣本為對照組。以P<0.05和|log2FC|>1作為標準篩選差異表達基因。與正常小梁網組織相比,地塞米松處理的小梁網組織有252個基因存在差異表達,其中141個為上調基因,111個為下調基因,見火山圖(圖1A)和差異基因聚類熱圖(圖1B)。

圖1 地塞米松處理的小梁網組織和正常小梁網組織之間的差異表達基因圖 A:基因火山圖;B:聚類熱圖。
2.2差異表達基因GO功能注釋和KEGG信號通路富集分析252個差異表達基因GO功能注釋結果顯示(圖2A), 差異表達基因主要定位于細胞外基質、細胞外區域、細胞外泌體、肌原纖維Z盤、細胞基底膜和細胞表面等細胞成分( cell component,CC);主要參與炎癥的正調控和細胞外基質重塑等生物學過程( biological processes,BP);主要參與細胞因子活性、肝素結合和生長因子活性等分子功能( molecular function,MF)。KEGG信號通路富集分析結果顯示(圖2B),差異表達基因主要參與血管平滑肌收縮、花生四烯酸代謝、醚脂質代謝和癌癥膽堿代謝等相關信號通路。
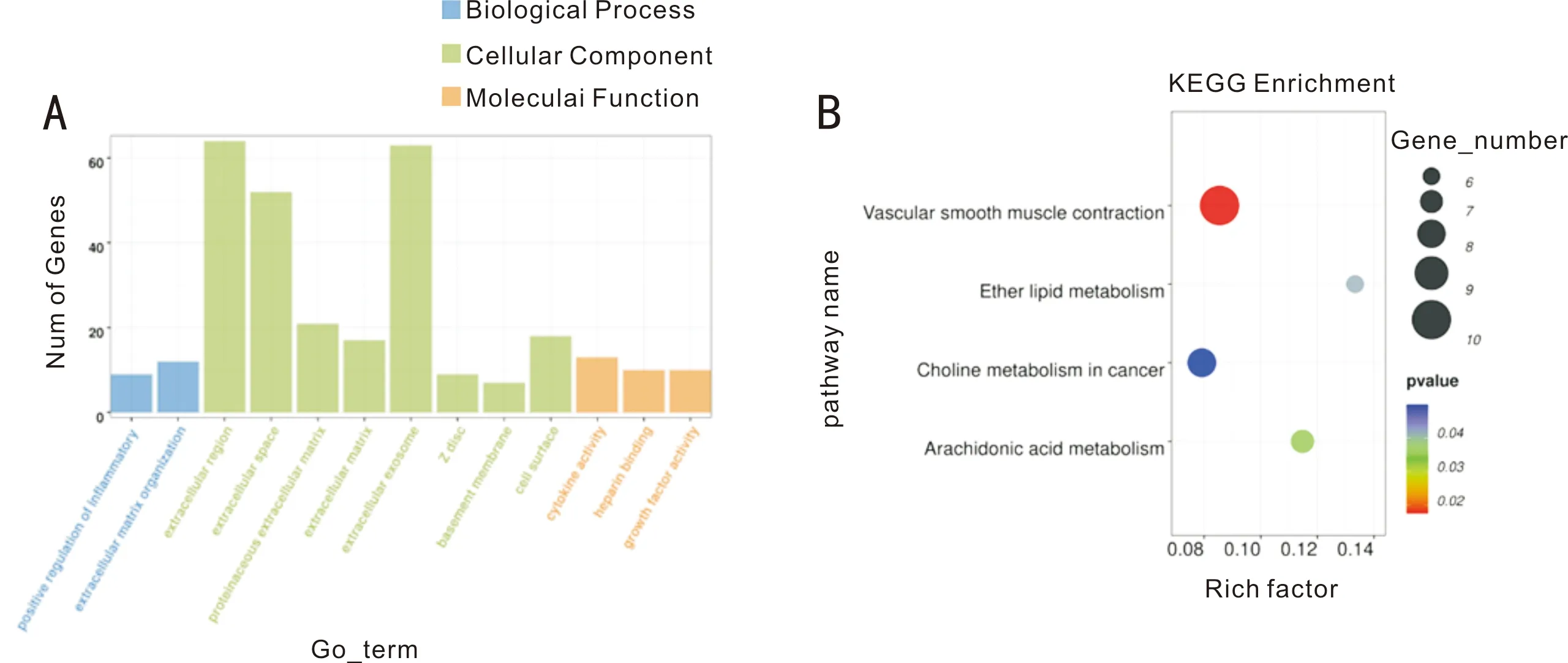
圖2 差異表達基因GO功能注釋和KEGG信號通路富集分析 A:差異表達基因的GO 功能注釋;B:KEGG 通路功能富集分析。
2.3PPI網絡的構建及關鍵樞紐基因的篩選用STRING 10.5數據庫和Cytoscape構建差異表達的基因之間蛋白質相互作用網絡。去除游離的蛋白影響后,得到了由179個節點,443條邊構成的網絡(圖3A)。用Cytoscape 軟件中的CytoHubba插件對網絡進行分析,基于EPC(邊緣滲透組件)、Degree(度)和MNC(最大鄰域組件)三種拓撲算法分別探索PPI網絡中的前10個重要節點(圖3B、C、D和表1)。將上述三種算法所獲得結果取交集,得出7個重疊差異表達基因,即關鍵樞紐基因,其中包括3個上調基因EDN1、FOS、LPL和4個下調基因CCL2、IGF1、PTGS2、CCL5(圖4和表2)。
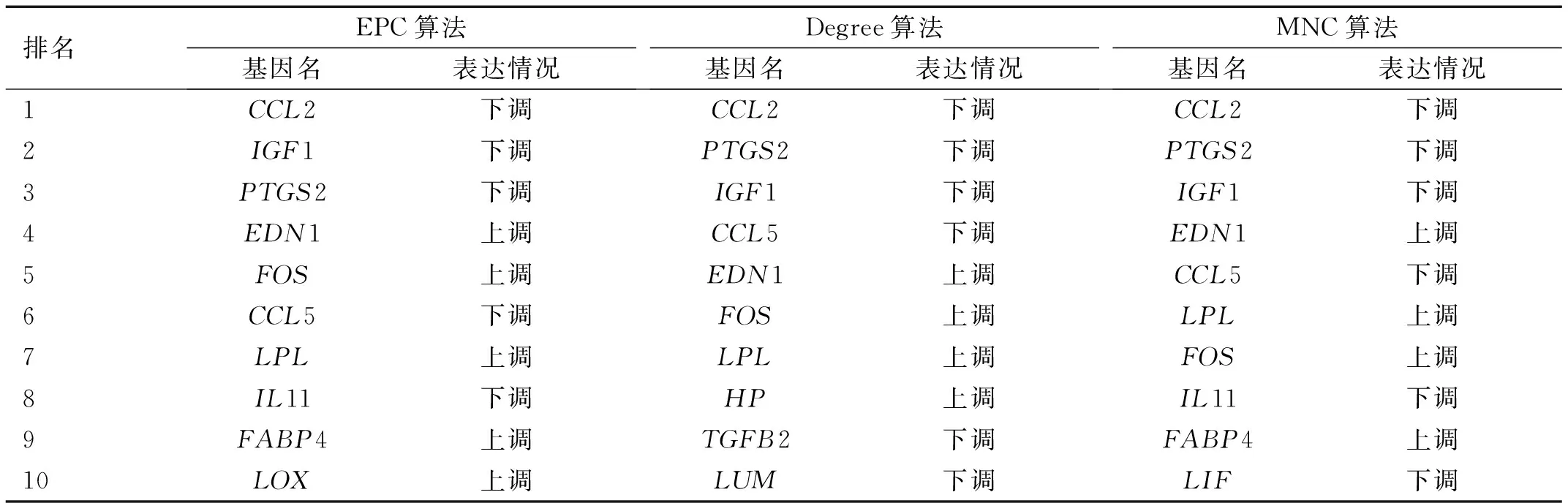
表1 基于EPC和Degree及MNC算法分別得出的前10名基因

圖3 差異表達基因的PPI網絡及關鍵樞紐基因的篩選(紅色代表上調基因,綠色代表下調基因) A:差異表達基因構建的PPI網絡;B:EPC算法中排名前10名的基因;C:Degree算法中排名前10名的基因;D:MNC算法中排名前10名的基因。

表2 基于EPC和Degree及MNC算法中前10名基因的交集
2.4關鍵樞紐基因RT-PCR驗證對篩選出來的7個關鍵樞紐基因(CCL2、IGF1、PTGS2、EDN1、FOS、CCL5、LPL)進行RT-PCR驗證(相關引物見表3)。相比正常小梁網組織,地塞米松處理的小梁網細胞中CCL2(P=0.006),IGF1(P=0.001),PTGS2(P=0.003)和CCL5(P=0.017)的mRNA表達量下降,而EDN1 (P=0.018),FOS(P=0.004)和LPL(P=0.023)的mRNA表達量上升,結果和基因表達譜芯片一致(圖5)。

表3 關鍵樞紐基因RT-PCR引物序列
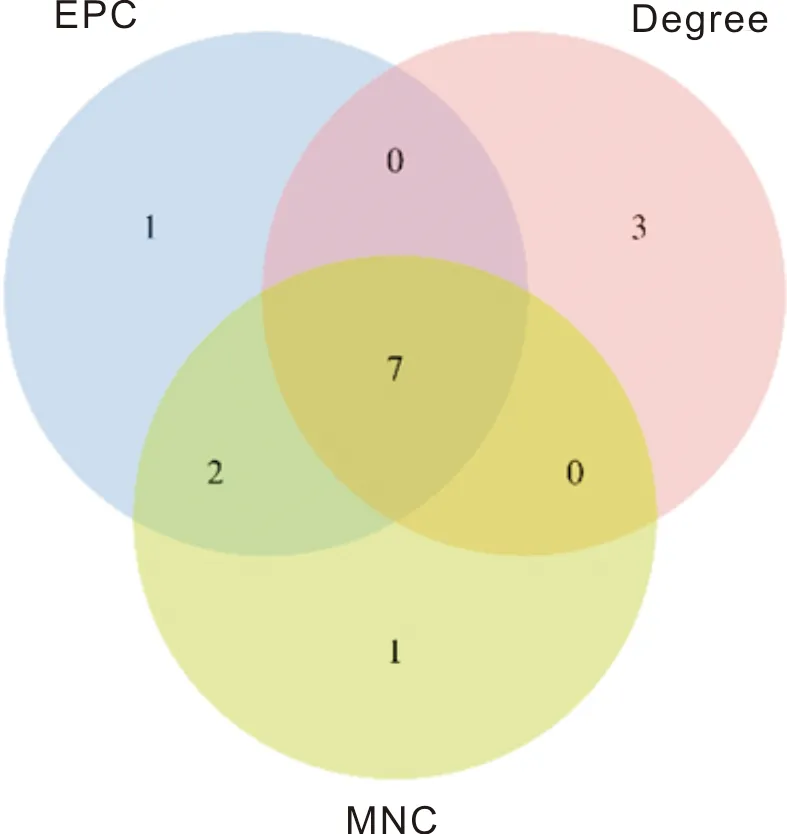
圖4 EPC和Degree及MNC算法中前10名基因交集的韋恩圖。

圖5 關鍵樞紐基因的RT-PCR驗證 aP<0.05, bP<0.01 vs 正常小梁網組織。
3討論
GIG的發病機制被認為和開角型青光眼相似,但其具體發病機制目前仍不清楚,目前認為可能與GC引起的小梁網細胞外基質重塑有關[4-6]。GO功能注釋結果提示,地塞米松引起的小梁網組織差異基因主要位于細胞外區域,參與細胞外基質重塑。這一結果表明,GC引起的小梁網變化主要發生在細胞外基質。KEGG通路分析顯示差異基因主要參與血管平滑肌收縮、花生四烯酸代謝、醚脂質代謝和癌癥膽堿代謝等相關信號通路。血管平滑肌細胞上存在GC受體,GC可誘導上調血管平滑肌細胞表達去甲腎上腺素和血管緊張素Ⅱ受體,引起血管收縮,使外周阻力增加,被認為是GC誘發高血壓的機制之一[7-9]。但目前尚無文獻報道GC引起的血管收縮是否在GIG的發病中起作用。KEGG分析提示差異基因還富集在脂質代謝過程,包括花生四烯酸代謝和醚脂質代謝,提示脂質代謝可能參與了GIG的發病。國外研究發現血脂水平升高和眼壓水平增高呈正相關,且長期服用他汀類藥物可以降低眼壓[10-11]。國內亦有研究報道,血總膽固醇水平與原發性開角型青光眼和眼壓具有相關性[12]。脂質代謝中花生四烯酸代謝和醚脂質代謝參與GIG發病的具體機制仍需進一步研究。另外,在開角型青光眼患者的房水中二酰基甘油磷酸膽堿和酰基甘油磷酸膽堿水平升高[13]。Leruez等[14]亦報道相對于正常人,開角型青光眼患者血漿中磷脂酰膽堿水平升高。結合KEGG通路富集結果,提示異常的膽堿代謝可能在GIG的病理生理學中起重要作用。
在最終確定的7個關鍵樞紐基因中,趨化因子(C-C基序)配體2(C-C motif chemokine ligand 2,CCL2)在三種算法中都顯示出最高的相關程度(得分最高),且在地塞米松處理組表達下調。CCL2也被稱為單核細胞趨化蛋白1(monocyte chemotactic protein-1,MCP-1),是促炎因子之一,可被內皮細胞,成纖維細胞和單核細胞等多種細胞分泌。正常的小梁網狀內皮細胞在沒有刺激的情況下會分泌大量的CCL2[15]。有研究表明,CCL2可通過改變Schlemm管內皮細胞間的接觸來增加房水流出,從而降低眼壓[16]。然而有研究報道,在開角型青光眼患者的房水中CCL2水平是升高的[17]。而本研究的結果提示CCL2在GIG中是下降的,這可能與GC可以下調CCL2的表達有關。CCL2在GC誘導的青光眼中的生理作用需要進一步研究。胰島素樣生長因子1(insulin like growth factor 1,IGF1)在地塞米松處理組亦表現為下調,IGF1可由小梁網細胞表達,被認為可促進基質金屬蛋白酶產生及減少細胞外基質的沉積,改善房水流出[18]。因此,IGF1的下調導致細胞外基質沉積可能是GIG的發病機制之一。但有報道稱開角型青光眼患者房水中IGF1表現為上調[19],IGF1在開角型青光眼中的升高可能是機體的負反饋調節。其他2個下調基因,前列腺素氧化環化酶2(prostaglandin-endoperoxide synthase 2,PTGS2)和趨化因子(C-C基序)配體5(CCL5),在青光眼研究中并未見報道,其表達和功能仍值得研究。
在上調基因中,內皮素1(endothelin 1,EDN1)是另一個重要的樞紐基因。EDN1是目前最強的血管收縮肽,在調控血管舒縮、細胞增殖、分化等方面發揮重要作用。同時,EDN1還具有強大的促纖維化作用,通過多種途徑促進成纖維細胞、心肌細胞、血管平滑肌細胞等合成細胞外基質,并干擾組織中基質金屬蛋白酶的活性,導致細胞外基質蓄積。EDN1通過活化Rho激酶來調節多種細胞骨架相關蛋白的磷酸化,從而介導細胞骨架的重構。在眼部,房水流出通道上小梁網和Schlemm管中含有豐富EDN1及其受體。非色素性睫狀上皮細胞可能是眼組織中EDN1產生的一種來源[20]。在原發性開角型青光眼、正常眼壓青光眼,色素剝脫綜合癥患者和青光眼動物模型房水中,EDN1的水平比正常明顯升高,因此認為其與青光眼發病密切相關[21]。GC可刺激EDN1的表達[22],因此在GIG中,GC可能通過上調EDN1從而導致小梁網細胞外基質增加和/或改變小梁細胞骨架和細胞形態,引起房水流出阻力增加,最后導致眼壓增高。
綜上,通過生物信息學分析,我們認為地塞米松引起的人小梁網病理改變主要在細胞外基質,引起的通路改變主要集中在血管平滑肌收縮、花生四烯酸代謝、醚脂質代謝和膽堿代謝,篩選出的7個關鍵樞紐基因中,有3個基因被報道與房水調節有關,包括2個下調基因(CCL2和IGF1)和一個上調基因(EDN1),這3個基因在GIG的發病機制中可能起著重要作用。其他2個下調基因(PTGS2和CCL5)和2個上調基因(FOS和LPL),在青光眼研究中并未見報道,其在青光眼中的作用仍值得探索。

