輸血輸液加溫儀在食道癌根治術中的應用效果
余 遙 閔燦梅 陸海霞
食道癌多見于中老年人,是我國常見惡性腫瘤。食道癌根治術是食道惡性腫瘤治療的有效治療手段,主要步驟為切除瘤體上下端足夠長度的食道及周圍受累組織、胃的游離(管狀胃的制作)以及食管-胃吻合等,其手術創傷大,時間長。術中常見并發癥包括出血、低體溫等。其中術中低體溫(核心體溫<36 ℃)在胸外科手術中發生率高達78.3%,是一種常見并發癥,低體溫可增加機體耗氧量,可導致術中出血和術中感染的風險加大,對循環系統和中樞神經系統造成損傷。在麻醉蘇醒期可增大寒戰、躁動的發生率,同時延長麻醉蘇醒時間,嚴重影響患者的手術安全及術后恢復。既往研究發現傳統保暖方式對降低低體溫、寒戰、躁動的發生率及減少麻醉蘇醒時間有一定效果,本研究旨在探討輸血輸液加溫儀在食道癌根治術中的應用效果。
1 資料與方法
1.1 入組標準 選取2019年2月-2021年2月在本院行食道癌根治術的108例手術患者,ASAⅠ~Ⅱ級。采用隨機數表法將患者隨機分為實驗組和對照組,對照組患者中男36例,女18例,年齡48~76歲;實驗組患者中男38例,女16例,年齡47~77歲。記錄兩組患者的體質量、圍手術期體溫、手術時間(從切皮到縫皮完畢)、術中失血量、輸液量、麻醉蘇醒時間,麻醉蘇醒期寒戰、躁動的發生率。兩組患者的環境條件為手術室室溫:22 ℃~25 ℃,濕度:40%~60%。①對照組:非手術部位以棉被保護,術中保持布類敷料干燥,保持整個手術野干燥清潔,術中所需輸注液體常溫下輸入。②實驗組:在常規保溫基礎上,加用輸血輸液加溫儀(奇匯FT2800醫用輸血輸液加溫儀),將預充的輸液管路填滿加熱管,初始將溫度設置到37.0 ℃,根據病情調節合適滴速,打開儀器開關開始加熱,根據患者體溫變化隨時調節輸血輸液加溫儀的設定溫度(具體見討論部分)。兩組胸腹腔沖洗液均采用恒溫箱加溫至37.0 ℃。排除標準:手術時間≤3 h或手術時間>5 h;過度肥胖或消瘦(即BMI>30或BMI<18);術前合并已存在的感染、發熱(腋溫>37.4 ℃)或低體溫(腋溫<36.0 ℃);神志不清或精神障礙;術中出血>1000 mL或術中輸血;既往有甲亢等影響基礎代謝和基礎體溫疾病者;嚴重心腦血管疾病者。
1.2 方法
1.2.1 對照組 手術方式:胸腹腔鏡聯合食道癌根治術1例、經腹右經胸食道癌根治術41例、左經胸食道癌根治術12例。術前30 min將室溫調節至22 ℃~25 ℃,濕度調至40%~60%,術中保持溫濕度恒定;患者推入手術室后,巡回護士給患者加蓋棉被,開放患者靜脈通路,術中輸液在常溫下進行;常規消毒手術區域后鋪無菌巾,非手術部位以棉被保溫,術中保持布類敷料干燥,保持整個手術野干燥清潔。
1.2.2 實驗組 手術方式:胸腹腔鏡聯合食道癌根治術3例、經腹右經胸食道癌根治術44例、左經胸食道癌根治術7例。在對照組的保溫基礎上,靜脈輸液通過輸血輸液加溫儀(奇匯FT2800醫用輸血輸液加溫儀)進行加溫后輸入患者體內,操作程序如下:①將儀器固定于輸液架上,高度在輸液袋口下面20~30 cm,和茂菲滴管平齊。②連接電源,將輸液器預充,排空空氣。③將預充的管路末端2~3 cm處壓入加熱管尾部,將管路向加熱管頭部方向捋壓過去,直到管路填滿加熱管。④將裝填了管路的加熱管頭尾分別掛靠在儀器相應的位置上,避免輸液管尾端觸碰地面。⑤初始將溫度設置為37 ℃(溫度設置范圍為33 ℃~41 ℃),根據病情調節合適滴速。
1.3 觀察指標 ①使用紅外耳溫槍(德國博朗)測量同側耳溫,記錄入室、麻醉誘導前、手術中0.5 h、1 h、1.5 h、2 h、2.5 h、3 h、3.5 h、4 h、4.5 h、5 h及手術結束時的耳溫,術中耳溫<35.4 ℃(正常值:35.4 ℃~37.7 ℃)標記為低體溫。②記錄麻醉蘇醒期躁動(肢體躁動且有反抗表現,或發出無法抑制的呼喊聲)與寒戰(術后30 min內肌肉不自主的收縮抽動)發生情況。③記錄麻醉蘇醒時間(從停用麻醉藥開始到能正確回答問題,定向力恢復等)。
2 結 果
2.1 兩組患者一般資料比較 兩組患者平均年齡、體質量、出血量、平均手術時間等一般資料方面比較,差異均無統計學意義(P>0.05),具有可比性。見表1。
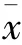
表1 兩組患者一般資料比較(±s)
2.2 兩組患者各個時間點體溫變化的比較 由于食管手術涉及到消化道切除及重建吻合,故手術較為復雜,兩組患者手術時間均在5 h以上。在手術開始前2 h內體溫變化差異無統計學意義(P>0.05),在2 h后,體溫差異逐漸明顯,且實驗組患者明顯高于對照組(P<0.05)。見表2。
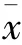
表2 兩組患者各個時間點體溫變化的比較(±s,℃)
2.3 兩組患者麻醉蘇醒時間,麻醉蘇醒期寒戰、躁動的發生率比較 對比表3和表4可得出,在使用血輸液加溫儀的情況下,實驗組患者麻醉蘇醒時間較對照組有明顯縮短,且蘇醒期的寒顫躁動發生率有明顯降低,差異有統計學意義(P<0.05)。
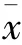
表3 兩組患者蘇醒時間比較(±s,min)

表4 兩組患者寒戰、躁動發生率比較 例(%)
3 討 論
3.1 低體溫的影響因素
3.1.1 麻醉藥物 機體的體溫是由下丘腦的體溫調節中樞進行控制的,通過前部的散熱中樞和后部的產熱中樞相互協調,使散發的熱量與產生的熱量保持相對平衡,以維持正常運轉。手術患者由于使用麻醉藥品阻斷了大部分神經的傳導,致患者的體溫調節中樞不能隨著外界環境溫度的變化而自由調節體溫,從而導致術中低體溫的發生。研究顯示發生低體溫的危險因素有:高齡、麻醉時間長、術中失血量大、術中補液量大、術中輸血量大等,其中全身麻醉是導致患者術中低體溫的重要危險因素。麻醉時間≥3 h,患者低體溫的發生率顯著增加。
3.1.2 環境溫度 手術間高效過濾器凈化送風口一般安裝在手術臺上方,空氣對流帶走機體部分熱量,從而使體溫下降;研究表明,手術室溫度≤21 ℃,可導致下丘腦對溫度調節能力下降,患者極易出現低體溫情況。
3.1.3 輸血、輸液 手術中輸入常溫液體可引起外周循環的“冷稀釋”,從而導致患者體溫下降及寒顫的出現,輸入越多,體溫下降就越快;低于機體溫度的液體進入人體需要吸收較多熱量才能達到人體溫度,而術中大量輸入常溫液體可增加機體散熱,表現出寒戰等癥狀,而麻醉時間延長則又會導致機體熱量額外的消耗。
3.2 術中低體溫的不利影響 全麻蘇醒期躁動是全身麻醉手術患者麻醉蘇醒期的一大并發癥,患者主要表現為興奮、躁動及定向力障礙,蘇醒期患者常常會因為疼痛、尿管、胸腔引流管刺激和低體溫等導致術后躁動的發生,嚴重影響了患者安全性以及舒適度。全身麻醉時,由于體表消毒、低溫藥物的攝入、手術時間長以及手術室溫度低等多種因素的影響,導致患者在進入麻醉期后會出現體溫降低的現象,而術中體溫的降低會導致藥物代謝速度下降,可能導致術后患者麻醉蘇醒時間的延長。
3.3 輸血輸液加溫儀溫度設置
3.3.1 輸液溫度設置 正常成人初始溫度設置為37 ℃,術中根據手術情況調節;如有以下情況,可設置為38 ℃~39 ℃,如嬰幼兒、新生兒、老年患者、血管彈性差以及術中出血量大等,其易受外界環境溫度的影響而變化,可適當調整。
3.3.2 輸血溫度設置 庫存血溫度與患者體溫有較大差異,常導致患者體溫降低以及寒戰反應等,研究表明,使用輸血輸液加溫儀,將溫度設置為38 ℃,復溫后的紅細胞懸液,紅細胞壓積、紅細胞計數及血清離子無明顯變化,并且在核對完后及時輸注,提高了輸血的效率,可為術中緊急輸血贏得寶貴的搶救時間。
3.4 加用輸血輸液加溫儀的重要意義 傳統的被動保暖方法主要包括自身棉襪保暖、提高室溫、增加敷料覆蓋等措施,因操作方便、成本低,被廣泛應用,但該措施單獨使用效果往往不佳,且機動性差,容易導致圍手術期低體溫的發生。主動加溫比被動保暖更有效,主要包括暖風加熱系統、輸液加溫系統、變溫毯等措施。食管手術由于其復雜性,一直以來都是胸外科的高難度手術,尤其是傳統開放性手術,手術創傷大,胸腹腔暴露時間長,輸液較多,都是影響患者手術后恢復的重要因素,其中如何預防低體溫是護理上迫切需要解決的問題。我們采用輸液加溫儀進行術中輸液加溫處理,是通過輸血輸液加溫儀控制患者的輸液溫度,讓其保持在36.0 ℃~37.0 ℃,有效避免因輸入低于機體溫度的液體而致的體溫下降,讓患者的體溫始終在恒定狀態,進而降低手術過程中低體溫的發生率,減少術后不良反應的發生,同時該方式對手術的影響較低,安全性較高,可改善患者手術的預后效果。本研究結果顯示,實驗組患者麻醉蘇醒期寒戰、躁動發生率明顯低于對照組,實驗組患者麻醉蘇醒時間早于對照組,也驗證了本實驗的效果。綜上所述,在食管癌手術中采用傳統保暖方式加用輸血輸液加溫儀,有助于減緩術中體溫下降的幅度及降低麻醉蘇醒期寒戰、躁動的發生率,縮短麻醉蘇醒時間,利于術后恢復。

