三種新冠病毒疫苗的比較
邵江樵
摘要 推行新冠病毒疫苗的接種是建立群體免疫,控制疫情最有效的辦法。文中闡述了我國目前廣為使用的1針、2針、3針疫苗制備的技術線路和疫苗的成分特點和接種。
關鍵詞 新冠疫苗 新型冠狀病毒滅活疫苗 腺病毒載體重組疫苗 重組新冠病毒疫苗
中圖分類號 Q-49
文獻標志碼 E
由新冠病毒引起的新冠肺炎對公共健康造成了極大的威脅,對經濟發展造成了嚴重影響。新冠病毒沒有細胞結構,是一種帶包膜的RNA病毒,其包膜主要來源于宿主細胞膜。膜表面主要由刺突蛋白(S)、包膜蛋白(E)和膜蛋白(M)3種結構蛋白組成。病毒膜內是由核衣殼蛋白(N)包裹的RNA。新冠病毒通過S蛋白(刺突蛋白)與細胞膜表面受體ACE2結合,以包膜與宿主細胞膜融合方式完成病毒內吞,進入人體宿主細胞,開始增殖,破壞宿主細胞,同時引起人體相應的免疫反應。新冠病毒疫苗的研制和疫苗接種是建立群體免疫、控制疫情最有效的辦法。目前,國內普遍使用的新冠疫苗有滅活疫苗、腺病毒載體疫苗、重組蛋白疫苗。研制思路大多以S蛋白(刺突蛋白)為抗原進行設計。
1新型冠狀病毒滅活疫苗(Vero細胞)滅活疫苗屬于比較傳統的疫苗類型,研發歷史比較悠久,技術也相對比較成熟。病原體在受控條件下
生長,培養過程中被殺死而失去致病能力,制成疫苗,利用失去活性的病毒刺激人體產生抗體。
新型冠狀病毒滅活疫苗(Vero細胞)的生產需要經過:細胞培養→病毒培養→滅活→純化→配比(半成品)→灌裝→包裝七大步驟,每一步還有更多更細致的環節,質控檢測則貫穿全程。
滅活疫苗生產的核心之一是生產疫苗原液,通過細胞培養、病毒培養、滅活、檢測、純化等流程,得到純度極高的疫苗原液。
細胞培養:Vero細胞是非洲綠猴的腎臟上皮細胞,是連續的非整倍體細胞,能無限增殖。用含質量分數為10%新生牛血清的199培養基培養,在pH控制在7.2~7.4,溫度34~37±0.2°C,微載體培養4d,讓細胞進入平臺期。
病毒培養:在Vero細胞平臺期接種新冠病毒(弱病毒株或高效價病毒株)。接種病毒后,更換為含質量分數為5%的新生牛血清的199病毒維持液,進行灌流培養。
滅活是用物理或化學手段使病原體失去感染、致病和繁殖的能力,但保留抗原性的過程。常見的滅活方法:把培養所得的病毒液,按一定比例加入甲醛或β-丙內酯等試劑進行滅活。甲醛為活潑的烷化劑,對病毒核酸和病毒蛋白質都有破壞作用,甲醛使病毒核酸滅活——與腺嘌呤、鳥嘌呤和胞嘧啶等含有胺基的堿基結合而使病毒核酸變性。甲醛使蛋白質變性,與病毒蛋白質中的氨基酸發生交聯反應,破壞空間結構,使蛋白質變性。甲醛對單鏈核酸最為有效,故常用于RNA病毒的滅活。滅活劑β-丙內酯直接與病毒核酸分子中的鳥嘌呤或腺嘌呤作用,引起單鏈斷裂或雙螺旋鏈交聯而達到滅活病毒的作用。
疫苗生產的核心之二是配比。配比是疫苗生產中的重要一環,配比是疫苗原液中加入佐劑、稀釋液等,將其制成半成品的過程。滅活疫苗誘導的免疫效果相對較差,佐劑能增強機體對抗原的免疫應答或改變免疫應答類型,減少抗原用量,進而降低疫苗成本。
新型冠狀病毒滅活疫苗(Vero細胞)的主要成分是殺死的新冠病毒,接種后不在宿主細胞內復制,無傳染性,保留的免疫原性可以刺激人體的體液免疫。目前,新冠病毒滅活疫苗(Vero細胞)需要接種兩劑;首劑與第2劑次的接種間隔要在3周及以上,第2劑在首劑接種后8周內盡早完成。也就是接種完第1劑次后的21~56天內完成第2劑接種。同種疫苗兩次接種的目的利用第一次接種產生的記憶細胞對相同抗原的特異性識別,迅速增殖分化,使人體產生更多的效應B細胞(漿細胞),從而產生更多的抗體,形成較好的免疫效果。
2腺病毒載體重組疫苗(5型腺病毒載體)
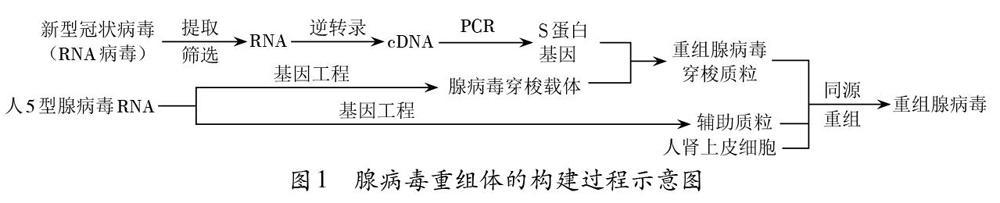
腺病毒(Ad)是一種無包膜的雙鏈線性的DNA病毒。腺病毒基因組包含與腺病毒復制相關的E1~E4基因,E1基因為病毒復制必需區,缺失則成為復制缺陷型載體。E3基因是病毒復制非必需區,可用于外源基因的插入。Ad5是一種普通感冒病毒,以人5型腺病毒(Ad5)為載體的重組新冠疫苗是能表達外源S蛋白但復制缺陷的Ad5載體疫苗。具體來說,通過基因工程,構建了一個插入S蛋白基因且E1基因缺失的腺病毒重組體(圖1)。重組體外殼仍然是腺病毒的正常外殼蛋白,使重組腺病毒具有同樣的感染力進入靶細胞;由于基因組的E1區域被外源目的基因取代,進入靶細胞后病毒不能復制,但含有編碼新冠病毒S蛋白的基因可以表達目的蛋白——S蛋白,并從細胞內轉移到細胞外,激發一系列的免疫反應。
由于新冠病毒為RNA病毒,其遺傳物質不能直接拼接到質粒上,因此在制備以上疫苗時需先通過逆轉錄過程獲得相應的目的基因——S蛋白基因。腺病毒病毒載體重組疫苗的巧妙之處在于改造后的腺病毒進入細胞后不會復制,但可使宿主細胞表達S蛋白(抗原)。腺病毒載體新冠疫苗可以同時刺激人體的體液免疫和細胞免疫。體液免疫產生的抗體可以直接與病毒結合,使其失去寄生能力;細胞免疫則可以殺傷被病原體感染的細胞(如被接種疫苗感染的細胞)。
目前,腺病毒載體疫苗免疫程序是接種1劑次。其優點體現在能持續表達抗原,免疫應答更持久。缺點:若在接種該種疫苗前機體曾感染過腺病毒,人體內會具有5型腺病毒的抗體,接種疫苗時會被體內相應抗體部分清除而降低免疫效果或導致不能攜帶S蛋白基因進入細胞內表達,使該種疫苗的有效性降低。
3重組新冠病毒疫苗(CHO細胞)
重組新冠病毒疫苗(CHO細胞)又叫重組亞單位疫苗,制備的技術線路:提取新冠病毒RNA→逆轉錄生產cDNA→擴增篩選RBD蛋白基因→構建基因表達載體→導入CHO細胞→純化RBD蛋白→加入佐劑、稀釋液等制成疫苗。
S蛋白通過與受體血管緊張素轉換酶2(ACE2)結合,介導病毒進入宿主細胞。S蛋白包含兩個功能性亞基S1和S2,其中S1負責與宿主細胞受體結合,S2亞基負責病毒膜和細胞膜融合。在感染過程中,S蛋白被宿主蛋白酶切割成N端的S1亞基和C端的S2亞基。RBD蛋白是真正與ACE2結合的蛋白。
CHO細胞是中國倉鼠卵巢細胞,是生物制藥最常用的細胞表達系統。重組新冠病毒疫苗(CHO細胞)生產工藝先進成熟,采用轉基因技術,通過成熟的CHO細胞重組表達RBD蛋白特異性抗原,能實現高產量、高純度、低成本;并且疫苗只含RBD蛋白,純度高,無病毒核酸成分,安全性好。接種重組新冠病毒疫苗(CHO細胞)——RBD蛋白,誘導人體產生中和抗體,可以阻斷新冠病毒與宿主細胞表面的ACE2結合,達到預防感染的目的。
目前,重組新冠病毒疫苗(CHO細胞)需要接種3劑:相鄰2劑之間的接種間隔建議≥4周。第2劑盡量在接種第1劑次后8周內完成,第3劑盡量在接種第1劑次后6個月內完成。
以上三種疫苗的技術路線各不相同,但都是利用新冠病毒的S蛋白,使人體產生特異性免疫反應,形成保護效應。
參考文獻:
[1]楊安納,王吟,楊東升,周艷萍,涂晶,盧佳,李茜,施金榮,王澤鋆,申碩.新型冠狀病毒滅活疫苗(Vero細胞)中β-丙內酯殘留氣相色譜檢測方法的建立、優化及驗證.中國生物制品學雜志[J].2021,(4):448-452.
[2]韓中山.生物反應器培養Vero細胞制備狂犬病毒.中國畜牧獸醫文摘[J].2013,(3):50-51.

