MRI斑塊診斷軟件定性評估頸動脈斑塊
魏夢嬌,高陽,吳瓊,郝祥程,王紅茹
頸動脈斑塊是腦卒中的致病原因之一,近年來已成為影像研究的熱點[1]。頸動脈斑塊有多種類型,有的相對穩定,有的極其高危隨時可能導致卒中發生,這主要取決于斑塊成分的類型、含量和分布[2]。
磁共振高分辨血管壁成像(magnetic resonance high-resolution vessel wall imaging,HR-VWI)具有常規MRI檢查不具備的高信噪比、高軟組織分辨率以及黑血、亮血等多對比序列,在頸動脈斑塊成分的定性分析方面具有獨到的價值,但HR-VWI檢查獲得的圖像數據量大,全手動處理費時費力,且人工定性分析非常依賴于評估者的臨床經驗,限制了這項技術在臨床的廣泛應用。而最新的磁共振圖像斑塊診斷(MRI-plaque view,MPV)軟件能實現對斑塊成分的自動識別和定性、定量分析。
本研究通過與病理結果對照,對比人工手動與軟件半自動方法在評估頸動脈斑塊成分中的差異性及可靠性,旨在探討頸動脈斑塊半自動軟件的臨床應用前景,并指導卒中預防和個體化治療。
材料與方法
1.研究對象
研究對象為2019年12月-2020年10月在本院神經外科接受頸動脈內膜剝脫術(carotid endarterectomy,CEA)治療的連續35例患者。納入標準:①經影像檢查確定頸動脈狹窄程度大于50%;②CEA手術前行HR-VWI檢查,且兩者間隔不超過3天。5例因以下原因被排除:①HR-VWI圖像質量差,無法進行斑塊成分的診斷及后處理;②CEA術中斑塊在剝離時受損,斑塊原始形態改變;③斑塊病理切片染色不成功。最終將符合要求的30例患者的頸動脈斑塊圖像用于斑塊成分分析。
本研究經倫理委員會批準,所有患者簽署知情同意書。
2.MRI掃描方法
使用SiemensSkyra 3.0T磁共振掃描儀和32通道頭頸動脈聯合線圈。本研究使用特定的掃描方案獲得高分辨率頸動脈血管壁圖像:首先,對患者雙側頸動脈行大范圍掃描,掃描序列包括3D TOF-MRA、3D磁化準備快速采集梯度回波序列(magnetization-prepared rapid acquisition with gradient-echo sequences,MPRAGE)和3D最優化采集可變翻轉角快速自旋回波序列(sampling perfection with application optimized contrasts using different flip angle evolutions sequences,SPACE)T1WI;為滿足軟件后處理要求,采用MIP法對3D TOF-MRA的原始圖像進行圖像重組,初步確定血管狹窄和斑塊所在部位,然后以該部位為中心進行小范圍掃描,掃描序列包括橫軸面3D TOF-MRA(36個層面)、2D-TSE-T1WI和2D-TSE-T2WI(20個層面);注射對比劑后進行大范圍掃描,掃描序列為3D-SPACE-T1WI,總掃描時間約45min。各序列掃描參數見表1。

表1 各序列主要掃描參數
3.人工評估標準
斑塊成分人工評估由兩位具備10年以上診斷經驗的影像科醫師分別獨立分析,若判斷意見不一致,則由另兩位更有經驗的高級職稱醫師共同商議,得出一致結果,評估標準如下。①脂質核心:T1WI呈等信號、T2WI呈等/稍高信號,TOF、MPRAGE圖像上無異常高信號,增強T1WI無明顯強化(圖1);②斑塊內出血:TOF、T1WI和MPRAGE圖像上均呈高信號,以MPRAGE圖像上最明顯(圖2)。③破裂纖維帽:完整的纖維帽在TOF、T1WI和T2WI上表現為鄰近管腔的帶狀或環狀低或等信號,破裂的纖維帽在TOF、T1WI和T2WI上表現為呈低或等信號的帶狀或環形區不連續,并與管腔相通形成龕影(圖3);④鈣化:所有序列上均表現為低信號(圖4~5)[2-5]。

圖1 頸動脈斑塊內脂質核心。a)T1WI上呈等信號(箭);b)T2WI上呈稍高信號(箭);b)3D-TOF圖像上呈等信號(箭);d)對比增強T1WI上無明顯強化(箭);e)三維融合圖像,清晰顯示斑塊內各種成分;f)鏡下可見斑塊內有膽固醇裂隙和泡沫細胞沉積(×100,HE)。

圖3 頸動脈斑塊破裂纖維帽HR-VWI和病理圖像。a)T1WI示斑塊表面有龕影(箭);b)T2WI示斑塊表面有龕影(箭);c)鏡下示纖維帽連續性中斷(箭;×100,HE)。 圖4 頸動脈斑塊內大片狀鈣化HR-VWI和病理圖像。a)T1WI上呈低信號(箭);B)T2WI上呈低信號(箭);c)三維融合圖像直觀顯示鈣化成分及其范圍;d)鏡下可見斑塊內大片狀鈣化成分(箭;×100,HE)。 圖5 頸動脈斑塊內散在小鈣化灶HR-VWI和病理圖像。a)T1WI上可見斑塊內散在低信號灶(箭);b)T2WI顯示斑塊內散在低信號灶(箭);c)3D TOF圖像上顯示斑塊內散在低信號灶(箭);d)三維融合圖像直觀顯示斑塊內散在鈣化灶;e)鏡下可見斑塊內有彌漫分布的小鈣化灶(×100,HE)。
4.MPV軟件處理和分析流程
軟件處理及分析步驟:將掃描圖像傳入MPV工作站(Version 2017),每例患者選取4個序列(2D-T1WI-TSE、2D-T2WI-TSE、3D TOF-MRA②、2D CE-T1WI-TSE)的圖像進行分析。由兩位具備10年以上診斷經驗的影像科醫師分別使用斑塊成分分析軟件進行后處理和分析,取兩位醫師多次勾畫并一致認定ROI的軟件分析結果為最終結果。選擇分析血管(左側或右側頸動脈),確定參考平面(一般以頸動脈分叉作為參考平面),將圖像放大200%,先自動勾畫血管管腔,全部勾畫完再勾畫管壁,管腔自上而下勾畫,管壁自下而上勾畫,之后手動調整邊界確保勾畫無遺漏。使用軟件自帶的配準圖像功能以確保多對比序列圖像位置匹配。進入研究模式后軟件即可進行自動分析,記錄每一例患者的斑塊成分分析結果并保存典型圖像。
5.病理標本處理
在CEA術中獲取斑塊標本送病理實驗室進行切片制作,切片厚度1~2mm,進行HE染色并于顯微鏡下觀察斑塊成分,此過程由2位資深病理科醫師協商完成。
6.統計學方法
使用SPSS 22.0統計軟件進行數據分析。計數資料以頻數及百分比表示,采用配對四格表χ2檢驗分別比較人工評估結果與病理診斷結果、MPV軟件分析結果與病理診斷結果、人工評估結果與MPV軟件分析結果,以P<0.05為差異有統計學意義。以病理結果為金標準,計算人工方法和MPV軟件對斑塊各征象的診斷敏感度、特異度、陽性預測值(positive predictive value,PPV)、陰性預測值(negative predictive value,NPV)、誤診率、漏診率和符合率。
結 果
1.臨床資料
共入選30例患者,男22例,女8例,年齡54~82歲,平均(68.38±5.49)歲。其中,高血脂2例(6.7%),高血壓病17例(56.7%),糖尿病9例(30.0%),有吸煙史20例(66.7%),有飲酒史14例(46.7%),發生缺血性卒中15例(50.0%),顱內血管斑塊23例(76.7%)。左側頸部動脈病變17例(56.7%),右側13例(43.3%);血管狹窄率為50%~60%者 2例(6.7%),60%~70%者8例(26.7%),70%~80%者10例(33.3%),80%~90%者8例(26.7%),90%以上者2例(6.7%)。
2.人工評估與病理診斷結果的比較
人工和病理方法對斑塊成分的診斷結果見表2~3。

表2 人工和病理方法對頸動脈斑塊成分檢出結果的比較 /例(率)
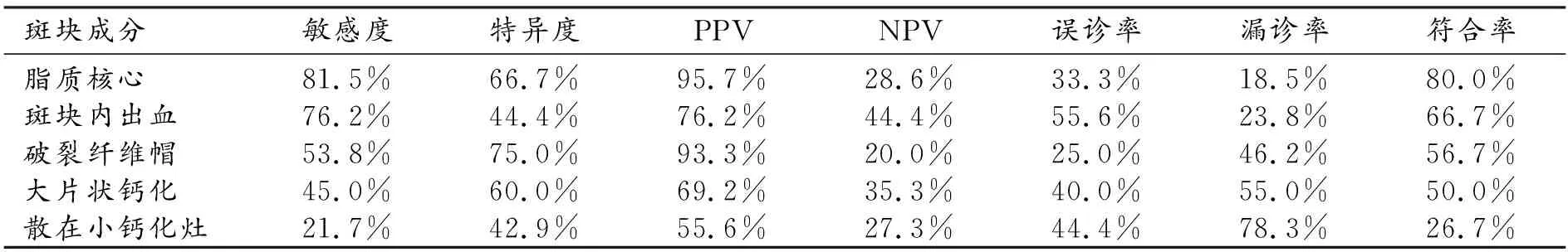
表3 人工評估頸動脈斑塊成分的效能指標
兩種方法對脂質核心、斑塊內出血和大片狀鈣化的檢出率的差異無統計學意義(P>0.05),對破裂纖維帽和散在小鈣化灶檢出率的差異有統計學意義(P<0.05)。
3.MPV軟件分析與病理診斷結果的比較
由于MPV軟件識別破裂纖維帽作用有限,因而本次研究未進行破裂纖維帽的軟件分析。MPV軟件和病理方法對斑塊成分的診斷結果見表4~5。兩種方法對各種斑塊成分檢出率的差異均無統計學意義(P>0.05)。

表4 MPV軟件和病理方法對頸動脈斑塊成分檢出結果的比較 /例(率)

表5 MPV軟件評估頸動脈斑塊成分的效能指標
4.人工評估與軟件分析結果的比較
人工評估和MPV軟件對斑塊成分檢出結果的比較見表6。兩種方法對散在小鈣化灶檢出率的差異有統計學意義(P<0.05),對脂質核心、斑塊內出血和大片狀鈣化檢出率的差異均無統計學意義(P>0.05)。

表6 人工與MPV軟件對頸動脈斑塊成分評估結果的對比
總體而言,MPV軟件評估頸動脈斑塊成分的診斷符合率較人工方法更高(圖6)。
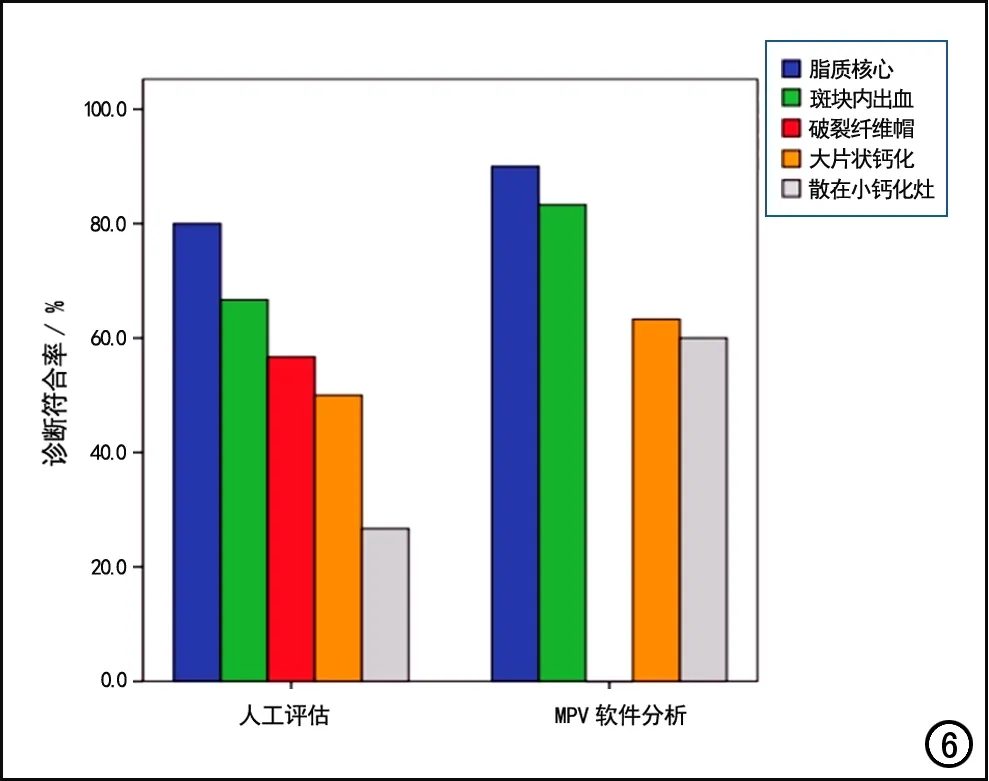
圖6 人工評估與MPV軟件對各種頸動脈斑塊成分診斷符合率的條形圖。
討 論
頸動脈粥樣硬化斑塊是臨床常見疾病,美國神經放射學會2018年發布的專家共識認為頸動脈斑塊的組成與斑塊破裂的脆弱性有關,而斑塊破裂被認為是腦卒中的潛在致病原因,因此準確識別復雜形態斑塊的成分對于預防腦卒中具有重要價值[2]。目前人工評估HR-VWI原始圖像可以實現對頸動脈斑塊各種成分(脂質核心、出血、破裂纖維帽、大片狀鈣化、散在小鈣化灶等)特征的定性分析,但面臨以下問題:(1)全手動處理及人工評估耗費時間長;(2)人工評估依賴于評估者的經驗,不同評估者之間的差異較大。為了解決以上問題,本研究引入了能夠半自動化分析斑塊成分的MPV軟件,該軟件已經被FDA/CFDA核準,具有獨特的磁共振圖像后處理技術,可以在手動勾畫血管的基礎上,直接呈現斑塊的成分特征,評估斑塊的性質,并提供三維融合圖像(圖1~5)。本研究通過人工評估結果和MPV軟件分析結果與病理結果的對比,發現兩者均有較高的敏感度和特異度,尤其是脂質核心(lipid-rich necrotic core,LRNC)和斑塊內出血(intra-plaque hemorrhage,IPH)等重要的易損指標。
在本研究中,人工評估和MPV軟件均表現出對LRNC強大的識別能力,其陽性預測率分別達95.7%和96.2%,我們認為原因有兩點:一是LRNC作為粥樣斑塊的主體組成部分占據很大的比例,并且大多數行CEA手術的患者,其頸動脈斑塊病變已經進展到晚期,斑塊內含有大量的脂質成分;二是通過既往大量的體內和體外研究,已較好地確立了如何根據T1WI、T2WI以及CE-T1WI圖像上的信號特征來識別LRNC[2]。Skagen等[6]發現易損斑塊分析軟件半自動分割評估LRNC在頸動脈斑塊內的體積百分比與病理組織學結果顯著相關,體現了易損斑塊分析軟件定量分析LRNC的應用價值,而Xu等[7]于2014年已驗證了基于LRNC含量評估頸動脈斑塊破裂危險度的頸動脈粥樣硬化危險度評分的應用價值,提示LRNC定量分析預測腦卒中的強大潛力,因此開發MPV軟件評估LRNC具有重要的臨床意義。
導致IPH的病因主要有兩個:一是新生血管破裂或斑塊本身破裂;二是由于炎癥、代謝疾病或糖尿病等基礎疾病所致。Sigovan等[8]通過與病理對照,證實人工評估IPH的敏感度和特異度分別為83%和100%,本研究中人工評估結果較其略差,敏感度和特異度分別為76.2%和44.4%,但軟件評估的敏感度和特異度可達85.7%和77.8%。回顧漏診及誤診病例,我們認為可能是由于斑塊內新鮮出血早期信號與LRNC類似而造成誤判,另一個誤差來源可能是信號平均的部分容積效應,另外在CEA術中,由于手術操作的復雜性和不確定性,可能損害斑塊從而造成病理上的陽性結果。目前已經證實對比增強技術能夠無創性定量檢測頸動脈斑塊內新生血管的程度和功能特征[9],并且Song等[10]發現半自動分割方法對IPH體積的量化分析具有很高的可靠性,這為人工評估和MPV軟件識別IPH以及預測未來缺血事件提供了更多信息。
斑塊表面纖維帽破裂和侵蝕是預測高風險卒中的關鍵特征[2]。Hatsukami等[11]的研究證實,HR-VWI人工評估能夠區分完整的厚纖維帽和破裂的薄纖維帽,與病理結果高度一致(Kappa=0.83)。在本研究中,30例患者的頸動脈斑塊中病理發現26例有纖維帽破裂,僅4例纖維帽完整,而術前人工評估中僅在14例患者中檢出了破裂纖維帽,敏感度、特異度及診斷符合率分別為53.8%、75.0%和56.7%,與病理結果對比差異具有統計學意義(P<0.05),我們認為原因可能是目前的HR-VWI技術分辨率不夠,對纖維帽的細小破裂尚無法準確顯示。
Liu等[12]認為鈣化的形態和位置與斑塊的易損性密切相關,本研究證實了Liu等的觀點。本研究結果顯示在易損斑塊中散在小鈣化灶存在的概率明顯高于大片狀鈣化灶,原因可能是小鈣化灶周圍更易產生炎癥和血栓,其局部應力和應變極易引起斑塊破裂,而大片狀鈣化似乎穩定了斑塊,這可能與M2巨噬細胞極化有關[13],因此能否準確區分鈣化的形態對于斑塊易損性的評估具有重要價值。本研究中人工評估與MPV軟件分析對不同形態鈣化的診斷效能不同,大片狀鈣化在T1WI、T2WI以及TOF序列上較散在小鈣化灶的顯示更加明顯,因此對其診斷符合率更高,可能的原因是貼近或延伸到管腔里的小鈣化灶很容易被遺漏。目前關于鈣化形態、位置與頸動脈斑塊易損相關的高分辨MRI研究較少,而且本研究中也僅僅對鈣化進行了定性分析,有待在今后的研究中針對鈣化進行定量分析等更深入的研究。
本研究的局限性:(1)病例數較少;(2)缺乏對斑塊內成分的定量分析。綜上所述,MPV軟件僅需對頸動脈管腔及管壁進行簡單勾畫,就可以對斑塊成分進行定性分析,省時、準確、高效,且與人工評估和病理檢查間均具有較好的一致性,值得在臨床中廣泛使用。

