JNK信號通路在右美托咪定預處理減輕大鼠離體心肌缺血再灌注損傷中的作用*
殷存芝,陳 慧,陳玉姣,楊在群,陳亞華
(遵義醫科大學附屬醫院麻醉科,貴州遵義 563003)
恢復心肌的血供是挽救缺血性心臟病的關鍵治療措施,但由此產生的心肌缺血再灌注損傷(myocardial ischemia-reperfusion injury,MIRI)卻嚴重影響了患者的治療及預后。細胞凋亡是MIRI的特征之一,抗凋亡成為近年防治MIRI的重要措施[1]。右美托咪定是新型高選擇性的α2腎上腺素受體激動劑,有研究表明其預處理可減輕大鼠MIRI,其機制與抑制細胞凋亡有關[2]。C-Jun氨基末端激酶(C-Jun N-terminal kinase,JNK)是絲裂原活化蛋白家族進化上高度保守的一員。研究表明JNK信號通路的激活可促進細胞凋亡[3]。本研究探討右美托咪定預處理減輕離體大鼠MIRI的作用是否與抑制JNK信號通路的過度激活從而減輕細胞凋亡有關。
1 材料與方法
1.1 材料
1.1.1主要試劑
右美托咪定購自江蘇恒瑞醫藥有限公司;JNK抑制劑SP600125、JNK小鼠抗大鼠單克隆抗體、p-JNK小鼠抗大鼠單克隆抗體、GAPDH小鼠抗大鼠單克隆抗體、葡萄糖調節蛋白78(GRP78)小鼠抗大鼠單克隆抗體、Goat熒光二抗購自美國Selleck公司;TTC購自北京百奧思科生物技術有限公司;原位細胞凋亡試劑盒購自美國Sigma公司。
1.1.2動物
SPF級健康雄性SD大鼠60只,8~10周,260~280 g,由重慶騰鑫生物技術有公司提供,動物許可證編號:SCXK(湘)2014-0011。
1.2 方法
1.2.1模型制備及分組
腹腔注射1%的戊巴比妥鈉50 mg/kg麻醉大鼠后充分暴露心臟,迅速剪下并放置于95% O2及5% CO2預充并冷凍的4 ℃ K-H液中,輕輕擠壓心臟排除瘀血。迅速懸掛并固定于Langendorff裝置上,進行K-H液灌注,同時置入乳膠水囊至左心室,使左室舒張末期壓力維持在4~7 mm Hg,移動保溫杯使心臟處于恒溫系統中。每只心臟平衡15 min后,對照組(N組)持續灌注190 min;缺血再灌注損傷(I/R)組持續灌注30 min后,停止灌注40 min,復灌120 min;右美托咪定預處理(D)組灌注含有右美托咪定(10 nmol/L)的K-H液30 min,JNK抑制劑SP600125(SP)組灌注含有SP600125(10 μmol/L)的K-H液30 min,右美托咪定與SP600125混合處理(D+SP)組灌注含右美托咪定(10 nmol/L)和SP600125(10 μmol/L)的K-H液30 min,之后處理均同I/R組。
1.2.2大鼠心功能檢測
各組分別于平衡末(T1)、缺血前(T2)、再灌注末(T3)3個時點記錄心率(heart rate,HR)、左心室發展壓(left ventricular developed pressure,LVDP)、左心室舒張末壓(left ventricular end-diastolic pressure,LVEDP)、左室內壓最大上升/下降速率(maximum rate of increase of left ventricular pressure,±dp/dtmax)。
1.2.3TTC檢測心肌梗死面積
再灌注末取下心臟后置于-80 ℃冰箱冰凍數分鐘后取出,將心臟沿心尖至心底以橫切面切成厚薄一致的5塊環形切片,放置于盛有1%TTC染液的無菌器皿內,避光、恒溫孵育后置于10%的甲醛內固定24 h。將心臟進行拍照,并在Image Pro軟件下計算梗死面積。
1.2.4TUNEL檢測心肌細胞凋亡率(AI)
再灌注末切取左心室心肌體積約1 mm3的組織塊,制成冰凍切片,按照試劑盒說明書操作,將切片置于熒光顯微鏡下觀察并拍照。每個標本觀察5張切片,每張切片選取5個視野于高倍顯微鏡下觀察,AI=(綠色熒光染色細胞核數/總的細胞核數)×100%。
1.2.5電鏡觀察心肌超微結構
留取再灌注末左心室心肌體積約1 mm3的標本,放置于4%戊二醛內固定,0.1 mol/L二甲胂酸鈉緩沖液漂洗,1%鋨酸固定,乙醇脫水,環氧樹脂進行包埋、聚合,制作超薄切片并染色,透射電鏡下觀察、拍照。
1.2.6Western blot檢測心肌組織GRP78、p-JNK、JNK蛋白表達
取左心室心肌組織,BCA法測定蛋白濃度,制備SDS-PAGE凝膠,樣品進行電泳分離,轉膜,封閉,分別加入GRP78、JNK、p-JNK的一抗稀釋液,4 ℃孵育過夜,加入山羊抗兔熒光二抗,使用化學發光成像系統分析,以目標蛋白條帶熒光強度值與內參蛋白條帶熒光強度值的比值反映蛋白表達水平。
1.3 統計學處理
2 結 果
2.1 各組大鼠心功能的變化
在T3時點,與N組比較,其余組HR、LVDP、±dp/dtmax下降,LVEDP增加(P<0.05);與I/R組比較,D組、SP組、D+SP組HR、LVDP、±dp/dtmax增加,LVEDP下降(P<0.05);D組、SP組、D+SP組在各項心功能指標上無明顯差異(P>0.05),見表1。
2.2 各組大鼠心肌梗死面積比較
與N組比較,其余組再灌注末心肌梗死面積均增加(P<0.05);與I/R組比較,D組、SP組、D+SP組心肌梗死面積均降低(P<0.05);D組、SP組、D+SP組變化不明顯(P>0.05),見表2、圖1。
2.3 各組大鼠心肌細胞AI比較
與N組比較,其余組心肌細胞AI增加(P<0.05);與 I/R組比較,D組、SP組、D+SP組心肌細胞AI降低(P<0.05);與D組比較, SP組AI增加(P<0.05);與SP組比較,D+SP組心肌細胞AI降低(P<0.05),見表2、圖2。
2.4 各組大鼠超微結構改變
N組心肌細胞超微結構基本完整,結構清楚,未見明顯凋亡小體;I/R組心肌細胞出現明顯損傷,細胞破碎嚴重,明顯可見凋亡小體,肌原纖維絲排列紊亂并局部出現斷裂;D組、SP組、D+SP組:心肌細胞形態基本完整,少量細胞核破壞,線粒體聚集呈輕微腫脹,部分線粒體脊消失,局部發現空泡,偶見凋亡小體,見圖3。

白色:梗死區域;紅色:正常區域。
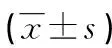
表1 各組大鼠不同時點心功能指標比較
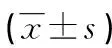
續表1 各組大鼠不同時點心功能指標比較

藍色:正常細胞核;綠色熒光:凋亡細胞核。
2.5 各組大鼠GRP78、p-JNK1/JNK1、p-JNK2/JNK2蛋白表達比較
與N組比較,其余組GRP78、p-JNK1/JNK1、p-JNK2/JNK2蛋白表達增加(P<0.05)。與I/R組比較,其余組GRP78、p-JNK1/JNK1、p-JNK2/JNK2蛋白表達降低(P<0.05)。與D組比較,SP組GRP78、p-JNK1/JNK1、p-JNK2/JNK2蛋白表達無明顯差異(P>0.05),D+SP組GRP78、p-JNK1/JNK1、p-JNK2/JNK2蛋白表達降低(P<0.05)。與SP組比較,D+SP組GRP78、p-JNK1/JNK1、p-JNK2/JNK2蛋白表達降低(P<0.05),見圖4~6。

黑色:細胞核出現核固縮現象;紅褐色:線粒體腫脹擴張脊消失,局部線粒體聚集;藍色:肌源纖維絲斷裂,排列紊亂;紫色:自噬體;標尺:5 μm。

圖4 各組大鼠GRP78、JNK、p-JNK蛋白印跡圖

a:P<0.05,與N組比較;b:P<0.05,與I/R組比較;c:P<0.05,與D組比較;d:P<0.05,與SP組比較。
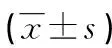
表2 各組大鼠心肌梗死面積與AI的比較
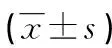
續表2 各組大鼠心肌梗死面積與AI的比較

a:P<0.05,與N組比較;b:P<0.05,與I/R組比較;c:P<0.05,與D組比較;d:P<0.05,與SP組比較。
3 討 論
右美托咪定是一種高選擇性α2腎上腺素受體激動劑,由于α2受體廣泛分布于心血管、中樞和外周系統及血小板,因此具有廣泛的生物學效應。右美托咪定不僅是一種良好的鎮靜劑,而且對于接受手術的高危心血管患者具有巨大的潛在保護效力[4]。大量研究表明右美托咪定對多種臟器均有良好的保護效應[5-6]。REN等[7]報道,右美托咪定可以減少缺血心肌無復流面積,改善心功能,減輕MIRI。胡杰等[8]研究表明,右美托咪定可以保護體外循環下冠脈旁路移植術患者的心肺功能。ZHANG等[9]報道,右美托咪定可以通過上調SIRT1/mTOR軸,減少心肌細胞凋亡、氧化應激及炎性反應、過度的心肌細胞自噬,減輕MIRI。本實驗結果顯示:與N組比較,I/R組大鼠心功能明顯降低,心肌梗死面積與AI明顯增加,心肌超微結構破壞嚴重,表明MIRI模型復制成功。而給予右美托咪定預處理后,大鼠心功能指標明顯改善,心肌梗死面積與AI明顯降低,電鏡所示的超微結構也顯示心肌結構破壞大大減輕,這些均可表明右美托咪定的確具有明顯的抗MIRI作用。
MIRI是治療多種心血管疾病過程中遭受的共同病理生理過程。在眾多的誘發因素中,細胞凋亡是其中的原因和特征之一。抑制凋亡對于防止MIRI意義重大。CHANG等[10]報道,右美托咪定預處理可以通過激活PI3K/AKT信號通路發揮抗凋亡作用,從而減輕MIRI。YUAN等[11]研究發現,右美托咪定可通過調控FKBP12.6/RyR2信號通路減輕H9C2心肌細胞缺氧復氧誘導的細胞內鈣超載與細胞凋亡。除了經典的線粒體途徑與死亡受體介導的凋亡途徑之外,內質網及介導的內質網應激(endoplasmic reticulum stress,ERS)途徑成為近年凋亡研究的熱點。MIRI時引起的缺血缺氧及鈣超載等會使內質網穩態失衡、功能紊亂,從而形成ERS。適度的ERS可通過處理異常蛋白等恢復內環境穩態,但持久或過度的ERS會通過活化相關因子及途徑誘發細胞凋亡[12],給機體帶來不利影響。GRP78是ERS的分子伴侶蛋白,當細胞受到外界刺激(缺氧、應激等)發生ERS時,細胞內會產生大量未折疊蛋白與錯誤折疊蛋白,GRP78也會相應大量增加并與錯誤折疊蛋白結合,維持內環境穩定。 因此,GRP78表達的急速增加被認為是ERS最敏感的標志物[13]。本實驗結果顯示:與N組相比,I/R組GRP78蛋白表達明顯增加;與I/R組比較,D組GRP78蛋白表達明顯降低。說明缺血再灌注誘發心肌組織出現嚴重的 ERS,而使用右美托咪定預處理后,ERS反應明顯減輕。
作為MAPK家族三大成員之一,JNK受細胞因子和各種應激的暴露而激活,被激活的JNK轉移至細胞核內,使底物C-Jun磷酸化,大量活化的C-Jun可誘導細胞凋亡反應[14]。JNK可通過導致凋亡的多條途徑誘導細胞發生凋亡, 其中主要是通過IRE1-TRAF2-ASK1-JNK通路參與到ERS介入的I/R的細胞凋亡過程,是缺血再灌注損傷與ERS之間重要的交叉通路。有研究報道,布托啡諾預處理可以明顯降低I/R組心肌組織JNK磷酸化水平,抑制JNK/NF-kB信號活化、心肌細胞凋亡,從而減輕MIRI[15]。本研究結果顯示,心肌缺血再灌注后JNK的活化形式p-JNK明顯升高,提示JNK通路參與了缺血再灌注對心肌的損傷。與I/R組相比,SP組的大鼠JNK蛋白表達、心肌梗死面積及AI明顯降低,說明通過抑制JNK通路可以明顯減少大鼠MIRI及細胞凋亡。而右美托咪定預處理對MIRI的保護作用中存在JNK水平的變化,結合右美托咪定預處理可以降低ERS標志物GRP78的表達,推測右美托咪定可通過某種作用下調JNK蛋白表達并抑制其活化,抑制過度的ERS,從而對JNK調控的細胞凋亡產生抑制作用。
綜上所述,右美托咪定預處理可以有效減輕大鼠離體心臟MIRI,且這種保護作用可能是通過抑制JNK信號通路的激活,從而減輕過度ERS及其介導的凋亡。

